Léčba sekukinumabem u dětí a adolescentů trpících artritidou s entezitidou a juvenilní psoriatickou artritidou: výsledky studie JUNIPERA
Artritida s entezitidou (ERA) a juvenilní psoriatická artritida (JPsA) představují dvě podskupiny juvenilní idiopatické artritidy (JIA). Účinnost a bezpečnost léčby sekukinumabem u těchto pediatrických revmatických onemocnění hodnotila randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie fáze III JUNIPERA.
Artritida s entezitidou (ERA) a juvenilní psoriatická artritida (JPsA) představují dvě podskupiny juvenilní idiopatické artritidy (JIA). Účinnost a bezpečnost léčby sekukinumabem u těchto pediatrických revmatických onemocnění hodnotila randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie fáze III JUNIPERA.
Obě podskupiny uvedených onemocnění korelují s axiální spondyloartritidou a psoriatickou artritidou v dospělosti. Sekukinumab prokázal účinnost a bezpečnost v léčbě psoriatické artritidy, ankylozující spondylitidy a neradiografické axiální spondyloartritidy u dospělých pacientů. Studie JUNIPERA sledovala účinnost a bezpečnost sekukinumabu u pacientů s aktivní ERA a JPsA [1].
Metody
Do studie byli zařazeni pacienti ve věku 2-18 let s více než šestiměsíčním trváním aktivního onemocnění (ERA nebo JPsA) podle kritérií ILAR (International League Against Rheumatism). Dvouletá studie sestávala z otevřené fáze na počátku, kdy byl podáván sekukinumab subkutánně v dávce 75 mg nebo 150 mg v závislosti na hmotnosti pacienta (< 50 kg/≥ 50 kg). Ve stejném dávkování byl studijní lék aplikován v týdnech 1, 2, 3, 4, 8 a 12 v první léčebné periodě. Respondéři, kteří dosáhli alespoň odpovědi JIA ACR 30 (30% zlepšení podle kritérií American College of Rheumatology) ve 12. týdnu, byli randomizováni do dvojitě zaslepené druhé léčebné periody k podávání sekukinumabu nebo placeba každé čtyři týdny až do vzplanutí nemoci, nebo maximálně do týdne 100. Primárním cílovým ukazatelem byla doba do vzplanutí choroby ve druhé léčebné periodě. Klíčové sekundární cílové ukazatele zahrnovaly kritérium JIA ACR 30/50/70/90/100, neaktivní onemocnění, skóre aktivity JIA (Juvenile Arthritis Disease Activity Score, JADAS), entezitidu a počet aktivních kloubů, bezpečnost. Analýza doby do vzplanutí choroby ve druhé léčebné periodě zahrnovala podíl pacientů se vzplanutím, Kaplanův-Meierův odhad mediánu počtu dnů do vzplanutí, odhad poměru rizika (hazard ratio, HR) a stratifikovanou hodnotu p podle log rank testu. Pro intent to treat (ITT, podle původního léčebného záměru) analýzu byla užita imputace non respondérů a sledovací analýza byla provedena pro odpovědi JIA ACR 30/50/70/90/100 a pro neaktivní nemoc [1].
Výsledky
Do první léčebné periody bylo zahrnuto 86/97 (88,7 %) pacientů (s průměrným věkem 13,1 roku; 33,7 % žen; ERA: n = 52; JPsA: n = 34) s průměrným skóre JADAS 27 15,1 a počtem entezitid 2,6 na počátku sledování. Ve 12
. týdnu
75/83 (90,4 %) pacientů dosáhlo JIA ACR 30 a vstoupilo
do druhé léčebné periody. Během této fáze bylo
v placebové skupině zaznamenáno 21 vzplanutí nemoci
a v sekukinumabové skupině 10 vzplanutí. Bylo dosaženo
primárního cíle, u pacientů léčených sekukinumabem byla
v porovnání s placebem zachycena signifikantně delší
doba do vzplanutí choroby – riziko vzplanutí bylo
sníženo o 72 % (HR 0,28; 95% interval spolehlivosti
[confidence interval, CI] 0,13-0,63;
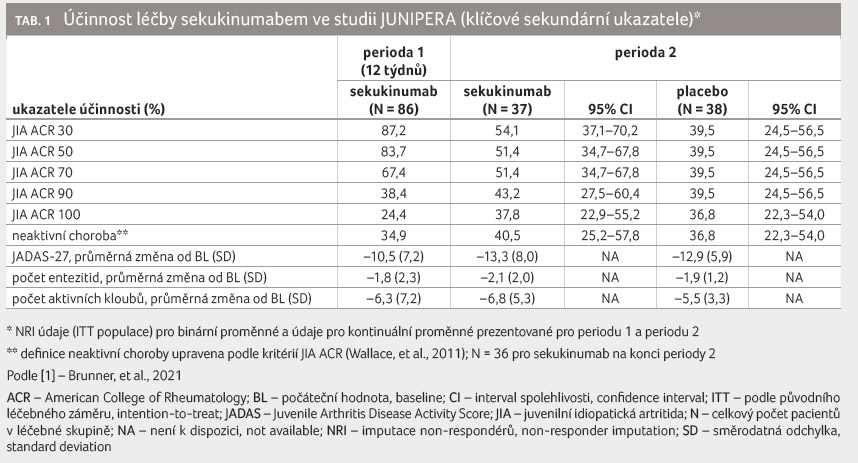
p < 0,001). Odpovědi JIA ACR, aktivitu nemoci,
počet entezitid a aktivních artritických kloubů shrnuje
tabulka 1. V první léčebné periodě byly mezi ITT
a sledovací analýzou zaznamenány pouze méně významné
rozdíly pro odpovědi JIA ACR a neaktivní chorobu. Zlepšení
ve skóre JADAS 27 bylo doloženo u obou onemocnění
(ERA i JPsA), graf 1. Počet nežádoucích účinků
(91,7 % vs. 92,1 %) a závažných nežádoucích účinků
(14,6 % vs. 10,5 %) byl srovnatelný pro sekukinumabovou
i placebovou skupinu po celou dobu sledování. Nebyly
zaznamenány žádné nové bezpečnostní signály u pacientů
léčených sekukinumabem (reakce v místě vpichu: n = 1;
celkem 141,5 pacientoroku) [1].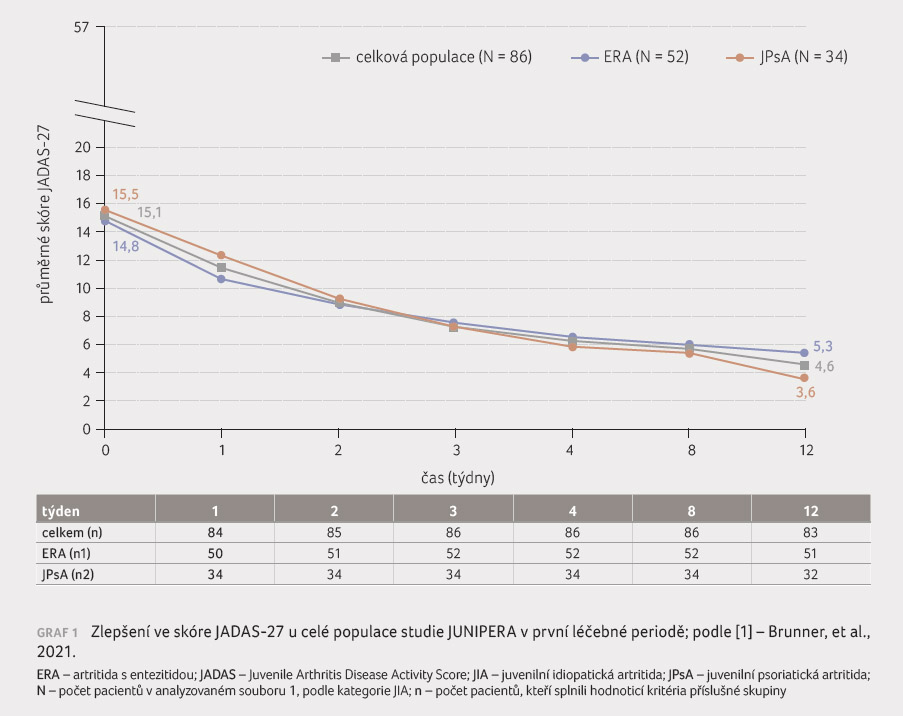
Závěr
U dětí a dospívajících pacientů trpících ERA a JPsA potvrdila studie JUNIPERA účinnost podávání sekukinumabu se signifikantně delší dobou do vzplanutí nemoci ve srovnání s placebem a se setrvalým zmírněním příznaků a symptomů až do týdne 104. Efektivnost léčby byla doložena jak u pacientů s ERA, tak u pacientů s JPsA, navíc s příznivým bezpečnostním profilem.
Redakčně zpracovala PhDr. Nikola
Homolová Richtrová
Komentář ke klinickému hodnocení JUNIPERA
Doc. MUDr. Mária Filková, Ph.D.
Revmatologický ústav; Klinika revmatologie 1. LF UK, Praha
Začátek milénia byl spojen s revolucí v léčbě zánětlivých revmatických onemocnění. Zatímco po uvedení převratné léčby inhibitory tumor nekrotizujícího faktoru alfa (TNFα) se paleta biologických léků a nyní i cílených syntetických chorobu modifikujících léků u dospělých pacientů rychle rozšiřuje, terapeutické možnosti u pacientů s juvenilní idiopatickou artritidou (JIA) jsou limitovanější.
Sekukinumab jako humánní monoklonální protilátka proti interleukinu 17 (IL 17) má stabilní postavení v léčbě dospělých pacientů s ankylozující spondylitidou, neradiografickou spondyloartritidou, psoriatickou artritidou a psoriázou, v pediatrické populaci je schválen pro léčbu psoriázy. Jeho účinnost u zánětlivých revmatických nemocí byla potvrzena v řadě klinických hodnocení u dospělých pacientů, kde ovlivňuje aktivitu axiálního postižení a periferní artritidy včetně inhibice radiografické progrese, vede k vymizení daktylitid a entezitid a psoriatického postižení kůže a nehtů. U léku nebyl prokázán efekt na uveitidu a idiopatický střevní zánět. Sekukinumab se setrvalým efektem zlepšuje kvalitu života, tělesné funkce a zpomaluje progresi choroby. První klinická studie hodnotící účinnost a bezpečnost léčby sekukinumabem u pacientů s JIA, a to konkrétně formy s artritidou a entezitidou (ERA) a psoriatickou artritidou (JPsA), prokázala v otevřené fázi po 12 týdnech léčby pokles počtu oteklých kloubů a oblastí s entezitidou, pokles klinické aktivity dle kritérií JIA ACR 30 (30% zlepšení podle American College of Rheumatology) v téměř 90 % a nárůst inaktivního onemocnění v téměř 35 %. V navazující zaslepené fázi bylo u pacientů léčených sekukinumabem dosaženo signifikantního oddálení relapsu nemoci s nižším rizikem jejího vzplanutí až o 72 %.
Jak nemocní s ERA, tak s JPsA tvoří přibližně 3–10 % všech pacientů s JIA. ERA se na rozdíl od spondyloartritidy dospělých projevuje zejména postižením periferních kloubů a entezitidou, postižení axiálního skeletu se projevuje spíše později. Každopádně neléčené axiální postižení vede k progresi do ankylozující spondylitidy, významný rizikový faktor progrese představují i pozitivita lidského leukocytárního antigenu B27 (HLA B27) a koxitida. Ukazuje se, že při předání pacienta s ERA do péče revmatologa pro dospělé přibližně 78 % nemocných s ERA splňuje klasifikační kritéria ASAS (Assessment of SpondyloArthritis International Society) pro periferní nebo axiální spondyloartritidu [1-4]. U pacientů s JPsA nemusí být v době manifestace přítomno postižení kůže psoriázou a začátek v adolescenci bývá často spojen se sakroiliitidou. Až 100 % pacientů s JPsA zároveň splňuje i klasifikační kritéria pro psoriatickou artritidu dospělých [1,5].
Jednotlivé zánětlivé cytokiny
(TNFα, IL 17, IL 1 a jiné) mají odlišnou roli
v patogenezi jednotlivých forem JIA. Pokud vycházíme
z klinických hodnocení a zkušeností z běžné
praxe u dospělých pacientů, lze očekávat, že sekukinumab
bude účinný i na projevy spojené s klinickou
manifestací ERA a JPsA. Klinické hodnocení JUNIPERA je první
vlaštovkou a inhibice IL 17 prostřednictvím sekukinumabu
jistě představuje slibnou účinnou léčbu a rozšíření
terapeutických možností v indikaci těchto vybraných forem
JIA.
Literatura
[
1] Debrach AC, Rougelot A, Beaumel A, et al. Comparison of paediatric and adult classification criteria in juvenile idiopathic arthritis during the transition from paediatric to adult care. Joint Bone Spine 2021; 88: 105047.[2] Rudwaleit M, van der Heijde D, Landewé R, et al. The development of Assessment of Spondyloarthritis International Society classification criteria for axial spondyloarthritis (part I): classification of paper patients by expert opinion including uncertainty appraisal. Ann Rheum Dis 2009; 68: 770−776.[3] Rudwaleit M, van der Heijde D, Landewé R, et al. The development of Assessment of Spondyloarthritis International Society classification criteria for axial spondyloarthritis (part II): validation and final selection. Ann Rheum Dis 2009; 68: 777−783.[4] Rudwaleit M, van der Heijde D, Landewé R, et al. The Assessment of SpondyloArthritis International Society classification criteria for peripheral spondyloarthritis and for spondyloarthritis in general. Ann Rheum Dis 2011; 70: 25−31.[5] Taylor W, Gladman D, Helliwell P, et al. Classification criteria for psoriatic arthritis: development of new criteria from a large international study. Arthritis Rheum 2006; 54: 2665−2673.
Seznam použité literatury
- [1] Brunner H, Foeldvari I, Alexeeva E, et al. Secukinumab Treatment in Children and Adolescents with Enthesitis‑related Arthritis and Juvenile Psoriatic Arthritis: Efficacy and Safety Results from a Phase 3 Study. Arthritis & Rheumatology 2021; 73(Suppl 9): 1–509; doi:10.1002/art.41966; Abstract Number 1424.