Nejnovější molekulární terapeutické cíle v revmatologii – data z kongresu American College of Rheumatology
Souhrn
Navrátilová A, Šenolt L. Nejnovější molekulární terapeutické cíle v revmatologii – data z kongresu American College of Rheumatology. Remedia 2025; 35: 6–12.
Nejnovější vývoj terapeutických cílů v revmatologii představuje průlom ve způsobu léčby různých autoimunitních a zánětlivých onemocnění, přičemž rok 2024 přinesl zásadní novinky v tomto oboru. Na kongresu American College of Rheumatology v listopadu minulého roku byly prezentovány studie, které odhalily významné pokroky v inhibici signálních drah zánětu a v rozvoji personalizované imunoterapie, jež může zásadně změnit přístup k léčbě. Významným pokrokem je modulace B buněčné komunikace pomocí nově vyvinutých inhibitorů, které umožňují cílenější a účinnější zásah do imunitních procesů. Dále byly představeny inovativní přístupy k léčbě bolesti, které využívají nové poznatky o neurologických aspektech zánětlivých onemocnění. Kromě toho pokročilé strategie využívající CAR‑T a CAR‑NK buňky pro cílenou imunoterapii nabízejí naději pro pacienty s refrakterními formami onemocnění, kde tradiční metody selhávají. Tyto inovace otevírají cestu k efektivnější a bezpečnější léčbě, která je přizpůsobena individuálním potřebám nemocných, a představují významný krok vpřed ve zlepšení kvality života pacientů trpících revmatickými onemocněními.
Klíčová slova: CAR terapie – management bolesti – personalizovaná imunoterapie.
Summary
Navratilova A, Senolt L. The newest molecular therapeutic targets for rheumatology – data from the American College of Rheumatology congress. Remedia 2025; 35: 6–12.
The latest developments in therapeutic targets for rheumatology represent a breakthrough in the treatment of various autoimmune and inflammatory diseases, with significant new insights emerging in 2024. Studies presented at the American College of Rheumatology congress revealed advances in the inhibition of inflammatory signaling pathways and the development of personalized immunotherapy, which could transform treatment approaches. A notable advancement is the modulation of B cell communication through newly developed inhibitors, which allow targeted and effective intervention in immune processes. Innovative approaches to pain treatment that utilize knowledge about the neurological aspects of inflammatory diseases were introduced. Furthermore, advanced strategies using CAR‑T and CAR‑NK cells for targeted immunotherapy offer hope for patients with refractory disease forms where standard of care medication fails. These innovations pave the way for more effective and safer treatments tailored to the individual needs of patients and represent a significant step forward in improving the quality of life for patients suffering from rheumatic diseases.
Key words: CAR therapy – pain management – personalized immunotherapy.
Úvod
Nové molekulární cíle jsou zásadní pro rozvoj inovativních terapií, které rozšiřují možnosti léčby pro široké spektrum pacientů napříč medicínskými obory. Klíčové aspekty moderní léčby zahrnují především vývoj léčiv s menšími nežádoucími účinky, zvýšení léčebné specificity, personalizaci terapie a otevírání nových možností pro pacienty trpící rezistentními formami nemocí. Tento souhrn představuje poznatky o nejnovějších a klinicky nejslibnějších terapeutických cílech v revmatologii za rok 2024 a vychází z výběru z konferenčních příspěvků kongresu American College of Rheumatology and Association of Rheumatology Professionals Convergence (ACR/ARP), který se konal ve dnech 14.–19. listopadu 2024 ve Washingtonu.
Inovativní přístup k modulaci imunitní odpovědi
Výzkum týmu Martina a kol. přinesl nové terapeutické možnosti inhibice molekulárních signalizačních drah zánětu [1]. Tento tým objevil a popsal cílený inhibitor TANK vazebné kinázy 1 (TANK‑binding kinase‑1, TBK1), která je řazena do skupiny serin/threonin‑protein kináz. TBK1 hraje klíčovou roli v mnoha signálních drahách a v závislosti na vazbě na různé adaptorové proteiny ovlivňuje buněčné procesy, jako jsou buněčný cyklus, apoptóza a antivirová obrana spojená s autofagií (obr. 1) [2]. V kontextu revmatických chorob je významná její úloha v regulaci transkripčních faktorů interferonové signalizace typu I (IFN I) a nukleárního faktoru kappa B (NFκB), jejichž aktivace je spojována s onemocněními, jako jsou systémový lupus erythematodes (SLE) [3], systémová sklerodermie (SSc) [4] nebo Sjögrenův syndrom [5].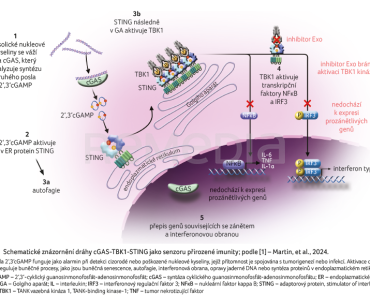
Martin a kol. vyvinuli molekulu, která selektivně inhibuje patologickou zánětlivou kaskádu TBK1, ale zároveň zachovává schopnost buněčné antivirové obrany a autofagie [1]. Unikátnost této molekuly spočívá ve vazebném místě TBK1 pro adaptorový protein STING (stimulator of interferon genes), které se nachází mimo aktivní doménu v tzv. exosite. Pomocí in vitro experimentů s imortalizovanými liniemi lidských a myších makrofágů autoři definovali toto „Exo“ místo a demonstrovali účinnost jeho blokace ve snižování fosforylace TBK1 a STING, a následně i transkripčních faktorů NFκB a interferonového regulačního faktoru 3 (IRF3). Navazující in vivo studie ukázaly, že podání inhibitoru Exo vedlo k poklesu fosforylace těchto elementů u myší s nadměrnou aktivitou STING. Testování na lidských buňkách přineslo slibné předběžné výsledky ve snížení prozánětlivé odpovědi u mononukleárních buněk izolovaných z periferní krve pacientů se SLE a na fibroblastech jedinců se SSc a zdravých kontrol autoři demonstrovali snížení aktivity profibrotických drah. U myší nesoucích v genu pro exonukleázu TREX1 (three prime repair exonuclease 1) mutaci, při níž dojde k narušení schopnosti štěpení a k hromadění buněčné jednovláknové DNA (podobně jako při virové nákaze) s následnou aktivací IRF elementů, vedla aplikace inhibitoru Exo ke zmírnění závažnosti zánětu [1]. Na základě uvedených výsledků se tato řada inhibitorů nabízí pro využití v léčbě interferonopatií, např. SLE.
Na vývoji dalšího perspektivního přípravku se podílelo 13 center z pěti zemí. Autoři vedení Clowsem a kol. se zaměřili na modulaci signalizační dráhy CD40‑CD40L [6]. CD40 je receptor skupiny tumor nekrotizujícího faktoru (TNF) lokalizovaný primárně na povrchu antigen prezentujících buněk (antigen‑presenting cells, APC) a z jejich řad je u SLE cíleno hlavně na B lymfocyty, které jsou deregulovány [7]. Interakce CD40 s jeho ligandem CD40L na aktivovaných Th lymfocytech je zásadní pro plnou funkci B buněk [8], a proto přerušení této komunikace mezi T a B lymfocyty představuje klíčový terapeutický cíl pro onemocnění spojená se zvýšenou aktivitou B lymfocytů. Dapirolizumab pegol (DZP) byl navržen jako modifikovaný Fab fragment monoklonální protilátky určený k inhibici signalizace CD40L. Proces PEGylace připojuje polyetylenglykolovou (PEG) skupinu a „nahrazuje“ Fc fragment protilátky. Tato modifikace odstraňuje imunogenní vlastnosti spojené s reaktivitou Fc a zároveň udržuje vysokou molekulovou hmotnost, což je klíčové pro stabilitu a délku setrvání léčiva v oběhu [9].
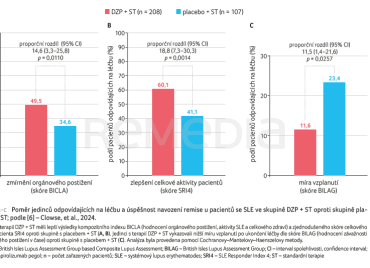 Autoři představili výsledky třetí fáze klinického testování, které sledovalo efektivitu a bezpečnost léčiva u 315 pacientů s aktivním SLE během 48 týdnů [6]. Pacienti ve věku 16 let a více s mírnou až těžkou aktivitou SLE (definováno perzistujícím zánětem nebo rekurentními atakami) navzdory standardní terapii (ST) byli náhodně rozděleni v poměru 2 : 1 do skupin s kombinací ST + DZP nebo ST + placebo. DZP byl podáván intravenózně v dávce 24 mg/kg každé čtyři týdny. Primárním měřítkem úspěšnosti byla efektivita léčby na základě indexu BICLA (British Isles Lupus Assessment Group based Composite Lupus Assessment), kde skupina s DZP vykazovala lepší skóre zmírnění orgánového poškození a aktivity oproti placebu (49,5 % vs. 34,6 %), graf 1A. Sekundární výstupy zahrnovaly zmírnění symptomů u pacientů s DZP (60,1 % vs. 41,1 %) dle zjednodušeného kompozitního indexu SRI4 (SLE Responder Index 4) a nižší míru vzplanutí po ukončení léčby (11,6 % vs. 23,4 %) dle kompozitního indexu BILAG (British Isles Lupus Assessment Group Index), který sleduje aktivitu SLE v čase (graf 1B, C).
Autoři představili výsledky třetí fáze klinického testování, které sledovalo efektivitu a bezpečnost léčiva u 315 pacientů s aktivním SLE během 48 týdnů [6]. Pacienti ve věku 16 let a více s mírnou až těžkou aktivitou SLE (definováno perzistujícím zánětem nebo rekurentními atakami) navzdory standardní terapii (ST) byli náhodně rozděleni v poměru 2 : 1 do skupin s kombinací ST + DZP nebo ST + placebo. DZP byl podáván intravenózně v dávce 24 mg/kg každé čtyři týdny. Primárním měřítkem úspěšnosti byla efektivita léčby na základě indexu BICLA (British Isles Lupus Assessment Group based Composite Lupus Assessment), kde skupina s DZP vykazovala lepší skóre zmírnění orgánového poškození a aktivity oproti placebu (49,5 % vs. 34,6 %), graf 1A. Sekundární výstupy zahrnovaly zmírnění symptomů u pacientů s DZP (60,1 % vs. 41,1 %) dle zjednodušeného kompozitního indexu SRI4 (SLE Responder Index 4) a nižší míru vzplanutí po ukončení léčby (11,6 % vs. 23,4 %) dle kompozitního indexu BILAG (British Isles Lupus Assessment Group Index), který sleduje aktivitu SLE v čase (graf 1B, C).
Co se týče bezpečnosti, ve skupině s DZP oproti placebu bylo zaznamenáno více nežádoucích účinků (82,6 % vs. 75 %), avšak s menší závažností (9,9 % vs. 14,8 %). Oportunní infekce byly pozorovány u obou skupin s lehčí převahou u DZP (2,8 % vs. 0,9 %). Byl zaznamenán jeden případ tromboembolické události a jedno úmrtí u predisponovaných jedinců při terapii DZP [6].
Vývoj léčiv inhibujících signalizaci CD40L byl v minulosti často komplikován vážnými nežádoucími účinky, zejména trombotického typu, což je pravděpodobně spojeno s výskytem CD40L nejen na T lymfocytech, ale i na aktivovaných trombocytech [10,11]. V současnosti probíhají klinické studie pro schválení léčiv tohoto typu pro léčbu B lymfopatií nebo v prevenci odhojování transplantátů, například s léky jako iskalimab a bleselumab [12–14]. Závažné komplikace vedou u léčiv k posunu vývojových strategií, kde by PEGylace mohla přinést možnosti snížení míry imunogenity a nežádoucích účinků u pacientů na biologické léčbě [15].
Terapeutické strategie zaměřené na bolest a zánět
Terapeutické strategie zaměřené na bolest a zánět jsou klíčové pro zvládání revmatických nemocí, které výrazně ovlivňují kvalitu života postižených. Efektivní léčba bolesti je zásadní pro zachování nezávislosti a fyzické kondice pacientů.
Bolest je hlavním problémem u osteoartrózy (OA), která postihuje přibližně 7,6 % populace, s vyšší prevalencí u žen ve věku vyšším než 60 let [16]. Vzhledem k omezeným možnostem léčby OA, která zůstává výzvou pro současný výzkum, se terapie obvykle zaměřuje na zmírnění symptomů. Standardní přístup zahrnuje podávání analgetik a antiflogistik nebo lokálních glukokortikoidů spolu s podpůrnou suplementací [17]. Současný výzkum je proto cílen na inovativní přístupy v léčbě OA, což je reflektováno v nejnovějších vědeckých publikacích.
Léčbě bolesti u OA byla věnována pozornost ve studii zaměřené na nový inhibiční cíl modulující neurologický původ bolesti [18]. Studie se zabývala molekulou patřící do skupiny neurotrofinů, které jsou diferenciačními a růstovými faktory pro neurony a jejich nadbytek je spojován s řadou bolestivých syndromů [19]. Struktura inhibitoru neurotrofinu‑3 (LEVI‑04) vychází z fúzního proteinu, který funguje jako tzv. decoy molekula, tzn. váže a neutralizuje nadbytečné množství neurotrofinu‑3 z oběhu a inhibuje tak jeho signalizační dráhu [18].
Dvacetitýdenní multicentrická klinická studie fáze II ukazuje slibné výsledky v léčbě bolesti u pacientů s OA kolenního kloubu. Studie zahrnovala 518 účastníků s OA kolene, přičemž ke vstupním kritériím patřily skóre bolestivosti dle WOMAC (Western Ontario and McMaster Universities Osteoarthritis Index) ≥ 4/10 a radiografické postižení dle Kellgrena–Lawrence ≥ 2. Pacienti byli randomizováni do dvou skupin s podáváním LEVI‑04 nebo placeba. Léčiva byla podávána intravenózně každé čtyři týdny (LEVI‑04 v dávkách 0,3–2 mg/kg) do 16. týdne, s následným monitorováním bezpečnosti do 30. týdne. Primárním cílovým ukazatelem studie bylo zmírnění bolestivosti dle indexu WOMAC (≥ 7). Více než 50 % jedinců skupiny s LEVI‑04 uvádělo snížení bolestivosti o 50 % již v pátém týdnu a 25 % respondentů zaznamenalo pokles bolestivosti až o 75 % v 17. týdnu, a to napříč všemi testovanými koncentracemi. Z hlediska bezpečnosti byl inhibitor neurotrofinu-3 dobře tolerován a nebyl zaznamenán vyšší podíl nežádoucích účinků nebo progrese nemoci ve srovnání s placebem [18]. V minulosti byly testovány inhibitory na podobné bázi, avšak jejich použití bylo spojeno s významnými kloubními patologiemi [20]. LEVI‑04 se proto jeví jako slibné léčivo ve své kategorii aktuálně studované při léčbě OA, které je zaměřeno na zlepšení kvality života a funkční schopnosti pacientů.
Zatímco tato studie přistupovala k léčbě OA na úrovni molekulární komunikace buněk, další zajímavá studie autorů Yadav a kol. z Oklahomy zvolila odlišný terapeutický přístup prostřednictvím modulace parasympatické dráhy nervus vagus (NVS) [21]. Bolestivé a zánětlivé signály z periferních tkání jsou přenášeny do mozku, kde mohou ovlivnit eferentní vagální odpověď, čehož se již využívá v některých terapiích, například při léčbě migrény, chronické bolesti nebo deprese [22]. V této studii autoři zkoumali účinek stimulace NVS na bolest, zánět a progresi OA u dvou experimentálních myších modelů [21]. V prvním modelu byla hodnocena progrese OA po narušení mediálního menisku u 20 samic myší kmene Black6. Čtyři týdny po chirurgickém zákroku byla zahájena osmitýdenní NVS léčba nebo simulovaná léčba „sham“ pro zhodnocení placebo efektu. Léčba byla aplikována pět dní v týdnu po dobu 10 minut. Bolestivost byla hodnocena pomocí algometrického měření tlakového stimulu nebo zátěžového testu, přičemž data byla sbírána před zahájením NVS a následně ve 4. a 8. týdnu studie.
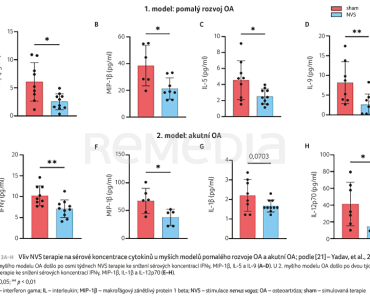
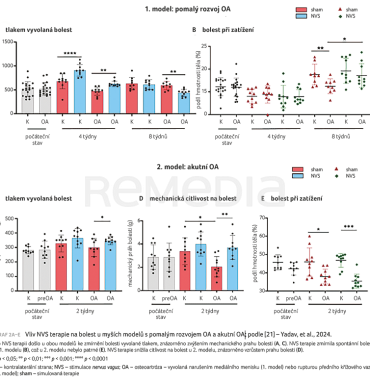 Druhý model simuloval akutní OA, která byla navozena rupturou předního křížového vazu pomocí komprese holenní kosti u 20 samic Black6. Léčba NVS nebo sham byla zahájena den po zákroku a trvala dva týdny. Citlivost (alodynie) byla hodnocena metodou Von Freyových filament, která umožňuje kvantifikovat úroveň citlivosti na mechanické podněty, a hyperalgezie byla měřena při zátěži. Výsledky ukazují, že u prvního modelu pomalého rozvoje OA došlo ke zmírnění tlakem evokované bolesti u skupiny léčené NVS již po čtvrtém týdnu a u zátěžové bolesti v osmém týdnu u NVS oproti sham (graf 2A, B). Sérová analýza navíc ukázala, že u myší léčených NVS došlo k významnému snížení koncentrací interferonu gama (IFNγ), makrofágového zánětlivého proteinu 1 beta (MIP‑1β), které podporují chronický zánět a tkáňové poškození [23,24], a interleukinů 5 a 9 (IL‑5, IL‑9) asociovaných s humorální složkou imunity (graf 3A–D) [25]. Oproti tomu u druhého modelu rychlé progrese OA vedla NVS léčba ke zlepšení skóre alodynie i hyperalgezie (graf 2C–E). Navíc bylo pozorováno zlepšení rentgenového nálezu kloubů hodnoceného dle skóre závažnosti OA OARSI (Osteoarthritis Research Society International). Sérová analýza v tomto modelu odhalila snížení koncentrací IFNγ a MIP‑1β, podobně jako v prvním modelu, spolu s poklesem hodnot IL‑12p70 a IL‑1β, které hrají roli u akutního zánětu (graf 3E–H). Dohromady tato předběžná data na obou myších modelech ukazují, že terapie zaměřená na nervovou modulaci může přinést úlevu od bolesti doprovázenou redukcí zánětu [21].
Druhý model simuloval akutní OA, která byla navozena rupturou předního křížového vazu pomocí komprese holenní kosti u 20 samic Black6. Léčba NVS nebo sham byla zahájena den po zákroku a trvala dva týdny. Citlivost (alodynie) byla hodnocena metodou Von Freyových filament, která umožňuje kvantifikovat úroveň citlivosti na mechanické podněty, a hyperalgezie byla měřena při zátěži. Výsledky ukazují, že u prvního modelu pomalého rozvoje OA došlo ke zmírnění tlakem evokované bolesti u skupiny léčené NVS již po čtvrtém týdnu a u zátěžové bolesti v osmém týdnu u NVS oproti sham (graf 2A, B). Sérová analýza navíc ukázala, že u myší léčených NVS došlo k významnému snížení koncentrací interferonu gama (IFNγ), makrofágového zánětlivého proteinu 1 beta (MIP‑1β), které podporují chronický zánět a tkáňové poškození [23,24], a interleukinů 5 a 9 (IL‑5, IL‑9) asociovaných s humorální složkou imunity (graf 3A–D) [25]. Oproti tomu u druhého modelu rychlé progrese OA vedla NVS léčba ke zlepšení skóre alodynie i hyperalgezie (graf 2C–E). Navíc bylo pozorováno zlepšení rentgenového nálezu kloubů hodnoceného dle skóre závažnosti OA OARSI (Osteoarthritis Research Society International). Sérová analýza v tomto modelu odhalila snížení koncentrací IFNγ a MIP‑1β, podobně jako v prvním modelu, spolu s poklesem hodnot IL‑12p70 a IL‑1β, které hrají roli u akutního zánětu (graf 3E–H). Dohromady tato předběžná data na obou myších modelech ukazují, že terapie zaměřená na nervovou modulaci může přinést úlevu od bolesti doprovázenou redukcí zánětu [21].
CAR‑T a CAR‑NK buněčná terapie
 Jedním z aktuálních „hot topics“ v revmatologii je léčba pomocí T buněk s chimérickým antigenním receptorem (CAR), tzv. CAR‑T terapie. Tato metoda zahrnuje genetickou úpravu autologních nebo alogenních T lymfocytů, do nichž je ex vivo vložen gen pro CAR. Upravené T buňky jsou následně namnoženy a po lymfodepleční terapii podány zpět pacientovi [26]. T lymfocyty vybavené CAR dokáží cíleně rozpoznat a zlikvidovat buňky nesoucí specifické struktury, proti nimž byl receptor navržen [26]. Zároveň tato léčba umožňuje aktivaci dalších imunitních buněk, které se podílejí na likvidaci cílových buněk [26]. Termín „chimérický“ odráží kombinaci dvou funkcí: rozpoznání cílových buněk („najdi“) a jejich eliminaci („zneškodni“). CAR‑T terapie je již déle využívána v onkologii, kde pomáhá imunitnímu systému ničit transformované buňky [27]. Díky rychlému rozvoji sahá její potenciál i do jiných oblastí, včetně léčby autoimunitních onemocnění [28]. Ačkoliv CAR‑T terapie vykazuje u části pacientů vysokou účinnost, u jiných přínosná není, a navíc je spojena s rizikem výskytu závažných nežádoucích účinků, jako jsou infekce, syndrom uvolnění cytokinů nebo neurotoxicita [29].
Jedním z aktuálních „hot topics“ v revmatologii je léčba pomocí T buněk s chimérickým antigenním receptorem (CAR), tzv. CAR‑T terapie. Tato metoda zahrnuje genetickou úpravu autologních nebo alogenních T lymfocytů, do nichž je ex vivo vložen gen pro CAR. Upravené T buňky jsou následně namnoženy a po lymfodepleční terapii podány zpět pacientovi [26]. T lymfocyty vybavené CAR dokáží cíleně rozpoznat a zlikvidovat buňky nesoucí specifické struktury, proti nimž byl receptor navržen [26]. Zároveň tato léčba umožňuje aktivaci dalších imunitních buněk, které se podílejí na likvidaci cílových buněk [26]. Termín „chimérický“ odráží kombinaci dvou funkcí: rozpoznání cílových buněk („najdi“) a jejich eliminaci („zneškodni“). CAR‑T terapie je již déle využívána v onkologii, kde pomáhá imunitnímu systému ničit transformované buňky [27]. Díky rychlému rozvoji sahá její potenciál i do jiných oblastí, včetně léčby autoimunitních onemocnění [28]. Ačkoliv CAR‑T terapie vykazuje u části pacientů vysokou účinnost, u jiných přínosná není, a navíc je spojena s rizikem výskytu závažných nežádoucích účinků, jako jsou infekce, syndrom uvolnění cytokinů nebo neurotoxicita [29].
Po vzoru CAR‑T terapie byla vyvinuta i CAR‑NK (natural killer) buněčná terapie, která má oproti CAR‑T výhodu nižšího rizika vzniku syndromu z uvolnění cytokinů a neurotoxicity [30]. NK buňky setrvávají v těle kratší dobu, což snižuje riziko dlouhodobých nežádoucích účinků a zároveň umožňuje alogenní dárcovství, a zvyšuje tedy dostupnost terapie [30]. Jedním z autoimunitních onemocnění, kde se testuje CAR‑T terapie pro depleci B lymfocytů, je SLE [31]. Vzhledem k výše zmíněným nežádoucím účinkům CAR‑T terapie byla navržena CAR‑NK terapie cílící na intenzivní depleci B buněk [32]. Tato nezaslepená pilotní studie bez kontrolní skupiny zahrnovala 20 pacientů s těžkou aktivní nebo refrakterní formou SLE s mediánem trvání 10 let, kteří byli léčeni alogenními CD19 CAR‑NK buňkami [32]. Pacientům byla před léčbou podána premedikace cyklofosfamidem a fludarabinem, následně byly buňky podány intravenózně ve třech dávkách. Jeden pacient obdržel 1 dávku (D), jeden pacient 2 D, pět pacientů 3 D a 13 pacientů 4 D. Pacienti byli poté sledováni (medián pět měsíců), přičemž u nich byla pozorována deplece s následným obnovením B lymfocytů po 2–3 měsících. Ani tato léčba se nevyhnula nežádoucím účinkům v podobě syndromu z uvolnění cytokinů, avšak pouze v mírné podobě u dvou pacientů (stupeň 1, krátce trvající horečka). Výsledky naznačují, že osm pacientů vykazovalo zlepšení v horizontu šesti měsíců; čtyři dosáhli remise dle indexu 2021 DORIS (Definition Of Remission In SLE) a u šesti pacientů došlo ke snížení aktivity onemocnění podle LLDAS (Lupus Low Disease Activity State) [32].
Slibné výsledky CAR‑T terapie u SLE inspirovaly tým čínských autorů Mei a kol., kteří využili T lymfocyty k depleci B buněk prostřednictvím bispecifické molekuly, jež spojuje povrchové molekuly CD3 a CD19 [33]. Tento typ molekuly je označován jako T cell engager (TCE). Molekula A‑319 je příkladem takového TCE. Studie zahrnovala šest pacientů se střední až těžkou aktivitou SLE hodnocenou pomocí skóre SLEDAI‑2K (Systemic Lupus Erythematosus Disease Activity Index 2000, hodnoty 8–16) nebo pacientů s refrakterní formou SLE, přičemž medián trvání onemocnění byl 7,5 roku. V prvním týdnu byl intravenózně podán A‑319 v den 1, 3 a 5 v dávce 0,05 µg/kg za 24 hodin. V druhém týdnu byl přípravek podán v den 1, 3 a 5 v navýšeném režimu 0,3 µg/kg za šest hodin. Následně byli pacienti sledováni po dobu 12 měsíců. Efektivita léčby byla individuálně hodnocena u pacientů P1–P3. Pacient P1 trpěl těžkým SLE s lupusovou nefritidou a překryvným syndromem SSc, pacient P2 měl SLE s překryvným syndromem revmatoidní artritidy a pacient P3 měl SLE s lupusovou nefritidou. U všech pacientů došlo k depleci B lymfocytů během jednoho týdne od zahájení léčby. U pacienta P1 došlo k obnovení počtu B lymfocytů mezi týdny 2 a 4. U tohoto nemocného se rovněž snížily koncentrace autoprotilátek (ANA, anti‑dsDNA, Sm, SSA, ribozomální protein P, chromatin, Scl‑70, RNP68) a normalizovaly se hodnoty komplementu (C3, C4). U pacientů P1–P3 došlo k poklesu aktivity SLE (SLEDAI‑2K) o 67–100 % v období mezi týdny 2 a 8, přičemž u P2 došlo ke snížení aktivity kloubního indexu DAS28‑CRP (Disease Activity Score 28 using C‑reactive protein) o 67 % během dvou týdnů. U P3 došlo ke zmírnění SLE vaskulitidy již po dvou týdnech. Všichni pacienti (P1–P6) měli horečku vyvolanou léky (stupeň I–II), ale nebyly pozorovány syndrom z uvolnění cytokinů, neurotoxicita, myelotoxicita ani infekční komplikace [33].
Závěr
V souhrnu lze z kongresu ACR/ARP v roce 2024 vyčíst několik významných trendů, které se soustředí na cílení a personalizaci léčby. Kromě otevření nových možností v oblasti CAR terapie a vývoje pokročilých biologických léčiv je patrný i posun při léčbě bolesti. Dalším významným směrem je rozvoj telemedicíny a vzdáleného monitorování prostřednictvím digitálních platforem, které se v jiných oborech již osvědčily [34,35]. Zajímavým tématem se rovněž stává personalizace léčby na základě prediktivního potenciálu využívajícího genetické a epigenetické markery [36]. I když některé z těchto nových přístupů čelí výzvám v oblasti bezpečnosti, jejich vývoj pravděpodobně nastaví směr pro optimalizaci léčby v nadcházejících letech. Tyto inovace mají potenciál přinést personalizované léčebné strategie, které mohou efektivněji cílit na individuální potřeby pacientů.
Mgr. Adéla Navrátilová
Revmatologický ústav
Na Slupi 450/4, 128 00 Praha 2
e-mail: navratilova@revma.cz
Literatura
[1] Martin M, Wilker E, Gikunju D, et al. Targeted exosite inhibition of STING activation of TBK1 selectively blocks type I interferon and NFkB responses for treatment of autoimmune diseases. ACR Convergence 2024, November 14–19, Washington, USA. Abstrakt L01. Dostupné na: https://acrabstracts.org/abstract/targeted‑exosite‑inhibition‑of‑sting‑activation‑of‑tbk1‑selectively‑blocks‑type‑i‑interferon‑and‑nf%ce%bab‑responses‑for‑treatment‑of‑autoimmune‑diseases/
[2] Hu L, Zhang Q. Mechanism of TBK1 activation in cancer cells. Cell Insight 2024; 3: 100197.
[3] Elkon KB, Stone VV. Type I interferon and systemic lupus erythematosus. J Interferon Cytokine Res 2011; 31: 803–812.
[4] Liu C, Tang J, Luo W, et al. DNA from macrophages induces fibrosis and vasculopathy through POLR3A/STING/type I interferon axis in systemic sclerosis. Rheumatology 2023; 62: 934–945.
[5] Hua F, Nass T Jr, Parvatiyar K. TRIM28 facilitates type I interferon activation by targeting TBK1. Front Immunol 2024; 15: 1279920.
[6] Clowse M, Isenberg D, Merrill J, et al. Dapirolizumab pegol demonstrated significant improvement in systemic lupus erythematosus disease activity: Safety results of a Phase 3 Trial. ACR Convergence 2024, November 14–19, Washington, USA. Abstrakt L16. Dostupné na: https://acrabstracts.org/abstract/
dapirolizumab‑pegol‑demonstrated‑significant‑improvement‑in‑systemic‑lupus‑erythematosus‑disease‑activity‑efficacy‑and‑safety‑results‑of‑a‑phase‑3‑trial/
[7] Stockfelt M, Teng YKO, Vital EM. Opportunities and limitations of B cell depletion approaches in SLE. Nat Rev Rheumatol 2025 Jan 15; doi: 10.1038/s41584‑024‑01210‑9. Epub ahead of print.
[8] Schonbeck U, Libby P. The CD40/CD154 receptor/ligand dyad. Cell Mol Life Sci 2001; 58: 4–43.
[9] Damodaran VB, Fee CJ. Protein PEGylation: An overview of chemistry and process considerations. Eur Pharmaceut Rev 2010; 15: 18–26.
[10] Michel NA, Zirlik A, Wolf D. CD40L and Its Receptors in Atherothrombosis – An Update. Front Cardiovasc Med 2017; 4; doi.org/10.3389/fcvm.2017.00040.
[11] Meyer T, Amirkhosravi A, Robson T, et al. Platelet Activation by a Humanized Monoclonal CD40 Ligand (CD40L) Antibody. Blood 2006; 108: 1516.
[12] Mariette X, Fisher B, Papas A, et al. OP0008 Safety and Efficacy of Iscalimab in Patients With Sjögrenʼs Disease: 48‑Week Results From a Randomised, Placebo‑Controlled, Phase 2B Dose‑Ranging Trial. Ann Rheum Dis 2024; 83: 124–125.
[13] de Graav GN, Udomkarnjananun S, Baan CC, et al. New Developments and Therapeutic Drug Monitoring Options in Costimulatory Blockade in Solid Organ Transplantation: A Systematic Critical Review. Ther Drug Monit 2025; 47: 64–76.
[14] Shoji J, Goggins WC, Wellen JR, et al. Efficacy and Safety of Bleselumab in Preventing the Recurrence of Primary Focal Segmental Glomerulosclerosis in Kidney Transplant Recipients: A Phase 2a, Randomized, Multicenter Study. Transplantation 2024; 108: 1782–1792.
[15] European Medicines Agency (2022). Cimzia: EPAR – Product Information. Dostupné na: https://www.ema.europa.eu/en/medicines/human/EPAR/cimzia [navštíveno 10. 9. 2025]
[16] Steinmetz JD, Culbreth GT, Haile LM, et al. Global, regional, and national burden of osteoarthritis, 1990–2020 and projections to 2050: a systematic analysis for the Global Burden of Disease Study 2021. Lancet Rheumatol 2023; 5: e508–e522.
[17] Šléglová O. Možnosti léčby bolesti u osteoartrózy. Vnitr Lek 2023; 69: 119–127.
[18] Conaghan P, Guermazi A, Katz N, et al. LEVI‑04, a Novel neurotrophin‑3 inhibitor, substantially improves pain and function without deleterious effects on joint structure in people with knee osteoarthritis: A randomized controlled Phase II Trial. ACR Convergence 2024, November 14–19, Washington, USA. Abstrakt L15. Dostupné na: https://acrabstracts.org/abstract/levi‑04‑a‑novel‑neurotrophin‑3‑inhibitor‑substantially‑improves‑pain‑and‑function‑without‑deleterious‑effects‑on‑joint‑structure‑in‑people‑with‑knee‑osteoarthritis‑a‑randomized‑controlled‑phase‑ii/
[19] Allen SJ, Dawbarn D. Clinical relevance of the neurotrophins and their receptors. Clin Sci (Lond) 2006; 110: 175–191.
[20] Dietz BW, Nakamura MC, Bell MT, et al. Targeting Nerve Growth Factor for Pain Management in Osteoarthritis‑Clinical Efficacy and Safety. Rheum Dis Clin North Am 2021; 47: 181–195.
[21] Yadav S, Griffin T, Jeffries M, et al. Vagus Nerve Stimulation: A Promising Approach to Alleviate Pain and Systemic Inflammation in Slow and Rapid Models of Osteoarthritis. ACR Convergence 2024, November 14–19, Washington, USA. Abstrakt 0025. Dostupné na: https://acrabstracts.org/abstract/vagus‑nerve‑stimulation‑a‑promising‑approach‑to‑alleviate‑pain‑and‑systemic‑inflammation‑in‑slow‑and‑rapid‑models‑of‑osteoarthritis/
[22] Johnson RL, Wilson CG. A review of vagus nerve stimulation as a therapeutic intervention. J Inflamm Res 2018; 11: 203–213.
[23] Bhavsar I, Miller CS, Al‑Sabbagh M. Macrophage Inflammatory Protein‑1 Alpha (MIP‑1 alpha)/CCL3: As a Biomarker. General Methods in Biomarker Research and their Applications 2015: 223–249; doi: 10.1007/978‑94‑007‑7696‑8_27
[24] Loucks A, Maerz T, Hankenson K, et al. The multifaceted role of mast cells in joint inflammation and arthritis. Osteoarthritis Cartilage 2023; 31: 567–575.
[25] Soussi‑Gounni A, Kontolemos M, Hamid Q. Role of IL‑9 in the pathophysiology of allergic diseases. J Allergy Clin Immunol 2001; 107: 575–582.
[26] Srivastava S, Riddell SR. Engineering CAR‑T cells: Design concepts. Trends Immunol 2015; 36: 494–502.
[27] Ibrahiam AT, Geddada S, Ullah N, et al. Chimeric Antigen Receptor (CAR) T‑cell Therapy in the Treatment of Diffuse Large B‑cell Lymphoma (DLBCL): A Systematic Review. Cureus 2024; 16: e75854.
[28] Berry CT, Frazee CS, Herman PJ, et al. Current advancements in cellular immunotherapy for autoimmune disease. Semin Immunopathol 2025; 47: 7.
[29] Norton J, Stiff P. CAR‑T therapy toxicities: the importance of macrophages in their development and possible targets for their management. Discov Oncol 2025; 16: 49.
[30] Xie G, Dong H, Liang Y, et al. CAR‑NK cells: A promising cellular immunotherapy for cancer. EBioMedicine 2020; 59: 102975.
[31] Guffroy A, Jacquel L, Guffroy B, et al. CAR‑T cells for treating systemic lupus erythematosus: A promising emerging therapy. Joint Bone Spine 2024; 91: 105702.
[32] Yu Y, Kong R, Xu X, et al. Allogenic CD19 CAR NK Cells Therapy in refractory systemic lupus erythematosus: An open‑label, Single arm, prospective and interventional clinical trial. ACR Convergence 2024, November 14–19, Washington, USA. Abstrakt L17. Dostupné na: https://acrabstracts.org/abstract/allogenic‑cd19‑car‑nk‑cells‑therapy‑in‑refractory‑systemic‑lupus‑erythematosus‑an‑open‑label‑single‑arm‑prospective‑and‑interventional‑clinical‑trial/
[33] Mei C, Guan X, Wu B, et al. A‑319, a CD3 x CD19 T Cell Engager (TCE), for the traetment of severe/refractory SLE: Early evidence of rapid reset of disease‑specific autoimmunity. ACR Convergence 2024, November 14–19, Washington, USA. Abstrakt L12. Dostupné na: https://acrabstracts.org/abstract/a‑319‑a‑cd3‑x‑cd19‑t‑cell‑engager‑tce‑for‑the‑treatment‑of‑severe‑refractory‑sle‑early‑evidence‑of‑rapid‑reset‑of‑disease‑specific‑autoimmunity/
[34] Blanchard M, Koller C, Maglione J, et al. Development of a Remote Patient Monitoring System Based on a Novel Digital Biomarker for Swelling in Rheumatoid Arthritis. ACR Convergence 2024, November 14–19, Washington, USA. Abstrakt 0867. Dostupné na: https://acrabstracts.org/abstract/development‑of‑a‑remote‑patient‑monitoring‑system‑based‑on‑a‑novel‑digital‑biomarker‑for‑swelling‑in‑rheumatoid‑arthritis/
[35] Malíčková K, Pešinová V, Bortlík M, et al. Telemedicína a idiopatické střevní záněty – výsledky pilotního projektu IBD Asistent. Gastroent Hepatol 2020; 74: 18–27.
[36] Miranda C, Hannebutt N, Dyson G, et al. The Development of Future Radiographic Knee Osteoarthritis Can Be Predicted by Peripheral Blood Epigenetic Models. ACR Convergence 2024, November 14–19, Washington, USA. Abstrakt 0863. Dostupné na: https://acrabstracts.org/abstract/the‑development‑of‑future‑radiographic‑knee‑osteoarthritis‑can‑be‑predicted‑by‑peripheral‑blood‑epigenetic‑models/