Subkutánní belimumab
Belimumab je lidská monoklonální protilátka IgG1λ, která blokuje vazbu solubilního aktivačního proteinu lidských B lymfocytů (BlyS) na jeho receptory. Prostřednictvím vazby BLyS inhibuje přežití B lymfocytů a snižuje jejich diferenciaci na plazmatické buňky produkující imunoglobuliny. Hladiny BLyS jsou u pacientů se systémovým lupus erythematodes (SLE) a dalšími autoimunitními onemocněními zvýšené, existuje rovněž souvislost mezi plazmatickými koncentracemi BLyS a aktivitou SLE [1].
Belimumab (Benlysta) byl dosud dostupný k intravenóznímu (i.v.) podání v infuzi. Nově bude pro pacienty v ČR dostupný a hrazený také v předplněném peru k subkutánnímu (s.c.) podání. Subkutánní forma podání zvyšuje dostupnost i komfort léčby, je přínosem pro pacienty i zdravotníky; vedle zlepšení kvality života pacientů a flexibility terapie zkracuje čas potřebný pro aplikaci léčiva i snižuje celkové náklady na léčbu. Přípravek je určen jako přídatná léčba u dospělých pacientů s aktivním SLE s pozitivními autoprotilátkami, s vysokým stupněm aktivity onemocnění navzdory standardní léčbě. Dále je v kombinaci se základní imunosupresivní léčbou indikován k léčbě dospělých pacientů s aktivní lupusovou nefritidou. Intravenózní forma má v případě aktivního SLE navíc indikaci pro podání u dětí ve věku od 5 let.
Zkušenosti z klinického hodnocení
Posoudit účinnost a bezpečnost s.c. belimumabu si dala za cíl 52týdenní randomizovaná, dvojitě zaslepená, placebem kontrolovaná studie fáze III (NCT01484496), která probíhala ve 30 zemích světa [2]. Do klinického hodnocení mohli být zařazeni dospělí pacienti se středně těžkým až těžkým SLE, s aktivním onemocněním definovaným hodnotou skóre SELENA‑SLEDAI (Safety of Estrogens in Lupus Erythematosus National Assessment‑SLE Disease Activity Index) ≥ 8 a s pozitivitou výsledků testu na antinukleární protilátky (ANA nebo anti‑dsDNA). Pacienti byli randomizováni v poměru 2 : 1 k podávání s.c. belimumabu v dávce 200 mg (n = 556) nebo placeba (n = 280) předplněnou injekční stříkačkou navíc ke standardní terapii. Primárním cílovým ukazatelem byla hodnota Systemic Lupus Erythematosus Responder Index (SRI) v týdnu 52. Jde o složený cílový ukazatel definující odpověď jako splnění všech následujících kritérií: ≥ 4bodové snížení skóre SELENA‑SLEDAI, žádné nové postižení orgánového systému podle skóre BILAG A (British Isles Lupus Assessment Group) nebo dvě nová orgánová postižení podle skóre BILAG B a žádné zhoršení v globálním hodnocení (Physician’s Global Assessment). Sekundárními cílovými ukazateli byly snížení dávky kortikosteroidů o ≥ 25 % (až na dávku ≤ 7,5 mg/den) během týdnů 40–52 a doba do těžkého relapsu. Bezpečnost léčby byla hodnocena dle nežádoucích účinků (adverse events, AE) a výsledků laboratorních testů.
Většinu pacientů tvořily ženy (93,7 % dostávalo belimumab, 95,7 % placebo), průměrný věk činil 38,6 roku (38,1 roku ve skupině s belimumabem, 39,6 roku ve skupině s placebem). Průměrné skóre SELENA-SLEDAI při vstupu do studie bylo 10,5 ve skupině s belimumabem a 10,3 ve skupině s placebem. Více než 85 % pacientů užívalo na počátku hodnocení kortikosteroidy.
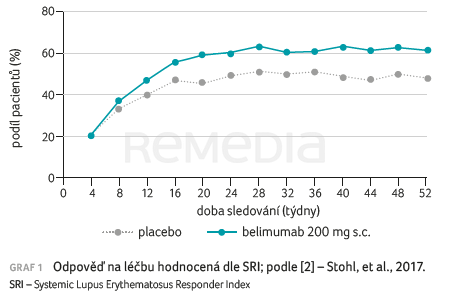 K výraznějšímu zlepšení došlo ve skupině léčené belimumabem. Odpověď dle SRI v 52. týdnu byla zaznamenána u 61,4 % vs. 48,4 % pacientů v placebové větvi (poměr šancí [OR] 1,68; 95% interval spolehlivosti [95% CI] 1,25–2,25; p = 0,0006). Výrazný rozdíl v odpovědi byl zaznamenán již v 16. týdnu (graf 1). Analýza podskupin doložila, že větší prospěch z léčby byl pozorován u pacientů s počáteční vyšší aktivitou onemocnění.
K výraznějšímu zlepšení došlo ve skupině léčené belimumabem. Odpověď dle SRI v 52. týdnu byla zaznamenána u 61,4 % vs. 48,4 % pacientů v placebové větvi (poměr šancí [OR] 1,68; 95% interval spolehlivosti [95% CI] 1,25–2,25; p = 0,0006). Výrazný rozdíl v odpovědi byl zaznamenán již v 16. týdnu (graf 1). Analýza podskupin doložila, že větší prospěch z léčby byl pozorován u pacientů s počáteční vyšší aktivitou onemocnění.
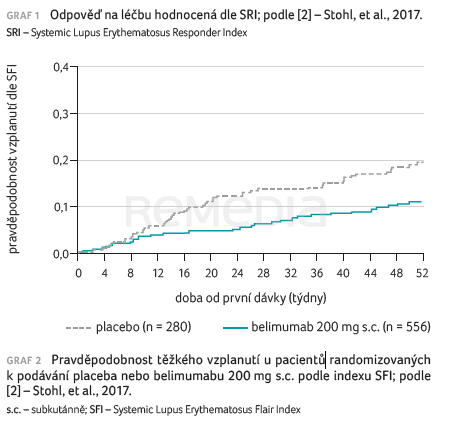 Pacienti léčení belimumabem měli během 52 týdnů sledování o 49 % nižší pravděpodobnost, že dojde k závažnému vzplanutí (poměr rizik, hazard ratio [HR] 0,51; 95% CI 0,35–0,74; p = 0,0004). U pacientů se závažným vzplanutím činila střední doba do vzplanutí 171,0 dnů oproti 118,0 dnům u placeba (graf 2). U většího podílu pacientů se také podařilo snížit dávku kortikosteroidů o ≥ 25 % (až na ≤ 7,5 mg/den) během týdnů 40–52 (18,2 % oproti 11,9 %; OR 1,65; 95% CI 0,95–2,84; p = 0,0732) ve srovnání s placebem. Signifikantní rozdíl mezi aktivní léčbou a placebem byl rovněž zaznamenán ve zmírnění únavy (hodnoceno dle skóre FACIT Fatigue).
Pacienti léčení belimumabem měli během 52 týdnů sledování o 49 % nižší pravděpodobnost, že dojde k závažnému vzplanutí (poměr rizik, hazard ratio [HR] 0,51; 95% CI 0,35–0,74; p = 0,0004). U pacientů se závažným vzplanutím činila střední doba do vzplanutí 171,0 dnů oproti 118,0 dnům u placeba (graf 2). U většího podílu pacientů se také podařilo snížit dávku kortikosteroidů o ≥ 25 % (až na ≤ 7,5 mg/den) během týdnů 40–52 (18,2 % oproti 11,9 %; OR 1,65; 95% CI 0,95–2,84; p = 0,0732) ve srovnání s placebem. Signifikantní rozdíl mezi aktivní léčbou a placebem byl rovněž zaznamenán ve zmírnění únavy (hodnoceno dle skóre FACIT Fatigue).
Výskyt AE byl srovnatelný mezi léčebnými rameny, nejčastěji šlo o běžné infekce a infestace. Lokální reakce v místě vpichu se objevily u 34 (6,1 %) pacientů ve skupině s belimumabem a u sedmi (2,5 %) pacientů ve skupině s placebem a všechny byly mírné nebo střední závažnosti. Závažné nežádoucí účinky (severe adverse events, SAE) byly hlášeny u 10,8 % pacientů léčených belimumabem a u 15,7 % pacientů, kteří dostávali placebo.
Vyhodnocení účinnosti a bezpečnosti léčby s.c. belimumabem v časovém horizontu delším než jeden rok prezentuje práce autorů Doria a kol. [3]. Šlo o 24týdenní otevřenou extenzi předchozího klinického hodnocení, kam mohli vstoupit pacienti, kteří dokončili dvojitě zaslepenou fázi. Všichni pacienti dostávali belimumab 200 mg s.c. 1× týdně plus standardní terapii SLE. Ze 677 pacientů, kteří dokončili 52týdenní dvojitě zaslepenou fázi, vstoupilo 662 do otevřené fáze; 206 pacientů dříve dostávalo placebo, 456 belimumab.
Odpověď na léčbu zůstala i v dalším období sledování zachována, odpovědi SRI dosáhlo ve skupině placebo‑belimumab 16,1 % pacientů, ve skupině s kontinuální terapií belimumabem 76,3 % pacientů. K závažnému vzplanutí došlo u 1,0 % pacientů ve skupině placebo‑belimumab a u 2,6 % s belimumabem.
Bezpečnostní profil subkutánního belimumabu byl v souladu s předchozími zkušenostmi. Navzdory rozdílům v celkové expozici belimumabu (24 týdnů v placebové skupině vs. 76 týdnů ve skupině s belimumabem) byl podíl pacientů s ≥ jedním AE nebo SAE v otevřené extenzi mezi skupinami podobný (AE a SAE pro placebo‑belimumab 51,5 % a 6,8 %, pro belimumab 48,2 % a 5,5 %). Většina AE byla mírné nebo střední intenzity.
Porovnání s.c. a i.v. belimumabu
Práce Ramachandrana a kol. [4] prezentuje porovnání účinnosti i.v. a s.c. belimumabu + standardní terapie u pacientů s aktivním SLE s pozitivitou protilátek a vysokou aktivitou nemoci. Jde o nepřímé srovnání léčby s využitím dat ze tří randomizovaných klinických studií (randomized controlled trial, RCT) fáze III s i.v. belimumabem a jedné RCT se s.c. belimumabem.
Primárním cílovým ukazatelem byla odpověď SRI, sekundárními cílovými ukazateli podíl pacientů s ≥ 4bodovým snížením skóre SELENA‑SLEDAI v 52. týdnu a četnost závažných vzplanutí. Zahrnuto bylo celkem 1 892 pacientů (i.v., n = 739; s.c., n = 421; placebo, n = 732).
Při porovnání jednotlivých způsobů podání byla zaznamenána obdobná účinnost, při porovnání s placebem výraznější zlepšení hodnocených cílových ukazatelů. Studie demonstrovala, že s.c. forma belimumabu je alternativní léčebnou možností i.v. belimumabu.
Posouzení relativní účinnosti i bezpečnosti i.v. nebo s.c. aplikovaného belimumabu ve srovnání s placebem u pacientů s aktivním SLE předkládá dále studie autorů Lee a Song [5]. Pomocí síťové bayesovské metaanalýzy byla porovnána přímá i nepřímá evidence z uskutečněných RCT zkoumajících účinnost a bezpečnost belimumabu 1 mg/kg a 10 mg/kg aplikovaného i.v., belimumabu 200 mg podaného s.c. injekcí a placeba u pacientů s aktivním SLE navzdory standardní léčbě. Zařazeno bylo 3 460 pacientů. Míra odpovědi hodnocená pomocí SRI v 52. týdnu byla významně vyšší ve skupině s belimumabem 10 mg/kg než ve skupině s placebem (OR 2,63; 95% CI 2,14–3,23). Podobně byla četnost odpovědí kvantifikovaná pomocí SRI významně vyšší ve skupinách s belimumabem 1 mg/kg a belimumabem 200 mg s.c. než v placebové skupině (OR 2,42; 95 % CI 1,90–3,09; OR 1,71; 95 % CI 1,27–2,29).
Belimumab v dávkách 1 a 10 mg/kg aplikovaný i.v. i belimumab 200 mg podávaný s.c. představují dle závěrů této metaanalýzy v kombinaci se standardní terapií účinnou intervenci u pacientů s aktivním SLE. Léčba není spojena s významným rizikem SAE, jejich počet se mezi čtyřmi léčebnými větvemi nelišil.
Sledování farmakokinetiky
Absolutní biologickou dostupnost, farmakokinetické děje, snášenlivost a bezpečnost belimumabu 200 mg/ml podávaného s.c. zdravým subjektům hodnotila studie fáze I [6]. Belimumab byl obecně dobře snášen po jednorázovém i opakovaném podání a očekává se, že podávání 200 mg s.c. týdně poskytne expozici podobnou té, jíž je dosaženo aplikací 10 mg/kg i.v. každých 28 dní. Konzistentní výsledky přinesly asijské studie [7,8].
Populační farmakokinetiku s.c. belimumabu a profily expozice belimumabu ve schválené dávce 10 mg/kg aplikované i.v. každé čtyři týdny a v dávce 200 mg podávané s.c. v týdenním intervalu hodnotila post hoc analýza autorů Yapa a kol. [9]. Biologická dostupnost s.c. belimumabu dosahuje přibližně 76 %, distribuční objem v ustáleném stavu 5 250 ml a odhadovaná clearance 208 ml/den. V ustáleném stavu dokládají simulované sérové profily srovnatelné průměrné koncentrace i.v. a s.c. belimumabu. Rozsahy koncentrací se při simulované expozici překrývají. Simulovaná akumulace belimumabu ukázala, že podání nasycovací dávky při s.c. aplikaci není nutné.
Aplikaci pomocí autoinjektoru na jedno použití a předplněné injekční stříkačky porovnávala studie Struempera a kol. [10]. Profily průměrných sérových koncentrací belimumabu byly pro obě zařízení podobné, s mírným trendem k vyšším koncentracím pro injekci do stehna ve srovnání s injekcemi do břicha. Maximální pozorovaná koncentrace v séru byla mírně vyšší při použití autoinjektoru ve srovnání s předplněnou stříkačkou (27,0 µg/ml vs. 25,3 µg/ml) a plocha pod křivkou koncentrace v čase mírně nižší (701 den · μg/ml vs. 735 den · μg/ml). Manipulaci s přístrojem uvedlo jako přijatelnou ≥ 95 % uživatelů autoinjektorů a ≥ 90 % uživatelů předplněných injekčních stříkaček. Tyto výsledky podporují použití obou zařízení pro s.c. podání belimumabu.
Doporučené dávkování
Doporučená dávka belimumabu v léčbě pacientů se SLE je 200 mg s.c. jednou týdně, u nemocných s aktivní lupusovou nefritidou 400 mg (ve dvou 200mg injekcích) jednou týdně po dobu čtyř týdnů a poté 200 mg jednou týdně. Doporučenými místy pro podání injekce jsou břicho nebo stehno. V případě lupusové nefritidy je přípravek doporučeno používat v kombinaci s kortikosteroidy a mykofenolátem či cyklofosfamidem jako indukční léčbu nebo s mykofenolátem či azathioprinem jako udržovací léčbu. Dávku belimumabu není třeba upravovat dle tělesné hmotnosti ani u pacientů s poruchou funkce jater či ledvin nebo u nemocných ve věku ≥ 65 let [1].
Přechod z i.v. na s.c. podání
U pacientů se SLE se první s.c. injekce má podat 1–4 týdny po poslední i.v. dávce, u pacientů s lupusovou nefritidou 1–2 týdny po poslední i.v. dávce. K převedení má dojít kdykoliv po dokončení prvních dvou intravenózních dávek [1].
Belimumab k s.c. podání bude v české republice dostupný ve formě předplněného pera.
Stanovení úhrady pro subkutánní belimumab
Přípravek BENLYSTA 200 mg inj sol pep 4×1 ml k subkutánnímu podání (s.c.) bude od 1. dubna 2025 hrazen z veřejného zdravotního pojištění.
Přípravek byl zařazen do skupiny v zásadě terapeuticky zaměnitelných léčivých přípravků s obsahem léčivé látky belimumab (dosud podávaných intravenózně, i.v.). Terapeutická účinnost a bezpečnost belimumabu pro s.c. podání oproti placebu byly u pacientů se středně závažným až závažným systémovým lupus erythematodes (SLE) považovány za prokázané a i.v. i s.c. forma belimumabu jako obdobně účinné a bezpečné.
Přípravek bude hrazen jako přídatná léčba u dospělých pacientů s aktivním SLE s pozitivními autoprotilátkami proti dvouvláknové DNA (anti‑dsDNA) a/nebo s antinukleárními protilátkami (ANAb) a nízkou hladinou komplementu, kteří navzdory obvyklé léčbě SLE sestávající z kortikoidů, antimalarik a dalších imunosupresiv setrvávají v klinicky aktivním onemocnění (SELENA‑SLEDAI ≥ 10). Léčba belimumabem se ukončí, pokud nedojde po 24 týdnech od zahájení léčby belimumabem k poklesu skóre SELENA‑SLEDAI alespoň o 4 body. Účinnost léčby belimumabem se následně vyhodnocuje každých šest měsíců, a pokud dojde ke zvýšení skóre SELENA‑SLEDAI na 10 a více bodů, bude ukončena.
Symbol „S“ stanovuje, že předmětný léčivý přípravek může být předepisován pouze v centrech se zvláštní smlouvou se zdravotními pojišťovnami na léčbu tímto typem léčivých přípravků.
Zdroj: Rozhodnutí BENLYSTA ze 3. 3. 2025, Sp. zn. SUKLS233457/2024, č. j. sukl78673/2025
Literatura
[1] SPC Benlysta 200 mg inj sol pep 4X1 ml. Dostupné na: https://www.sukl.cz
[2] Stohl W, Schwarting A, Okada M, et al. Efficacy and Safety of Subcutaneous Belimumab in Systemic Lupus Erythematosus: A Fifty‐Two‑Week Randomized, Double‐Blind, Placebo‐Controlled Study. Arthritis Rheumatol 2017; 69: 1016–1027.
[3] Doria A, Bass D, Schwarting A, et al. A 6‑month open‑label extension study of the safety and efficacy of subcutaneous belimumab in patients with systemic lupus erythematosus. Lupus 2018; 27: 1489–1498.
[4] Ramachandran S, Parks D, Kurtinecz M, et al. An indirect comparison of intravenous and subcutaneous belimumab efficacy in patients with SLE and high disease activity. J Comp Eff Res 2018; 7: 581–593.
[5] Lee YH, Song GG. Comparative efficacy and safety of intravenous or subcutaneous belimumab in combination with standard therapy in patients with active systemic lupus erythematosus: a Bayesian network meta‑analysis of randomized controlled trials. Lupus 2018; 27: 112–119.
[6] Cai WW, Fiscella M, Chen C, et al. Bioavailability, Pharmacokinetics, and Safety of Belimumab Administered Subcutaneously in Healthy Subjects. Clin Pharmacol Drug Dev 2013; 2: 349–357.
[7] Shida Y, Takahashi N, Sakamoto T, et al. The pharmacokinetics and safety profiles of belimumab after single subcutaneous and intravenous doses in healthy Japanese volunteers. J Clin Pharm Ther 2014; 39: 97–101.
[8] Meng X, Wang Q, Wu S, et al. Pharmacokinetics and Safety of Intravenous and Subcutaneous Auto‑injector Single‑dose Belimumab in Healthy Chinese Volunteers: A phase 1, Randomized, Open‑label Study. Rheumatol Ther 2021; 8: 1711–1724.
[9] Yapa SWS, Roth D, Gordon D, Struemper H. Comparison of intravenous and subcutaneous exposure supporting dose selection of subcutaneous belimumab systemic lupus erythematosus Phase 3 program. Lupus 2016; 25: 1448–1455.
[10] Struemper H, Murtaugh T, Gilbert J, et al. Relative Bioavailability of a Single Dose of Belimumab Administered Subcutaneously by Prefilled Syringe or Autoinjector in Healthy Subjects. Clin Pharmacol Drug Dev 2016; 5: 208–215.