Možná strategie hypolipidemické léčby ve světle nových důkazů
Studie z reálného prostředí opakovaně prokazují, že až 80 % pacientů s aterosklerotickým kardiovaskulárním onemocněním (ASKVO) nedosahuje cílových hodnot LDL cholesterolu (LDL‑C) dle doporučených postupů [1–3]. Mezi faktory, které mohou být příčinou špatných výsledků, jsou uváděny klinická inercie, non‑adherence k léčbě a nežádoucí účinky léčby.
V prevenci a léčbě pacientů s ASKVO zůstávají statiny první linií farmakoterapie. Vysoce intenzivní každodenní léčba statiny představuje pro většinu pacientů bezpečnou a spolehlivou léčebnou metodu, která může snížit hodnoty LDL‑C o ~50 %. Současné studie nicméně ukazují, že na léčbě statiny zůstává po roce léčby méně než 50 % pacientů, dokonce vysoce rizikových, nebo nedosahují cílových hodnot. Řada pacientů potřebuje k dosažení cílových hodnot další hypolipidemickou terapii (ezetimib, kyselina bempedoová a inhibitory proprotein konvertázy subtilisin/kexin typu 9 [PCSK9]). I tyto léčebné modality jsou dle průzkumů v klinické praxi nedostatečně využívány [2,3]. Inklisiran, malá interferující ribonukleová kyselina (siRNA), která cílí na jaterní PCSK9 mRNA s cílem potlačit translaci, představuje účinnou léčbu aplikovanou dvakrát ročně (po iniciálním dávkování v den 0 a 90). Je schopna významně snížit hodnoty LDL‑C (zhruba o 50 %) i dalších aterogenních lipoproteinů [4–6].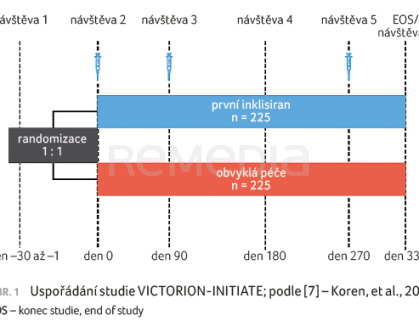
VICTORION‑INITIATE
Klinická studie VICTORION‑INITIATE (NCT04929249) si dala za cíl zhodnotit účinnost léčby inklisiranem v případě jeho okamžitého zařazení do léčby při nedosažení hodnot LDL‑C < 70 mg/dl navzdory maximální tolerované dávce statinu. Porovnávána byla s obvyklou péčí u pacientů s ASKVO v americké klinické praxi.
Metodika
VICTORION‑INITIATE je prospektivní pragmaticky navržená studie fáze IIIb, v níž byli pacienti randomizováni v poměru 1 : 1 k subkutánnímu podávání inklisiranu (284 mg ve dnech 0, 90 a 270) + k obvyklé péči (management hyperlipidemie dle uvážení ošetřujícího lékaře) oproti samotné obvyklé péči. Pacienti ve větvi „první inklisiran“ mohli, pokud by bylo potřeba, dostat pro dosažení cílových hodnot LDL‑C i další hypolipidemickou terapii vyjma inhibitorů PCSK9. Pacienti ve větvi „obvyklá péče“ mohli dostat všechny hypolipidemické léčebné modality vyjma inklisiranu. Uspořádání studie přehledně uvádí obrázek 1 [7].
Zařazeni byli dospělí pacienti (≥ 18 let) s anamnézou ASKVO (koronární srdeční onemocnění, cerebrovaskulární onemocnění nebo onemocnění periferních tepen), s hodnotou LDL‑C ≥ 70 mg/dl nebo non‑HDL cholesterolu (non‑HDL‑C) ≥ 100 mg/dl a s triglyceridemií nalačno < 500 mg/dl.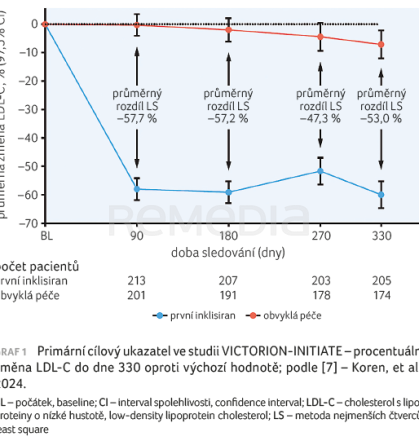
Primárními cílovými parametry byly stanoveny procentuální změna LDL‑C do dne 330 oproti výchozí hodnotě a četnost vysazení statinů (definováno jako ≥ 30 dní bez statinů na konci studie). Sekundární cílové ukazatele zahrnovaly procentuální a absolutní změnu LDL‑C od výchozí hodnoty do každé další návštěvy lékaře; podíl pacientů splňujících předem stanovené cíle LDL‑C (≥ 50% snížení LDL‑C oproti výchozí hodnotě, hodnota < 100 mg/dl u pacientů s LDL‑C ≥ 100 mg/dl na počátku sledování, < 70 mg/dl a < 55 mg/dl) v den 330; absolutní a procentuální změnu hodnot apolipoproteinu B, non‑HDL‑C, lipoproteinu s velmi nízkou hustotou [VLDL], celkového cholesterolu, lipoproteinu (a), HDL‑C a triglyceridů od počátku do dne 330; změny v intenzitě statinové terapie a v adherenci k hypolipidemické léčbě (statin, ezetimib, kyselina bempedoová a inhibitory PCSK9); variabilitu hodnot LDL‑C mezi jednotlivými návštěvami (od 90. do 330. dne) a celkovou bezpečnost a snášenlivost inklisiranu.
Výsledky
Ze 450 randomizovaných pacientů jich bylo do každého ramene zařazeno 225. Medián věku pacientů byl 67,0 (27–89) let, 30,9 % tvořily ženy, 12,4 % bylo černochů a 15,3 % Hispánců nebo latino. Ischemickou chorobu srdeční v anamnéze nebo přítomnou hlásilo 91,8 %. Přibližně jedna čtvrtina pacientů (25,8 %) měla v anamnéze intoleranci statinů a 90,0 % na začátku užívalo statiny, především v monoterapii (88,9 %). Většina pacientů dokončila studii (94,2 % ve skupině „první inklisiran“, 86,7 % ve skupině „obvyklá péče“).
V den 330 byla průměrná procentuální změna LDL‑C oproti výchozí hodnotě –60,0 % (97,5% interval spolehlivosti [CI] –64,7 až –55,2 %) ve větvi „první inklisiran“ a –7,0 % (97,5 % CI –12,0 až –1,9 %) ve větvi s obvyklou péčí, což znamená statisticky významný rozdíl mezi skupinami – 53,0 procentních bodů (97,5% CI 60,0–46,0 %; p < 0,001), graf 1. U pacientů bez intolerance statinů v anamnéze („první inklisiran“ n = 166; „obvyklá péče“ n = 168) činila míra vysazení statinů ve větvi „první inklisiran“ 6,0 % (97,5% CI 1,9–10,2 %) a ve větvi „obvyklá péče“ 16,7 % (97,5% CI 10,2–23,1 %), graf 2. Rozdíl spadal do meze non‑inferiority (a priori nastavená na 15 %) (–10,6 % 97,5% CI –18,3 až –3 %) [7].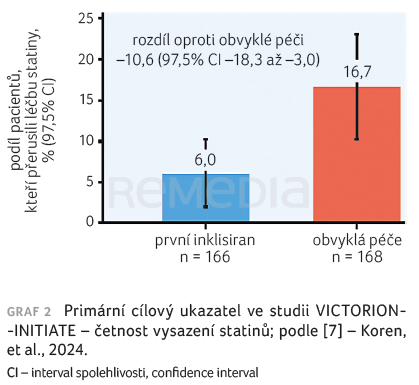
Dle analýzy sociodemografických podskupin došlo ve všech skupinách k významnému snížení hodnoty LDL‑C při léčebné strategii „první inklisiran“ ve srovnání s „obvyklou péčí“ a odpověď na léčbu se nelišila podle pohlaví, příjmu, rasy nebo etnického původu.
Průměrná absolutní změna LDL‑C oproti výchozí hodnotě byla 58,0 mg/dl (95% CI 61,6–54,4 mg/dl) ve větvi „první inklisiran“ a 10,5 mg/dl (95% CI 14,3–6,6 mg/dl) v rameni „obvyklá péče“; rozdíl mezi skupinami byl 47,6 mg/dl (95% CI 52,8–42,3 mg/dl; p < 0,001). Signifikantně větší podíl pacientů se strategií „první inklisiran“ dosáhl prespecifikovaných cílových hodnot LDL‑C (< 70 mg/dl: 81,8 % vs. 22,2 %; < 55 mg/dl: 71,6 % vs. 8,9 %; p < 0,001) a také větší procentuální i absolutní redukce hodnot celkového cholesterolu, non‑HDL‑C, VLDL, triglyceridů, apolipoproteinu B a lipoproteinu (a) a výraznějšího vzestupu hodnot HDL‑C.
Nežádoucí příhody související s léčbou (TEAEs) a závažné TEAEs (TESAEs) se při obou léčebných strategiích vyskytovaly s podobnou četností (62,8 % vs. 53,7 % a 11,5 % vs. 13,4 %). TEAEs v místě vpichu a TEAEs způsobující vysazení léčby se vyskytovaly častěji v rameni „první inklisiran“ (10,3 % vs. 0,0 % a 2,6 % vs. 0,0 %).
Léčebná strategie, která zařadila inklisiran do léčby ihned po nedosažení cílové hodnoty LDL‑C maximální tolerovanou dávkou statinu, vedla k výrazně většímu snížení hodnoty LDL‑C, které přetrvávalo až do konce studie, bez větších obav o bezpečnost ve srovnání s běžnou péčí (obr. 2). Studie VICTORION‑INITIATE potvrzuje v souladu s předchozím klinickým sledováním účinnost inklisiranu v reálném prostředí. Referenční léčebná skupina odrážela běžnou praxi ve Spojených státech amerických (ošetřující lékaři mohli v průběhu sledování měnit léčbu dle uvážení). Navzdory evidenci z klinického hodnocení, která podporuje přidání nestatinové hypolipidemické terapie k maximální tolerované dávce statinu u vysoce rizikových pacientů s ASKVO, a neustále se snižující cílové hodnotě LDL‑C s každou aktualizací doporučených postupů, se model předepisování za poslední dvě dekády v praxi příliš nezměnil. U velké většiny pacientů s ASKVO zůstává nepřijatelně vysoká míra reziduálního rizika, které pramení z neadekvátní léčby jejich aterogenní lipoproteinové zátěže.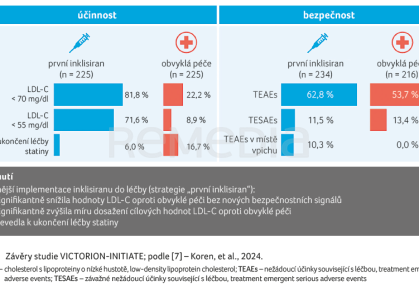
ORION‑8
Dlouhodobá data o účinnosti a bezpečnosti jsou u nových léčiv omezená. Na doplnění těchto informací u inklisiranu se zaměřila studie ORION‑8 (NCT03814187) [8], otevřená extenze placebem kontrolovaných studií fáze III ORION‑9, ORION‑10, ORION‑11 a studie fáze II ORION‑3.
Klíčová data o účinnosti inklisiranu byla získána ze tří placebem kontrolovaných studií fáze III (ORION‑9, ORION‑10 a ORION‑11), které dohromady zahrnuly 3 660 pacientů se zvýšenými sérovými koncentracemi LDL‑C navzdory optimalizované perorální hypolipidemické terapii [5,9]. Souhrnná analýza těchto studií prokázala, že inklisiran snížil hodnotu LDL‑C o ~51 % ve srovnání s placebem během 18měsíčního období s podobnou frekvencí TEAEs v obou skupinách [4].
Všechny předchozí placebem kontrolované studie zkoumaly účinnost iklisiranu po dobu až 18 měsíců, přičemž žádný pacient nedostal více než čtyři injekce inklisiranu. Účinnost inklisiranu po dobu čtyř let hodnotila otevřená studie ORION‑3 (extenze studie fáze II ORION‑1); do této studie však bylo zahrnuto pouze 382 pacientů, z nichž každý dostal až devět injekcí inklisiranu.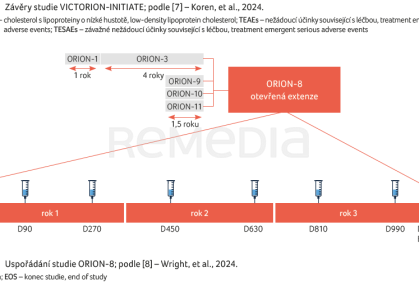
Metodika
Uspořádání studie ORION‑8 nastiňuje obrázek 3. Po dokončení mateřských studií pokračovali dospělí pacienti s ASKVO (koronární srdeční onemocnění, cerebrovaskulární onemocnění nebo onemocnění periferních tepen), ekvivalentem rizika ASKVO (definované jako diabetes mellitus typu 2, familiární hypercholesterolemie nebo 10leté riziko kardiovaskulární příhody ≥ 20 % podle Framinghamského skóre rizika) nebo s heterozygotní familiární hypercholesterolemií a zvýšenou hodnotou LDL‑C v otevřeném podávání inklisiranu dvakrát ročně až do dne 990. Po něm následovala konečná návštěva lékaře v den 1 080 nebo ≥ 90 dnů po poslední dávce. Cílové ukazatele zahrnuly podíl pacientů dosahujících předem specifikovaných cílových hodnot LDL‑C (pro ASKVO < 1,8 mmol/l [< 70 mg/dl]; pro ekvivalent rizika ASKVO < 2,6 mmol/l [< 100 mg/dl]). Sekundární cílové ukazatele sledovaly procentuální a absolutní změny hodnoty LDL‑C a dalších lipidových částic na konci studie. Primární bezpečnostní cílové ukazatele představovaly bezpečnost a snášenlivost dlouhodobého podávání inklisiranu.
Výsledky
Populace zařazených do studie ORION‑8 čítala 3 275 pacientů, tříleté sledování dokončilo 2 446 z nich. Průměrný věk pacientů byl 64,9 (± 9,9) roku, 67,7 % (2 216) pacientů tvořili muži, 92,9 % (3 041) pacientů byli běloši a 6,1 % (199) Hispánci. Většina (82,7 %) pacientů měla klinické ASKVO, 17,3 % pacientů bylo klasifikováno jako ekvivalent rizika ASKVO. Průměrná výchozí hodnota LDL‑C byla 2,9 (± 1,2 mmol/l). Celkově 88,6 % (2 902) pacientů užívalo statiny na začátku studie, 68,5 % (2 244) pacientů dostávalo intenzivní statinovou léčbu a 16,6 % (544) pacientů ezetimib.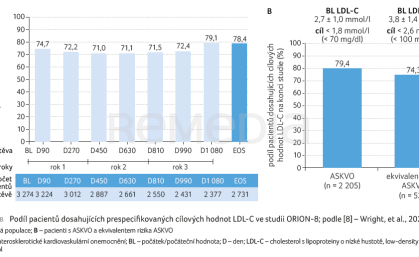
Průměrná expozice inklisiranu během studie ORION‑8 byla 2,6 roku, což odpovídá 8 530 pacientorokům expozice. Přičtením časové expozice v mateřských studiích dosáhla průměrná kumulativní expozice inklisiranu 3,7 roku, což odpovídá 12 109 pacientorokům expozice.
Inklisiran prokázal během období kontrolovaných placebem i během období extenze ve studii ORION‑8 setrvalou a konzistentní účinnost. Při každé návštěvě v klinické studii ORION‑8 dosáhlo více než 70 % pacientů cílových hodnot LDL‑C pro svou úroveň rizika (graf 3A). Podíl pacientů, kteří dosáhli primárního předem stanoveného cíle LDL‑C relevantního pro svoji klinickou kategorii na konci studie, byl 78,4 % (95% CI 76,8–80,0) z 2 731 pacientů; 79,4 % (95% CI 77,7–81,1) z 2 205 pacientů s ASKVO a 74,3 % (95% CI 70,4–78,0) z 526 pacientů s ekvivalentem rizika ASKVO (graf 3B).
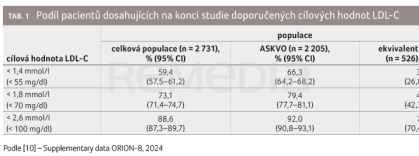 Podíl pacientů, kteří dosáhli na konci studie LDL‑C hodnot stanovených doporučenými postupy, shrnuje přehledně tabulka 1 [10].
Podíl pacientů, kteří dosáhli na konci studie LDL‑C hodnot stanovených doporučenými postupy, shrnuje přehledně tabulka 1 [10].
Průměrná výchozí hodnota LDL‑C byla 2,7 ± 1,0 mmol/l, resp. 3,8 ± 1,4 mmol/l v populacích s ASKVO a ekvivalentem rizika ASKVO. Procentuální změny hodnot LDL‑C od výchozí hodnoty znázorňuje přehledně graf 4A, B.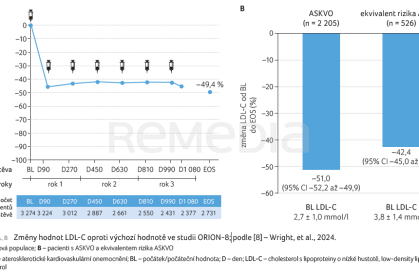
Bezpečnostní profil inklisiranu zůstal příznivý a v souladu s předchozím hodnocením, během prodloužené expozice se neobjevily žádné nové bezpečnostní signály. Přibližně 77,8 % (2 548) pacientů mělo TEAEs a 30,2 % (989) TESAEs. Nejčastějšími TEAEs byly covid‑19 (13,8 %), nedostatečná kontrola diabetes mellitus (7 %) a hypertenze (7 %). Nejčastějšími TESAEs byly ischemická choroba srdeční (2 %), covid‑19 (1,5 %) a akutní infarkt myokardu (1,3 %). Sledována byla také tvorba protilátek proti inklisiranu. Její incidence byla nízká (5,5 %), neovlivnila redukci hodnot LDL‑C ani nebyla asociována se zvýšenou incidencí TEAEs.
Shrnutí
Studie ORION‑8, která analyzovala 3 274 pacientů až po dobu 6,8 roku, poskytla dosud nejrozsáhlejší data a nejdelší sledování léčby inklisiranem (> 12 000 pacientoroků). Podávání inklisiranu dvakrát ročně (po počáteční dávce a navazující dávce po třech měsících) prokázalo konzistentní a účinné snížení hodnot LDL‑C bez nových bezpečnostních signálů během další léčebné expozice po mateřských studiích, s průměrnou kumulativní expozicí 3,7 roku a maximální expozicí 6,8 roku.
Globální doporučené postupy progresivně snižují cílové hodnoty LDL‑C zejména u pacientů s nejvyšším rizikem ASKVO a na základě dostupných dat zdůrazňují přínos dosažení velmi nízkých (< 1,4 mmol/l [< 55 mg/dl]) a nízkých (< 1,8 mmol/l [< 70 mg/dl]] hodnot LDL‑C [11–13]. Léčba statiny samotná nebo v kombinaci s ezetimibem často k dosažení těchto cílů nestačí. Bohužel v praxi nebývá ani při zjevném nedosažení vytčených cílů dále upravována. Výsledky studií VICTORION‑INITIATE i ORION‑8 jsou dalším vodítkem, jak je možné léčbu rizikových pacientů optimalizovat.
Literatura
[1] Ray KK, Molemans B, Schoonen WM, et al. Euwide cross‑sectional observational study of lipidmodifying therapy use in secondary and primary care: The Da Vinci study. Eur J Prev Cardiol 2021; 28: 1279–1289.
[2] Gu J, Sanchez RJ, Chauhan A, et al. Lipid treatment status and goal attainment among patients with atherosclerotic cardiovascular disease in the United States: a 2019 update. Am J Prevent Cardiol 2022; 10: 100336.
[3] Cannon CP, de Lemos JA, Rosenson RS, et al. Use of lipid‑lowering therapies over 2 years in GOULD, a registry of patients with atherosclerotic cardiovascular disease in the US. JAMA Cardiol 2021; 6: 1060–1068.
[4] Wright RS, Ray KK, Raal FJ, et al. Pooled patient‑level analysis of inclisiran trials in patients with familial hypercholesterolemia or atherosclerosis. J Am Coll Cardiol 2021; 77: 1182–1193.
[5] Ray KK, Wright RS, Kallend D, et al. Two Phase 3 trials of inclisiran in patients with elevated LDL cholesterol. N Engl J Med 2020; 382: 1507–1519.
[6] Ray KK, Troquay RPT, Visseren FLJ, et al. Long‑term efficacy and safety of inclisiran in patients with high cardiovascular risk and elevated LDL cholesterol (ORION‑3): results from the 4‑year open‑label extension of the ORION‑1 trial. Lancet Diabetes Endocrinol 2023; 11: 109–119.
[7] Koren MJ, Rodriguez F, East C, et al. An “Inclisiran First” Strategy vs Usual Care in Patients With Atherosclerotic Cardiovascular Disease. J Am Coll Cardiol 2024; 83: 1939–1952.
[8] Wright RS, Raal FJ, Koenig W, et al. Inclisiran administration potently and durably lowers LDL‑C over an extended‑term follow‑up: the ORION‑8 trial. Cardiovasc Res 2024: cvae109, doi: 10.1093/cvr/cvae109.
[9] Raal FJ, Kallend D, Ray KK, et al. Inclisiran for the treatment of heterozygous familial hypercholesterolemia. N Engl J Med 2020; 382: 1520–1530.
[10] Supplementary data k studii ORION‑8. Dostupná na: https://acade-
mic.oup.com/cardiovascres/advance‑article/doi/10.1093/cvr/
cvae109/7675310#supplementary‑data
[11] Mach F, Baigent C, Catapano AL, et al. 2019 ESC/EAS Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk: the Task Force for the management of dyslipidaemias of the European Society of Cardiology (ESC) and European Atherosclerosis Society (EAS). Eur Heart J 2019; 41: 111–188.
[12] Visseren FLJ, Mach F, Smulders YM, et al. 2021 ESC Guidelines on cardiovascular disease prevention in clinical practice. Eur Heart J 2021; 42: 3227–3337.
[13] Grundy SM, Stone NJ, Bailey AL, et al. 2018 AHA/ACC/AACVPR/AAPA/
ABC/ACPM/ADA/AGS/APhA/ASPC/NLA/PCNA Guideline on the management of blood cholesterol: a report of the American College of Cardiology/American Heart Association Task Force on Clinical Practice Guidelines. Circulation 2019; 139: e1082–e1143.