Ribociklib v kombinaci s endokrinní terapií u časného karcinomu prsu
Inhibitor cyklin‑dependentní kinázy 4 a 6 ribociklib prokázal u pacientů s HR pozitivním/HER2 negativním pokročilým karcinomem prsu významný přínos pro celkové přežití. Efektivitu a bezpečnost této léčby v kombinaci s nesteroidním inhibitorem aromatázy u časného karcinomu prsu zkoumá klinická studie NATALEE. Publikace Slamona a kol. se zaměřila na výsledky předem specifikované interim analýzy přežití bez invazivního onemocnění [1].
Karcinom prsu s pozitivitou hormonálního receptoru (HR) a negativitou receptoru 2 pro lidský epidermální růstový faktor (HER2) je nejčastějším podtypem karcinomu prsu, který představuje 70–75 % případů [2]. Většina pacientů s tímto podtypem je diagnostikována časně (ve stadiu I–III) [3]. Časný karcinom prsu je léčen s kurativním záměrem; u HR+/HER2– podtypu se uplatňuje chirurgický zákrok s radioterapií nebo chemoterapií nebo bez ní a s následnou adjuvantní endokrinní terapií po dobu 5–10 let [4]. Adjuvantní endokrinní terapie u těchto pacientů zlepšuje léčebné výsledky, nicméně k recidivě onemocnění dochází ve 27–37 % případů ve stadiu II a ve 46–57 % případů ve stadiu III a může nastat až 20 let po diagnóze [5].
Výsledky studií, v nichž byly hodnoceny inhibitory cyklin‑dependentní kinázy 4 a 6 (CDK4/6) ribociklib, palbociklib a abemaciklib, ukázaly významné zlepšení v přežití bez progrese u pacientů s HR+/HER2– pokročilým karcinomem prsu [6–11]. Ribociklib a abemaciklib mají také významný přínos pro celkové přežití [12–15]. U časného karcinomu prsu mělo použití inhibitorů CDK4/6 různé výsledky. Ve studiích PENELOPE‑B a PALLAS neprokázaly palbociklib plus endokrinní terapie významný přínos pro přežití bez invazivního onemocnění (invasive disease‑free survival, iDFS) [16,17]. Naopak významný efekt pro iDFS byl pozorován ve studii monarchE po dvou letech adjuvantní terapie s abemaciklibem [18–20].
Prokázaná účinnost, která byla pozorována u ribociklibu v případě pokročilého karcinomu prsu, podnítila jeho zkoumání u časného karcinomu prsu. NATALEE je studie fáze III srovnávající ribociklib v kombinaci s endokrinní terapií se samotnou endokrinní terapií, jež byla navržena k testování inhibice CDK4/6 u široké populace pacientů s HR+/HER2– časným karcinomem prsu stadia II nebo III. Uvádíme výsledky protokolem specifikované prozatímní analýzy účinnosti.
Metody
Do mezinárodní otevřené randomizované studie fáze III bylo zahrnuto více než 5 000 pacientů s HR+/HER2– časným karcinomem prsu, z nichž asi 40 % mělo onemocnění stadia II. Uspořádání a zdůvodnění studie byly popsány dříve [21]. Pacienti byli náhodně rozděleni v poměru 1 : 1 k podávání ribociklibu (v dávce 400 mg perorálně jednou denně po dobu 21 po sobě jdoucích dnů, po nichž následovalo 7 dní bez pauzy, což tvořilo 28denní cyklus podávaný po dobu 36 měsíců) a současně nesteroidního inhibitoru aromatázy (NSAI) letrozolu v dá vce 2,5 mg perorálně jednou denně, popř. anastrozolu v dávce 1 mg perorálně jednou denně v kontinuálním režimu po dobu 60 měsíců nebo k podávání samotného NSAI. Muži a premenopauzální ženy v obou skupinách také dostávali goserelin k potlačení aktivity gonád.
Vhodnými pacienty byli muži nebo premenopauzální či postmenopauzální ženy ve věku 18 let a starší s histologicky potvrzeným HR+/HER2– časným karcinomem prsu. Pacienti museli mít onemocnění stadia II nebo III dle American Joint Committee on Cancer Staging Manual, 8. vydání [22], s použitím klasifikace TNM (tumour, node, metastasis). Všichni pacienti s onemocněním stadia III nebo IIB se mohli studie zúčastnit bez ohledu na stav uzlin. Pacienti s onemocněním stadia IIA byli vhodní, pokud měli postiženu alespoň jednu lymfatickou uzlinu; zařazeni do studie byli pacienti, kteří neměli postižení uzlin a měli nádor 2. stupně s proliferačním indexem Ki‑67 alespoň 20 % nebo byli považováni za pacienty s vysokým genomickým rizikem. Rovněž pacienti s onemocněním stadia IIA bez uzlinového postižení a s tumorem stupně 3 byli způsobilí k zařazení do studie.
Pacienti mohli před randomizací dostávat jakoukoliv adjuvantní nebo neoadjuvantní endokrinní terapii po dobu až 12 měsíců. Zařazeny nebyly osoby, které již dříve dostávaly inhibitor CDK4/6 nebo měly klinicky významné nekontrolované srdeční onemocnění, abnormality srdeční repolarizace nebo obojí. Randomizace byla stratifikována podle anatomického stadia (II nebo III), menopauzálního stavu (premenopauzální ženy a muži nebo postmenopauzální ženy), předchozí adjuvantní nebo neoadjuvantní chemoterapie (ano nebo ne) a geografické polohy (Severní Amerika, západní Evropa, Oceánie, zbytek světa).
Primárním cílovým ukazatelem bylo iDFS, které bylo charakterizováno na základě standardizovaných definic pro kritéria účinnosti (Standardized Definitions for Efficacy End Points, STEEP), verze 1.0, podle hodnocení zkoušejícího [23]. Sekundárními cílovými ukazateli byly dlouhodobé přežití bez nemoci, přežití bez recidivy, celkové přežití, bezpečnost, kvalita života a farmakokinetika. Dlouhodobé přežití bez recidivy představovalo explorativní cílový ukazatel. Nežádoucí účinky byly monitorovány po dobu 36 měsíců počínaje dobou randomizace a závažné nežádoucí účinky byly sledovány v průběhu studie. Události byly hodnoceny podle Common Terminology Criteria for Adverse Events, verze 4.03.
Výsledky
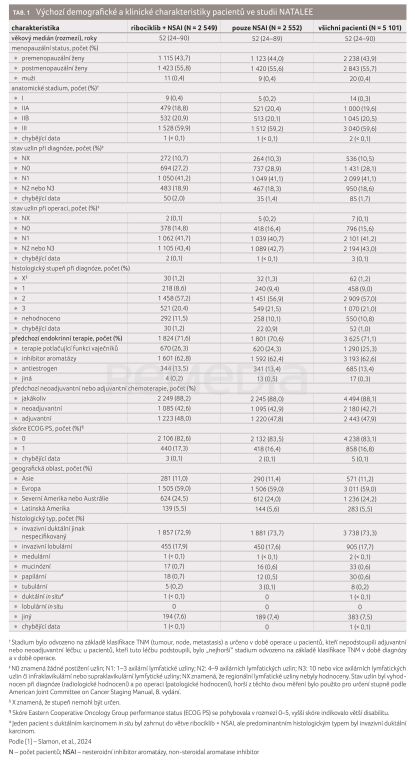 Od 10. ledna 2019 do 20. dubna 2021 bylo celkem 5 101 pacientů náhodně rozděleno do skupin, které dostávaly buď ribociklib v kombinaci s NSAI (n = 2 549), nebo samotný NSAI (n = 2 552). Demografické a výchozí klinické charakteristiky byly v obou skupinách vyvážené (tab. 1). Celkem 515 pacientů (20,2 %) dokončilo plánované tři roky léčby ribociklibem. Ve skupině ribociklib + NSAI pokračovalo v léčbě ribociklibem 1 147 pacientů (45,0 %) a 1 449 (56,8 %) dokončilo alespoň dva roky léčby ribociklibem + NSAI. Medián doby sledování činil 34 měsíců (minimum 21 měsíců). Medián trvání expozice studijní léčbě činil 30 měsíců ve skupině ribociklib + NSAI a 30 měsíců ve skupině NSAI. Ve větvi s kombinovanou léčbou byla střední doba expozice samotnému ribociklibu 27 měsíců [1].
Od 10. ledna 2019 do 20. dubna 2021 bylo celkem 5 101 pacientů náhodně rozděleno do skupin, které dostávaly buď ribociklib v kombinaci s NSAI (n = 2 549), nebo samotný NSAI (n = 2 552). Demografické a výchozí klinické charakteristiky byly v obou skupinách vyvážené (tab. 1). Celkem 515 pacientů (20,2 %) dokončilo plánované tři roky léčby ribociklibem. Ve skupině ribociklib + NSAI pokračovalo v léčbě ribociklibem 1 147 pacientů (45,0 %) a 1 449 (56,8 %) dokončilo alespoň dva roky léčby ribociklibem + NSAI. Medián doby sledování činil 34 měsíců (minimum 21 měsíců). Medián trvání expozice studijní léčbě činil 30 měsíců ve skupině ribociklib + NSAI a 30 měsíců ve skupině NSAI. Ve větvi s kombinovanou léčbou byla střední doba expozice samotnému ribociklibu 27 měsíců [1].
Účinnost
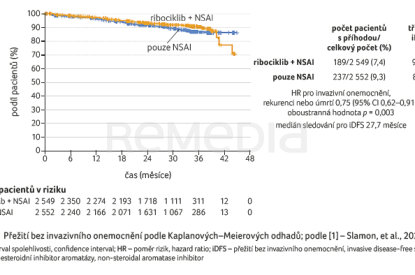 Druhá prozatímní analýza účinnosti pro iDFS (datum uzávěrky dat 11. ledna 2023) byla provedena poté, kdy u 426 pacientů bylo zaznamenáno invazivní onemocnění, recidiva nebo smrt – 189 osob (7,4 %) ve skupině ribociklib + NSAI a 237 pacientů (9,3 %) ve skupině NSAI. Medián doby sledování (od randomizace do posledního dokončeného hodnocení recidivy) byl 28 měsíců. Riziko invazivního onemocnění, recidivy nebo úmrtí bylo významně nižší (o 25,2 %) při přidání ribociklibu k NSAI než u samotného NSAI. Kaplanovy–Meierovy odhady iDFS po třech letech byly 90,4 % v rameni s kombinovanou léčbou a 87,1 % v rameni se samotným NSAI (poměr rizik [HR] pro invazivní nemoc, recidivu nebo smrt 0,75; 95% interval spolehlivosti [CI] 0,62–0,91), graf 1. Ve skupině s ribociklibem + NSAI byla prokázána statisticky významná a klinicky vyšší účinnost. Vzdálené recidivy byly nejčastěji hlášeným typem příhody v analýze iDFS, k nimž došlo u 120 pacientů (4,7 %) ve skupině ribociklib + NSAI a u 170 pacientů (6,7 %) ve skupině s NSAI; nejčastějšími místy recidivy onemocnění byly kosti a játra v každé skupině [1].
Druhá prozatímní analýza účinnosti pro iDFS (datum uzávěrky dat 11. ledna 2023) byla provedena poté, kdy u 426 pacientů bylo zaznamenáno invazivní onemocnění, recidiva nebo smrt – 189 osob (7,4 %) ve skupině ribociklib + NSAI a 237 pacientů (9,3 %) ve skupině NSAI. Medián doby sledování (od randomizace do posledního dokončeného hodnocení recidivy) byl 28 měsíců. Riziko invazivního onemocnění, recidivy nebo úmrtí bylo významně nižší (o 25,2 %) při přidání ribociklibu k NSAI než u samotného NSAI. Kaplanovy–Meierovy odhady iDFS po třech letech byly 90,4 % v rameni s kombinovanou léčbou a 87,1 % v rameni se samotným NSAI (poměr rizik [HR] pro invazivní nemoc, recidivu nebo smrt 0,75; 95% interval spolehlivosti [CI] 0,62–0,91), graf 1. Ve skupině s ribociklibem + NSAI byla prokázána statisticky významná a klinicky vyšší účinnost. Vzdálené recidivy byly nejčastěji hlášeným typem příhody v analýze iDFS, k nimž došlo u 120 pacientů (4,7 %) ve skupině ribociklib + NSAI a u 170 pacientů (6,7 %) ve skupině s NSAI; nejčastějšími místy recidivy onemocnění byly kosti a játra v každé skupině [1].
Byla provedena analýza iDFS napříč předem specifikovanými podskupinami. Po třech letech byl absolutní přínos v parametru iDFS u pacientů s ribociklibem + NSAI 3,0 procentního bodu v případě onemocnění stadia II a 3,2 procentního bodu stadia III [1].
Několik sekundárních cílových ukazatelů účinnosti rovněž doložilo konzistentní přínos ribociklibu. Po třech letech bylo dlouhodobé přežití bez nemoci 90,8 % ve skupině s ribociklibem + NSAI a 88,6 % ve skupině se samotným NSAI (HR 0,74; 95% CI 0,60–0,91). Po třech letech bylo přežití bez recidivy potvrzeno u 91,7 % pacientů léčených ribociklibem + NSAI a u 88,6 % pacientů léčených pouze NSAI (HR 0,72; 95% CI 0,58–0,88). Střední doba sledování celkového přežití byla 30 měsíců. V době uzávěrky dat zemřelo 61 z 2 549 (2,4 %) pacientů ve skupině s ribociklibem + NSAI a 73 z 2 552 (2,9 %) pacientů ve skupině s NSAI (HR 0,76; 95% CI 0,54–1,07) [1].
V případě explorativního cílového ukazatele – přežití bez vzdáleného onemocnění – bylo také doloženo zlepšení ve skupině s ribociklibem + NSAI oproti samotnému NSAI (HR 0,72; 95% CI 0,58–0,89) [1].
Bezpečnost
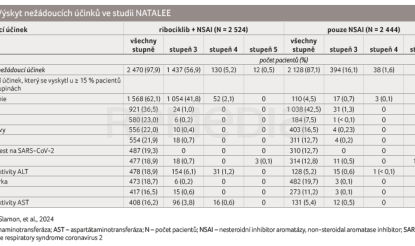 Bezpečnostní analýzy zahrnovaly 2 524 pacientů ve skupině s kombinovanou léčbou a 2 444 pacientů ve skupině s NSAI (tab. 2). Nejméně jeden nežádoucí účinek se vyskytl u 2 470 (97,9 %) pacientů ve větvi s ribociklibem + NSAI a u 2 128 (87,1 %) pacientů ve větvi s NSAI. Závažné nežádoucí účinky byly hlášeny u 336 (13,3 %) pacientů, resp. u 242 (9,9 %) pacientů. Nežádoucí události, které vedly k předčasnému přerušení podávání ribociklibu, byly hlášeny u 477 (18,9 %) pacientů. Nežádoucí účinky vedoucí k časnému vysazení ribociklibu i NSAI se vyskytly u 83 (3,3 %) pacientů. Podíl pacientů, kteří přerušili léčbu NSAI z jakékoliv příčiny nebo z důvodu výskytu nežádoucích účinků, byl v obou skupinách podobný [1].
Bezpečnostní analýzy zahrnovaly 2 524 pacientů ve skupině s kombinovanou léčbou a 2 444 pacientů ve skupině s NSAI (tab. 2). Nejméně jeden nežádoucí účinek se vyskytl u 2 470 (97,9 %) pacientů ve větvi s ribociklibem + NSAI a u 2 128 (87,1 %) pacientů ve větvi s NSAI. Závažné nežádoucí účinky byly hlášeny u 336 (13,3 %) pacientů, resp. u 242 (9,9 %) pacientů. Nežádoucí události, které vedly k předčasnému přerušení podávání ribociklibu, byly hlášeny u 477 (18,9 %) pacientů. Nežádoucí účinky vedoucí k časnému vysazení ribociklibu i NSAI se vyskytly u 83 (3,3 %) pacientů. Podíl pacientů, kteří přerušili léčbu NSAI z jakékoliv příčiny nebo z důvodu výskytu nežádoucích účinků, byl v obou skupinách podobný [1].
Nejčastějšími nežádoucími účinky jakéhokoliv stupně byly neutropenie (u 62,1 % pacientů ve skupině ribociklib + NSAI a u 4,5 % pacientů ve skupině NSAI), artralgie (u 36,5 %, resp. 42,5 % pacientů) a příhody související s jaterními poruchami (u 25,4 %, resp. 10,6 % pacientů). Tyto příhody byly také nejběžnějšími nežádoucími účinky stupně 3 nebo vyššího; nejčastější příhodou stupně 3 nebo vyššího byla neutropenie, která se vyskytla u 43,8 % pacientů ve skupině ribociklib + NSAI a u 0,8 % pacientů ve skupině NSAI [1].
Nejčastějšími nežádoucími příhodami jakéhokoliv stupně, které vedly k přerušení jakékoliv studijní léčby, byly příhody související s játry (u 8,9 % pacientů ve skupině ribociklib + NSAI a u 0,1 % pacientů ve skupině NSAI) a artralgie (u 1,3 %, resp. 1,9 % pacientů). K většině přerušení podávání ribociklibu došlo časně v průběhu léčby, s mediánem doby do ukončení medikace čtyři měsíce. Výskyt příhod souvisejících s NSAI vedoucích k přerušení terapie byl v obou léčebných skupinách podobný. Snížení dávky ribociklibu bylo zaznamenáno u 554 (21,9 %) pacientů [1].
Nežádoucí účinky související s jaterními poruchami 3. nebo 4. stupně byly hlášeny u 209 (8,3 %) pacientů ve větvi s ribociklibem + NSAI a u 37 (1,5 %) pacientů ve větvi s NSAI.
Prodloužení intervalu QT jakéhokoliv stupně bylo pozorováno v 5,2 % u kombinované léčby a v 1,2 % u NSAI. Nový interval QT korigovaný na srdeční frekvenci vyšší než 500 ms se vyskytl u 3 z 2 505 pacientů (0,1 %), resp. u 1 z 2 380 pacientů (< 0,1 %), ke zvýšení od výchozí hodnoty o více než 60 ms došlo u 19 z 2 505 pacientů (0,8 %), resp. u 2 z 2 380 pacientů (0,1 %) [1].
Úmrtí z jakékoliv příčiny bylo hlášeno u 60 (2,4 %) pacientů ve skupině ribociklib + NSAI a u 74 (3,0 %) pacientů ve skupině NSAI. Žádná úmrtí nebyla považována za související se studijní léčbou. K úmrtí bez progrese nebo recidivy onemocnění došlo u 19 pacientů ve větvi s ribociklibem + NSAI a u 13 pacientů ve větvi s NSAI. K úmrtí během léčby nebo do 30 dnů po poslední dávce studijní léčby došlo u 17 (0,7 %) pacientů, resp. u 9 (0,4 %) pacientů; z těchto úmrtí se 10 (0,4 %) vyskytlo do 30 dnů po poslední dávce ribociklibu [1].
Farmakokinetika
Průměrná minimální plazmatická koncentrace ribociklibu v ustáleném stavu činila 289,5 ng/ml v cyklu 1, den 15. Na základě tohoto zjištění a předchozích zpráv se odhaduje přibližně 80% inhibice CDK4/6 při průměrné minimální koncentraci v ustáleném stavu, což naznačuje více než 80% cílovou inhibici během léčby ribociklibem v ustáleném stavu [24,25].
Diskuse
Po publikaci zaměřené na inhibiční účinky inhibitorů CDK4/6 na růst nádorových buněk u HR+/HER2– karcinomu prsu [26] bylo provedeno několik klinických studií s cílem posoudit účinnost a bezpečnost těchto terapií jak u pokročilého, tak u časného karcinomu prsu [6–20]. Ve studii NATALEE byla zkoumána inhibice CDK4/6 u HR+/HER2–onemocnění v průběhu tříleté léčby ribociklibem přidané ke standardnímu NSAI jako adjuvantní terapie u široké populace pacientek s časným karcinomem prsu. Výsledky této studie ukázaly významný přínos pro iDFS oproti samotnému NSAI jako adjuvantní léčbě u HR+/HER2– časného karcinomu prsu stadia II nebo III; o 25,2 % nižší riziko invazivního onemocnění, recidivy nebo úmrtí a absolutní přínos v iDFS ve výši 3,3 procentního bodu po třech letech. Údaje o celkovém přežití jsou v současnosti nezralé. Nebyly pozorovány žádné nové bezpečnostní signály ani pro ribociklib, ani pro NSAI [6–8]. Léčba ribociklibem v dávce 400 mg denně byla spojena s nižším výskytem nežádoucích účinků závislých na dávce ve srovnání s počáteční dávkou 600 mg, která se používá u pacientů s pokročilým karcinomem prsu, a neovlivnila nepříznivě bezpečnostní profil NSAI v kombinaci. V době této analýzy studie probíhala a 20 % pacientů dokončilo tři roky léčby ribociklibem + NSAI, z tohoto důvodu pokračují další analýzy s delším sledováním, aby bylo možné plně posoudit klinický účinek tříleté inhibice CDK4/6 u dané populace pacientů.
Na loňském kongresu European Society for Medical Oncology byly prezentovány výsledky čtyřleté explorativní analýzy studie NATALEE s mediánem sledování iDFS 44,2 měsíce, které rovněž prokázaly signifikantní prospěch z léčby ribociklibem v kombinaci s NSAI ve srovnání se samotným NSAI (absolutní iDFS vzrostlo z 2,7 % ve třech letech na 4,9 % ve čtyřech letech) [27].
Studie NATALEE ukázala, že léčba ribociklibem je účinná u široké populace pacientů s časným karcinomem prsu, u nichž je zvýšeno riziko recidivy onemocnění. Terapie abemaciklibem rovněž ukázala významný přínos v parametru iDFS u pacientů s časným karcinomem prsu s pozitivními uzlinami ve studii monarchE, která byla provedena v populaci obohacené o vysoce rizikové nemocné. V případě studie monarchE byla vyžadována další vysoce riziková kritéria zařazení u pacientů s jednou až třemi lymfatickými uzlinami [20]. Naproti tomu studie NATALEE zahrnovala pacienty s onemocněním s negativními nebo pozitivními uzlinami, stejně jako pacienty s onemocněním ve stadiu II nebo III. Rozdíl v rizikovém profilu populace ve studiích NATALEE a monarchE je zřejmý, pokud srovnáme tříleté odhady iDFS prostřednictvím Kaplanových–Meierových křivek ve skupinách se samotnou endokrinní terapií. Ve studii NATALEE byl po 28 měsících sledování tříletý odhad iDFS 87,1 % pro samotný NSAI, ve studii monarchE po 27 měsících sledování činil odhad 83,4 % pro samotnou endokrinní terapii, což je výsledek, který odpovídá populaci s vyšším rizikem v daném klinickém hodnocení [19].
Endokrinní terapie použitá v těchto dvou studiích se lišila – v monarchE byl povolen NSAI a tamoxifen (dostávalo jej přibližně 30 % pacientů), v NATALEE pouze NSAI [18]. Inhibitory aromatázy prokázaly vyšší účinnost u pacientů se zvýšeným rizikem recidivy časného karcinomu prsu. Výsledky studií SOFT (Suppression of Ovarian Function Trial), TEXT (Tamoxifen and Exemestane Trial) a BIG (Breast International Group) 1‑98 ukázaly, že inhibitory aromatázy mají výhody oproti tamoxifenu [28,29]. Všechny premenopauzální ženy ve studii NATALEE dostávaly kromě NSAI terapii potlačující funkci vaječníků, na rozdíl od studie monarchE, v níž tuto terapii obdrželo pouze 48 % žen. Ve studii monarchE byla incidence žilních tromboembolických příhod vyšší u premenopauzálních pacientek, které užívaly tamoxifen, oproti pacientkám s inhibitorem aromatázy [30]. Ribociklib není indikován u pacientů, kteří jsou současně léčeni tamoxifenem.
V případě pokročilého karcinomu prsu představuje většina nežádoucích účinků spojených s léčbou ribociklibem, jako jsou neutropenie a transaminitidy, asymptomatické laboratorní nálezy, které lze monitorovat a zvládat. V souhrnné analýze studií MONALEESA‑2, ‑3 a ‑7 byly nejčastějšími nežádoucími účinky, které vedly k přerušení podávání ribociklibu v dávce 600 mg, zvýšené aktivity alaninaminotransferázy (4,0 % pacientů s ribociklibem a endokrinní terapií vs. 0,4 % s placebem a endokrinní terapií) nebo zvýšené aktivity aspartátaminotransferázy (2,4 % vs. 0,6 %) [31]. Klíčové ve studii NATALEE bylo použití snížené dávky ribociklibu (400 mg denně) ke zlepšení bezpečnosti a adherence po dobu tří let při zachování účinnosti. Kromě toho byla tříletá léčba ribociklibem stanovena s cílem zabránit recidivám onemocnění prostřednictvím prodloužení zástavy buněčného cyklu a potenciálním přesunem většího počtu nádorových buněk k nevratné senescenci. Ačkoliv je doporučována obezřetnost při srovnávání výše dávek mezi časným a pokročilým karcinomem prsu, 400 mg ribociklibu bylo spojeno s nižším výskytem známých nežádoucích účinků závislých na dávce – konkrétně neutropenie a prodloužení intervalu QT – oproti dávce 600 mg. Toto zjištění bylo rovněž pozorováno ve studii AMALEE [32].
Shrnutí
Předem specifikovaná průběžná analýza prokázala signifikantně nižší riziko výskytu invazivního onemocnění, recidivy nebo úmrtí při adjuvantní léčbě ribociklibem a NSAI než při léčbě samotným NSAI u pacientů s HR+/HER2– časným karcinomem prsu stadia II nebo III. Absolutní přínos kombinace ribociklib + NSAI po třech letech byl 3,3 procentního bodu. Uvedené výsledky podporují použití ribociklibu v léčbě HR+/HER2– časného karcinomu prsu [1].
Literatura
[1] Slamon D, Lipatov O, Nowecki Z, et al. Ribociclib plus Endocrine Therapy in Early Breast Cancer. N Engl J Med 2024; 390: 1080–1091.
[2] Howlader N, Altekruse SF, Li CI, et al. US incidence of breast cancer subtypes defined by joint hormone receptor and HER2 status. J Natl Cancer Inst 2014; 106: dju055.
[3] Iqbal J, Ginsburg O, Rochon PA, et al. Differences in breast cancer stage at diagnosis and cancer‑specific survival by race and ethnicity in the United States. JAMA 2015; 313: 165–173.
[4] Pistilli B, Lohrisch C, Sheade J, Fleming GF. Personalizing adjuvant endocrine therapy for early‑stage hormone receptor‑positive breast cancer. Am Soc Clin Oncol Educ Book 2022; 42: 1–13.
[5] Pan H, Gray R, Braybrooke J, et al. 20‑Year risks of breast‑cancer recurrence after stopping endocrine therapy at 5 years. N Engl J Med 2017; 377: 1836–1846.
[6] Hortobagyi GN, Stemmer SM, Burris HA, et al. Ribociclib as first‑line therapy for HR‑positive, advanced breast cancer. N Engl J Med 2016; 375: 1738–1748.
[7] Slamon DJ, Neven P, Chia S, et al. Phase III randomized study of ribociclib and fulvestrant in hormone receptor‑positive, human epidermal growth factor receptor 2‑negative advanced breast cancer: MONALEESA‑3. J Clin Oncol 2018; 36: 2465–2472.
[8] Tripathy D, Im S‑A, Colleoni M, et al. Ribociclib plus endocrine therapy for premenopausal women with hormone‑receptor‑positive, advanced breast cancer (MONALEESA‑7): a randomised phase 3 trial. Lancet Oncol 2018; 19: 904–915.
[9] Sledge GW Jr, Toi M, Neven P, et al. MONARCH 2: abemaciclib in combination with fulvestrant in women with HR+/HER2‑ advanced breast cancer who had progressed while receiving endocrine therapy. J Clin Oncol 2017; 35: 2875–2884.
[10] Goetz MP, Toi M, Campone M, et al. MONARCH 3: abemaciclib as initial therapy for advanced breast cancer. J Clin Oncol 2017; 35: 3638–3646.
[11] Turner NC, Ro J, André F, et al. Palbociclib in hormone‑receptor–positive advanced breast cancer. N Engl J Med 2015; 373: 209–219.
[12] Hortobagyi GN, Stemmer SM, Burris HA, et al. Overall survival with ribociclib plus letrozole in advanced breast cancer. N Engl J Med 2022; 386: 942–950.
[13] Slamon DJ, Neven P, Chia S, et al. Overall survival with ribociclib plus fulvestrant in advanced breast cancer. N Engl J Med 2020; 382: 514–524.
[14] Im S‑A, Lu Y‑S, Bardia A, et al. Overall survival with ribociclib plus endocrine therapy in breast cancer. N Engl J Med 2019; 381: 307–316.
[15] Sledge GW Jr, Toi M, Neven P, et al. The effect of abemaciclib plus fulvestrant on overall survival in hormone receptor‑positive, ERBB2‑negative breast cancer that progressed on endocrine therapy – MONARCH 2: a randomized clinical trial. JAMA Oncol 2020; 6: 116–124.
[16] Loibl S, Marmé F, Martin M, et al. Palbociclib for residual high‑risk invasive HR‑positive and HER2‑negative early breast cancer – the Penelope‑B Trial. J Clin Oncol 2021; 39: 1518–1530.
[17] Gnant M, Dueck AC, Frantal S, et al. Adjuvant palbociclib for early breast cancer: the PALLAS trial results (ABCSG‑42/AFT‑05/BIG‑14‑03). J Clin Oncol 2022; 40: 282–293.
[18] Johnston SRD, Harbeck N, Hegg R, et al. Abemaciclib combined with endocrine therapy for the adjuvant treatment of HR+, HER2‑, node‑positive, high‑risk, early breast cancer (monarchE). J Clin Oncol 2020; 38: 3987–3998.
[19] Harbeck N, Rastogi P, Martin M, et al. Adjuvant abemaciclib combined with endocrine therapy for high‑risk early breast cancer: updated efficacy and Ki‑67 analysis from the monarchE study. Ann Oncol 2021; 32: 1571–1581.
[20] Johnston SRD, Toi M, O’Shaughnessy J, et al. Abemaciclib plus endocrine therapy for hormone receptor‑positive, HER2‑negative, node‑positive, high‑risk early breast cancer (monarchE): results from a preplanned interim analysis of a randomised, open‑label, phase 3 trial. Lancet Oncol 2023; 24: 77–90.
[21] Slamon DJ, Fasching PA, Hurvitz S, et al. Rationale and trial design of NATALEE: a phase III trial of adjuvant ribociclib + endocrine therapy versus endocrine therapy alone in patients with HR+/HER2‑ early breast cancer. Ther Adv Med Oncol 2023; 15: 17588359231178125.
[22] Amin MB, Edge SB, Greene FL, et al., eds. AJCC cancer staging manual. 8th ed. New York: Springer, 2017.
[23] Hudis CA, Barlow WE, Costantino JP, et al. Proposal for standardized definitions for efficacy end points in adjuvant breast cancer trials: the STEEP system. J Clin Oncol 2007; 25: 2127–2132.
[24] James AD, Schiller H, Marvalin C, et al. An integrated assessment of the ADME properties of the CDK4/6 Inhibitor ribociclib utilizing preclinical in vitro, in vivo, and human ADME data. Pharmacol Res Perspect 2020; 8: e00599.
[25] Chen P, Lee NV, Hu W, et al. Spectrum and degree of CDK drug interactions predicts clinical performance. Mol Cancer Ther 2016; 15: 2273–2281.
[26] Finn RS, Dering J, Conklin D, et al. PD 0332991, a selective cyclin D kinase 4/6 inhibitor, preferentially inhibits proliferation of luminal estrogen receptor‑positive human breast cancer cell lines in vitro. Breast Cancer Res 2009; 11: R77.
[27] Fasching PA, Stroyakovskiy D, Yardley DA, et al. Adjuvant Ribociclib Plus Nonsteroidal Aromatase Inhibitor in Patients With HR+/HER2– Early Breast Cancer: 4‑Year Outcomes From the NATALEE Trial. ESMO Congress, September 16, 2024, Barcelona. Presentation LBA13.
[28] Francis PA, Pagani O, Fleming GF, et al. Tailoring adjuvant endocrine therapy for premenopausal breast cancer. N Engl J Med 2018; 379: 122–137.
[29] Regan MM, Neven P, Giobbie‑Hurder A, et al. Assessment of letrozole and tamoxifen alone and in sequence for postmenopausal women with steroid hormone receptor‑positive breast cancer: the BIG 1‑98 randomised clinical trial at 8·1 years median follow‑up. Lancet Oncol 2011; 12: 1101–1108.
[30] Paluch‑Shimon S, Neven P, Huober J, et al. Efficacy and safety results by menopausal status in monarchE: adjuvant abemaciclib combined with endocrine therapy in patients with HR+, HER2‑, node‑positive, high‑risk early breast cancer. Ther Adv Med Oncol 2023; 15: 17588359231151840.
[31] Burris HA, Chan A, Bardia A, et al. Safety and impact of dose reductions on efficacy in the randomised MONALEESA‑2, ‑3 and ‑7 trials in hormone receptor‑positive, HER2‑negative advanced breast cancer. Br J Cancer 2021; 125: 679–686.
[32] Cardoso F, Jacot W, Kummel S, et al. Primary efficacy and safety results from the AMALEE trial evaluating 600 mg vs 400 mg starting doses of first‑line ribociclib in patients with HR+/HER2− advanced breast cancer. Cancer Res 2023; 83(Suppl): PD17–12. Abstract (https://doi.org/10.1158/1538‑7445.SABCS22‑PD17‑12).