Zkušenosti se subkutánně aplikovaným infliximabem u pediatrických pacientů s nespecifickým střevním zánětem
Souhrn
Šuláková A. Zkušenosti se subkutánně aplikovaným infliximabem u pediatrických pacientů s nespecifickým střevním zánětem. Remedia 2025; 35: 75–80.
Infliximab (IFX) je lékem první linie biologické léčby idiopatických střevních zánětů u pediatrických pacientů. Intravenózní aplikace IFX (IV‑IFX) způsobuje kolísání jeho koncentrací v séru, a to je v současné době považováno za hlavní příčinu imunogenicity a tvorby neutralizačních protilátek s následnou ztrátou účinnosti terapie. Subkutánní forma IFX (SC‑IFX) udržuje dlouhodobě vyrovnané koncentrace a je spojena s nižším rizikem tvorby neutralizačních protilátek. Nízké riziko imunogenicity snižuje potřebu kombinované terapie s imunomodulátory a následně riziko komplikací (infekce, nádory). Data týkající se udržovací terapie SC‑IFX v dětském věku jsou v současnosti ojedinělá. Uvádíme zkušenosti jednoho centra se switchem z biosimilárního IV‑IFX na SC‑IFX u vybrané skupiny osmi dětí a adolescentů dlouhodobě léčených IV‑IFX s intenzifikovaným režimem. Klinická a laboratorní data byla hodnocena před switchem a šest měsíců po něm. U pěti pacientů jsme zaznamenali perzistenci na terapii a klinickou remisi, u dvou z nich i laboratorní remisi. U tří pacientů byla léčba ukončena, u jednoho z důvodu rozvoje nežádoucí reakce na IFX, u dvou pro selhání terapie. Pouze u jednoho pacienta došlo k vytvoření neutralizačních protilátek. Zaznamenali jsme statisticky významné zvýšení koncentrací IFX po switchi. Data tohoto souboru jsou malá, ale podporují názor, že switch z intenzifikovaného režimu IV‑IFX na SC‑IFX 120 mg každých 14 dnů je efektivní i bezpečný u dobře zvolených pediatrických pacientů nejen v klinické remisi Crohnovy nemoci, ale také v reindukci remise onemocnění.
Klíčová slova: Crohnova nemoc – ulcerózní kolitida – infliximab – subkutánní infliximab – biobetter – děti – adolescenti.
Summary
Sulakova A. Experience with subcutaneously applied infliximab in pediatric patients suffering from non‑specific bowel inflammation. Remedia 2025; 35: 75–80.
Infliximab (IFX) represents a first‑line biological agent in the treatment of idiopathic bowel inflammations affecting pediatric patients. Intravenous application of IFX (IV‑IFX) is associated with fluctuations of its serum concentrations, these fluctuations currently being viewed as the main cause of immunogenicity and production of neutralizing antibodies responsible for the loss of therapeutic effectiveness. Subcutaneous IFX (SC‑IFX) administration leads to steady long‑term concentrations and is associated with a lower risk of neutralizing antibodies synthesis. The low risk of immunogenicity diminishes the need of combination therapy with immunomodulators and the related risk of complications (infections, tumors). Data concerning maintenance therapy with SC‑IFX in childhood are still scarce. Here, we present single center experience with a switch from biosimilar IV‑IFX to SC‑IFX in a selected group of eight children and adolescents who have been on a long‑term intensified IV‑IFX treatment. Clinical and laboratory data were assessed before the switch and six months later. In five patients, we noted persistence on therapy and clinical remission while two patients achieved laboratory remission as well. The treatment was stopped in three patients, this step being motivated by adverse reaction to IFX in one and therapy failure in two. Neutralizing antibodies were only detected in one patient. After the switch, we noted a statistically significant increase of IFX concentrations. The set of data obtained in this cohort is small but supports the view that switch from intensified IV‑IFX regime to 120mg SC‑IFX once every 2 weeks is effective and safe for well selected pediatric patients not only in clinical remission of Crohn’s disease but also in the context of reinduction of disease remission.
Key words: Crohn’s disease – ulcerative colitis – infliximab – subcutaneous infliximab – biobetter – children – adolescents.
Úvod
Od roku 2013 jsou pro terapii nespecifických střevních zánětů schváleny biosimilární verze infliximabu (IFX). Mezi referenčním a biosimilárním lékem nejsou žádné klinicky významné rozdíly v účinnosti a bezpečnosti. Biobetters jsou inovativní biologické léky, které patří do stejné třídy jako stávající léčiva a cílí na stejný epitop. Jsou to vylepšené verze originálních biologik ve smyslu lepšího farmakologického účinku, výhodnějšího způsobu podání či dávkovacího režimu, snížení antigenního potenciálu nebo počtu nežádoucích účinků [1,2].
Subkutánní biosimilární infliximab (SC‑IFX) prokázal při porovnání s biosimilárním IFX s intravenózním podáváním (IV‑IFX) non‑inferioritu v účinnosti, bezpečnosti a imunogenicitě [3]. Koncentrace léčiva v séru je signifikantně vyšší a stabilnější, než je tomu u intravenózního podávání [4]. Vyšší a vyrovnané koncentrace IFX jsou spojeny s vyšším a setrvalým efektem terapie, který není závislý na současném podávání imunomodulátorů, což výrazně zvyšuje bezpečnost léčby. Vyrovnané koncentrace IFX jsou spojeny s výrazně nižší imunogenicitou [4,5]. Na SC‑IFX lze převést i pacienty s intenzifikovaným režimem nebo může být řešením v případě, kdy je žádoucí reindukce terapie IFX u nemocných po několikanásobném selhání jiných biologických léčiv, dokonce i u pacientů s přítomností neutralizačních protilátek proti léčivu [6].
Terapeutické monitorování hladin léčiva lze provést kdykoliv během 14denního intervalu, protože sérové koncentrace jsou stabilní ve všech časových bodech [7]. Subkutánní IFX zlepšuje komfort pacientů, kteří nemusejí docházet do center biologické léčby, šetří čas zdravotnického personálu a náklady spojené s aplikací léčby. Data týkající se udržovací léčby SC‑IFX v dětském věku jsou v současnosti ojedinělá [8]. Cílem této práce bylo popsat zkušenosti s přechodem na SC‑IFX u pediatrických pacientů s nespecifickým střevním zánětem léčených dlouhodobě IV‑IFX.
Pacienti a metody
Charakteristika souboru
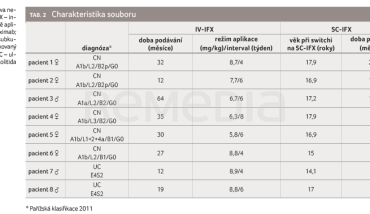
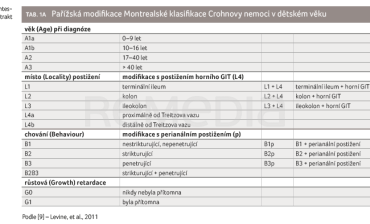 Retrospektivní sběr dat pacientů byl prováděn od prosince 2022 do listopadu 2024 na Klinice dětského lékařství Fakultní nemocnice Ostrava u dětí a adolescentů léčených pro ulcerózní kolitidu (UC) a Crohnovu nemoc (CN) biosimilárním IV‑IFX. Do souboru bylo zařazeno osm pacientů (3 chlapci, 37,5 %; CN/UC = 6/2) ve věku 14,1–17,9 roku (průměr 16,6 roku) léčených IV‑IFX. Typ onemocnění byl hodnocen podle pediatrické modifikace Montrealské klasifikace (Paříž 2011; tab. 1A, B) [9]. Základní charakteristika souboru – typ onemocnění, délka a režim podávání IV‑IFX, věk pacientů v době switche na SC‑IFX a délka podávání SC‑IFX jsou uvedeny v tabulce 2. Všichni pacienti byli léčeni IV‑IFX dlouhodobě, v době přechodu na subkutánní formu v průměru 28,9 měsíce (12–64 měsíců). Sedm pacientů mělo intenzifikovaný režim aplikace (dávka a/nebo interval) na základě nízké údolní koncentrace (Ctrough) IV‑IFX a/nebo klinické aktivity onemocnění. Léčba IV‑IFX byla dobře tolerovaná, u žádného pacienta nedošlo k vytvoření neutralizačních protilátek. Čtyři pacienti v době přechodu na SC‑IFX užívali současně azatioprin v dávce 0,72–0,88 mg/kg/den. Jeden pacient s UC byl dependentní na prednisonu, dávku 20 mg denně (= 0,44 mg/kg/den) nebylo možné redukovat.
Retrospektivní sběr dat pacientů byl prováděn od prosince 2022 do listopadu 2024 na Klinice dětského lékařství Fakultní nemocnice Ostrava u dětí a adolescentů léčených pro ulcerózní kolitidu (UC) a Crohnovu nemoc (CN) biosimilárním IV‑IFX. Do souboru bylo zařazeno osm pacientů (3 chlapci, 37,5 %; CN/UC = 6/2) ve věku 14,1–17,9 roku (průměr 16,6 roku) léčených IV‑IFX. Typ onemocnění byl hodnocen podle pediatrické modifikace Montrealské klasifikace (Paříž 2011; tab. 1A, B) [9]. Základní charakteristika souboru – typ onemocnění, délka a režim podávání IV‑IFX, věk pacientů v době switche na SC‑IFX a délka podávání SC‑IFX jsou uvedeny v tabulce 2. Všichni pacienti byli léčeni IV‑IFX dlouhodobě, v době přechodu na subkutánní formu v průměru 28,9 měsíce (12–64 měsíců). Sedm pacientů mělo intenzifikovaný režim aplikace (dávka a/nebo interval) na základě nízké údolní koncentrace (Ctrough) IV‑IFX a/nebo klinické aktivity onemocnění. Léčba IV‑IFX byla dobře tolerovaná, u žádného pacienta nedošlo k vytvoření neutralizačních protilátek. Čtyři pacienti v době přechodu na SC‑IFX užívali současně azatioprin v dávce 0,72–0,88 mg/kg/den. Jeden pacient s UC byl dependentní na prednisonu, dávku 20 mg denně (= 0,44 mg/kg/den) nebylo možné redukovat.
Laboratorní hodnocení aktivity nemoci
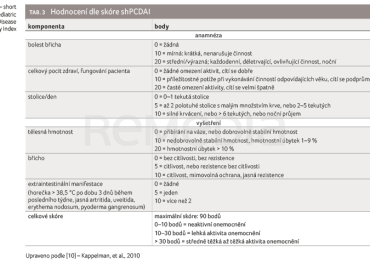
 Efekt SC‑IFX terapie na Ctrough IFX jsme hodnotili po šesti měsících, současně s aktivitou onemocnění pomocí fekálního kalprotektinu a skórovacích indexů aktivity CN či UC (short Pediatric Crohn’s Disease Activity Index, shPCDAI; Pediatric Ulcerative Colitis Activity Index, PUCAI; tab. 3, 4) [10,11].
Efekt SC‑IFX terapie na Ctrough IFX jsme hodnotili po šesti měsících, současně s aktivitou onemocnění pomocí fekálního kalprotektinu a skórovacích indexů aktivity CN či UC (short Pediatric Crohn’s Disease Activity Index, shPCDAI; Pediatric Ulcerative Colitis Activity Index, PUCAI; tab. 3, 4) [10,11].
Statistika
 Porovnání nominálních hodnot bylo provedeno parametrickým T‑testem, statistickým programem GrafPad Prism 6 for Windows.
Porovnání nominálních hodnot bylo provedeno parametrickým T‑testem, statistickým programem GrafPad Prism 6 for Windows.
Výsledky
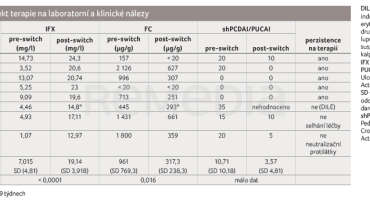
Výsledky sledovaných parametrů jsou uvedeny v tabulce 5. Sedm (87,5 %) pacientů mělo před switchem na SC‑IFX intenzifikovaný režim aplikace (dávkou i intervalem) pro nízké Ctrough IFX a nedostatečnou klinickou odpověď. Ani jeden pacient ale nedostal dávku 10 mg/kg IFX. Průměrná dávka IV‑IFX byla 7,7 mg/kg, interval 4–6 týdnů. Jeden pacient s CN při dávce 5,8 mg/kg a intervalu osm týdnů byl v klinické i laboratorní remisi při Ctrough 5,3 mg/l. Dva pacienti s CN byli pouze v klinické remisi i při koncentraci IFX 13,07, resp. 9,09 mg/l. Ostatní pacienti s CN měli lehkou aktivitu onemocnění dle shPCDAI a oba pacienti s UC měli mírnou zánětlivou aktivitu onemocnění dle PUCAI. Ke switchi na SC‑IFX došlo vždy v polovině intervalu aplikace IV‑IFX.
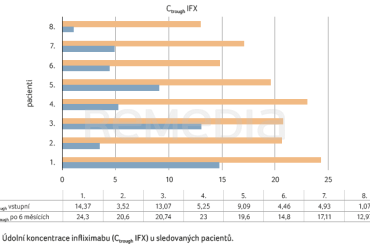
 Při aplikaci SC‑IFX v běžném dávkování 120 mg každých 14 dnů došlo u všech pacientů k vzestupu Ctrough IFX a k poklesu hodnoty fekálního kalprotektinu. Ctrough IFX po switchi byla statisticky významně vyšší a hodnoty fekálního kalprotektinu statisticky významně nižší (tab. 5, graf 1). Hodnoty C‑reaktivního proteinu (CRP) byly v období před switchem a po něm na SC‑IFX u sedmi pacientů negativní, pouze u pacienta č. 8 byla hodnota CRP zvýšena v obou odběrech.
Při aplikaci SC‑IFX v běžném dávkování 120 mg každých 14 dnů došlo u všech pacientů k vzestupu Ctrough IFX a k poklesu hodnoty fekálního kalprotektinu. Ctrough IFX po switchi byla statisticky významně vyšší a hodnoty fekálního kalprotektinu statisticky významně nižší (tab. 5, graf 1). Hodnoty C‑reaktivního proteinu (CRP) byly v období před switchem a po něm na SC‑IFX u sedmi pacientů negativní, pouze u pacienta č. 8 byla hodnota CRP zvýšena v obou odběrech.
U pěti pacientů s CN se standardním režimem SC‑IFX došlo k navození/udržení klinické remise a u dvou z nich i laboratorní remise. U jednoho pacienta s CN došlo dva měsíce po switchi k rozvoji léky indukovaného lupus erythematodes (drug induced lupus erythematosus, DILE). Léčba IFX byla u tohoto pacienta ukončena a byl převeden na biologikum mimo skupinu přípravků proti tumor nekrotizujícímu faktoru (anti‑TNF).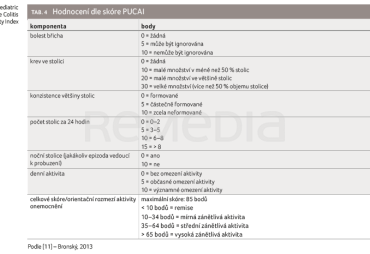
U obou pacientů s UC byla terapie SC‑IFX ukončena po sedmi měsících. V jednom případě nastalo pouze zlepšení klinického stavu a nepodařilo se vysadit prednison, došlo pouze ke snížení jeho dávky na 7,5 mg (0,15 mg/kg) denně. Ve druhém případě byla přechodně navozena krátkodobá klinické remise, ale léčba selhala při vytvoření vysokého titru neutralizačních protilátek proti IFX.
Diskuse
 Výsledky naší malé kohortové retrospektivní studie u osmi pacientů ukazují na významný efekt SC‑IFX na zlepšení koncentrací IFX, snížení laboratorně hodnocené aktivity onemocnění a navození klinické remise.
Výsledky naší malé kohortové retrospektivní studie u osmi pacientů ukazují na významný efekt SC‑IFX na zlepšení koncentrací IFX, snížení laboratorně hodnocené aktivity onemocnění a navození klinické remise.
 U dětí a adolescentů dosud nebyly provedeny studie se SC‑IFX. Byla publikována pouze kohortová studie z jednoho centra u sedmi pacientů v klinické remisi, kteří byli převedeni na SC‑IFX [8]. V této studii byla popsána vysoká perzistence na terapii, všichni pacienti zůstali v klinické remisi a zvýšila se Ctrough IFX. U žádného pacienta se nově nevytvořily neutralizační protilátky. Pouze u jednoho pacienta byly přítomny protilátky již v době switche na SC‑IFX. Na rozdíl od této studie jsme v našem souboru pozorovali selhání terapie po switchi na SC‑IFX u dvou pacientů, u jednoho z nich pak nově vznik neutralizačních protilátek. Jedním z možných vysvětlujících faktorů byla snížená adherence pacienta k terapii po zlepšení klinického stavu. Imunogenicita IFX je důsledkem velkých výkyvů jeho koncentrací při intravenózní aplikaci (vysoký peak po infuzi a následný pokles až po/pod Ctrough ≤ 5 mg/l). Naopak vyrovnané koncentrace infliximabu snižují imunogenicitu a riziko tvorby neutralizačních protilátek, což zvyšuje pravděpodobnost delšího setrvání na léčbě proti IV‑IFX.
U dětí a adolescentů dosud nebyly provedeny studie se SC‑IFX. Byla publikována pouze kohortová studie z jednoho centra u sedmi pacientů v klinické remisi, kteří byli převedeni na SC‑IFX [8]. V této studii byla popsána vysoká perzistence na terapii, všichni pacienti zůstali v klinické remisi a zvýšila se Ctrough IFX. U žádného pacienta se nově nevytvořily neutralizační protilátky. Pouze u jednoho pacienta byly přítomny protilátky již v době switche na SC‑IFX. Na rozdíl od této studie jsme v našem souboru pozorovali selhání terapie po switchi na SC‑IFX u dvou pacientů, u jednoho z nich pak nově vznik neutralizačních protilátek. Jedním z možných vysvětlujících faktorů byla snížená adherence pacienta k terapii po zlepšení klinického stavu. Imunogenicita IFX je důsledkem velkých výkyvů jeho koncentrací při intravenózní aplikaci (vysoký peak po infuzi a následný pokles až po/pod Ctrough ≤ 5 mg/l). Naopak vyrovnané koncentrace infliximabu snižují imunogenicitu a riziko tvorby neutralizačních protilátek, což zvyšuje pravděpodobnost delšího setrvání na léčbě proti IV‑IFX.
Subkutánně aplikovaný IFX prokázal ve studiích u dospělých non‑inferioritu v účinnosti, bezpečnosti a imunogenicitě v porovnání s biosimilárním IV‑IFX [3,12]. Ctrough u SC‑IFX je signifikantně vyšší a stabilnější proti IV‑IFX [3,12] a tito pacienti pak produkují méně protilátek proti léčivu [13]. Vyšší Ctrough signalizují vyšší pravděpodobnost setrvalé remise (zhruba o 25 %) a vyšší podíl pacientů se slizničním hojením (68 % vs. 55,6 %) [12]. V našem souboru došlo ke statisticky významnému zvýšení Ctrough u všech pacientů. U čtyř ze šesti pacientů s CN byla navozena klinická a u jednoho i laboratorní remise, která přetrvává na standardním režimu SC‑IFX 120 mg/2 týdny. Jeden pacient byl v době switche v klinické i laboratorní remisi, která přetrvává i po převedení na SC‑IFX. U jednoho ze dvou pacientů s UC došlo k navození krátkodobé klinické remise, ale nakonec k selhání terapie na podkladě vytvoření neutralizačních protilátek. U druhého pacienta s UC pak sice došlo ke zlepšení klinického stavu, ale nebylo dosaženo klinické remise. Naše data tedy odpovídají již publikovaným výsledkům u dospělých pacientů. DILE pozorovaný u jednoho pacienta se začal rozvíjet již při intravenózní aplikaci a nemá pravděpodobně souvislost se subkutánní formou léčiva.
Stabilita a koncentrace IFX jsou nezávislé na současném podávání imunomodulátorů (azatioprin, metotrexát), což zvyšuje bezpečnost léčby (snižuje riziko rozvoje infekce a malignity). Redukce počtu užívaných léků také zvyšuje adherenci k terapii [14]. V našem souboru dostávalo duální imunosupresivní terapii před switchem na SC‑IFX pět pacientů (4 pacienti – azatioprin, 1 pacient – prednison). U čtyř pacientů s azatioprinem (pacienti s CN) se jej podařilo po přechodu na SC‑IFX vysadit, u jednoho pacienta s UC bylo nutné ponechat minimální dávku prednisonu 7,5 mg denně.
Byla popsána reindukce IFX u pacientů po předchozím selhání řady jiných biologik a s imunogenicitou vůči IV‑IFX a setrvání na terapii u nemocných s předchozí senzibilizací na IV‑IFX a také sérokonverze a vymizení neutralizačních protilátek proti IFX u části nemocných [15,16]. V našem souboru byl IFX prvním biologikem u všech pacientů.
Závěr
Data našeho souboru jsou malá, ale podporují názor, že switch z intenzifikovaného režimu IV‑IFX na SC‑IFX 120 mg každých 14 dnů je efektivní i bezpečný u dobře zvolených pediatrických pacientů nejen v klinické remisi Crohnovy nemoci, ale také v reindukci remise onemocnění.
Také u našich pacientů jsme potvrdili vyšší a stabilnější koncentrace infliximabu, nízkou aktivitu onemocnění a vyšší perzistenci na léčbě při standardním režimu dávkování. Subkutánní forma léčby zlepšuje komfort pacientů, kteří nemusejí docházet do center biologické léčby, šetří čas zdravotnického personálu a náklady spojené s aplikací terapie.
MUDr. Astrida Šuláková, Ph.D.
Klinika dětského lékařství FN Ostrava
17. listopadu 1790/5, 708 52 Ostrava‑Poruba
e‑mail: astrida.sulakova@fno.cz
Literatura
[1] Sharma A, Kumar N, Kuppermann BD, et al. Biologics, biosilimars, and biobetters: different terms or different drugs? Eye (Lond) 2019; 33: 1032−1034.
[2] Kim H, Alten R, Cummings F, et al. Innovative approaches to biologic development on the trail of CT‑P13: biosimilars, value‑added medicines, and biobetters. MAbs 2021; 13: 1868078.
[3] Schreiber S, Ben‑Horin S, Leszczyszyn J, et al. Randomized Controlled Trial: Subcutaneous vs Intravenous Infliximab CT‑P13 Maintenance in Inflammatory Bowel Disease. Gastroenterology 2021; 160: 2340–2353.
[4] Little RD, Ward MG, Wright E, et al. Therapeutic Drug Monitoring of Subcutaneous Infliximab in Inflammatory Bowel Disease‑Understanding Pharmacokinetics and Exposure Response in a New Era of Subcutaneous Biologics. J Clin Med 2022; 11: 6173.
[5] Schreiber S, Jang BI, Borzan V, et al. Novel Formulation of CT‑P13 (Infliximab Biosimilar) for subcutaneous Administration: Initial Results from a Phase I Open‑Label Randomized Controlled Trial in Patient with Active Crohn’s Disease. Gastroenterology 2018; 154: 1371.
[6] Černá K, Ďuricová D, Lukáš M, et al. Subkutánní infliximab v léčbě refrakterních pacientů s Crohnovou nemocí – pilotní studie imunogenicity léčiva. Gastroent Hepatol 2023; 77: 419–426.
[7] Černá K. Kulatý stůl: Subkutánní infliximab v léčbě IBD a terapeutické monitorování hladin léčiva v praxi. Gastroent Hepatol 2023; 77: 147–153.
[8] Gianolio L, Armstrong K, Swann E, et al. Effectiveness of Switching to Subcutaneous Infliximab in Pediatric Inflammatory Bowel Disease Patients on Intravenous Maintenance Therapy. J Pediatr Gastroenterol Nutr 2023; 77: 235–239.
[9] Levine A, Griffiths A, Markowitz J, et al. Pediatric modification of the Montreal classification for inflammatory bowel disease: the Paris classification. Inflamm Bowel Dis 2011; 17: 1314–1321.
[10] Kappelman MD, Crandall WV, Colletti RB, et al. A Short Pediatric Crohn’s Disease Activity Index for Quality Improvement and Observational Research. Inflamm Bowel Dis 2010; 17: 112–117.
[11] Bronský J. Nespecifická zánětlivá střevní onemocnění u dětí. Praha: IPVZ, 2013.
[12] Hong SN, Song JH, Kim SJ, et al. One‑Year Clinical Outcomes of Subcutaneous Infliximab Maintenance Therapy Compared With Intravenous Infliximab Maintenance Therapy in Patients With Inflammatory Bowel Disease: A Prospective Cohort Study. Inflamm Bowel Dis 2024; 30: 517–528.
[13] Reinisch W. Predictors of Immunogenicity in Patients With Inflammatory Bowel Disease Treated With Infliximab: A Post Hoc Analysis of the Randomised Phase I CT‑P13 SC Study. Digestive Disease Week 2023. Abstract Tu1726.
[14] DʼHaens G, Reinisch W, Schreiber S, et al. Comparison of combination subcutaneous infliximab and an immunomodulator versus subcutaneous infliximab monotherapy: post hoc analysis of a randomised clinical trial. Clin Drug Investig 2023; 43: 277–288.
[15] Husman J, Černá K, Matthes K, et al. Effectiveness and safety of subcutaneous infliximab in Crohn’s disease patients with immunogenic failure of intravenous infliximab. Int J Colorectal Dis 2024; 39: 151.
[16] Cerna K, Duricova D, Lukas M, et al. Subcutaneous Infliximab in Refractory Crohn’s Disease Patients: A Possible Biobetter? Crohns Colitis 360 2023; 5: otad040.