Studie RECORD
Rosiglitazon, který je řazen mezi perorální antidiabetika ze skupiny thiazolidindionů, je indikován pro léčbu pacientů s diabetem 2. typu, a to buď v monoterapii, v dvojkombinaci s metforminem nebo sulfonylureou, či v trojkombinaci s metforminem a sulfonylureou. Je selektivním agonistou jaderných .....
Rosiglitazon, který je řazen mezi perorální antidiabetika ze skupiny thiazolidindionů, je indikován pro léčbu pacientů s diabetem 2. typu, a to buď v monoterapii, v dvojkombinaci s metforminem nebo sulfonylureou, či v trojkombinaci s metforminem a sulfonylureou. Je selektivním agonistou jaderných receptorů PPAR-g (receptor gama aktivovaný peroxizomálním proliferátorem). Rosiglitazon snižuje glykemii snížením inzulinové rezistence v tukové tkáni, v kosterních svalech a v játrech. Je známo, že thiazolidindiony (pioglitazon, rosiglitazon) mohou způsobovat retenci tekutin a jejich podávání může vést k srdečnímu selhání. Z tohoto důvodu po jejich uvedení na trh požadovaly regulační autority doplnění studií, které by hodnotily vztah mezi podáváním thiazolidindionů a výskytem kardiovaskulárních onemocnění.
Cílem studie RECORD bylo zhodnotit výskyt kardiovaskulárních komplikací u pacientů, kterým byl ke stávající léčbě metforminem nebo sulfonylureou přidán rosiglitazon, ve srovnání se skupinou pacientů, kterým byla podávána kombinovaná léčba metforminem a sulfonylureou [5]. Rovněž byla hodnocena bezpečnost léčby rosiglitazonem.
V této prospektivní otevřené multicentrické randomizované studii bylo zahrnuto celkem 4447 pacientů s diabetem 2. typu, kteří byli již dříve léčeni monoterapií metforminem nebo sulfonylureou. Kritéria pro vstup do studie zahrnovala: věk 40–75 let, BMI > 25 kg/m2 a stávající terapie metforminem nebo sulfonylureou v maximální tolerované dávce. Vylučovacími kritérii byly: hospitalizace pro velkou kardiovaskulární příhodu v předchozích třech měsících, plánovaná kardiovaskulární intervence a výskyt srdečního selhání v minulosti nebo v současnosti nebo léčba srdečního selhání. Průměrná vstupní hodnota glykovaného hemoglobinu (HbA1c) byla 7,9 %. Pacienti byli randomizováni do dvou skupin. V první skupině (n = 2220) byl ke stávající medikaci (metformin nebo sulfonylurea) přidán rosiglitazon, ve druhé skupině (n = 2227) byli pacienti léčeni kombinovanou terapií metforminem a sulfonylureou. Volba derivátu sulfonylurey (glimepirid, gliklazid, glibenklamid) byla ponechána na zvyklosti pracoviště. Žádná další léčiva snižující glykemii nebyla povolena (výjimku tvořili nedostatečně kompenzovaní pacienti s HbA1c > 8,5 %). Studijní medikace byla titrována až k dosažení cílové hodnoty HbA1c 7 % a nižší. Úvodní dávka rosiglitazonu byla 4 mg, po 8 týdnech léčby mohla být dávka zvýšena postupnou titrací až na 8 mg. Počáteční dávka metforminu a sulfonylurey se lišila dle lokálních zvyklostí. Po úvodních 8 týdnech bylo rovněž možné postupné zvyšování dávky až do maxima 2550 mg metforminu, 15 mg glibenklamidu, 240 mg gliklazidu a 4 mg glimepiridu.
Primárním ukazatelem (endpointem) byla doba do první hospitalizace z kardiovaskulárních příčin nebo doba do úmrtí z kardiovaskulárních příčin. Studie byla noninferiorní, hranice HR (hazard ratio) pro zjištění noninferiority byla stanovena na hodnotu 1,2. Hodnoceny byly také nežádoucí účinky a závažné nežádoucí účinky léčby.
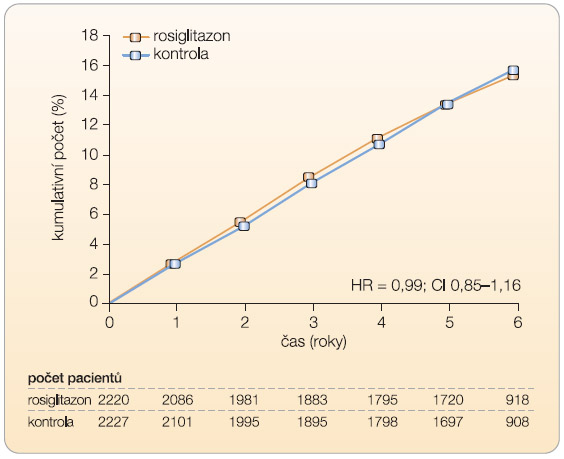 Po pěti letech sledování byla ve skupině pacientů léčených rosiglitazonem zjištěna nižší průměrná hodnota HbA1c, vyšší tělesná hmotnost, vyšší hladina HDL cholesterolu a rovněž vyšší hladina LDL cholesterolu než ve skupině kontrolní. Celkem 321 pacientů ve skupině s rosiglitazonem a 323 pacientů v kontrolní skupině dosáhlo v průměru za 5,5 roku sledování primárního ukazatele (HR = 0,99; CI 0,85–1,16, bylo dosaženo noninferiority), viz graf 1. Počet kardiovaskulárních úmrtí
Po pěti letech sledování byla ve skupině pacientů léčených rosiglitazonem zjištěna nižší průměrná hodnota HbA1c, vyšší tělesná hmotnost, vyšší hladina HDL cholesterolu a rovněž vyšší hladina LDL cholesterolu než ve skupině kontrolní. Celkem 321 pacientů ve skupině s rosiglitazonem a 323 pacientů v kontrolní skupině dosáhlo v průměru za 5,5 roku sledování primárního ukazatele (HR = 0,99; CI 0,85–1,16, bylo dosaženo noninferiority), viz graf 1. Počet kardiovaskulárních úmrtí 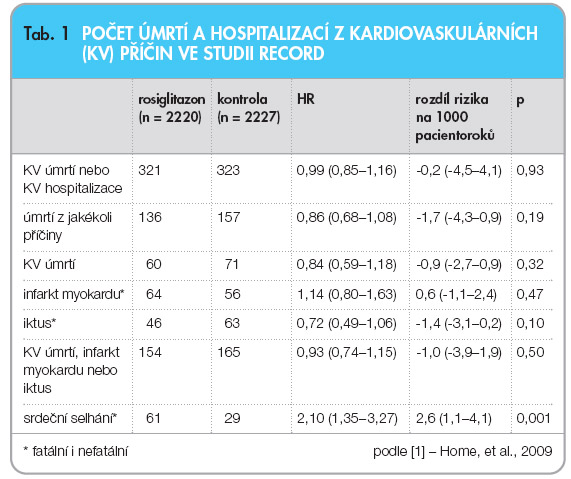 a celkový počet úmrtí byl nižší ve skupině s rosiglitazonem, rozdíl však nebyl statisticky signifikantní. Parametr HR pro úmrtí z kardiovaskulárních příčin činil 0,84 (0,59–1,18), pro infarkt myokardu 1,14 (0,80–1,63) a pro iktus 0,72 (0,49–1,06). Srdeční selhání bylo příčinou hospitalizace nebo úmrtí u 61 osob léčených rosiglitazonem a u 29 osob léčených kombinací metformin + sulfonylurea (HR = 2,10; 1,35–3,27, rozdíl rizika na 1000 pacientoroků je 2,6; 1,1–4,1), viz tab. 1. Oproti kontrolní skupině bylo v rosiglitazonové skupině zaznamenáno více úmrtí z důvodu
a celkový počet úmrtí byl nižší ve skupině s rosiglitazonem, rozdíl však nebyl statisticky signifikantní. Parametr HR pro úmrtí z kardiovaskulárních příčin činil 0,84 (0,59–1,18), pro infarkt myokardu 1,14 (0,80–1,63) a pro iktus 0,72 (0,49–1,06). Srdeční selhání bylo příčinou hospitalizace nebo úmrtí u 61 osob léčených rosiglitazonem a u 29 osob léčených kombinací metformin + sulfonylurea (HR = 2,10; 1,35–3,27, rozdíl rizika na 1000 pacientoroků je 2,6; 1,1–4,1), viz tab. 1. Oproti kontrolní skupině bylo v rosiglitazonové skupině zaznamenáno více úmrtí z důvodu 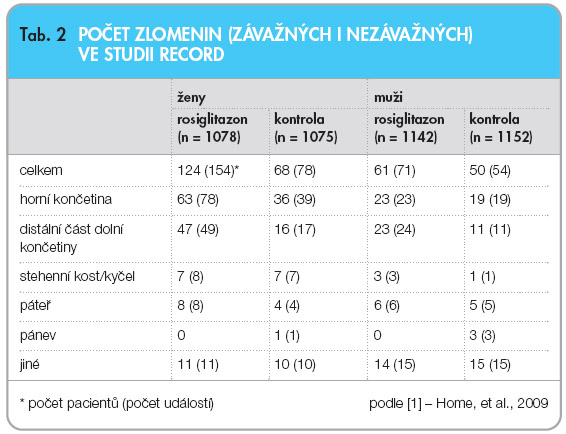 srdečního selhání a méně úmrtí na iktus či jiná vaskulární onemocnění. V rosiglitazonové skupině byl zaznamenán signifikantně vyšší počet srdečních selhání (82 vs. 42), přibližně stejný počet infarktů myokardu (74 vs. 67) a nižší počet cerebrovaskulárních příhod (43 vs. 63). Výskyt závažných hyperglykemií byl ve skupině s rosiglitazonem méně častý (27 vs. 55) než v kontrolní skupině, u hypoglykemií tomu bylo naopak (15 vs. 6). Logicky nejvyšší výskyt hypoglykemií (závažných i nezávažných) byl ve skupinách, které měly v algoritmu léčby sulfonylureu. Zlomeniny horních a distálních částí dolních končetin se vyskytovaly zejména u žen ve skupině užívající rosiglitazon, podrobněji viz tab. 2.
srdečního selhání a méně úmrtí na iktus či jiná vaskulární onemocnění. V rosiglitazonové skupině byl zaznamenán signifikantně vyšší počet srdečních selhání (82 vs. 42), přibližně stejný počet infarktů myokardu (74 vs. 67) a nižší počet cerebrovaskulárních příhod (43 vs. 63). Výskyt závažných hyperglykemií byl ve skupině s rosiglitazonem méně častý (27 vs. 55) než v kontrolní skupině, u hypoglykemií tomu bylo naopak (15 vs. 6). Logicky nejvyšší výskyt hypoglykemií (závažných i nezávažných) byl ve skupinách, které měly v algoritmu léčby sulfonylureu. Zlomeniny horních a distálních částí dolních končetin se vyskytovaly zejména u žen ve skupině užívající rosiglitazon, podrobněji viz tab. 2.
Ze studie vyplývá, že rosiglitazon nezvyšuje riziko kardiovaskulární morbidity a mortality ve srovnání se standardními léčivy (metformin, sulfonylurea), která snižují glykemii. Data ohledně vlivu rosiglitazonu na výskyt infarktu myokardu nejsou jednoznačná. Ze studie dále vyplývá, že přidání rosiglitazonu k terapii snižující glykemii u osob s diabetem 2. typu zvyšuje riziko srdečního selhání, a zvláště u žen také riziko některých zlomenin.
Výsledky studie RECORD redakčně zpracovala: Mgr. Helena Koblihová
Komentář ke studii RECORD
Prof. MUDr. Milan Kvapil, CSc., MBA
Po dlouhou dobu nebylo jasně prokázáno, že zlepšování glykemie u jinak asymptomatického pacienta s diabetem 2. typu znamená přínos pro prevenci komplikací. Až v roce 1997 byly publikovány výsledky rozsáhlé observační studie UKPDS, které byly podkladem změny doporučených postupů pro léčbu diabetu 2. typu. Bylo jasně dokázáno, že lepší kompenzace diabetu znamená nižší pravděpodobnost vzniku mikroangiopatických komplikací. Také se ukázalo, že zahájení terapie metforminem u obézních osob snižuje významně mortalitu, proto metformin zaujal pozici léku první volby. V roce 2008 byla uveřejněna extenze studie UKPDS, jejíž výsledky potvrdily výsadní postavení metforminu ve smyslu jednoznačného přínosu pro snížení kardiovaskulárních komplikací a mortality [1]. Tato extenze přinesla také důkaz, že snížení glykemie (zlepšení kompenzace) snižuje také riziko všech, i makrovaskulárních, komplikací, zejména, je-li s intenzivní léčbou započato co nejdříve po stanovení diagnózy diabetu 2. typu. Nezávisle pak byl metaanalýzou velkých prospektivních studií (UKPDS, ADVANCE, ACCORD, VADT, PROactive) potvrzen příznivý vliv kompenzace na snížení rizika makrovaskulárních komplikací.
Začátkem tohoto desetiletí převládl tedy názor, že je účelné snižovat nejen glykemii, ale také ovlivňovat inzulinovou rezistenci, jelikož přítomnost některých rizikových faktorů pro rozvoj aterosklerózy je přímým důsledkem inzulinové rezistence. Naděje se upíraly k nové skupině léků – thiazolidindionů (glitazonů), které prokazatelně nejen snižovaly glykemii, ale i zlepšovaly inzulinovou rezistenci. První důkazy byly nadějné (zlepšení rizikových faktorů při léčbě rosiglitazonem) a první klinické výsledky jistě neznamenaly zklamání: při léčbě pioglitazonem ve studii PROactive [2] se podařilo snížit riziko základního ukazatele (smrt, infarkt myokardu, cévní mozková příhoda). Jisté rozpaky však zavládly po zveřejnění ne zcela profesionálně provedené metaanalýzy Nissena [3], která upozornila na možnost, že terapie rosiglitazonem nesnižuje riziko vzniku infarktu myokardu. Od té doby byla uveřejněna řada dalších metaanalýz s rozporuplnými výsledky, byla provedena řada podrobných analýz velkých prospektivních studií (ADVANCE, VADT, ACCORD), z nichž žádná nepotvrdila obavy. Nicméně, jedinou prospektivní studií, která byla od začátku zaměřena na zodpovězení otázky vlivu rosiglitazonu na kardiovaskulární komplikace, byla studie RECORD. Její interim analýza vyzněla pozitivně, proto byla dokončena a v letošním roce byly publikovány výsledky na sjezdu ADA a současně v časopise Lancet [4].
Výsledek je z hlediska statistického jednoznačný – terapie rosiglitazonem nezvyšuje mortalitu a nezvyšuje riziko koronární příhody. Terapie rosiglitazonem zlepšuje kompenzaci oproti léčbě standardní kombinací metformin/sulfonylurea. Studie byla koncipována jako noninferiorní, proto by její výsledky měly být přijaty jako jednoznačný důkaz relativní bezpečnosti rosiglitazonu.
Ve studii RECORD byly porovnávány dvě skupiny pacientů, jedna léčená kombinací metforminu nebo sulfonylurey s rosiglitazonem, druhá kombinací metforminu a sulfonylurey. Dávka rosiglitazonu byla až 8 mg. Celkový počet komplikací a mortalita byly nižší, než se očekávalo, i přesto však měla studie dostatečnou sílu k jednoznačnému statistickému průkazu. Studii po zveřejnění Nissenovy metaanalýzy ukončilo 1,4 % z randomizovaných pacientů, což výsledek nijak neovlivnilo.
Speciální pozornost si zaslouží vliv terapie rosiglitazonem na mortalitu a incidenci infarktu myokardu. Celková mortalita (136 vs. 157) i kardiovaskulární mortalita (60 vs. 71) byla ve studii RECORD nesignifikantně nižší při léčbě rosiglitazonem, a to i v porovnání jednotlivých kombinací. Je třeba připomenout, že rosiglitazon tedy z hlediska nejtvrdšího ukazatele (mortality) není horší než terapie první volby – metformin. Roční celková mortalita u osob léčených rosiglitazonem byla 1,1 %, což je podstatně méně, než bylo očekáváno. Ale je to také mnohem méně, než bylo zaznamenáno ve studii UKPDS (kde byla mortalita téměř dvojnásobná). V tomto smyslu je tedy rosiglitazon nutno považovat za velmi kvalitní perorální antidiabetikum.
Možný vliv zlepšené kompenzace (0,27 %, resp. 0,26 % HbA1c) ve větvi léčené rosiglitazonem není diskutován, nicméně, i když není klinicky zanedbatelný, není natolik významný, aby mohl ovlivnit celkový výsledek.
Ve skupině léčené rosiglitazonem bylo na konci léčby zjištěno, že průměrný HDL cholesterol je vyšší a průměrný LDL cholesterol také, což bylo pravděpodobně důvodem, proč v této skupině bylo také o něco více pacientů léčeno statiny (rozdíl však nebyl natolik významný, aby mohl ovlivnit celkový výsledek, jak je dokázáno v diskusi ke studii).
Z hlediska nežádoucích účinků studie RECORD potvrdila rizika terapie glitazony, která jsou již všeobecně známa – vyšší riziko vzniku zlomenin a srdečního selhání.
Studie RECORD snad uzavřela kapitolu diskusí o potenciálním riziku terapie rosiglitazonem. Rizika léčby glitazony jsou známa, přínos léčby spočívá zejména v tom, že významně ovlivňují inzulinovou rezistenci, a proto u řady pacientů vedou k významnému zlepšení kompenzace. Jsem přesvědčen, že rosiglitazon uhájil své místo v terapii diabetu 2. typu, a soudím, že při správné indikaci, je-li jeho účinek na zlepšení kompenzace významný, přínos léčby rosiglitazonem převáží nad možnými riziky, kterých není prosta žádná terapie.
Seznam použité literatury
- [1] Holman RR, Paul SK, Bethel MA, et al. 10-year follow-up of intensive glucose control in type 2 diabetes. N Engl J Med 2008; 359: 1577–1589.
- [2] Dormandy JA, Charbonnel B, Eckland DJ, et al. Secondary prevention of macrovascular events in patients with type 2 diabetes in the PROactive Study (PROspective pioglitAzone Clinical Trial In macroVascular Events): a randomised controlled trial. Lancet 2005; 366: 1279–1289.
- [3] Nissen SE, Wolski K. Effect of rosiglitazone on the risk of myocardial infarction and death from cardiovascular causes. N Engl J Med 2007; 356: 2457–2471.
- [4] Home PD, Pocock SJ, Beck-Nielsen H, et al. Rosiglitazone evaluated for cardiovascular outcomes in oral agent combination therapy for type 2 diabetes (RECORD): a multicentre, randomised, open-label trial. Lancet 2009; 373: 2125–2135.
- [5] Home PD, Pocock SJ, Beck-Nielsen H, et al. Rosiglitazone evaluated for cardiovascular outcomes in oral agent combination therapy for type 2 diabetes (RECORD): a multicentre, randomised, open-label trial. Lancet 2009; 373: 2125–2135.