Certolizumab pegol je vysoce účinný i u pacientů s revmatoidní artritidou s vysokými titry revmatoidních faktorů
Souhrn
Pavelka K, Šenolt L. Certolizumab pegol je vysoce účinný i u pacientů s revmatoidní artritidou s vysokými titry revmatoidních faktorů. Remedia 2025; 35: 42–46.
Vysoké titry revmatoidních faktorů (RF) u pacientů s revmatoidní artritidou (RA) jsou nepříznivým prognostickým faktorem; jsou asociovány s vyšší aktivitou onemocnění, vyšším rizikem radiografické progrese a s nižší odpovědí na léčbu cílenou proti tumor nekrotizujícímu faktoru (anti‑TNF). Několik studií včetně velké kohortové mezinárodní studie z registrů prokázalo, že u pacientů s pozitivními RF jsou účinnější rituximab a abatacept a nejsou doklady o odlišné účinnosti anti‑TNF přípravků. Předmětem článku jsou nová data získaná na základě analýz lékových studií a registrů z posledních let. Tyto studie demonstrovaly, že rozdílná struktura anti‑TNF přípravků, např. přítomnost či nepřítomnost Fc fragmentu, může ovlivňovat sérové koncentrace léků a také účinnost léčby. Představiteli přípravků s Fc fragmentem jsou anti‑TNF monoklonální protilátky (infliximab, adalimumab a solubilní receptor etanercept). Účinnou látkou bez Fc fragmentu je certolizumab pegol. V textu jsou prezentovány výsledky několika studií, které prokázaly, že titry RF na začátku léčby mohou ovlivňovat účinné hladiny léků a tím také jejich klinickou účinnost. Zatímco u pacientů s nízkými titry RF (< 200 IU/ml) nejsou sérové koncentrace anti‑TNF léků ovlivněny, u pacientů s nejvyššími titry RF (> 200 IU/ml) již dochází k rozdílům. Certolizumab pegol zachovává své lékové koncentrace stabilní bez signifikantních změn, zatímco anti‑TNF léčiva s Fc fragmentem mají sérové koncentrace snížené, což má negativní dopad na jejich klinickou účinnost. Teoretickým vysvětlením odlišné účinnosti anti‑TNF léčiv podle přítomnosti Fc fragmentu je předpoklad, že RF se může vázat na Fc část anti‑TNF protilátek a tím ovlivňovat jejich farmakokinetiku a snížit jejich terapeutickou účinnost. Certolizumab pegol tak může být výhodným lékem pro pacienty s RA a vysokými titry RF.
Klíčová slova: revmatoidní faktory – biologická léčba – certolizumab pegol.
Summary
Pavelka K, Šenolt L. Certolizumab pegol is very effective even in patients with rheumatoid arthritis and high titers of rheumatoid factors. Remedia 2025; 35: 42–46.
High titers of rheumatoid factors (RF) in patients with rheumatoid arthritis (RA) represent an adverse prognostic factor, being associated with higher disease activity, higher risk of radiographic progression, and lower responsiveness to treatment targeted against the tumor necrosis factor (anti‑TNF). Several trials including a large international cohort register‑based study have shown that rituximab and abatacept are more effective in patients with RF positivity while there are no data supporting different effectiveness of anti‑TNF agents. This article deals with new data obtained from analyses of pharmacological trials and registers during several past years. These studies have demonstrated that the structure of individual anti‑TNF agents, e.g. the presence or absence of Fc fragments, may influence serum concentrations of the medications and the effectiveness of therapy. Anti‑TNF agents with Fc fragments include monoclonal antibodies (infliximab, adalimumab and soluble receptor etanercept). Certolizumab pegol does not contain the Fc fragment. Trials demonstrating that RF titers at the beginning of therapy may influence effective concentrations of therapeutic agents and thus the clinical impact of the treatments are being presented. While serum concentrations of anti‑TNF drugs are not influenced in patients with low RF titers (< 200 IU/ml), differences may already be seen in patients with the highest RF titers (> 200 IU/ml). Certolizumab pegol keeps its stabile concentration with no significant changes unlike anti‑TNF agents with Fc fragment the concentrations of which become lower, with a negative impact on their clinical effectiveness. Theoretically, this feature may be explained by binding of RF to the Fc part of anti‑TNF antibodies, altering their pharmacokinetics and therapeutic effectiveness. Certolizumab pegol may thus be suitable for RA patients with high RF titers.
Key words: rheumatoid factors – biological therapy – certolizumab pegol.
Revmatoidní artritida (RA) je chronické autoimunitní onemocnění charakterizované polyartritidou, destrukcí kloubů, zhoršením jejich funkce a kvality života. Kolem 80 % pacientů s RA je tzv. séropozitivních, to znamená, že má pozitivní revmatoidní faktory (RF) a/nebo protilátky proti citrulinovaným peptidům (ACPA). RF se váží na Fc část imunoglobulinu G (IgG) a tvoří imunokomplexy, které hrají významnou roli v patogenezi RA. V kohortových studiích bylo prokázáno, že RF jsou nepříznivým prognostickým faktorem RA, jsou asociovány s vyšší aktivitou onemocnění a s rizikem rychlejší rentgenové progrese [1,2].
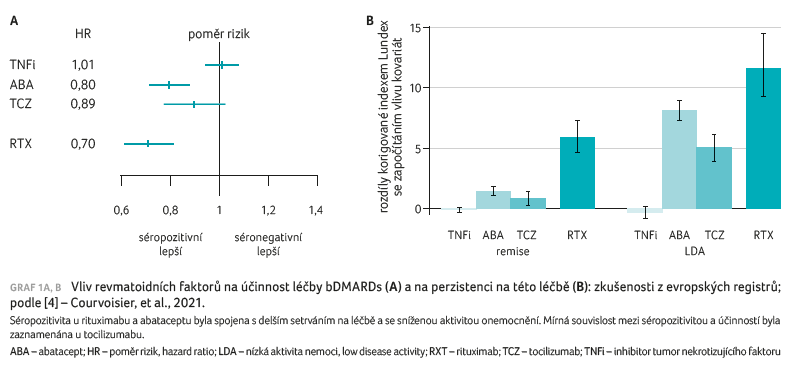 Přítomnost RF a ACPA může být důležitá pro výběr optimálního biologického léku modifikujícího průběh choroby (bDMARD). Byla provedena řada studií, které potvrdily, že séropozitivita může ovlivňovat účinnost bDMARD při léčbě RA. Metaanalýza studií autorů Lv a kol. prokázala, že séropozitivita neovlivňuje účinnost anti‑TNF léčby, zatímco účinnost rituximabu zvyšuje [3]. Souhrnná analýza 16 registrů zahrnula celkem 27 583 pacientů. Po adjustaci jednotlivých skupin a při použití indexu Lundex byla zvýšená šance na dosažení stavu nízké aktivity nemoci a remise u pacientů séropozitivních oproti séronegativním u rituximabu, dále u abataceptu, poněkud nižší byla u tocilizumabu a žádný rozdíl nebyl zaznamenán u anti‑TNF léčby [4], graf 1A, B. Limitací studie je ale fakt, že všechny anti‑TNF léky byly hodnoceny dohromady.
Přítomnost RF a ACPA může být důležitá pro výběr optimálního biologického léku modifikujícího průběh choroby (bDMARD). Byla provedena řada studií, které potvrdily, že séropozitivita může ovlivňovat účinnost bDMARD při léčbě RA. Metaanalýza studií autorů Lv a kol. prokázala, že séropozitivita neovlivňuje účinnost anti‑TNF léčby, zatímco účinnost rituximabu zvyšuje [3]. Souhrnná analýza 16 registrů zahrnula celkem 27 583 pacientů. Po adjustaci jednotlivých skupin a při použití indexu Lundex byla zvýšená šance na dosažení stavu nízké aktivity nemoci a remise u pacientů séropozitivních oproti séronegativním u rituximabu, dále u abataceptu, poněkud nižší byla u tocilizumabu a žádný rozdíl nebyl zaznamenán u anti‑TNF léčby [4], graf 1A, B. Limitací studie je ale fakt, že všechny anti‑TNF léky byly hodnoceny dohromady.
Odlišný přístup k hodnocení vlivu séropozitivity na účinnost anti‑TNF léčby zvolili japonští autoři, kteří použili retrospektivní data z kohortové studie ANSWER [5]. Vycházeli z předpokladu, že anti‑TNF léky mají odlišnou strukturu. Infliximab (INF), adalimumab (ADA) a golimumab (GOL) jsou plně funkční monoklonální IgG1 protilátky, které obsahují Fc část, INF je chimérická, ADA a GOL jsou plně humánní protilátky. Etanercept (ETA) je solubilní receptor anti‑TNF fúzovaný s Fc částí humánního IgG1. Certolizumab pegol (CZP) je monovalentní Fab fragment fúzovaný s polyetylenglykolem, který neobsahuje Fc fragment imunoglobulinu. Teoretickým předpokladem odlišné účinnosti anti‑TNF přípravků s Fc fragmentem a bez Fc fragmentu byl fakt, že RF se mohou vázat na Fc část a tím ovlivňovat jejich účinnost. Autoři studie vytvořili dvě skupiny pacientů; do jedné skupiny zařadili pacienty léčené INF, ADA, ETA a GOL a do druhé léčené CZP. Pacienti byli dále rozděleni do čtyř skupin podle výše titru RF. K hodnocení rozdílů mezi skupinami byla použita metodika mnohočetné lineární regrese. Primárním ukazatelem účinnosti bylo skóre DAS28 (disease activity score‑28 for rheumatoid arthritis) hodnocené v intervalech 3, 6 a 12 měsíců. Zatímco ve třech skupinách s nižšími a středními titry RF byl pouze určitý numerický trend ve prospěch CZP, ve skupině s nejvyššími titry byl rozdíl ve prospěch CZP signifikantní. Ve skupině s Fc fragmentem dosahovala hodnota DAS28 po 12 měsících 3,2 (2,3–4), ve skupině bez Fc fragmentu 2,7 (2,0–3,0). Při hodnocení potenciálních dalších přispívajících faktorů (confounders) bylo zjištěno, že titry RF byly nezávislým faktorem asociovaným s hodnotou DAS28. Tanaka a kol. pak analyzovali účinnost CZP v šesti studiích u časné a etablované RA a zjistili, že jeho účinnost zůstává stabilní bez ohledu na výši titru RF [6].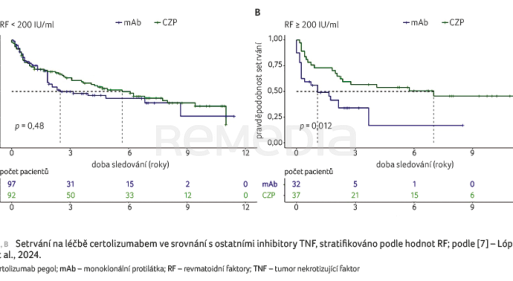
Hypotézu, zda je retence na léčbě odlišná mezi CZP a ostatními anti‑TNF přípravky (monoklonální protilátky, ETA), a to na základě titru RF na začátku léčby, si dala za cíl ověřit studie autorů López‑Medina a kol [7]. Do studie bylo zařazeno 638 pacientů a hodnoceno bylo 752 terapeutických period. Pacienti byli rozděleni do skupiny CZP a ostatní anti‑TNF léky. Po adjustaci skupin za použití propensity skóre byly stanoveny bazální hodnoty RF a pacienti byli zařazeni do skupin s titry RF ≥ 200 IU/ml a s RF < 200 IU/ml. Pacienti s RF ≥ 200 IU/ml měli delší retenci na CZP než na anti‑TNF monoklonálních protilátkách (poměr rizik [hazard ratio, HR] 2,3, 95% interval spolehlivosti [confidence interval, CI] 1,2–4,3) nebo ETA (HR 2,8, 95% CI 1,5–5,2), graf 2A, B. Ve skupině s titry RF < 200 IU/ml nebyly rozdíly mezi CZP a anti‑TNF přípravky průkazné. Tyto rozdíly byly zjištěny nezávisle na věku, současném užívání metotrexátu nebo na předchozí léčbě bDMARD. Výsledky této studie tedy podporují hypotézu o možné roli Fc fragmentu (který není u CZP přítomen) při neutralizaci efektu anti‑TNF léků vazbou RF na Fc část.
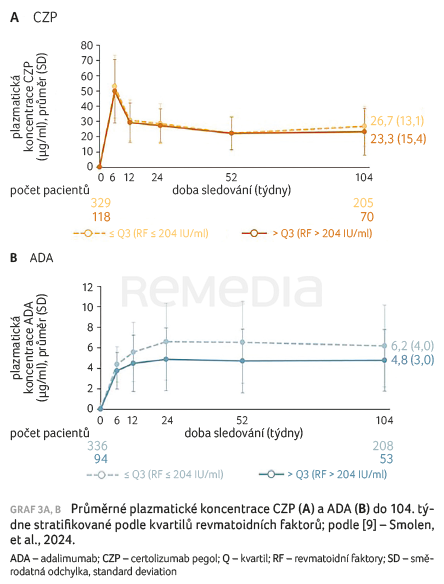 Velmi významnou studií, která mohla řešit význam séropozitivity pro účinnost různých anti‑TNF přípravků, byla EXXELERATE [8]. Byla ojedinělá v tom, že šlo o srovnávací studii (tzv. head‑to‑head) mezi CZP a ADA. Metodologicky vzato se jednalo o randomizované, zaslepené klinické hodnocení (dvojitě zaslepené do týdne 12 a pro investigátora zaslepené až do týdne 104). Jednalo se o tzv. superioritní studii, která měla prokázat vyšší účinnost (superioritu) CZP oproti ADA. Primární cíl studie nebyl splněn; superiorita nebyla prokázána. Nicméně zajímavé výsledky přinesla post hoc subanalýza studie, která hodnotila dvě skupiny pacientů léčených anti‑TNF bez Fc fragmentu (CZP) a anti‑TNF s Fc částí (ADA) podle vstupních hodnot RF. Do studie bylo zařazeno celkem 453 pacientů léčených CZP a 454 s léčbou ADA. Pacienti byli rozděleni do čtyř skupin podle výše hodnot RF bazálně. Od týdne 12 byla plocha pod křivkou koncentrace ADA v kvartilu s nejvyššími hodnotami RF (> 204 IU/ml) signifikantně nižší než u pacientů léčených ADA s titry RF < 204 IU/ml. Ve skupině léčené CZP ale nebyly zjištěny žádné rozdíly v sérové koncentraci léku mezi pacienty s vysokými a nízkými titry RF, graf 3A, B. Pro pacienty s nízkými titry RF (< 204 IU/ml) byla účinnost léčby při hodnocení pomocí DAS28 stejná pro CZP i ADA, ale u pacientů s vysokými titry RF (> 204 IU/ml) byly hodnoty DAS28 nižší pro CZP než pro ADA. Rozdíl byl nejen signifikantní numericky, ale převyšoval hodnoty klinicky významného rozdílu. Studie tedy potvrdila hypotézu, že anti‑TNF přípravek bez Fc fragmentu u pacientů s vysokými titry RF na rozdíl od anti‑TNF léku s Fc fragmentem nevede ke snížení sérové koncentrace léků a je také u těchto pacientů účinnější. Vliv titru ACPA nebyl v této studii zjištěn [9].
Velmi významnou studií, která mohla řešit význam séropozitivity pro účinnost různých anti‑TNF přípravků, byla EXXELERATE [8]. Byla ojedinělá v tom, že šlo o srovnávací studii (tzv. head‑to‑head) mezi CZP a ADA. Metodologicky vzato se jednalo o randomizované, zaslepené klinické hodnocení (dvojitě zaslepené do týdne 12 a pro investigátora zaslepené až do týdne 104). Jednalo se o tzv. superioritní studii, která měla prokázat vyšší účinnost (superioritu) CZP oproti ADA. Primární cíl studie nebyl splněn; superiorita nebyla prokázána. Nicméně zajímavé výsledky přinesla post hoc subanalýza studie, která hodnotila dvě skupiny pacientů léčených anti‑TNF bez Fc fragmentu (CZP) a anti‑TNF s Fc částí (ADA) podle vstupních hodnot RF. Do studie bylo zařazeno celkem 453 pacientů léčených CZP a 454 s léčbou ADA. Pacienti byli rozděleni do čtyř skupin podle výše hodnot RF bazálně. Od týdne 12 byla plocha pod křivkou koncentrace ADA v kvartilu s nejvyššími hodnotami RF (> 204 IU/ml) signifikantně nižší než u pacientů léčených ADA s titry RF < 204 IU/ml. Ve skupině léčené CZP ale nebyly zjištěny žádné rozdíly v sérové koncentraci léku mezi pacienty s vysokými a nízkými titry RF, graf 3A, B. Pro pacienty s nízkými titry RF (< 204 IU/ml) byla účinnost léčby při hodnocení pomocí DAS28 stejná pro CZP i ADA, ale u pacientů s vysokými titry RF (> 204 IU/ml) byly hodnoty DAS28 nižší pro CZP než pro ADA. Rozdíl byl nejen signifikantní numericky, ale převyšoval hodnoty klinicky významného rozdílu. Studie tedy potvrdila hypotézu, že anti‑TNF přípravek bez Fc fragmentu u pacientů s vysokými titry RF na rozdíl od anti‑TNF léku s Fc fragmentem nevede ke snížení sérové koncentrace léků a je také u těchto pacientů účinnější. Vliv titru ACPA nebyl v této studii zjištěn [9].
Vliv titru RF na sérové koncentrace inhibitorů TNF s různou strukturou byl také hodnocen ve studii Martineze-Feito a kol. [10]. Šlo o retrospektivní studii z běžné klinické praxe. Celkem bylo zařazeno 170 pacientů s RA, z nichž 90 dostávalo INF, 48 ADA a 32 CZP. Pacienti byli stratifikováni podle titrů RF na skupinu s negativním RF, nízkým RF, středním RF a vysokým titrem RF na začátku léčby. Po šesti měsících léčby nebyly zjištěny žádné rozdíly ve skupinách s různými titry RF pro CZP, ve skupině s Fc fragmentem (ADA, INF) však byly u pacientů s vysokými titry RF zjištěny signifikantně nižší lékové hladiny. Pacienti s vysokými bazálními titry RF také častěji ukončovali léčbu pro sekundární selhání léčby INF a ADA, než tomu bylo v případě CZP (80 % vs. 33 % p = 0,002). Závěry této studie opět potvrzují, že sérové koncentrace CZP nejsou ovlivněny titry RF. Naopak u kompletních protilátek s Fc fragmentem (ADA, INF) jsou vysoké titry RF asociovány s nižšími sérovými koncentracemi léku a častějším terapeutickým selháním. V této studii nebyl prokázán žádný vliv ACPA protilátek na koncentraci biologického léku.
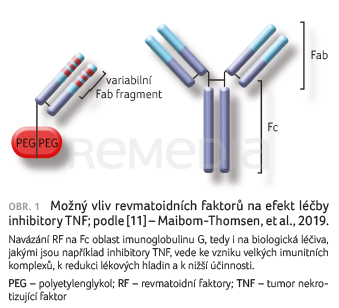 Jaká je hypotéza vysvětlující fakt větší účinnosti CZP než ADA u pacientů s RA? To, že hodnoty ACPA neovlivňovaly sérovou koncentraci léků, zatímco vysoké titry RF měly vliv pouze u pacientů léčených kompletními monoklonálními protilátkami obsahujícími Fc fragment, ale ne u pacientů léčených protilátkami bez tohoto fragmentu, zdůrazňuje klíčovou roli Fc fragmentu v tomto procesu. Je možné předpokládat, že navázání RF na Fc oblast IgG, včetně biologických léčiv, jakými jsou anti‑TNF přípravky, vede ke vzniku velkých imunitních komplexů, což může způsobit snížení lékových hladin a následně i nižší klinickou účinnost [11], obr. 1.
Jaká je hypotéza vysvětlující fakt větší účinnosti CZP než ADA u pacientů s RA? To, že hodnoty ACPA neovlivňovaly sérovou koncentraci léků, zatímco vysoké titry RF měly vliv pouze u pacientů léčených kompletními monoklonálními protilátkami obsahujícími Fc fragment, ale ne u pacientů léčených protilátkami bez tohoto fragmentu, zdůrazňuje klíčovou roli Fc fragmentu v tomto procesu. Je možné předpokládat, že navázání RF na Fc oblast IgG, včetně biologických léčiv, jakými jsou anti‑TNF přípravky, vede ke vzniku velkých imunitních komplexů, což může způsobit snížení lékových hladin a následně i nižší klinickou účinnost [11], obr. 1.
Výsledky výše uvedených studií konzistentně potvrzují, že u pacientů s vysokými titry RF je certolizumab pegol vhodnou volbou, jelikož si u těchto pacientů udržuje stabilně vysoké hladiny a vykazuje vyšší klinickou účinnost než anti‑TNF přípravky obsahující Fc fragment.
Vypracováno za podpory MZ ČR 00023728.
Prof. MUDr. Karel Pavelka, DrSc.
Revmatologický ústav
Na Slupi 450, 128 00 Praha
e-mail: pavelka@revma.cz
Literatura
[1] Katchamart W, Koolvisoot A, Aromdee E, et al. Associations of rheumatoid factor and anti CCP with disease progression and treatment outcomes in patients with rheumatoid arthritis. Rheumatol Int 2015; 36: 1693–1699.
[2] Cuchacovich M, Bueno D, Carvajal R, et al. Clinical parameters and biomarkers for anti‑TNF treatment prognosis in rheumatoid arthritis patients. Clin Rheumatol 2014; 33: 1707–1714.
[3] Lv Q, Yin Y, Li X, et al. The status of rheumatoid factor and anti CCP are not associated with the effect of anti agent treatment in patients with rheumatoid arthritis: a metaanalysis. PLoS One 2014; 9: e89442.
[4] Courvoisier DS, Chatzidionysiou K, Mongin D, et al. The impact of seropositivity on the effectivness of biologic anti‑rheumatic agents: results from a collaboration of 16 registries. Rheumatology (Oxford) 2021; 60: 820–828.
[5] Nakayama Y, Watanabe R, Murakami K, et al. Differential efficacy of anti‑TNF inhibitots with and without the immunoglobulin fragment crystallizable /FC/ portion in rheumatoid arthritis:the ANSWWER cohort study. Rheumatol Int 2022; 42: 1227–1234.
[6] Tanaka Y, Takeuchi T, Haaland D, et al. Efficacy of certolizumab pegol across baseline rheumatoid factor subgroups in patients with rheumatoid arthritis: Post‑hoc analysis of clinical trials. Int J Rheumatol Dis 2023; 26: 1248–1259.
[7] López‑Medina C, Calvo‑Gutiérrez, Ábalos‑Aquilera MC, et al. Exploring the influence of baseline RF levels in TNF inhibitor retension rate in patients with rheumatoid arthritis. RMD Open 2024; 10: e003975.
[8] Smolen J, Burmester GR, Combe B, et al. Head to head comparison of certolizumab pegol versus adlimumab un rheumatoid arthritis: 2 year results efficacy and safety results from the randomised EXXELERATE study. Lancet 2016; 388: 2763–2774.
[9] Smolen J, Taylor PC, Tanaka Y, et al. Impact of high RF levels on treatment outcomes with certolizumab pegol and adalimumab in patients with rheumatoid arthritis. Rheumatology 2024; 63: 3015–3024.
[10] Martínez‑Feito A, Plasencia‑Rodríguez C, Novella‑Navarro M, et al. Influence rheumatoid factor on serum drug levels of anti‑TNF inhibitors with different strastions in rheumatoid arthritis. Clin Exp Rheumatol 2024; 42: 999–1005.
[11] Maibom‑Thomsen SL, Trier NH, Holm BE, et al. Imunoglobulin G structures and RF epitopes, Plos One 2019. Dostupné na: https://doi.org/10.1371/journal.pone.0217624.