Genová léčba spinální svalové atrofie
Spinální svalová atrofie je charakterizována progresivní svalovou slabostí a atrofií s následnými poruchami hybnosti, dýchacími a polykacími potížemi a opožděným motorickým vývojem. V rámci 37. českého a slovenského neurologického sjezdu, který se konal v Clarion Congress Hotelu Ostrava ve dnech 27.–29. listopadu 2024, věnovala tomuto onemocnění svoji přednášku MUDr. Lenka Juříková z Kliniky dětské neurologie Fakultní nemocnice Brno.
„Jsem ráda, že jako dětský neurolog mohu přiblížit problematiku tohoto oboru, protože genová léčba spinální svalové atrofie je zatím omezena pouze na pediatrické pacienty, nicméně tato choroba se zdaleka netýká jen dětí, ale i dospělých osob,“ uvedla svoji prezentaci přednášející.
Charakteristika onemocnění a fenotypy
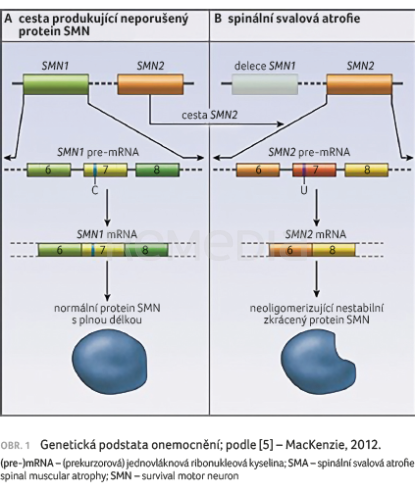 Spinální svalová atrofie (spinal muscular atrophy, SMA) představuje skupinu geneticky podmíněných degenerativních chorob, které postihují alfa motoneurony předních rohů míšních. Většina pacientů se SMA má deleci 7. a/nebo 8. exonu genu SMN1 zodpovědného za tvorbu proteinu SMN (survival motor neuron). Tento protein, jak už název napovídá, je nezbytný pro přežití motorických neuronů. Nositelem mutace genu SMN1 je jedna z 58 osob. U pacientů naštěstí ještě existuje druhý gen – SMN2, který také částečně tvoří protein SMN, a čím více kopií SMN2 nemocní mají, tím příznivější je jejich fenotyp [1–4]. Genetickou podstatu onemocnění ilustruje obrázek 1 [5].
Spinální svalová atrofie (spinal muscular atrophy, SMA) představuje skupinu geneticky podmíněných degenerativních chorob, které postihují alfa motoneurony předních rohů míšních. Většina pacientů se SMA má deleci 7. a/nebo 8. exonu genu SMN1 zodpovědného za tvorbu proteinu SMN (survival motor neuron). Tento protein, jak už název napovídá, je nezbytný pro přežití motorických neuronů. Nositelem mutace genu SMN1 je jedna z 58 osob. U pacientů naštěstí ještě existuje druhý gen – SMN2, který také částečně tvoří protein SMN, a čím více kopií SMN2 nemocní mají, tím příznivější je jejich fenotyp [1–4]. Genetickou podstatu onemocnění ilustruje obrázek 1 [5].
Každý rok se v České republice narodí zhruba 10 dětí s tímto vzácným onemocněním a kolem 60 % pacientů má ten nejtěžší fenotyp označovaný jako typ 1, který je charakterizován rychlou progresí s ireverzibilní ztrátou motoneuronů. Jedná se tedy o ty nemocné, kteří by bez léčby umírali v časném věku. Toto vše činí ze SMA druhou nejčastější závažnou dědičnou nemoc hned po cystické fibróze [3,6–12].
Pacienti se SMA typu 1 mají maximálně dvě kopie genu SMN2 a onemocnění u nich velmi rychle progreduje – už v prvních šesti měsících je ztraceno až 95 % motoneuronů. Přibližně 92 % těchto dětí bez léčby umíralo před dosažením věku dvou let. Pokud tito pacienti přežívali, byli nehybní a kvalita jejich života byla velmi špatná [8,10,11,13–19].
U druhého typu SMA se při přirozeném průběhu onemocnění bez efektivní léčby jedná o pacienty, kteří prakticky nikdy nechodí. Jsou to děti schopné samostatně sedět, ale chůze u nich není možná, mají velmi těžkou skoliózu. Přežívání je u těchto pacientů podstatně lepší – asi 70 % jedinců je stále naživu ve věku 25 let. V pozdějším věku však nastupují výrazné komplikace, např. dechové.
Nejmírnější variantu nemoci představuje typ 3, kdy je řada pacientů schopna chůze v dětském věku, nicméně i u nich onemocnění progreduje. Přežívají do dospělosti, ale samozřejmě v průběhu života trpí těžkým postižením – jsou to stále pacienti, které bychom měli odhalovat i v dospělé neurologii [20,21].
Diagnostika a léčba
Diagnostika SMA se v případě dětského věku až donedávna opírala především o klinický obraz. Při stanovení diagnózy příliš nepomáhá zjištění hodnoty kreatinkinázy, které běžně používáme u svalových onemocnění, neboť je u většiny pacientů se SMA v normě. Co nám naopak velmi pomůže, je elektromyografické vyšetření, kde se objevuje typický obraz denervace, a nejdůležitější je genetické vyšetření. V současné době jsou na toto genetické vyšetření odesílány všechny děti s podezřením na SMA, a to z toho důvodu, že existuje dostupná léčba. A rovněž je důležitá aktuální dostupnost novorozeneckého screeningu.
Onemocnění je aktuálně ovlivnitelné léčbou. Do roku 2016 jsme pacientům mohli nabídnout léky typu kyselina valproová nebo karnitin, které však byly bez většího efektu. V roce 2016 byl americkým Úřadem pro kontrolu potravin a léčiv (FDA) a v roce 2017 Evropskou lékovou agenturou (EMA) schválen první lék pro terapii SMA nusinersen, o tři roky později byla schválena genová terapie přípravkem onasemnogen abeparvovek a v roce 2020, resp. 2021 risdiplam [22–27].
Genová terapie onasemnogenem abeparvovekem
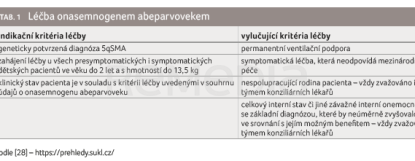 Onasemnogen abeparvovek představuje první genovou terapii SMA. Jedná se o vektor na bázi nereplikujícího rekombinantního adenoasociovaného viru sérotypu 9 (AAV9) obsahující cDNA lidského genu SMN pod kontrolou hybridového promotoru tvořeného cytamegalovirovým „enhancerem“ a kuřecím β‑aktinovým promotorem. Tato léčba je v ČR indikována pro dětské pacienty ve věku do dvou let s hmotností do 13,5 kg. Pacienti mohou být v době začátku léčby asymptomatičtí i symptomatičtí, nicméně jejich klinický stav musí odpovídat kritériím pro zahájení této terapie (viz tab. 1) [28]. Oproti léčbě nusinersenem nebo risdiplamem je genová terapie omezena počtem kopií genu SMN2 (2 nebo 3 kopie).
Onasemnogen abeparvovek představuje první genovou terapii SMA. Jedná se o vektor na bázi nereplikujícího rekombinantního adenoasociovaného viru sérotypu 9 (AAV9) obsahující cDNA lidského genu SMN pod kontrolou hybridového promotoru tvořeného cytamegalovirovým „enhancerem“ a kuřecím β‑aktinovým promotorem. Tato léčba je v ČR indikována pro dětské pacienty ve věku do dvou let s hmotností do 13,5 kg. Pacienti mohou být v době začátku léčby asymptomatičtí i symptomatičtí, nicméně jejich klinický stav musí odpovídat kritériím pro zahájení této terapie (viz tab. 1) [28]. Oproti léčbě nusinersenem nebo risdiplamem je genová terapie omezena počtem kopií genu SMN2 (2 nebo 3 kopie).
Před léčbou onasemnogenem abeparvovekem je nutné stanovit titr anti‑AAV9 protilátek. Většina pacientů má tento titr negativní, občas se však stává – hlavně u pacientů, kteří jsou odhaleni díky novorozeneckému screeningu –, že je přechodně pozitivní titr anti‑AAV9 protilátek přenesených od matky. V tuto chvíli nemůže tedy být u pacientů genová terapie zahájena a jsou přechodně léčeni nusinersenem nebo risdiplamem. Po úpravě titru jsou pak indikováni k léčbě onasemnogenem abeparvovekem.
Lék se vyrábí pro každého pacienta individuálně, je tedy nutné odeslat objednávku na výrobu, v níž nejdůležitějším kritériem je hmotnost nemocného. Za velmi přísných podmínek a při teplotě –60 °C je poté lék transportován do lékárny nemocnice, v níž bude léčba podána. Jakmile je pacient připraven na aplikaci, přípravek je rozmražen a do osmi hodin při uchování v lednici je nutné jej aplikovat.
Samotná aplikace je jednoduchá, jedná se o klasickou žilní infuzi, která probíhá jednu hodinu. Zajišťuje se klasický periferní vstup a injektor, pacient je po celou dobu aplikace monitorován. S lékem zacházíme na úrovni stupně biologické bezpečnosti 1, je to virový vektor, proto je doporučeno používat ochranné pomůcky. AAV9 vektor není schopen replikace, je neinfekční a je citlivý na běžné dezinfekční prostředky. Virus se po podání vylučuje močí a stolicí (močí dokonce několik týdnů), na což je nutné upozornit rodinu kvůli adekvátní likvidaci odpadu.
Zaznamenané nežádoucí účinky léčby onasemnogenem abeparvovekem jsou relativně méně závažné a ovlivnitelné a je možno se na ně připravit. Patří k nim především elevace hodnot transamináz, trombocytopenie, změny srdečního rytmu a změny hodnoty troponinu I. Celosvětově byla popsána tři úmrtí u pacientů, jimž byla podána genová terapie, nicméně po provedení pitvy bylo prokázáno, že tato úmrtí nesouvisela s danou léčbou [28,29]. Všichni pacienti s genovou terapií musejí přechodně užívat kortikoterapii, neboť rekombinantní AAV9 vektor vykazuje určitou míru imunogenicity. Kortikosteroidy (ve standardním dávkování 1 mg/kg) jsou podány 24 hodin před plánovanou genovou terapií, pacienti v ní pokračují minimálně měsíc, a pokud jsou laboratorní hodnoty (především jaterní testy a trombocyty) v pořádku, další měsíc se dávka kortikosteroidů snižuje. Jestliže dochází k pomalejší úpravě stavu, pokračuje kortikoterapie delší dobu [28].
Důležitá je monitorace pacientů po genové terapii. Po dobu tří měsíců je nutná kontrola každý týden, nejen z klinického hlediska, ale především laboratorních hodnot – krevních destiček a jaterních parametrů. Podle nových doporučení mají být jaterní funkce kontrolovány v prvních dvou měsících každý týden. Jestliže jsou po prvním měsíci jaterní testy v pořádku, kontrola v nemocnici probíhá jednou za 14 dní a kontrola u praktického lékaře jednou za týden. Opatření směřují k detekci nežádoucích účinků – akutního jaterního selhání a trombotické mikroangiopatie [28].
Novorozenecký screening
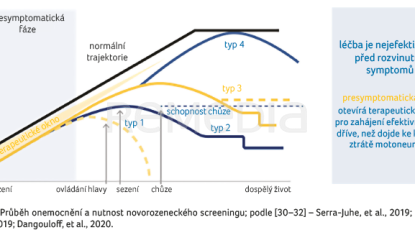 Efekt terapie závisí nejen na tom, kolik kopií genu SMN2 dítě má, ale také na včasnosti podání léčby (graf 1) [30–32].
Efekt terapie závisí nejen na tom, kolik kopií genu SMN2 dítě má, ale také na včasnosti podání léčby (graf 1) [30–32].
Od roku 2022 v České republice funguje novorozenecký screening SMA a současně těžkého imunodeficitu. V letech 2022 a 2023 probíhal pilotní screening. Projektu se zúčastnili téměř všichni porodníci, ale bylo nutné získat informovaný souhlas rodičů. V rámci screeningu bylo otestováno více než 90 % novorozenců a došlo k záchytu zhruba 10 pacientů ročně. Tito nemocní jsou následně odesláni do specializovaného centra v pražské FN Motol nebo ve FN Brno. Testování probíhá stejně jako klasický test na metabolická novorozenecká onemocnění. Pokud je výsledek pozitivní, rodina je okamžitě kontaktována a přizvána do nemocnice, kde je provedeno genetické vyšetření. Jeho výsledky jsou k dispozici do 24 hodin a v případě potvrzení diagnózy lze u pacienta zahájit léčbu. Od ledna 2024 je vyšetření SMA součástí běžného screeningu vrozených onemocnění.
Kazuistika
V závěru prezentace představila MUDr. Juříková kazuistiku chlapce Matěje narozeného v červnu 2024, na jehož případu demonstrovala ukázkového pacienta odhaleného na základě novorozeneckého screeningu. Kvůli pozitivnímu výsledku screeningu byl Matěj devět dní po narození odeslán k hospitalizaci na Dětskou interní kliniku FN Brno. V objektivním nálezu už byly patrné známky onemocnění – hypotonie, hyporeflexie a mírné fascikulace jazyka. Chlapec byl ihned indikován k doplnění genetického vyšetření, jehož výsledek byl k dispozici 11. den věku dítěte a prokázal deleci exonu 7 a 8 genu SMN1 a tři kopie genu SMN2. Bez léčby by se tedy jednalo o klasického pacienta se SMA 2. typu. V ten samý den byla zahájena terapie risdiplamem, kterou chlapec snášel velmi dobře, a prakticky hned druhý den bylo znát, že je dítě aktivnější a lépe jí. Následně byla podána žádost o zahájení genové terapie. Uvedená léčba je nákladná a na vyjádření od zdravotní pojišťovny se čeká přibližně po dobu jednoho měsíce. I po toto období je však možné pacienty léčit právě risdiplamem nebo nusinersenem, tedy tzv. bridging terapií, díky níž mohou být nemocní adekvátně zaléčeni už v den potvrzení onemocnění.
Třicátý den byla pro Matěje k dispozici genová terapie. Pacient byl hospitalizován na jednotce intenzivní péče kvůli monitoraci stavu. Hypotonie u něj přetrvávala, nicméně reflexy už byly výbavné, byla zlepšena aktivní hybnost zejména na dolních končetinách a fascikulace jazyka už nebyly pozorovány. Ve vstupních testech bylo zaznamenáno 46 bodů, což je zhruba počet u zdravého novorozence. Třicátý první den byla chlapci podána genová terapie, kterou toleroval bez problémů bez jakýchkoliv nežádoucích účinků, došlo pouze k přechodnému výraznému zvýšení hodnot D dimerů, jež se ale postupně normalizovaly. Dokonce nebyla v tomto případě pozorována hepatopatie ani trombocytopenie. Preventivně byl pacientovi podán prednison s postupným vysazováním v následujícím měsíci a byla zahájena rehabilitace. Deset dní po aplikaci genové terapie byl chlapec propuštěn domů a následovaly týdenní a poté měsíční kontroly.
Vývoj Matěje odpovídal v listopadu 2024 věku šest měsíců, byl pouze lehce hypotonický. „Vše tedy nasvědčuje tomu, že se chlapec bude vyvíjet prakticky normálně,“ uzavřela svoji přednášku MUDr. Juříková.
Tématu spinální svalové atrofie se budeme věnovat také v příštím čísle časopisu Remedia.
Literatura
[1] Mercuri E, Finkel RS, Muntoni F, et al. Diagnosis and management of spinal muscular atrophy: Part 1: recommendations for diagnosis, rehabilitation, orthopedic and nutritional care. Neuromuscul Disord 2018; 28: 103–115.
[2] Kolb SJ, Kissel JT. Spinal Muscular Atrophy. Neurol Clin 2015; 33: 831–846.
[3] D’Amico A, Mercuri E, Tiziano FD, Bertini E. Spinal Muscular Atrophy. Orphanet J Rare Dis 2011; 6: 71.
[4] Lunn MR, Wang CH. Spinal Muscular Atrophy. Lancet 2008; 371: 2120–2133.
[5] MacKenzie A. Sense in Antisense Therapy for Spinal Muscular Atrophy. N Engl J Med 2012; 366: 761–763.
[6] Farrar MA, Kieran MC. The Genetics of Spinal Muscular Atrophy: Progress and Challenges. Neurotherapeutics 2015; 12: 290–302.
[7] Verhaart IEC, Robertson A, Wilson IJ, et al. Prevalence, incidence and carrier frequency of 5q‑linked spinal muscular atrophy – a literature review. Orphanet J Rare Dis 2017; 12: 124.
[8] Glascock J, Sampson J, Haidet‑Philips A, et al. Treatment Algorithm for Infants Diagnosed with Spinal Muscular Atrophy through Newborn Screening. J Neuromuscul Dis 2018; 5: 145–158.
[9] Swoboda KJ, Prior TW, Scott CB, et al. Natural history of denervation in SMA: relation to age, SMN2 copy number, and function. Ann Neurol 2005; 57: 704–712.
[10] Kolb SJ, Coffey CS, Yankey JW, et al. Natural history of infantile‑onset spinal muscular atrophy. Ann Neurol 2017; 82: 883–891.
[11] Govoni A, Gagliardi D, Comi GP, Corti S. Time Is Motor Neuron: Therapeutic Window and Its Correlation with Pathogenetic Mechanisms in Spinal Muscular Atrophy. Mol Neurobiol 2018; 55: 6307–6318.
[12] Armstrong EP, Malone DC, Yeh W‑S, et al. The economic burden of spinal muscular atrophy. J Med Econ 2016; 19: 822–826.
[13] Lin C‑W, Kalb SJ, Yeh W‑S, et al. Delay in Diagnosis of Spinal Muscular Atrophy: A Systematic Literature Review. Ped Neural 2015; 53: 293–300.
[14] Chien Y‑H, Chiang S‑C, Weng W‑C, et al. Presymptomatic Diagnosis of Spinal Muscular Atrophy Through Newborn Screening. J Pediatr 2017; 190: 124–129.e1.
[15] Prior TW, Leach ME, Finanger EL. Spinal Muscular Atrophy. 2000 Feb 24 [Updated 2019 Nov 14]. In: Adam MP, Ardinger HH, Pagon RA, et al (ed). GeneReviews® [Internet]. Seattle (WA): University of Washington, Seattle; 1993–2020.
[16] De Sanctis R, Coratti G, Pasternak A, et al. Developmental milestones in type I spinal muscular atrophy. Neuromusc Disord 2016; 26: 754–759.
[17] Finkel RS, McDermott MP, Kaufmann P, et al. Observational study of spinal muscular atrophy type I and implications for clinical trials. Neurology 2014; 83: 810–817.
[18] Mendell JR, Al‑Zaidy S, Shell R, et al. Single‑Dose Gene‑Replacement Therapy for Spinal Muscular Atrophy. N Engl J Med 2017; 377: 1713–1722.
[19] Saffari A, Kölker S, Hoffmann GF, et al. Novel challenges in spinal muscular atrophy – How to screen and whom to treat? Ann Clin Transl Neurol 2019; 6: 197–205.
[20] Chen T‑H. New and Developing Therapies in Spinal Muscular Atrophy: From Genotype to Phenotype to Treatment and Where Do We Stand? Int J Mol Sci 2020; 21: 3297.
[21] Qian Y, McGraw S, Henne J, et al. Understanding the experiences and needs of individuals with Spinal Muscular Atrophy and their parents: a qualitative study. BMC Neurology 2015; 15: 217.
[22] Talbot K, Tizzano EF. The clinical landscape for SMA in a new therapeutic era. Gene Ther 2017; 24: 529–533.
[23] Gidaro T, Servais L. Nusinersen treatment of spinal muscular atrophy: current knowledge and existing gaps. Dev Med Child Neurol 2019; 61: 19–24.
[24] Farrar MA, Park SB, Vucic S, et al. Emerging therapies and challenges in spinal muscular atrophy. Ann Neurol 2017; 81: 355–368.
[25] Onasemnogene abeparvovec‑xioi BLA Approval. Food and Drug Administration. Dostupné na: https://www.fda.gov/media/126130/download [navštíveno září 2022]
[26] New gene therapy to treat spinal muscular atrophy (corrected). European Medicines Agency. Dostupné na: https://www.ema.europa.eu/en/news/new‑gene‑therapy‑treat‑spinal‑muscular‑atrophy‑corrected [navštíveno září 2022]
[27] SPC Evrysdi. Dostupné na: https://ec.europa.eu/health/documents/community‑register/2023/20230816160248/anx_160248_cs.pdf
[28] https://prehledy.sukl.cz/
[29] Day JW, Mendell JR, Mercuri E, et al. Clinical Trial and Postmarketing Safety of Onasemnogene Abeparvovec Therapy. Drug Saf 2021; 44: 1109–1119.
[30] Serra‑Juhe C, Tizzano EF. Perspectives in genetic counseling for spinal muscular atrophy in the new therapeutic era: early pre‑symptomatic intervention and test in minors. Eur J Human Genet 2019; 27: 1774–1782.
[31] De Vivo DC, Bertini E, Swoboda KJ, et al. Nusinersen initiated in infants during the presymptomatic stage of spinal muscular atrophy: Interim efficacy and safety results from the Phase 2 NURTURE study. Neuromuscul Disord 2019; 29: 842–856.
[32] Dangouloff T, Vrščaj E, Servais L, Osredkar D. Newborn screening programs for spinal muscular atrophy worldwide: Where we stand and where to go. Neuromuscul Disord 2020; 30: 93–103.