Kde hledat klíč k úspěchu v léčbě psoriatické artritidy a ankylozující spondylitidy
Aspektům úspěšné léčby psoriatické artritidy a ankylozující spondylitidy věnovali v rámci sympozia společnosti Novartis na Zimních revmatologických dnech své přednášky MUDr. Jana Hurňáková, Ph.D., a prof. MUDr. Ladislav Šenolt, Ph.D.
Lze zabránit vývoji psoriatické artritidy, či alespoň oddálit její nástup?
MUDr. Jana Hurňáková, Ph.D., z Oddělení revmatologie dětí a dospělých FN Motol ve své přednášce shrnula poznatky o přechodu psoriázy do psoriatické artritidy (PsA) a zaměřila se na otázku, zda je možné u některých pacientů s psoriázou včasnou terapeutickou intervencí zabránit budoucímu rozvoji PsA.
Psoriatická artritida se vyvine přibližně u jedné třetiny pacientů s psoriázou, obvykle za 7–10 let. V roce 2023 představili Zabotti a kol. nomenklaturu přechodu psoriázy do PsA a definovali čtyři stadia:
- psoriáza;
- zvýšené riziko rozvoje PsA – pacient trpí psoriázou a má přítomny rizikové faktory (např. závažné kožní postižení, postižení nehtů, vysoký index tělesné hmotnosti [BMI], PsA v rodinné anamnéze);
- subklinická PsA – pacient s psoriázou má přítomny artralgie a/nebo zobrazovacími metodami prokazatelné zánětlivé postižení synovie/entezí, ale bez klinické synovitidy;
- klinicky manifestní PsA – psoriáza doprovázená klinickou synovitidou [1].
Aby bylo možné předejít rozvoji PsA, je klíčové určit správný moment pro terapeutickou intervenci, tedy identifikovat tzv. okno příležitosti. Ideálním scénářem by bylo zahájit u pacientů s psoriázou preventivní léčbu, která by v budoucnu zabránila vzniku PsA. V této souvislosti je důležité zvážit, zda léky s různými mechanismy účinku mohou mít odlišný vliv na prevenci nebo oddálení rozvoje PsA.
Studie prevence vývoje psoriázy do PsA
MUDr. Hurňáková ve své prezentaci představila výsledky šesti retrospektivních studií, které byly zaměřeny na prevenci přechodu psoriázy do PsA a provedeny na základě analýzy elektronických zdravotních záznamů. První, menší studie naznačila, že roční incidence PsA je nižší u pacientů léčených biologickými chorobu modifikujícími antirevmatickými léky (bDMARDs) ve srovnání s fototerapií. Druhá studie potvrdila, že biologická léčba snižuje riziko rozvoje PsA ve srovnání s topickou terapií, avšak významný rozdíl oproti pacientům léčeným konvenčními syntetickými DMARDs (csDMARDs) nebyl zaznamenán [2,3]. V následujících letech byly publikovány studie na větších kohortách. Meer a kol. analyzovali data více než 200 000 pacientů a zjistili, že terapie biologickými léky je spojena s vyšším rizikem rozvoje PsA [4]. Autoři však tento výsledek přisuzují protopatickému biasu, tedy situaci, kdy pacienti zařazení do studie mohli mít časné příznaky PsA ještě před zahájením léčby. Ve studii Singly a kol. autoři zjistili, že pacienti léčení bDMARDs mají nižší riziko přechodu do PsA, a zároveň upozornili na rozdíly mezi jednotlivými biologickými léky [5]. Výsledky mírně favorizovaly inhibitory interleukinu (IL)‑12/23 a IL‑23 (IL‑12/23i, IL‑23i) oproti inhibitorům tumor nekrotizujícího faktoru (TNFi) a inhibitorům IL‑17 (IL‑17i). Podobné závěry přinesla i studie Strobera a kol. z roku 2024, která na vzorku 7 000 pacientů prokázala, že inhibice IL‑23 je účinnější ve snížení rizika rozvoje inflamatorní artropatie ve srovnání s IL‑17i a TNFi [6]. Koncem loňského roku byla publikována rozsáhlá izraelská studie s kohortou téměř 60 000 pacientů, která potvrdila, že riziko přechodu do PsA je nižší u pacientů léčených biologiky ve srovnání s metotrexátem (MTX) [7]. Mezi jednotlivými bDMARDs však nebyl zjištěn významný rozdíl.
Limitace analýzy a intepretace dat retrospektivních studií
Přednášející, která podrobně analyzovala uvedené studie, zdůraznila omezení retrospektivních analýz a nutnost opatrné interpretace výsledků. Tento typ hodnocení neposkytuje dostatek informací o rozsahu postižení ani o přítomnosti rizikových faktorů. Volba mezi systémovou a topickou léčbou často závisí na závažnosti kožního postižení, což samo o sobě může být rizikovým faktorem pro rozvoj PsA. Navíc v minulosti, kdy bylo dostupných méně léčebných možností, dermatologové často preferovali terapii TNFi u pacientů s psoriázou a přítomnými artralgickými obtížemi. Tento přístup mohl ovlivnit hodnocení rizikových faktorů rozvoje PsA, stejně jako výběr terapie. Interpretačně limitujícím může být také protopatický bias, tedy situace, kdy volba léčby může být ovlivněna přítomnými, ale dosud nediagnostikovanými symptomy PsA. Z těchto důvodů jsou nezbytná prospektivní data, která by umožnila přesnější identifikaci rizikových faktorů a stanovení optimálního časového bodu pro terapeutickou intervenci.
Potřeba prospektivních dat
Pro lepší pochopení přechodu psoriázy do PsA a možností prevence probíhají dvě velké prospektivní studie – PAMPA a HIPPOCRATES. PAMPA je randomizovaná, zaslepená a integrační studie, která zařadí 350 pacientů s určitou závažností kožního postižení a ultrasonografickými (USG) nálezy. U 200 pacientů proběhne randomizace v poměru 1 : 1 k léčbě guselkumabem nebo placebem po dobu 24 týdnů, následně budou všichni nemocní léčeni guselkumabem. Část pacientů bude sledována bez léčby. Primárním cílovým ukazatelem studie je zmírnění subklinického zánětu podle USG ve 24. týdnu a hodnocení progrese do klinicky vyjádřené PsA v 96. týdnu.
HIPPOCRATES je rozsáhlý mezinárodní projekt, do kterého bude zařazeno 25 000 pacientů s psoriázou ze 17 zemí. Po dobu tří let budou shromažďována demografická a klinická data, probíhat genomové sekvenování a analýza biomarkerů. Krevní vzorky budou uchovávány po dobu 30 let. Cílem projektu vedeného profesorkou Laurou Coates z Univerzity v Oxfordu je prohloubení znalostí o molekulární podstatě přechodu psoriázy do PsA. Výsledky této studie mohou přispět k identifikaci časnějších intervencí, které by minimalizovaly dlouhodobé negativní dopady nemoci, nebo dokonce zabránily rozvoji PsA. Koordinačním centrem pro Českou republiku je Oddělení revmatologie dětí a dospělých FN Motol v Praze.
Shrnutí
Otázka, zda lze zabránit vzniku PsA, nebo alespoň oddálit její nástup, zatím nemá jednoznačnou odpověď. Dosud publikované studie přinášejí určité náznaky, avšak retrospektivní data jsou zatížena metodologickými omezeními a interpretačními výzvami. Na základě dosavadních studií nelze jednoznačně preferovat konkrétní skupinu bDMARDs jako nejúčinnější v prevenci PsA. K potvrzení těchto hypotéz jsou nezbytná prospektivní data, přičemž právě probíhající multicentrické projekty by mohly přinést potřebné odpovědi, shrnula na závěr MUDr. Hurňáková.
Profil ideálního pacienta pro léčbu inhibitory IL‑17
Profesor MUDr. Ladislav Šenolt, Ph.D., z Revmatologického ústavu v Praze se zaměřil na ideální profil pacienta pro terapii IL‑17i a hned v úvodu představil v této souvislosti tři typy nemocných trpících axiální spondyloartritidou (axSpA), kteří byli léčeni secukinumabem (IL‑17Ai).
První pacient, narozený v roce 1977, byl secukinumabem léčen v první linii od listopadu 2016, kdy byly jeho hodnoty C‑reaktivního proteinu (CRP) 5, skóre aktivity onemocnění (Bath Ankylosing Spondylitis Disease Activity Index, BASDAI) 5,1 a ranní ztuhlost přibližně 60 minut. V prosinci 2024 byly tyto hodnoty následující: CRP 1, BASDAI 0,1, ranní ztuhlost 0 minut. Druhou linii léčby představoval pacient narozený v roce 1985, který byl v období od dubna 2016 do května 2018 v rámci klinického hodnocení léčen nejprve certolizumabem, přičemž při ukončení sledování byly hodnoty CRP 75 a BASDAI 7,6. Léčba secukinumabem byla u nemocného zahájena v červnu 2018 s následnými hodnotami monitorovaných parametrů: CRP 6, BASDAI 0,8, ranní ztuhlost 0 minut. Třetí pacient, narozený v roce 1971, byl léčen infliximabem v období od dubna 2009 do července 2024 (hodnota CRP poklesla z 24 na 12, BASDAI 3,9, ranní ztuhlost 60 minut). Při léčbě secukinumabem od září 2024 byly v prosinci téhož roku zjištěny CRP 21, BASDAI 4,0 a ranní ztuhlost 30 minut.
Výběr biologické léčby
Podle aktuálních doporučených postupů pro léčbu axSpA ASAS‑EULAR (Assessment of Spondyloarthritis international Society‑European Alliance of Associations for Rheumatology) [8] jsou při selhání léčby nesteroidními antirevmatiky tři terapeutické možnosti: TNFi, IL‑17i nebo inhibitory Janus kináz (JAKi), přičemž běžnější pro praxi jsou TNFi nebo IL‑17i.
V poslední době se hovoří o personalizaci biologické léčby podle dominantního postižení. Například publikace autorů Najm a kol. vychází z heterogenity onemocnění PsA a ověřuje koncepci, že patogenetické mechanismy se mohou lišit v různých tkáních v rámci jednoho onemocnění, což by mohlo vysvětlit tkáňově odlišné úrovně odpovědi na různé terapie [9].
V případě axSpA neexistují důkazy pro to, že jeden typ léčby je na muskuloskeletální aparát účinnější než jiný. Rozhodnutí o výběru biologické léčby v klinické praxi by mělo vycházet z bezpečnostního profilu léku, z přítomnosti mimokloubních projevů a komorbidit a z preferencí pacienta. Inhibitory IL‑17 nejsou doporučeny jako první volba u pacientů s aktivním idiopatickým střevním zánětem nebo aktivní uveitidou [10,11].
Prediktory léčebné odpovědi při terapii TNFi a IL‑17Ai u axSpA
Mezi tyto prediktory patří mužské pohlaví, mladý věk, krátké trvání onemocnění, pozitivita lidského leukocytárního antigenu B27 (HLA‑B27), aktivita onemocnění (dle skóre BASDAI, ASDAS [Ankylosing Spondylitis Disease Activity Score]), přítomnost systémového zánětu (CRP > 10 mg/l), přítomnost zánětu sakroiliakálních kloubů na magnetické rezonanci. Podle dat evropského registru EuroSpA představuje dobrou odpověď na léčbu inaktivita onemocnění po šesti měsících terapie a setrvání na terapii po 12 měsících [12–14].
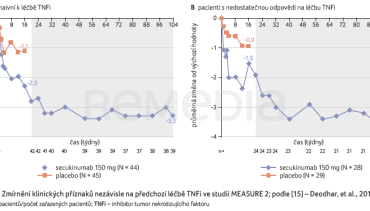
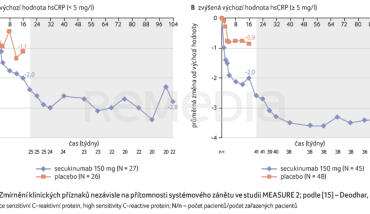 Studie MEASURE 2 potvrdila zmírnění klinických příznaků (dle BASDAI) při léčbě secukinumabem nezávisle na přítomnosti systémového zánětu a na předchozí léčbě TNFi po dobu dvou let (graf 1A, B; graf 2A, B) [15].
Studie MEASURE 2 potvrdila zmírnění klinických příznaků (dle BASDAI) při léčbě secukinumabem nezávisle na přítomnosti systémového zánětu a na předchozí léčbě TNFi po dobu dvou let (graf 1A, B; graf 2A, B) [15].
 V rámci EuroSpA byl sledován vliv předchozí léčby TNFi na dosažení a udržení nízké aktivity axSpA. Doba dosažení nízké aktivity (low disease activity, LDA) se prodlužovala s počtem předchozích TNFi u léčby TNFi i IL‑17Ai. V případě léčby TNFi předchozí expozice TNFi trvání LDA neovlivnila, ale u léčby IL‑17Ai s předchozí expozicí TNFi byla doba setrvání LDA kratší než u pacientů naivních k biologické terapii [16].
V rámci EuroSpA byl sledován vliv předchozí léčby TNFi na dosažení a udržení nízké aktivity axSpA. Doba dosažení nízké aktivity (low disease activity, LDA) se prodlužovala s počtem předchozích TNFi u léčby TNFi i IL‑17Ai. V případě léčby TNFi předchozí expozice TNFi trvání LDA neovlivnila, ale u léčby IL‑17Ai s předchozí expozicí TNFi byla doba setrvání LDA kratší než u pacientů naivních k biologické terapii [16].
Cílem studie autorů Armağan a kol. bylo posoudit setrvání na léčbě secukinumabem u radiografické axSpA (r‑axSpA) a vyhodnotit prediktivní faktory tohoto setrvání na základě údajů z kohorty z běžné praxe. Celková míra setrvání na léčbě secukinumabem byla po 12 měsících 55 %. Pacienti s r‑axSpA s obezitou měli nižší frekvenci ukončení léčby secukinumabem (29 % vs. 50 %) ve srovnání s pacienty s r‑axSpA bez obezity. V multivariační analýze bylo zjištěno, že větší počet předchozích TNFi s sebou nese vyšší riziko ukončení léčby secukinumabem, v případě obezity bylo toto riziko nižší [17].
Prediktory léčebné odpovědi při terapii IL‑17Ai u PsA
Na pacienty s PsA zahajující léčbu secukinumabem v klinické praxi (dle výsledků z registru EuroSpA) a na identifikaci výchozích prediktorů dosažení nízké aktivity onemocnění se zaměřila publikace Georgiadise a kol. Hodnocenými parametry byly nízká aktivita PsA (DAPSA28 [Disease Activity in Psoriatic Arthritis‑28] LDA) po šesti měsících a setrvání na léčbě po 12 měsících. Sledování zahrnulo 2 790 pacientů ze 14 registrů, 24 % bylo léčeno v první linii, 52 % dříve užívalo ≥ 2 biologické nebo cílené syntetické DMARDs (b/tsDMARDs). Bylo identifikováno osm prediktorů pro DAPSA28 LDA, sedm pro střední odpověď DAPSA28 a čtyři pro pokračování v léčbě. Vyšší hodnota CRP (> 10 mg/l vs. ≤ 10 mg/l) zvýšila šance na dosažení všech tří výsledků a byla jediným společným prediktorem. Dalšími pozitivními společnými prediktory dosažení DAPSA28 LDA a střední odpovědi DAPSA28 byly: mužské pohlaví, méně předchozích b/tsDMARDs, nižší skóre hodnocení celkového stavu pacienta a nižší skóre v dotazníku hodnocení zdraví (HAQ), zatímco počet citlivých kloubů vykazoval nekonzistentní výsledky napříč hodnocenými parametry [18].
Ahmadzay a kol. zkoumali výsledky léčby secukinumabem u pacientů s PsA a jejich souvislost s kouřením a hodnotou BMI. Bývalí a současní kuřáci měli přibližně o 30 % zvýšené riziko ukončení léčby secukinumabem do 12 měsíců ve srovnání s těmi, kteří nikdy nekouřili; vliv BMI nebyl doložen. Ani kouření, ani BMI nebyly spojeny s pravděpodobností dosažení DAPSA28 LDA po šesti měsících. Tato zjištění naznačují, že kouření ovlivňuje setrvání na léčbě IL‑17Ai podobně, jako to bylo prokázáno u TNFi [19].
Závada a kol. porovnávali setrvání na terapii IL‑17i a její účinnost a bezpečnost oproti TNFi u pacientů s PsA s využitím reálných dat z českého registru biologické léčby ATTRA.
Bylo pozorováno delší setrvání na léčbě IL‑17Ai ve srovnání s TNFi navzdory nižšímu účinku na skóre aktivity onemocnění (Disease Activity Score‑28, DAS28) a kvalitu života pacientů s PsA [20]. Také podle italského registru BIRRA (Biologics Retention Rate Assessment), který zkoumá setrvání na léčbě inovativními antirevmatiky v průběhu času, přechod na léčbu IL‑17i vykazuje u pacientů s PsA delší setrvání na terapii než tzv. cyklování TNFi [21].
Systémové účinky IL‑17
Zánětlivá artritida se vyskytuje u mnoha onemocnění a je charakterizována zánětem a poškozením kloubů. Zánětlivý stav u artritidy je spojen se systémovými projevy, které většinou znamenají špatnou prognózu. Prozánětlivý cytokin IL‑17 přispívá k patogenezi různých inflamatorních onemocnění. Na systémové účinky IL‑17 u zánětlivé artritidy se zaměřila publikace autorů Beringer a Miossec [22]. Zvýšené cirkulující koncentrace bioaktivního IL‑17 zprostředkovávají změny v krevních cévách, játrech a srdečních a kosterních svalech. Účinky IL‑17 na vaskulární a srdeční buňky mohou zvyšovat riziko rozvoje kardiovaskulárních příhod. V játrech přispívá IL‑17 k vysokým cirkulujícím koncentracím proteinů akutní fáze, jako je CRP, a ke vzniku jaterních lézí. V kosterním svalu způsobuje IL‑17 poruchy svalové kontraktility a slabost. Inhibice IL‑17 má tedy příznivé účinky na lokální i systémové úrovni a může být efektivní v léčbě širšího počtu zánětlivých onemocnění.
Závěr
Závěrem profesor Šenolt shrnul základní body využití inhibice IL‑17. Inhibitory IL‑17 jsou účinnou léčebnou možností pro pacienty s axiální i periferní SpA a zajišťují kontrolu nad různými doménami onemocnění, jejich užití je výhodné při převládající psoriáze. U přípravků byly popsány podobné prediktory léčebné odpovědi jako v případě TNFi. Inhibice IL‑17 je klinicky účinná nezávisle na přítomnosti systémového zánětu. Klinické výsledky potvrzují přínos u pacientů jak v první linii, tak po selhání TNFi, ale vyšší počet předchozích b/tsDMARDs je spojen s horším výsledkem terapie. Obezita nemusí mít zásadní vliv na účinnost IL‑17i; jsou preferovány při anamnéze srdečního selhání, malignity, roztroušené sklerózy a dalších onemocnění. Volba terapie by měla být přizpůsobena klinickému obrazu, přítomnosti mimokloubních projevů a komorbidit. Data z reálné praxe potvrzují dlouhodobé setrvání na léčbě a stabilní účinnost IL‑17i.
Literatura
[1] Zabotti A, De Marco G, Gossec L, et al. EULAR points to consider for the definition of clinical and imaging features suspicious for progression from psoriasis to psoriatic arthritis. Ann Rheum Dis 2023; 82: 1162–1170.
[2] Gisondi P, Bellinato F, Targher G. Biological disease‑modifying antirheumatic drugs may mitigate the risk of psoriatic arthritis in patients with chronic plaque psoriasis. Ann Rheum Dis 2022; 81: 68–73.
[3] Acosta Felquer ML, LoGiudice L, Galimberti ML, et al. Treating the skin with biologics in patients with psoriasis decreases the incidence of psoriatic arthritis. Ann Rheum Dis 2022; 81: 74–77.
[4] Meer E, Merola JF, Fitzsimmons R, et al. Does biologic therapy impact the development of PsA among patients with psoriasis? Ann Rheum Dis 2022; 81: 80–86.
[5] Singla S, Putman M, Liew J, Gordon K. Association between biological immunotherapy for psoriasis and time to incident inflammatory arthritis: a retrospective cohort study. Lancet Rheumatol 2023; 5: e200–e207.
[6] Strober B, Soliman AM, Li C, et al. Risk of developing inflammatory arthritis in patients with psoriasis initiating treatment with biologics: A population‑based analysis. J Am Acad Dermatol 2024; 91: 1143–1149.
[7] Watad A, Zabotti A, Patt YS, et al. From Psoriasis to Psoriatic Arthritis: Decoding the Impact of Treatment Modalities on the Prevention of Psoriatic Arthritis. Rheumatol Ther 2024; 11: 963–976.
[8] Ramiro S, Nikiphorou E, Sepriano A, et al. ASAS‑EULAR recommendations for the management of axial spondyloarthritis: 2022 update. Ann Rheum Dis 2023; 82: 19–34.
[9] Najm A, Goodyear CS, McInnes IB, Siebert S. Phenotypic heterogeneity in psoriatic arthritis: towards tissue pathology‑based therapy. Nat Rev Rheumatol 2023; 19: 153–165.
[10] Proft F, Duran TI, Ghoreschci K, et al. Treatment strategies for Spondyloarthritis: Implementation of precision medicine – Or “one size fits all” concept? Autoimmun Rev 2024; 23: 103638.
[11] Atzeni F, Carriero A, Boccassini L, DʼAngelo S. Anti‑IL‑17 Agents in the Treatment of Axial Spondyloarthritis. Immunotargets Ther 2021; 10: 141–153.
[12] Goupille P, Vuitton L, Wendling D. Axial spondyloarthritis and inflammatory bowel disease: Therapeutic implications. Joint Bone Spine 2024; 91: 105662.
[13] Pinto AS, Farisogullari B, Machado PM, et al. Predictors of remission in people with axial spondyloarthritis: A systematic literature review. Semin Arthritis Rheum 2022; 56: 152078.
[14] Ørnbjerg LM, Linde L, Georgiadis S, et al. Predictors of ASDAS‑CRP inactive disease in axial spondyloarthritis during treatment with TNF‑inhibitors: Data from the EuroSpA collaboration. Semin Arthritis Rheum 2022; 56: 152081.
[15] Deodhar A, Conaghan PG, Kvien TK, et al. Secukinumab provides rapid and persistent relief in pain and fatigue symptoms in patients with ankylosing spondylitis irrespective of baseline C‑reactive protein levels or prior tumour necrosis factor inhibitor therapy: 2‑year data from the MEASURE 2 study. Clin Exp Rheumatol 2019; 37: 260–269.
[16] Heberg J, Georgiadis S, Pons M, et al. What Is the Impact of Prior TNF Inhibitor Treatment on the Time to Achieve Low Disease Activity and the Durability of Low Disease Activity? Real‑world Results Based on 17 858 European Patients with Axial Spondyloarthritis Initiating a TNF Inhibitor or an IL‑17A Inhibitor. Arthritis Rheumatol 2024; 76(Suppl 9). Abstract 1756.
[17] Armağan B, Kiliç L, Farisoğulları B, et al. Drug retention rate and predictive factors of drug survival for secukinumab in radiographic axial spondyloarthritis. Rheumatol Int 2023; 43: 147–156.
[18] Georgiadis S, Ostergaard M, Heberg J, et al. Predictors of Treatment Response and Continuation in Patients with Psoriatic Arthritis Initiating Secukinumab – Results from the EuroSpA Collaboration. Arthritis Rheumatol 2024; 76(Suppl 9). Abstract 2325.
[19] Ahmadzay Z, Georgiadis S, Ostergaard M, et al. Do Smoking and Obesity Impact Secukinumab Treatment Outcomes? Real‑world Data from 1,202 European Patients with Psoriatic Arthritis. Arthritis Rheumatol 2024; 76(Suppl 9). Abstract 2350.
[20] Zavada J, Baranová J, Pavelka K, et al. Better Drug Retention on anti‑IL17A Compared to Anti‑TNF Therapy Despite Its Inferior Effect on Composite Joint Indexes and Quality of Life in Patients with PsA–analysis from the Czech Biologics Registry ATTRA. Arthritis Rheumatol 2023; 75(Suppl 9). Abstract 1439.
[21] Ariani A, Lumetti F, Parisi S, et al. Cycling vs Swap TNFi and IL17i in Psoriatic Arthritis: Results From the BIRRA Retrospective Observational Study. Ann Rheum Dis 2024; 83: 374–375. Abstract POS0266.
[22] Beringer A, Miossec P. Systemic effects of IL‑17 in inflammatory arthritis. Nat Rev Rheumatol 2019; 15: 491–501.