Léčebné cíle u systémového lupusu dle nových doporučení EULAR 2023 a možnosti využití anifrolumabu
Letošní Zimní revmatologické dny se uskutečnily 15.–17. ledna na Výstavišti České Budějovice. MUDr. Dana Tegzová (Revmatologický ústav, Praha) zaměřila svoji pozornost na léčebné cíle u pacientů se systémovým lupus erythematodes (SLE) a na postavení anifrolumabu v léčbě SLE.
Jedním z hlavních problémů SLE je, že dlouhodobá aktivita onemocnění může vést k ireverzibilnímu orgánovému postižení. Jak ale dosáhnout remise onemocnění? Bohužel i léčba, kterou v terapii SLE efektivně používáme ke snížení aktivity SLE s cílem dosažení remise, se svými nežádoucími účinky může podílet na nevratném poškození orgánů. Proto je třeba vždy zohlednit poměr mezi přínosem a rizikem léčby. SLE má u většiny pacientů relabující, případně chronicky aktivní průběh a dosažení trvalé remise je poměrně obtížné. Je doloženo, že pacienti, kteří dosáhnou kompletní nebo klinické remise bez nutnosti kortikoterapie (měřeno jako prolongovaná remise trvající ≥ 5 let), mají výrazně nižší riziko rozvoje orgánového poškození než pacienti, kteří v remisi nejsou a užívají vysoké dávky glukokortikoidů (GK) [1].
I při standardní terapii (antimalarika ± GK ± imunosupresiva) je průběh SLE komplikovaný. Uvádí se, že více než 60 % pacientů má perzistentní nebo relabující formu onemocnění [2] a zhruba čtvrtina pacientů prodělá i přes standardní léčbu minimálně jeden závažný relaps za rok. Více než 80 % nemocných trpí zvýšenou únavou, kterou považují za jeden z nejvýznamnějších a nejvíce obtěžujících projevů nemoci [3]. Zvýšená dávka GK se jeví jako hlavní příčina orgánového poškození [4]. K poškození orgánů může dojít i v době, kdy je pacient adekvátně léčen a kdy je aktivita onemocnění potlačena, i když v menším rozsahu, než kdyby pacient léčen nebyl [5].
Přednášející shrnula, že cílem léčby SLE je dosažení remise, nebo alespoň stavu nízké aktivity nemoci, pokud remise není možné dosáhnout (léčba k cíli, treat‑to‑target) [6]. Tak je možné omezit nárůst poškození, počet vzplanutí a zlepšit kvalitu života pacientů. GK používané při léčbě SLE, ač stále zůstávají základním lékem, bohužel přispívají k nevratnému poškození orgánů. Riziko poškození je asociováno s dávkou. Bylo doloženo, že snížení průměrné dávky prednisonu o 1 mg/den je spojeno s 3% snížením rizika orgánového poškození [7].
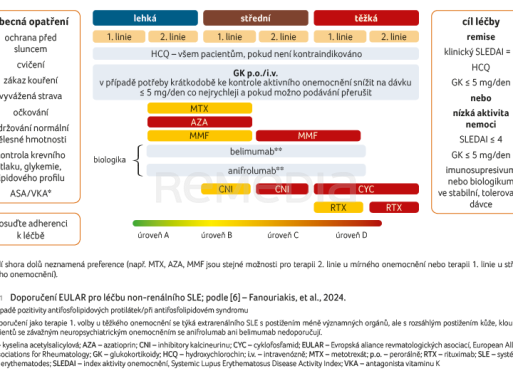 Mezi důležité změny v recentním doporučení EULAR (Evropská aliance revmatologických asociací, European Alliance of Associations for Rheumatology) 2023 pro terapii SLE bez poškození ledvin patří změny v indikaci GK a změny v postavení biologické léčby (obr. 1) [6]. Je doporučeno používat nižší cílovou udržovací dávku GK (≤ 5 mg/den), a pokud je to možné, terapii ukončit. GK by měly být používány pouze jako překlenovací terapie, protože jejich dlouhodobé užívání představuje pro pacienty velké riziko. Imunosupresivní léčba by měla být zahájena časně, aby se zabránilo dlouhodobé expozici GK. Dle doporučení EULAR není již povinné použití konvenčních imunosupresiv před zahájením biologické terapie. Biologickou léčbu je doporučeno zvážit u pacientů, kteří neodpovídají na hydroxychlorochin a GK nebo u nichž není možné snížit dávku GK ≤ 5 mg/den. Biologická léčba prokázala dobrou kontrolu aktivity onemocnění, redukci počtu vzplanutí, zastavení nárůstu orgánového poškození a rovněž usnadňuje snížení dávky GK.
Mezi důležité změny v recentním doporučení EULAR (Evropská aliance revmatologických asociací, European Alliance of Associations for Rheumatology) 2023 pro terapii SLE bez poškození ledvin patří změny v indikaci GK a změny v postavení biologické léčby (obr. 1) [6]. Je doporučeno používat nižší cílovou udržovací dávku GK (≤ 5 mg/den), a pokud je to možné, terapii ukončit. GK by měly být používány pouze jako překlenovací terapie, protože jejich dlouhodobé užívání představuje pro pacienty velké riziko. Imunosupresivní léčba by měla být zahájena časně, aby se zabránilo dlouhodobé expozici GK. Dle doporučení EULAR není již povinné použití konvenčních imunosupresiv před zahájením biologické terapie. Biologickou léčbu je doporučeno zvážit u pacientů, kteří neodpovídají na hydroxychlorochin a GK nebo u nichž není možné snížit dávku GK ≤ 5 mg/den. Biologická léčba prokázala dobrou kontrolu aktivity onemocnění, redukci počtu vzplanutí, zastavení nárůstu orgánového poškození a rovněž usnadňuje snížení dávky GK.
Anifrolumab v terapii SLE
V etiopatogenezi SLE hraje důležitou roli interferon (IFN) typu 1. Logickým důsledkem při vývoji účinné léčby je snaha potlačit aktivitu tohoto cytokinu. Anifrolumab je monoklonální protilátka, která se s vysokou specificitou a afinitou váže na podjednotku 1 interferonového receptoru typu 1 (IFNAR1) a inhibuje signalizaci zprostředkovanou IFN typu 1 s potlačením exprese genů regulovaných IFN.
Účinnost a bezpečnost anifrolumabu v léčbě pacientů se SLE demonstrovaly robustní studie fáze III TULIP 1 a 2 [8,9] a navazující dlouhodobé sledování TULIP‑LTE [10]. Efekt léčby byl porovnáván se standardní terapií. Dlouhodobá extenze studie doložila, že anifrolumab snižoval dávku GK konzistentně po dobu čtyř let. Po čtyřech letech terapie dostávalo 90,1 % pacientů léčených anifrolumabem dávku GK ≤ 7,5 mg/den (oproti 70,7 % v placebové větvi), 74,7 % dávku ≤ 5 mg/den (63,4 % v placebové větvi) a 36,4 % pacientů bylo bez kortikoterapie (26,8 % v placebové větvi). Snížení skóre SLEDAI‑2K (SLE Disease Activity Index 2000) bylo dosaženo paralelně se snížením průměrné dávky GK. Dostupná jsou aktuálně data z klinických hodnocení pro non‑renální SLE, nicméně již probíhají studie s indikací SLE s lupusovou nefritidou, myozitidou, se systémovou sklerózou a čistě kožním lupusem.
SLE je chronické autoimunitní onemocnění charakterizované multisystémovým postižením. Přednášející prezentovala účinnost anifrolumabu na aktivitu onemocnění dle jednotlivých orgánových domén. Jedním z nejvíce obtěžujících projevů SLE jsou kožní projevy. Z hlediska mortality není toto postižení tak závažné, nicméně pro pacienty je velmi frustrující. Navíc není léčbou vždy snadno ovlivnitelné. V tomto směru vyzdvihla doktorka Tegzová právě anifrolumab, který byl ve studiích TULIP 1 a 2 schopen výrazně snížit skóre aktivity kožních projevů (CLASI). Přednášející demonstrovala výborný efekt anifrolumabu snímky konkrétních pacientů. Dalšími projevy SLE, které bývají standardní léčbou hůře ovlivnitelné, jsou hematologické projevy. Post hoc analýza dat ze studií TULIP 1 a 2 potvrdila, že léčba anifrolumabem zmírnila aktivitu onemocnění napříč různými orgánovými doménami [11]. V hematologické doméně SLEDAI‑2K došlo v týdnu 52 k významně vyššímu zlepšení u pacientů léčených anifrolumabem ve srovnání s pacienty, kteří dostávali ke standardní léčbě placebo (rozdíl činil 25 %).
K hodnocení efektu léčby SLE jsou využívány indexy DORIS (Definition Of Remision In SLE) a LLDAS (Lupus Low Disease Activity Score). Jejich dosažení je spojeno s lepšími léčebnými výsledky. Během čtyřletého sledování ve studiích TULIP a TULIP‑LTE byla léčba anifrolumabem ve srovnání s placebem spojena s dřívějším, častějším a trvalejším dosažením poklesu aktivity onemocnění a remise dle skóre LLDAS [12] a DORIS [13]. Výsledky naznačují, že dosažení remise dle definice DORIS je při dlouhodobém užívání anifrolumabu dosažitelným terapeutickým cílem.
Vedle účinnosti anifrolumabu byly samozřejmě sledovány také bezpečnost a snášenlivost léčby. V klinickém hodnocení (studie fáze II MUSE, studie fáze III TULIP 1 a 2 a extenze TULIP‑LTE) byl u pacientů léčených anifrolumabem oproti placebu zaznamenán zvýšený výskyt infekcí dýchacích cest a herpes zoster [14]. Přednášející upozornila, že podrobnější rozbor výsledků ukazuje, že vyšší výskyt herpes zoster je pouze v prvním roce léčby.
Shrnutí
Doktorka Tegzová v závěru shrnula, že SLE představuje komplexní heterogenní onemocnění, kde se jako centrální faktor patogeneze uplatňuje IFN typu 1. Anifrolumab je jedinou biologickou léčbou, která cílí na signální dráhu IFN typu 1. Anifrolumab poskytuje konzistentní účinnost, rychlý nástup účinku, vede ke snížení aktivity onemocnění a dávky GK. Efekt léčby byl zaznamenán napříč jednotlivými orgánovými systémy. Strategie treat‑to‑target může zlepšit výsledky léčby. Anifrolumab zvyšuje pravděpodobnost dosažení nízké aktivity onemocnění i remise a prodlužuje dobu setrvání v ní. Bezpečnost léčby se jeví jako příznivá, je prověřena čtyřletým sledováním, během něhož se neobjevily nové bezpečnostní signály.
Terapie anifrolumabem byla zavzata do oficiálních doporučení EULAR 2023 pro léčbu SLE bez poškození ledvin. Léčbu je možné indikovat u všech závažností postižení, u lehčích forem je možné anifrolumab zařadit do 2. linie do kombinace s antimalariky, která jsou základem terapie (pokud nejsou kontraindikována).
V České republice je anifrolumab hrazen jako přídatná léčba u dospělých pacientů s aktivním SLE s pozitivními autoprotilátkami anti‑dsDNA a/nebo ANAb a nízkou hladinou komplementu, kteří navzdory obvyklé léčbě SLE sestávající se z GK, antimalarik a dalších imunosupresiv setrvávají v klinicky aktivním onemocnění (SELENA‑SLEDAI ≥ 10) [15].
Literatura
[1] Zen M, Iaccarino L, Gatto M, et al. Prolonged remission in Caucasian patients with SLE: prevalence and outcomes. Ann Rheum Dis 2015; 74: 2117–2122.
[2] Tselios K, Gladman DD, Touma Z, et al. Disease course patterns in systemic lupus erythematosus. Lupus 2019; 28: 114–122.
[3] Cornet A, Andersen J, Myllys K, et al. Living with systemic lupus erythematosus in 2020: a European patient survey. Lupus Sci Med 2021; 8: e000469.
[4] Urowitz MB, Gladman DD, Ibañez D, et al. Effect of Disease Activity on Organ Damage Progression in Systemic Lupus Erythematosus: University of Toronto Lupus Clinic Cohort. J Rheumatol 2021; 48: 67–73.
[5] Urowitz MB, Gladman DD, Ibañez D, et al. Evolution of disease burden over five years in a multicenter inception systemic lupus erythematosus cohort. Arthritis Care Res (Hoboken) 2012; 64: 132–137.
[6] Fanouriakis A, Kostopoulou M, Andersen J, et al. EULAR recommendations for the management of systemic lupus erythematosus: 2023 update. Ann Rheum Dis 2024; 83: 15–29.
[7] Sawah SA, Zhang X, Zhu B, et al. Effect of corticosteroid use by dose on the risk of developing organ damage over time in systemic lupus erythematosus‑the Hopkins Lupus Cohort. Lupus Sci Med 2015; 2: e000066.
[8] Furie RA, Morand EF, Bruce IN, et al. Type I interferon inhibitor anifrolumab in active systemic lupus erythematosus (TULIP‑1): a randomised, controlled, phase 3 trial. Lancet Rheumatol 2019; 1: e208–e219.
[9] Morand EF, Furie R, Tanaka Y, et al. Trial of Anifrolumab in Active Systemic Lupus Erythematosus. N Engl J Med 2020; 382: 211–221.
[10] Kalunian KC, Furie R, Morand EF, et al. A Randomized, Placebo‑Controlled Phase III Extension Trial of the Long‑Term Safety and Tolerability of Anifrolumab in Active Systemic Lupus Erythematosus. Arthritis Rheumatol 2023; 75: 253–265.
[11] Morand EF, Furie RA, Bruce IN, et al. Efficacy of anifrolumab across organ domains in patients with moderate‑to‑severe systemic lupus erythematosus: a post‑hoc analysis of pooled data from the TULIP‑1 and TULIP‑2 trials. Lancet Rheumatol 2022; 4: e282–e292.
[12] Morand EF, Abreu G, Furie RA, et al. Lupus low disease activity state attainment in the phase 3 TULIP trials of anifrolumab in active systemic lupus erythematosus. Ann Rheum Dis 2023; 82: 639–645.
[13] van Vollenhoven R, Morand E, Furie RA, et al. Remission Attainment in Patients with Systemic Lupus Erythematosus Treated with Anifrolumab Compared with Placebo over a 4‑Year Period.: ACR Convergence 2022, Abstr. Nr. 2334.
[14] Tummala R, Abreu G, Pineda L, et al. Safety profile of anifrolumab in patients with active SLE: an integrated analysis of phase II and III trials. Lupus Sci Med 2021; 8: e000464.
[15] Detail léčivého přípravku Saphnelo. Dostupné na: https://prehledy.sukl.cz/prehled_leciv.html#/leciva/0255465