Riziko rekurence u časného hormonálně pozitivního HER2 negativního karcinomu prsu
Souhrn
Hauserová Š, Palkovský M, Soumarová R. Riziko rekurence u časného hormonálně pozitivního HER2 negativního karcinomu prsu. Remedia 2025; 35: 52–55.
Karcinom prsu je v České republice nejčastějším zhoubným nádorem u žen. Ačkoliv pokroky v diagnostice a léčbě vedou k vysoké míře přežití, riziko recidivy zůstává vážným problémem, zejména u pacientek s histopatologickými znaky, jako jsou pozitivní lymfatické uzliny nebo vysoký grade nádoru. Identifikace pacientek s vyšším rizikem recidivy a optimalizace adjuvantní léčby je klíčová pro zlepšení prognózy. V poslední době se pozornost zaměřuje na inhibitory cyklin‑dependentních kináz 4 a 6 (CDK4/6), které prokázaly účinnost jak v léčbě metastatického karcinomu prsu, tak i v adjuvantní terapii. Klinické studie jako monarchE a NATALEE prokázaly zlepšení přežití bez invazivního onemocnění v adjuvantní léčbě u pacientek s HR+/HER2– karcinomem prsu. Abemaciklib i ribociklib statisticky významně snížily riziko invazivní recidivy ve srovnání s endokrinní terapií samotnou. Průběžné výsledky naznačují, že kombinace těchto inhibitorů s hormonální léčbou může poskytnout novou naději pro pacientky s vysokým rizikem recidivy a zlepšit jejich klinické výsledky. Novou léčebnou modalitou v (neo)adjuvantní terapii hormonálně pozitivního karcinomu prsu se již brzy může stát i imunoterapie inhibitory kontrolního bodu, stejně jako tomu bylo v minulosti v případě triple‑negativního karcinomu prsu. Předběžné výsledky klinických studií fáze III demonstrovaly signifikantně vyšší zastoupení patologických kompletních remisí v kohortách s kombinací chemo‑imunoterapie než se samostatnou chemoterapií. Zda se však vliv imunoterapie promítne i do prodloužení celkového přežívání nebo přežívání bez relapsu onemocnění, dosud není jasné.
Klíčová slova: časný karcinom prsu – rekurence – endokrinní terapie – inhibitory CDK4/6 – imunoterapie.
Summary
Hauserova S, Palkovsky M, Soumarova R. Risk of recurrence of early hormone receptor positive HER2 negative breast cancer. Remedia 2025; 35: 52–55.
Breast cancer is the most common malignant tumor diagnosed in women in the Czech Republic. While the advances in the diagnostics and treatment ensure high survival rates, the risk of recurrence remains a serious problem, especially in patients with histopathological traits such as positive lymphatic nodes or high tumor grade. Identification of patients with a higher risk of recurrence and optimization of the adjuvant treatment are crucial prerequisites of prognosis improvement. Lately, much attention has been paid to inhibitors of cyclin‑dependent kinases 4 and 6 (CDK4/6) that proved to be effective in both metastatic breast cancer treatment and in adjuvant therapy. Clinical trials like monarchE and NATALEE have shown improved survival without invasive disease in adjuvant treatment concerning HR+/HER2– breast cancer. Abemaciclib and ribociclib have decreased statistically significant the risk of invasive recurrence compared to endocrine therapy alone. Preliminary results show promise in the sense that the combination of these inhibitors with hormonal treatment may offer a new hope to patients with a high risk of recurrence and may improve their clinical results. Moreover, immunotherapy using checkpoint inhibitors may soon become a novel modality within the (neo)adjuvant therapy of hormone receptor positive breast cancer, i.e. may start to play a similar role here like in triple negative breast cancer in the past. Early results of phase III clinical trials have demonstrated significantly higher rates of complete pathological remissions in the cohorts treated with combined chemo‑immunotherapy compared to chemotherapy alone. It remains to be elucidated, however, whether the impact of immunotherapy will transfer into prolongation of overall survival or survival without disease relapse.
Key words: early breast cancer – recurrence – endocrine therapy – CDK4/6 inhibitors – immunotherapy.
Úvod
Karcinom prsu představuje v České republice nejčastější zhoubný nádor u žen. Díky mamografickému screeningu se podaří zachytit až 80 % nádorů prsu ve stadiu I a II, kdy můžeme hovořit o časném karcinomu prsu [1]. Karcinomy prsu představují značně heterogenní skupinu, přičemž nejčastějším podtypem je karcinom prsu s pozitivními hormonální receptory a s negativním receptorem pro lidský epidermální růstový faktor (HR+/HER2–); představuje 70–75 % případů [2]. Přestože se u časného karcinomu prsu dosahuje v současnosti vysoké míry přežití díky pokrokům v diagnostice a léčbě, riziko rekurence zůstává významným klinickým problémem. Rekurence onemocnění může být lokální, regionální nebo vzdálená a bývá spojena s horší prognózou. Identifikace pacientek s vyšším rizikem rekurence a optimalizace adjuvantní léčby je klíčová.
V poslední době se pozornost zaměřuje na inhibitory cyklin‑dependentních kináz 4 a 6 (CDK4/6), které prokázaly slibné výsledky nejen v léčbě metastatického karcinomu prsu, ale také v adjuvantní terapii [3–7].
Rekurence časného karcinomu prsu je ovlivněna mnoha faktory, mezi něž patří histopatologické charakteristiky nádoru (velikost nádoru, přítomnost pozitivních lymfatických uzlin, grading nádoru, přítomnost negativních prognostických znaků, jako je vaskulární invaze), molekulární podtyp nádoru nebo proliferační aktivita. Dále je riziko recidivy ovlivněno faktory na straně pacienta, jako jsou věk, přítomnost komorbidit nebo genetické predispozice (mutace v predispozičních genech) [8–11].
Množství nádorových buněčných a molekulárních charakteristik může být použito k výpočtu rizika recidivy u pacientek s časným karcinomem prsu. Existují různé skórovací systémy, které se zaměřují na kombinaci těchto faktorů k odhadu individuálního rizika recidivy. Například Nottingham Prognostic Index (NPI) je v klinické praxi využíván k predikci rizika recidivy na základě velikosti nádoru, uzlinového postižení a histologického grade nádoru [12]. Zásadní roli v predikci rizika rekurence však hrají multigenové testy, jako jsou Oncotype DX nebo MammaPrint, které umožňují stratifikovat pacientky podle rizika a upravit léčebné postupy. Testy mohou identifikovat pacientky s nízkým rizikem recidivy, které neprofitují z chemoterapie, zatímco jiné pacientky s vysokým rizikem mohou mít prospěch z intenzivnější léčby [13,14].
V průběhu posledních dvaceti let byly provedeny desítky klinických studií a metaanalýz, které přinesly zásadní informace o riziku recidivy a přístupech k prevenci. Metaanalýza Early Breast Cancer Trialists’ Collaborative Group (EBCTCG) zahrnovala více než 100 000 pacientek a prokázala, že chemoterapie výrazně zlepšuje přežívání pacientek s časným karcinomem prsu, zejména těch s pozitivními lymfatickými uzlinami [15]. Tato metaanalýza byla klíčová pro podporu širšího použití adjuvantní chemoterapie u pacientek s vysokým rizikem recidivy. Studie ATLAS (Adjuvant Tamoxifen, Longer Against Shorter) ukázala, že prodloužení doby užívání tamoxifenu na 10 let místo původních pěti let u pacientek s HR pozitivním karcinomem výrazně snižuje riziko recidivy [16]. Pan a kolektiv publikovali data o vlivu chemoterapie na přežití pacientek s časným hormonálně pozitivním karcinomem prsu. Metaanalýza prokázala, že chemoterapie kombinovaná s endokrinní terapií má zásadní vliv na snížení rizika vzdálené recidivy, zejména u pacientek s pozitivními lymfatickými uzlinami. Riziko vzdálené recidivy během prvních pěti let úzce souviselo s počtem pozitivních uzlin (6 % u žen bez pozitivních uzlin a 22 % u žen se 4–9 pozitivními uzlinami). Tento výsledek posílil roli chemoterapie v adjuvantní léčbě a zdůraznil její význam pro pacientky s vysoce rizikovými faktory [17].
Skupina EBCTCG prokázala u 63 000 pacientek s ER (estrogenový receptor) pozitivním časným karcinomem prsu zařazených do 88 studií endokrinní léčby přetrvávající riziko recidivy v letech 5–20 po ukončení léčby; velikost rizika souvisela s velikostí nádoru, grade a stavem uzlin a přetrvávala i u nemocných s dobrou prognózou. Roční riziko vzdálené recidivy po pěti letech endokrinní léčby činilo 3 % u pacientek s více než 3 postiženými lymfatickými uzlinami, 2 % s 1–3 pozitivními uzlinami, 1 % u nádorů ≥ 20 mm s negativními uzlinami a 0,5–1,0 % u menších nádorů s negativními uzlinami [18].
Adjuvantní terapie hraje klíčovou roli v prevenci rekurence u pacientek s časným karcinomem prsu. U pacientek s HR+/HER2– karcinomem prsu je endokrinní terapie zásadní součástí adjuvantní léčby. Endokrinní léčba výrazně snižuje riziko recidivy tím, že blokuje účinky estrogenu na nádorové buňky. Standardní délka adjuvantní hormonální léčby je 5–10 let a signifikantně prodlužuje přežívání pacientek bez recidivy onemocnění. I přesto dochází k relapsu u 27–37 % pacientů s onemocněním stadia II a u 46–57 % pacientů s onemocněním stadia III a může se objevit také až 20 let po diagnóze [17]. Nové terapeutické možnosti, jako jsou inhibitory CDK4/6, představují slibnou možnost pro pacientky s HR+/HER2– karcinomem.
Inhibitory CDK4/6 – mechanismus účinku a preklinické důkazy
Cyklin‑dependentní kinázy 4 a 6 hrají klíčovou roli v regulaci buněčného cyklu. U HR+/HER2– nádorů prsu je často pozorována zvýšená exprese i aktivita osy cyklin D‑CDK4/6. Komplex cyklin D‑CDK4/6 vede k inhibici fosforylace retinoblastomového proteinu (Rb). Inaktivovaný Rb se tak nemůže vázat na transkripční faktor E2F, který zůstává ve své aktivní formě a podporuje transkripci genů nutných pro přechod z fáze G1 a do fáze S buněčného cyklu. Inhibitory CDK4/6 (ribociklib, abemaciklib, palbociklib) blokují aktivaci komplexů cyklin D‑CDK4/6, čímž nepřímo blokují přechod nádorových buněk z fáze G1 do fáze S buněčného cyklu [19,20]. Preklinické studie navíc demonstrovaly synergický efekt kombinace inhibitorů CDK4/6 s hormonální terapií, kombinace snižuje rozvoj rezistence na endokrinní léčbu a prodlužuje dobu do progrese nádoru [21,22].
 Abemaciklib v adjuvantní terapii byl schválen na základě výsledků studie monarchE, která se zaměřila na pacientky s HR+/HER2– časným karcinomem prsu s vysokým rizikem rekurence. Vysoce rizikové onemocnění bylo definováno přítomností čtyř a více pozitivních axilárních lymfatických uzlin, střední riziko 1–3 pozitivními axilárními lymfatickými uzlinami a grade 3 nebo velikostí tumoru 5 cm a větší. Menší skupinu tvořili pacienti s 1–3 pozitivními axilárními lymfatickými uzlinami a Ki‑67 (marker proliferační aktivity nádoru) alespoň 20 % jako dalším rizikovým znakem. Výsledky ukázaly, že dvouletá léčba abemaciklibem (150 mg 2× denně kontinuálně) v kombinaci s endokrinní terapií statisticky signifikantně snižuje riziko invazivní rekurence (invasive disease‑free survival, iDFS) ve srovnání se samotnou endokrinní terapií (poměr rizik [HR] 0,75; 95% interval spolehlivosti [CI] 0,60–0,93; p = 0,01), s dvouletým iDFS 92,2 % vs. 88,7 % [5].
Abemaciklib v adjuvantní terapii byl schválen na základě výsledků studie monarchE, která se zaměřila na pacientky s HR+/HER2– časným karcinomem prsu s vysokým rizikem rekurence. Vysoce rizikové onemocnění bylo definováno přítomností čtyř a více pozitivních axilárních lymfatických uzlin, střední riziko 1–3 pozitivními axilárními lymfatickými uzlinami a grade 3 nebo velikostí tumoru 5 cm a větší. Menší skupinu tvořili pacienti s 1–3 pozitivními axilárními lymfatickými uzlinami a Ki‑67 (marker proliferační aktivity nádoru) alespoň 20 % jako dalším rizikovým znakem. Výsledky ukázaly, že dvouletá léčba abemaciklibem (150 mg 2× denně kontinuálně) v kombinaci s endokrinní terapií statisticky signifikantně snižuje riziko invazivní rekurence (invasive disease‑free survival, iDFS) ve srovnání se samotnou endokrinní terapií (poměr rizik [HR] 0,75; 95% interval spolehlivosti [CI] 0,60–0,93; p = 0,01), s dvouletým iDFS 92,2 % vs. 88,7 % [5].
Na základě slibných výsledků ribociklibu v paliativní systémové léčbě (studie MONALEESA‑2, ‑3 a ‑7) byl posléze ribociklib zkoumán v adjuvantním podání [3,23,24]. Studie NATALEE zahrnovala středně i vysoce rizikové pacientky, které byly definovány následovně: a) pacientky s klinickým stadiem III, b) pacientky s onemocněním ve stadiu IIA s postižením lymfatických uzlin, a c) pacientky klinického stadia IIA bez postižených lymfatických uzlin a současně s přítomností rizikových faktorů, tzn. grade 3, nebo grade 2 současně s Ki‑67 ≥ 20 % nebo s vysokým rizikem rekurence na základě genomického testu. Tato studie demonstrovala statisticky významný celkový přínos pro přežití u pacientek s pokročilým HR+/HER2– karcinomem prsu léčených ribociklibem (v dávce 400 mg denně po dobu tří týdnů a poté jeden týden, pauza po dobu tří let) a nesteroidním inhibitorem aromatázy (NSAI; letrozol v dávce 2,5 mg denně nebo anastrozol v dávce 1 mg denně po dobu ≥ 5 let) oproti pacientkám léčeným pouze NSAI. Premenopauzální ženy a muži dostávali 3,6 mg goserelinu každých 28 dní. Ribociklib s endokrinní terapií statisticky signifikantně prodlužuje iDFS u pacientek s HR+/HER2– karcinomem prsu stadia II a III. Po třech letech bylo iDFS 90,4 % vs. 87,1 % ve prospěch ribociklibu v kombinaci s NSAI oproti samotnému NSAI (HR 0,75; 95% CI 0,62–0,91; p = 0,003) [6]. Přidání ribociklibu ke standardní hormonální léčbě vedlo k relativnímu snížení míry recidivy o 25 %.
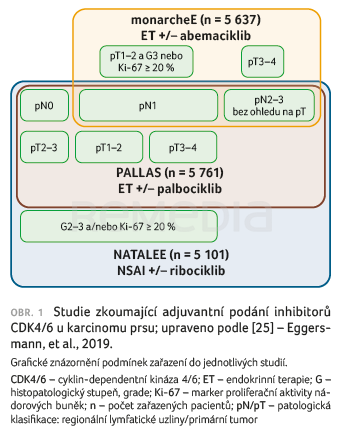
Studie PALLAS hodnotila účinnost palbociklibu (v dávce 125 mg tři týdny s jednotýdenní pauzou po dobu dvou let) v kombinaci s hormonální terapií oproti samotné hormonální terapii u pacientek s časným HR+/HER2– karcinomem prsu. Na rozdíl od studií monarchE a NATALEE mohly být do studie PALLAS zahrnuty všechny pacientky klinického stadia II a III bez ohledu na přítomnost rizikových faktorů (postižení lymfatických uzlin, grade, Ki‑67). Jako u jediné ze tří studií zkoumajících adjuvantní podání inhibitoru CDK4/6 zde nebylo dosaženo statisticky významného zlepšení iDFS pro kombinaci inhibitoru CDK4/6 s hormonální léčbou (HR 0,75; 95% CI 0,48–1,19; p = 0,23). Důvodem může být nízký podíl vysoce rizikových pacientek a vysoký podíl pacientek, které předčasně ukončily léčbu [4]. Rozdílné výsledky napříč studiemi mohou být rovněž způsobeny rozdílným zastoupením různých podskupin pacientek, inkluzivní kritéria jednotlivých studií jsou blíže vyjádřena na obrázku 1 [25].
Ribociklib a abemaciklib v kombinaci s hormonální terapií ve studiích monarchE a NATALEE statisticky signifikantně prodloužily iDFS v adjuvantním podání u pacientek s HR+/HER2– časným karcinomem mammy. Naopak ve studii PALLAS palbociklib v kombinaci s endokrinní terapií neprokázal významný přínos pro iDFS. Tyto výsledky vedly ke schválení abemaciklibu a ribociklibu v adjuvantní léčbě HR+/HER2– časného karcinomu prsu u pacientek s vysokým rizikem recidivy, avšak indikační kritéria se pro oba inhibitory CDK4/6 liší. Ribociklib je indikován k léčbě pre‑/postmenopauzálních žen a mužů s HR+/HER2– časným karcinomem prsu s anatomickým stadiem II nebo III bez ohledu na stav uzlin s vysokým rizikem recidivy v kombinaci s NSAI (anastrozol nebo letrozol), avšak zatím nemá v ČR v současné době úhradu [26]. Abemaciklib je hrazen v indikaci adjuvantní léčby časného stadia karcinomu prsu HR+/HER2– s postižením uzlin a vysokým rizikem rekurence definovaným buď jako přítomnost nejméně čtyř pozitivních axilárních lymfatických uzlin, nebo 1–3 pozitivních axilárních lymfatických uzlin a alespoň jedno z následujících kritérií: a) velikost nádoru nejméně 5 cm nebo b) grade 3, a to v kombinaci s endokrinní terapií u dospělých pacientů ve výkonnostním stavu dle ECOG (Eastern Cooperative Oncology Group) 0–1. Terapie abemaciklibem v rámci adjuvantní léčby je hrazena v maximální délce 24 měsíců. U pre‑ nebo perimenopauzálních žen je třeba endokrinní léčbu kombinovat s agonistou hormonu uvolňujícího luteinizační hormon (LHRH) [27].
Tarantino a kol. prezentovali v prosinci 2024 na San Antonio Breast Cancer Symposium výsledky komparativní analýzy pacientů splňujících inkluzivní kritéria studií NATALEE a monarchE léčených adjuvantní hormonální terapií v běžné populaci, data byla získána z Flatiron US EHR databáze. Celkem 2 534 jedinců (33,9 % z celkového počtu léčených pacientů) by splňovalo kritéria léčby adjuvantním ribociklibem (kohorta NAT) a 1 157 kritéria studie monarchE (kohorta MonE). Tříleté a pětileté přežívání bez vzdáleného relapsu (distant recurrence‑free survival, DRFS) bylo 89,2 % a 81,4 % v kohortě NAT vs. 83,4 % a 72,1 % v kohortě MonE. Pětileté přežití iDFS bylo závislé na klinickém stadiu (kohorta NAT: stadium II 87,1 %, stadium III 66,5 %; kohorta MonE: stadium I 97,3 %, stadium II 80,1 %, stadium III 64,9 %) a na postižení lymfatických uzlin (kohorta NAT: N0 86,4 %, N1 85,3 %, N2/3 63,8 %; kohorta MonE: N1 78,2 %, N2/3 63,8 %). Pětileté celkové přežití bylo rovněž delší u kohorty NAT v porovnání s kohortou MonE (89,5 % vs. 84,6 %). Tato real‑world analýza ukazuje, že kritéria pro zařazení do studie NATALEE oproti monarchE splňuje přibližně dvakrát více pacientů s časným HR+/HER2– karcinomem prsu, navíc data demonstrují suboptimální efekt samostatné hormonální adjuvantní terapie a naznačují, že až třetina pacientek může profitovat z přidání inhibitoru CDK4/6 do adjuvantní terapie [28]. Podobných závěrů se dobrala i Jhaveriho skupina. Na základě „real‑world“ retrospektivních dat autoři identifikovali, že pacientky s uzlinovým postižením mají až 2,9× vyšší riziko celkové rekurence (16,9 % vs. 5,9 %), 4,4× vyšší riziko vzdálené rekurence (13,6 % vs. 3,1 %) a 1,6× vyšší riziko mortality (16,8 % vs. 10,4 %) v porovnání s pacientkami bez postižení lymfatických uzlin [29].
Imunoterapie a novější přístupy v léčbě recidivy
Imunoterapie zatím není standardní léčbou pro HR+/HER2– karcinom prsu [30]. V několika novějších studiích je testována kombinace imunoterapie (inhibitory receptoru a ligandu receptoru programované buněčné smrti 1, PD‑1/PD‑L1) s adjuvantní chemoterapií nebo hormonální terapií. Tyto studie jsou stále ve fázi raných klinických hodnocení, ale výsledky naznačují, že imunoterapie může být perspektivní možností pro pacientky s vysokým rizikem recidivy, zejména pokud mají genetické nebo molekulární znaky predikující špatnou odpověď na standardní léčbu [31–35].
Nedávno byly publikovány výsledky dvou kontrolovaných randomizovaných studií fáze III zkoumajících použití inhibitoru kontrolního bodu u vysoce rizikových HR+ časných karcinomů prsu. Studie CheckMate 7FL (CK7FL) a KEYNOTE‑756 (KN756) zkoumaly přidání nivolumabu (CK7FL) a pembrolizumabu (KN756) k neoadjuvantní chemoterapii na bázi antracyklinu/taxanu s následnou adjuvantní hormonální léčbou. Primárním cílovým ukazatelem obou studií bylo dosažení kompletní patologické odpovědi. Obě ramena s inhibitorem kontrolního bodu dosáhla vyšší míry patologické kompletní odpovědi (rozdíl pCR 10,7 % v CK7FL a 8,7 % v KN756), přičemž v obou studiích byla potvrzena statistická signifikance (CK7FL 24,5 % vs. 13,8 %; p = 0,0021; KN756 24,3 % vs. 15,6 %; p = 0,00005). V obou studiích byla populace s vysokým rizikem relapsu definována podobně – grade 3, pozitivní lymfatické uzliny nebo cT3–4 cN0 HR+ karcinom prsu. Do studie CK7FL mohly být zařazeny také pacientky se středně diferencovaným karcinomem s nízkou expresí estrogenových receptorů (ER 1–10 %) [30,31,35,36]. Do předchozích klinických studií, např. do studie GIADA fáze II, mohly být zařazeny i pacientky s časným karcinomem prsu s ER ≥ 10 % a/nebo PR (progesteronový receptor) ≥ 10 % a současně s grade 3 a/nebo Ki‑67 ≥ 20 %. Tato studie zkoumající sekvenční podávání neoadjuvantní chemoterapie na bázi antracyklinů a nivolumabu společně s endokrinní terapií nesplnila primární cíl (dosažení pCR ≥ 25 %). Patologická kompletní odpověď byla zaznamenána pouze u 16 % pacientek s nízce diferencovaným HR+ časným karcinomem prsu [37].
Závěr
Riziko rekurence u časného karcinomu prsu zůstává významnou klinickou výzvou. Včasná detekce, personalizovaná terapie a využívání prognostických nástrojů jsou klíčové pro zlepšení léčby a snížení rizika recidivy. Studie NATALEE a monarchE přinášejí zásadní pokrok v oblasti adjuvantní léčby časného HR+/HER2– karcinomu prsu. Kombinace inhibitorů CDK4/6 s hormonální terapií prokázala výrazné zlepšení přežití bez progrese u pacientek s vysokým rizikem recidivy. Výsledky studií NATALEE a monarchE podporují zařazení abemaciklibu a ribociklibu do standardní praxe léčby časného HR+/HER2– karcinomu prsu. S registrací ribociklibu se rozšiřuje možnost léčby i pro N0 pacientky s rizikovými faktory. Role imunoterapie se jeví slibná prozatím především ve zvýšení míry dosažení patologické celkové odpovědi. Zda se však promítne i do výsledků přežívání bez relapsu onemocnění či celkového přežívání, bude vyžadovat další výzkum.
MUDr. Štěpánka Hauserová
Onkologická klinika 3. LF UK a FNKV
Šrobárova 1150/50, 100 00 Praha 10
e‑mail: stepanka.hauserova@fnkv.cz
Literatura
[1] Pehalová L, Krejčí D, Šnajdrová L, Dušek L. Cancer incidence trends in the Czech Republic. Cancer Epidemiol 2021; 74: 101975.
[2] National Cancer Institute. SEER Cancer Stat Facts: Female Breast Cancer Subtypes. Dostupné na: https://seer.cancer.gov/statfacts/html/breast‑subtypes.html
[3] Tripathy D, Im SA, Colleoni M, et al. Ribociclib plus endocrine therapy for premenopausal women with hormone‑receptor‑positive, advanced breast cancer (MONALEESA‑7): a randomised phase 3 trial. Lancet Oncol 2018; 19: 904–915.
[4] Mayer EL, Dueck AC, Martin M, et al. Palbociclib with adjuvant endocrine therapy in early breast cancer (PALLAS): interim analysis of a multicentre, open‑label, randomised, phase 3 study. Lancet Oncol 2021; 22: 212–222.
[5] Johnston SRD, Harbeck N, Hegg R, et al.; monarchE Committee Members and Investigators. Abemaciclib Combined With Endocrine Therapy for the Adjuvant Treatment of HR+, HER2‑, Node‑Positive, High‑Risk, Early Breast Cancer (monarchE). J Clin Oncol 2020; 38: 3987–3998.
[6] Slamon D, Lipatov O, Nowecki Z, et al. Ribociclib plus Endocrine Therapy in Early Breast Cancer. N Engl J Med 2024; 390: 1080–1091.
[7] Cristofanilli M, Rugo HS, Im SA, et al. Overall Survival with Palbociclib and Fulvestrant in Women with HR+/HER2‑ ABC: Updated Exploratory Analyses of PALOMA‑3, a Double‑blind, Phase III Randomized Study. Clin Cancer Res 2022; 28: 3433–3442.
[8] Rosenberg J, Chia YL, Plevritis S. The effect of age, race, tumor size, tumor grade, and disease stage on invasive ductal breast cancer survival in the U.S. SEER database. Breast Cancer Res Treat 2005; 89: 47–54.
[9] Fisher B, Bauer M, Wickerham DL, et al. Relation of number of positive axillary nodes to the prognosis of patients with primary breast cancer. An NSABP update. Cancer 1983; 52: 1551–1557.
[10] Baak JP, Gudlaugsson E, Skaland I, et al. Proliferation is the strongest prognosticator in node‑negative breast cancer: significance, error sources, alternatives and comparison with molecular prognostic markers. Breast Cancer Res Treat 2009; 115: 241–254.
[11] Koscielny S, Tubiana M, Lê MG, et al. Breast cancer: relationship between the size of the primary tumour and the probability of metastatic dissemination. Br J Cancer 1984; 49: 709–715.
[12] Fong Y, Evans J, Brook D, et al. The Nottingham Prognostic Index: five‑ and ten‑year data for all‑cause survival within a screened population. Ann R Coll Surg Engl 2015; 97: 137–139.
[13] Klein ME, Dabbs DJ, Shuai Y, et al. Prediction of the Oncotype DX recurrence score: use of pathology‑generated equations derived by linear regression analysis. Mod Pathol 2013; 26: 658–664.
[14] Cardoso F, vanʼt Veer LJ, Bogaerts J, et al.; MINDACT Investigators. 70‑Gene Signature as an Aid to Treatment Decisions in Early‑Stage Breast Cancer. N Engl J Med 2016; 375: 717–729.
[15] Early Breast Cancer Trialistsʼ Collaborative Group (EBCTCG). Effects of chemotherapy and hormonal therapy for early breast cancer on recurrence and 15‑year survival: an overview of the randomised trials. Lancet 2005; 365: 1687–1717.
[16] Davies C, Pan H, Godwin J, et al.; Adjuvant Tamoxifen: Longer Against Shorter (ATLAS) Collaborative Group. Long‑term effects of continuing adjuvant tamoxifen to 10 years versus stopping at 5 years after diagnosis of oestrogen receptor‑positive breast cancer: ATLAS, a randomised trial. Lancet 2013; 381: 805–816. Erratum in: Lancet 2013; 381: 804. Erratum in: Lancet 2017; 389: 1884.
[17] Pan H, Gray R, Braybrooke J, et al.; EBCTCG. 20‑Year Risks of Breast‑Cancer Recurrence after Stopping Endocrine Therapy at 5 Years. N Engl J Med 2017; 377: 1836–1846.
[18] Battisti NML, Smith IA. Preventing late recurrence in hormone receptor‑positive early breast cancer: a review. Eur J Cancer 2022; 172: 53–64.
[19] Scott SC, Lee SS, Abraham J. Mechanisms of therapeutic CDK4/6 inhibition in breast cancer. Semin Oncol 2017; 44: 385–394.
[20] Partridge AH, Rumble RB, Carey LA, et al. Chemotherapy and targeted therapy for women with human epidermal growth factor receptor 2–negative (or unknown) advanced breast cancer: American Society of Clinical Oncology clinical practice guideline. J Clin Oncol 2014; 32: 3307–3329.
[21] Deng Y, Ma G, Li W, et al. CDK4/6 Inhibitors in Combination With Hormone Therapy for HR+/HER2‑ Advanced Breast Cancer: A Systematic Review and Meta‑analysis of Randomized Controlled Trials. Clin Breast Cancer 2018; 18: e943–e953.
[22] Finn RS, Dering J, Conklin D, et al. PD 0332991, a selective cyclin D kinase 4/6 inhibitor, preferentially inhibits proliferation of luminal estrogen receptor‑positive human breast cancer cell lines in vitro. Breast Cancer Res 2009; 11: R77.
[23] Verma S, OʼShaughnessy J, Burris HA, et al. Health‑related quality of life of postmenopausal women with hormone receptor‑positive, human epidermal growth factor receptor 2‑negative advanced breast cancer treated with ribociclib + letrozole: results from MONALEESA‑2. Breast Cancer Res Treat 2018; 170: 535–545.
[24] Slamon DJ, Neven P, Chia S, et al. Phase III Randomized Study of Ribociclib and Fulvestrant in Hormone Receptor‑Positive, Human Epidermal Growth Factor Receptor 2‑Negative Advanced Breast Cancer: MONALEESA‑3. J Clin Oncol 2018; 36: 2465–2472.
[25] Eggersmann TK, Degenhardt T, Gluz O, et al. CDK4/6 Inhibitors Expand the Therapeutic Options in Breast Cancer: Palbociclib, Ribociclib and Abemaciclib. BioDrugs 2019; 33: 125–135.
[26] SPC Kisqali. Dostupné na: https://www.ema.europa.eu/cs/documents/product‑information/kisqali‑epar‑product‑information_cs.pdf
[27] SPC Verzenios. Dostupné na: https://www.ema.europa.eu/cs/documents/product‑information/verzenios‑epar‑product‑information_cs.pdf
[28] Tarantino P, Rugo H, Curigliano G, et al. Risk of recurrence in real‑world (RW) NATALEE‑ and monarchE‑eligible populations of patients with HR+/HER2− early breast cancer (EBC) in an electronic health record (EHR)‑derived database. Presented at the San Antonio Breast Cancer Symposium, December 11, 2024. Texas, USA.
[29] Jhaveri K, Pegram M, Neven P, et al. Real‑world evidence on risk of recurrence (ROR) in patients (pts) with node‑negative (N0) and node‑positive HR+/HER2– early breast cancer (EBC) from US electronic health records (EHR). Presented at the San Antonio Breast Cancer Symposium, December 11, 2024. Texas, USA.
[30] Loibl S, André F, Bachelot T, et al.; ESMO Guidelines Committee. Early breast cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow‑up. Ann Oncol 2024; 35: 159–182.
[31] Cardoso F, McArthur H, Schmid P, et al. Lba21 KEYNOTE 756: phase III study of neoadjuvant pembrolizumab (Pembro) or placebo (PBO)+ chemotherapy (Chemo), followed by adjuvant Pembro or PBO+ endocrine therapy (ET) for early‑stage high‑risk ER+/Her2‑breast cancer. Ann Oncol 2023; 34: 1260–1261.
[32] Cardoso F, OʼShaughnessy J, McArthur H. (GS01‑02) Phase 3 study of neoadjuvant pembrolizumab or placebo plus chemotherapy, followed by adjuvant pembrolizumab or placebo plus endocrine therapy for early‑stage high‑risk ER+/HER2− breast cancer: KEYNOTE‑756. Paper presented at the San Antonio Breast Cancer Symposium. 2023; San Antonio, Texas.
[33] Loi S, Curigliano G, Salgado RF, et al. LBA20 A randomized, double‑blind trial of nivolumab (NIVO) vs placebo (PBO) with neoadjuvant chemotherapy (NACT) followed by adjuvant endocrine therapy (ET) ± NIVO in patients (pts) with high‑risk, ER+ HER2− primary breast cancer (BC). Ann Oncol 2023; 34: S1259–S1260.
[34] Loi S, Curigliano G, Salgado R. (GS01‑01) Biomarker results in high‑risk estrogen receptor positive, human epidermal growth factor receptor 2 negative primary breast cancer following neoadjuvant chemotherapy ± nivolumab: an exploratory analysis of CheckMate 7FL. Paper presented at the San Antonio Breast Cancer Symposium. 2023; San Antonio, Texas.
[35] Nanda R, Liu MC, Yau C, et al. Effect of pembrolizumab plus neoadjuvant chemotherapy on pathologic complete response in women with early‑stage breast cancer: an analysis of the ongoing phase 2 adaptively randomized I‑SPY2 trial. JAMA Oncol 2020; 6: 676–684.
[36] Loi S, Salgado R, Curigliano G, et al. Neoadjuvant nivolumab and chemotherapy in early estrogen receptor‑positive breast cancer: a randomized phase 3 trial. Nat Med 2025; https://doi.org/10.1038/s41591‑024‑03414‑8.
[37] Dieci MV, Guarneri V, Tosi A, et al. Neoadjuvant Chemotherapy and Immunotherapy in Luminal B‑like Breast Cancer: Results of the Phase II GIADA Trial. Clin Cancer Res 2022; 28: 308–317.