Vliv nadužívání nesteroidních antirevmatik – pohled na kardotoxicitu a nefrotoxicitu
Souhrn
Vranová V. Vliv nadužívání nesteroidních antirevmatik – pohled na kardiotoxicitu a nefrotoxicitu. Remedia 2025; 35: 102–106.
Nesteroidní antirevmatika (NSA) snižují tvorbu prostaglandinů, a tím omezují bolest i zánět. Prostaglandiny významně ovlivňují např. reprodukční cyklus ženy i porod, srážlivost krve, prokrvení orgánů nebo výši krevního tlaku. Nadužívání NSA má tak vliv na mnoho fyziologických funkcí a může způsobit nežádoucí účinky léčby, zejména v gastrointestinálním a kardiovaskulárním aparátu. Toto riziko je zvýšeno zejména u geriatrických a polymorbidních pacientů.
Klíčová slova: nadužívání – NSA – kardiotoxicita – nefrotoxicita.
Summary
Vranova V. The impact of non‑steroid antirheumatic drug overuse – view of cardiotoxicity and nephrotoxicity. Remedia 2025; 35: 102–106.
Non‑steroid antirheumatic (NSA) drugs lower the prostaglandin synthesis, thus limiting both pain and inflammation. Prostaglandins have a great impact e.g. on the female reproductive cycle and birth, hemocoagulation, and blood pressure. Therefore, NSA overuse influences many physiological functions and may lead to adverse effects, concerning especially gastrointestinal and cardiovascular systems. This risk is namely increased in geriatric and polymorbid patients.
Key words: overuse – NSA – cardiotoxicity – nephrotoxicity.
Úvod
 Nesteroidní antirevmatika (NSA) snižují tvorbu prostaglandinů, a tím omezují bolest i zánět. Účinky prostaglandinů jsou však mnohočetné a proměnlivé, zvláště důležité jsou pro reprodukční cyklus ženy i porod, dále ovlivňují srážlivost krve, prokrvení orgánů, výši krevního tlaku, významnou roli hrají při zánětlivé odpovědi a vzniku bolesti. Potlačení jejich tvorby tak může způsobit velké potíže. Prostaglandiny vznikají z kyseliny arachidonové pomocí enzymu cyklooxygenázy (tab. 1). Ta má dvě izoformy – cyklooxygenázu 1 (COX‑1) a cyklooxygenázu 2 (COX‑2). Látky vznikající činností COX‑1 ovlivňují zejména srážlivost krve a vazokonstrikci/vazodilataci, zatímco činností COX‑2 vznikají hlavně růstové faktory nebo cytokiny ovládající zánět a bolest. Protizánětlivé steroidy, jako je kortizol, inhibují tvorbu všech derivátů kyseliny arachidonové, mají tak nejsilnější protizánětlivý efekt, ovšem jejich podávání je provázeno značnou mírou nežádoucích účinků. Nesteroidní protizánětlivé léky inhibují COX (podle selektivity buď obě, nebo přednostně COX‑1). Existuje i další cesta metabolizace kyseliny arachidonové pomocí enzymů lipoxygenázy, kdy vznikají např. leukotrieny, které hrají významnou roli v genezi astmatu. Důležité je, že pokud je potlačena činnost COX, roste význam lipoxygenázové cesty s následnými nežádoucími účinky, jako je např. tzv. aspirinové astma (tab. 1).
Nesteroidní antirevmatika (NSA) snižují tvorbu prostaglandinů, a tím omezují bolest i zánět. Účinky prostaglandinů jsou však mnohočetné a proměnlivé, zvláště důležité jsou pro reprodukční cyklus ženy i porod, dále ovlivňují srážlivost krve, prokrvení orgánů, výši krevního tlaku, významnou roli hrají při zánětlivé odpovědi a vzniku bolesti. Potlačení jejich tvorby tak může způsobit velké potíže. Prostaglandiny vznikají z kyseliny arachidonové pomocí enzymu cyklooxygenázy (tab. 1). Ta má dvě izoformy – cyklooxygenázu 1 (COX‑1) a cyklooxygenázu 2 (COX‑2). Látky vznikající činností COX‑1 ovlivňují zejména srážlivost krve a vazokonstrikci/vazodilataci, zatímco činností COX‑2 vznikají hlavně růstové faktory nebo cytokiny ovládající zánět a bolest. Protizánětlivé steroidy, jako je kortizol, inhibují tvorbu všech derivátů kyseliny arachidonové, mají tak nejsilnější protizánětlivý efekt, ovšem jejich podávání je provázeno značnou mírou nežádoucích účinků. Nesteroidní protizánětlivé léky inhibují COX (podle selektivity buď obě, nebo přednostně COX‑1). Existuje i další cesta metabolizace kyseliny arachidonové pomocí enzymů lipoxygenázy, kdy vznikají např. leukotrieny, které hrají významnou roli v genezi astmatu. Důležité je, že pokud je potlačena činnost COX, roste význam lipoxygenázové cesty s následnými nežádoucími účinky, jako je např. tzv. aspirinové astma (tab. 1).
Nesteroidní antirevmatika
Jak je uvedeno výše, společným mechanismem účinku NSA je inhibice COX, což je klíčový enzym tvorby prostaglandinů. Ze dvou izoenzymů COX má COX‑1 hlavně homeostatické a protektivní funkce (např. udržování prokrvení tkáně úměrného metabolickým nárokům, produkce hlenu na sliznicích apod.), zatímco COX‑2 je, mimo jiné, mohutně indukována při zánětu. Analgetický efekt NSA je prozkoumán méně než účinek antiflogistický. Předpokládá se, že je umožněn jak působením prostaglandinů na TRPV (transient receptor potential vanilloid) receptory (tzv. kapsaicinové), tak samotným potlačením zánětu [1].
Nežádoucí účinky nesteroidních antirevmatik
Pravidelné užívání NSA je spjato se zvýšeným rizikem výskytu závažných, potenciálně letálních komplikací, zejména v oblasti trávicího traktu. Další komplikace nadměrného nebo nevhodného užívání NSA zahrnují poruchy renálních funkcí, ovlivnění výše krevního tlaku, narušení srážlivosti krve, případně poškození jater. Zatímco řešením gastrointestinální toxicity těchto léků by mohla být NSA se selektivní inhibicí COX‑2, v jiných orgánech (ledviny, kardiovaskulární aparát) se nežádoucí účinky selektivních inhibitorů COX‑2 od „tradičních“ NSA významně neliší, nebo naopak znamenají vyšší riziko [2]. Dalším problémem je skutečnost, že neselektivní NSA ruší selektivitu selektivních přípravků COX‑2, takže nežádoucí účinky současného podávání např. kyseliny acetylsalicylové a celekoxibu se neliší od nežádoucích účinků konkomitantního podávání kyseliny acetylsalicylové a ibuprofenu [3]. Tuto skutečnost potvrdily i další studie [4].
Gastrointestinální nežádoucí účinky
Pod tento pojem patří dyspeptické obtíže, endoskopicky zjistitelné léze, vředy, eroze, hemoragie a jejich komplikace: krvácení, perforace, komplikované vředy apod. Enteropatie z NSA zahrnuje změnu permeability stěny střeva, vředy, striktury, krvácení nebo perforaci [5].
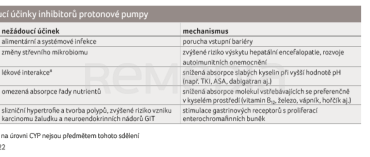 Tato rizika a nežádoucí účinky jsou dobře známy, často se jim předchází preventivním nasazením inhibitorů protonové pumpy (IPP), čímž může dojít k dalším problémům. Inhibitory protonové pumpy jsou léčiva velmi silně tlumící sekreci kyseliny chlorovodíkové, jejich vlivem tedy dochází, především při chronickém podávání, k významné elevaci intragastrického pH. Analogicky tak může docházet ke změnám absorpce konkomitantně podávaných léčiv (tab. 2) [6,7].
Tato rizika a nežádoucí účinky jsou dobře známy, často se jim předchází preventivním nasazením inhibitorů protonové pumpy (IPP), čímž může dojít k dalším problémům. Inhibitory protonové pumpy jsou léčiva velmi silně tlumící sekreci kyseliny chlorovodíkové, jejich vlivem tedy dochází, především při chronickém podávání, k významné elevaci intragastrického pH. Analogicky tak může docházet ke změnám absorpce konkomitantně podávaných léčiv (tab. 2) [6,7].
Nežádoucí účinky dlouhodobého užívání inhibitorů protonové pumpy
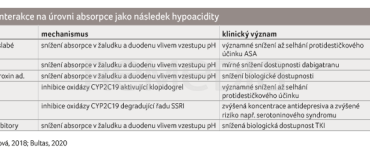 Jak je výše uvedeno, zvýšení pH v žaludku významně ovlivňuje biologickou dostupnost mnoha léčiv. Některé příklady uvádí tabulka 3 [8,9]. Málo známý je významný vliv IPP na vstřebávání a eliminaci vápníku a hořčíku. Vlivem IPP se oba tyto ionty méně vstřebávají a více vylučují, zvýšenou pozornost je třeba věnovat IPP indukované hypomagnezemii.
Jak je výše uvedeno, zvýšení pH v žaludku významně ovlivňuje biologickou dostupnost mnoha léčiv. Některé příklady uvádí tabulka 3 [8,9]. Málo známý je významný vliv IPP na vstřebávání a eliminaci vápníku a hořčíku. Vlivem IPP se oba tyto ionty méně vstřebávají a více vylučují, zvýšenou pozornost je třeba věnovat IPP indukované hypomagnezemii.
Kardiovaskulární rizika
Výsledky intervenčních i observačních studií poukazují na vyšší kardiovaskulární riziko u pacientů užívajících NSA [10]. Zvýšený zájem o kardiovaskulární bezpečnost celé skupiny NSA nastal po potvrzení kardiovaskulárních rizik koxibů [11] a stažení rofekoxibu z trhu. Jak je uvedeno výše, prostaglandiny jsou mimo jiné silnými vazodilatátory, zvyšují srdeční frekvenci a minutový srdeční objem. COX‑1 je v krevních destičkách zodpovědná za tvorbu proagregačního tromboxanu, COX‑2 je zodpovědná za syntézu antiagregačního prostacyklinu [12]. Selektivní inhibice COX‑2 snižuje produkci prostacyklinů, aniž by inhibovala vazokonstrikci a trombogenezi způsobenou tromboxanem. Výsledná nerovnováha mezi protrombotickými a antiagregačními faktory může vést k trombóze [10]. Prostaglandiny odvozené jak z COX‑1, tak i COX‑2 mají zásadní roli také v regulaci cévní homeostázy [11]. Kromě své role ve vzniku trombózy může inhibice COX‑2 přispívat k rozvoji aterosklerotických lézí přímým vlivem na vývoj plaku [13]. Nesteroidní antirevmatika jsou spojována i se zhoršením rizika srdečního selhání. Riziko se zvyšuje u pacientů se sníženou funkcí ledvin nebo srdeční nedostatečností [10].
Poruchy funkce ledvin
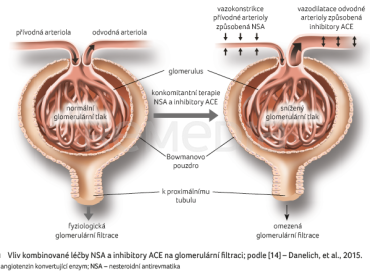 Další komplikace užívání NSA zahrnují poruchy renálních funkcí, jako jsou porucha průtoku krve ledvinami, porucha glomerulární filtrace (obr. 1) [14], narušení exkrece sodíku a sekrece draslíku [15]. Ohroženi jsou zejména pacienti s již existujícím onemocněním ledvin, kardiaci a obecně křehčí polymorbidní pacienti, hlavně senioři.
Další komplikace užívání NSA zahrnují poruchy renálních funkcí, jako jsou porucha průtoku krve ledvinami, porucha glomerulární filtrace (obr. 1) [14], narušení exkrece sodíku a sekrece draslíku [15]. Ohroženi jsou zejména pacienti s již existujícím onemocněním ledvin, kardiaci a obecně křehčí polymorbidní pacienti, hlavně senioři.
Hemodynamické změny
V případě těžšího onemocnění ledvin nebo srdce, popř. jaterní cirhózy, stejně jako u geriatrických pacientů udržují průtok krve ledvinami a glomerulární filtraci zejména vazodilatační prostaglandiny, především prostacyklin PGI2 a prostaglandin PGE2 [15]. U těchto pacientů tak může blokáda tvorby vazodilatačních prostaglandinů navodit převahu vazokonstrikčních působků, výsledkem je renální ischemie, pokles glomerulárního hydrostatického tlaku až selhání ledvin. U uvedených rizikových skupin nemocných mohou nepříznivě ovlivnit funkci ledvin i selektivní inhibitory COX‑2, a to v obdobném rozsahu jako neselektivní NSA.
Akutní intersticiální nefritida
Akutní intersticiální nefritida je imunologicky podmíněné onemocnění ledvin, nezřídka vede k akutnímu renálnímu selhání. Hlavními vyvolávajícími příčinami akutní intersticiální nefritidy jsou polékové reakce, které tvoří nadpoloviční většinu případů. Morfologicky je akutní intersticiální nefritida charakterizována přítomností intersticiálního infiltrátu, jehož dominující součástí jsou T lymfocyty. Předpokládá se, že aktivace T lymfocytů je navozena zvýšenou tvorbou leukotrienů v důsledku inhibice COX (viz tab. 1) [15].
Retence sodíku a tvorba otoků
Za normálních podmínek nemá útlum tvorby prostaglandinů navozený NSA na vodní a elektrolytové hospodářství významnější vliv, klinického významu nabývá u pacientů s onemocněním ledvin a u stavů spojených s poklesem celkového objemu tělesných tekutin, zejména v krevním řečišti, např. u dehydratovaných pacientů, pacientů užívajících značná množství diuretik apod. Za těchto podmínek může léčba NSA a následná inhibice tvorby prostaglandinů vést k retenci tekutin s tvorbou otoků, hyponatremii a hyperkalemii. Tyto děje navíc interferují s léčbou kličkovými diuretiky nebo inhibitory angiotenzin konvertujícího enzymu (ACE) [15,16], obrázek 1.
Hypertenze
U hypertoniků bývá často zvýšena aktivita sympatického nervového systému a systému renin‑angiotenzin‑aldosteron. Ve snaze minimalizovat stupeň renální ischemie způsobené vazokonstrikcí dochází v ledvinách ke zvýšenému uvolňování prostaglandinů. Inhibice této kompenzační schopnosti způsobená NSA vede k převaze vazokonstrikčních mechanismů a k možnému vzestupu tlaku krve nebo k akcentaci stávající hypertenze [16].
Reprodukční nežádoucí účinky
U pacientek ve fertilním věku je třeba mít na paměti, že užívání NSA inhibuje ovulaci a snižuje koncentrace progesteronu nejen u animálních modelů, ale také u žen [17]. Je tak namístě zvážit jejich dlouhodobé užití u pacientek, které plánují založit rodinu.
Hepatální nežádoucí účinky
Riziko vzniku hepatopatie během léčby NSA není vysoké, u pacientů s revmatoidní artritidou je však asi desetinásobně vyšší [5].
Respirační potíže asociované s NSA
U predisponovaných jedinců, zejména astmatiků, mohou po použití NSA vznikat respirační potíže, tzv. aspirinové astma. Zablokováním COX dráhy se zvýší metabolická aktivita enzymu lipoxygenázy, která syntetizuje leukotrieny (tab. 1). Leukotrieny jsou mediátory akutního i chronického zánětu, stejně jako zánětu alergického. Zvyšují cévní permeabilitu za vzniku edému, dále produkci hlenu a buněčnou infiltraci, vykazují bronchokonstrikční účinek. U predisponovaných jedinců tak mohou NSA vyvolat kopřivku, rinitidu, bronchokonstrikci až astmatický záchvat. Nesteroidní antirevmatika jsou kontraindikována u pacientů, u nichž předchozí podání vyvolalo astmatický záchvat nebo hypersenzitivní reakci [12].
Nesteroidní antirevmatika u seniorů
Přestože jsou senioři velmi častými uživateli NSA, jsou tato léčiva pro geriatrické pacienty riziková. Riziko vzniku závažných gastrointestinálních nežádoucích účinků, zejména krvácení do gastrointestinálního traktu, je totiž zvýšeno především u starších osob (ve věku ≥ 65 let), stejně jako při současném podávání kortikosteroidů, antiagregancií, antikoagulancií (včetně nových perorálních antikoagulancií) nebo dalších NSA, což je případ zejména starších pacientů. Výše popsanými chorobami kardiovaskulárního aparátu a ledvin také častěji trpí starší lidé. Nesteroidní antirevmatika pak tato onemocnění zhoršují, je zde výrazně vyšší riziko rozvoje závažných kardiovaskulárních nežádoucích účinků (infarktu myokardu, iktu, hypertenze, srdečního selhání) a poškození ledvin či jater. Proto se zejména u seniorů doporučuje dávat přednost paracetamolu, opioidům, případně jejich kombinaci před dlouhodobě systémově užívanými NSA [2].
Závěr
Nesteroidní antirevmatika patří k nejčastěji používaným lékům. Mají své nezastupitelné místo především při léčbě bolesti a zánětlivých projevů v oblasti pohybového aparátu, revmatických chorob, menstruačních obtíží, cefalgií a jiných bolestivých stavů, v mnoha indikacích jsou léčivy první volby. Podle analgetického žebříčku Světové zdravotnické organizace (WHO) se používají zejména k léčbě bolesti I. stupně nebo v kombinacích se slabými či silnými opioidy k léčbě bolesti II. nebo III. stupně.
Nesteroidní antirevmatika jsou často považována za léky první volby i u onemocnění pohybového aparátu, zřejmě díky svému protizánětlivému účinku. I když odhlédneme od rozdílného dávkování pro dosažení analgetického a antiflogistického efektu, je třeba respektovat Doporučení České revmatologické společnosti pro léčbu osteoartrózy kolenních, kyčelních a ručních kloubů, kde je v této indikaci lékem volby paracetamol a lokální NSA; užívání celkových NSA, zejména u starších pacientů, by mělo být časově omezeno na řádově 2–3 týdny [18]. Aplikace opioidů je doporučena po selhání paracetamolu a lokálních NSA jako další krok, alternativní k použití celkových NSA, především u starších nemocných s rizikovými faktory gastrointestinálními, renálními a kardiovaskulárními pro aplikaci NSA [18].
Dá se říci, že NSA jsou nezastupitelná v krátkodobé léčbě, ale nepříliš vhodná k dlouhodobému užívání, zejména u geriatrických pacientů, kteří ovšem představují většinu jejich uživatelů. To reflektují i recentní Metodické pokyny pro farmakoterapii chronické bolesti, které doporučují užívání minimální analgeticky účinné dávky po co nejkratší dobu [2].
PharmDr. MVDr. Vilma Vranová, Ph.D.
Ústav aplikované farmacie, Farmaceutická fakulta MU
Palackého tř. 1946/1, 612 00 Brno
e‑mail: vranavi@seznam.cz
Literatura
[1] Štětkářová I (ed), et al. Moderní farmakoterapie v neurologii. Praha: Maxdorf, 2015.
[2] Kozák J, et al. Metodické pokyny pro farmakoterapii chronické bolesti – speciální část. Bolest 2022; 25(Suppl 1): 7–44.
[3] Silverstein FE, Faich G, Goldstein JL, et al. Gastrointestinal toxicity with celecoxib vs nonsteroidal anti‑inflammatory drugs for osteoarthritis and rheumatoid arthritis: the CLASS study: A randomized controlled trial. Celecoxib Long‑term Arthritis Safety Study. JAMA 2000; 284: 1247–1255.
[4] Suchopár J, Prokeš M, Suchopár Š. Lékové interakce DrugAgency. Praha: DrugAgency, a.s., 2023. 1. vydání.
[5] Suchý D, Lejčko J. Léčba chronické bolesti u zánětlivých revmatických onemocnění. Vnitř Lék 2018; 64: 209–217.
[6] Scarpignato C, Tolone S. Addressing long‑term PPI safety. Dig Liver Dis 2020; 52: 853–856.
[7] Bultas J. Inhibice žaludeční sekrece – pohled farmakologa. Remedia 2022; 32: 304–311.
[8] Rychlíčková J. Následky hypoacidity navozené inhibitory protonové pumpy – tipy pro praxi. Klin Onkol 2018; 31: 409–413.
[9] Bultas J. Inhibitory protonové pumpy – známe je dobře? Jsou skutečně tak bezpečné? – část 1. Gastroent Hepatol 2020; 74: 431–441.
[10] Varga Z, Sabzwari SRA, Vargova V. Cardiovascular Risk of Nonsteroidal Anti‑Inflammatory Drugs: An Under‑Recognized Public Health Issue. Cureus 2017; 9: e1144.
[11] Rao P, Knaus EE. Evolution of nonsteroidal anti‑inflammatory drugs (NSAIDs): cyclooxygenase (COX) inhibition and beyond. J Pharm Pharm Sci 2008; 11: 81s–110s.
[12] Kotolová H, Nováková J. Nejvýznamnější nežádoucí účinky neopioidních analgetik a jejich farmakologické mechanismy. Prakt lékáren 2021; 17: e33–e41.
[13] Grosser T, Ricciotti E, FitzGerald GA. The Cardiovascular Pharmacology of Nonsteroidal Anti‑Inflammatory Drugs. Trends Pharmacol Sci 2017; 38: 733–748.
[14] Danelich IM, Wright SS, Lose JM, et al. Safety of Nonsteroidal Antiinflammatory Drugs in Patients with Cardiovascular Disease. Pharmacother 2015; 35: 520–535.
[15] Zadražil J. Nesteroidní antirevmatika a ledviny. Vnitř Lék 2006; 52: 609–613.
[16] Bindu S, Mazumder S, Bandyopadhyay U. Non‑steroidal anti‑inflammatory drugs (NSAIDs) and organ damage: A current perspective. Biochem Pharmacol 2020; 180: 114147.
[17] Gaytán M, Morales C, Bellido C, et al. Non‑steroidal anti‑inflammatory drugs (NSAIDs) and ovulation: lessons from morphology. Histol Histopathol 2006; 21: 541–556.
[18] Pavelka K. Doporučení České revmatologické společnosti pro léčbu osteoartrózy kolenních, kyčelních a ručních kloubů. Dostupné na: https://www.revmatologicka‑spolecnost.cz/doporucene‑postupy‑crs/ [cit. 18. 11. 2024]