Aktuální možnosti a perspektivy farmakoterapie obezity
Souhrn
Haluzík M, Jakubíková I, Kudláčková M, Žižka O, Horváth L. Aktuální možnosti a perspektivy farmakoterapie obezity. Remedia 2024; 34: 336–342.
Obezita představuje jeden z nejzásadnějších a nejobtížněji řešitelných problémů současné medicíny. Je to dáno především její vzrůstající prevalencí a nízkou úspěšností prevence jejího vzniku i dlouhodobého snížení hmotnosti. Obezita je jedním z nejvýznamnějších rizikových faktorů pro vznik diabetes mellitus 2. typu, arteriální hypertenze, dyslipidemie, syndromu spánkové apnoe a mnoha dalších onemocnění. Kombinace obezity a výše uvedených přidružených nemocí, často označovaná jako metabolický syndrom, zapříčiňuje výrazné zvýšení rizika kardiovaskulární morbidity a mortality a v případě diabetu také mikrovaskulárních komplikací. Obezita tak vede k významnému zkrácení délky života a zhoršení jeho kvality, na čemž se významně podílí přítomnost výše uvedených komorbidit a komplikací. V tomto článku se zaměřujeme na současné možnosti léčby obezity pomocí farmakoterapie. Věnujeme se zejména lékům s nejvyšší účinností, které fungují na principu stimulace receptorů pro glukagon‑like peptide 1 (GLP‑1) a další gastrointestinální hormony (glukózo‑dependentní inzulinotropní peptid, glukagon) a měly by být v nejbližších letech uvedeny na český trh. Diskutujeme však také antiobezitika nacházející se v časnějších fázích klinického vývoje a jejich postavení v kontextu dalších možností léčby obezity včetně bariatrické chirurgie a bariatrické endoskopie.
Klíčová slova: obezita – diabetes mellitus – agonisté GLP‑1R – bariatrická chirurgie – endoskopická léčba – semaglutid – tirzepatid.
Summary
Haluzik M, Jakubikova I, Kudlackova M, Zizka O, Horvath L. Current options and perspectives of pharmacotherapy of obesity. Remedia 2024; 34: 336–342.
Obesity represents one of the most fundamental and difficult to solve problems in contemporary medicine. This is mainly due to its increasing prevalence and the low success rate of prevention and long‑term weight loss. Obesity is one of the most important risk factors for the development of type 2 diabetes mellitus, arterial hypertension, dyslipidemia, sleep apnoea syndrome and many others. The combination of obesity and the aforementioned associated diseases, often referred to as metabolic syndrome, leads to a significant increase in the risk of cardiovascular morbidity and mortality and, in the case of diabetes, microvascular complications. Obesity causes a significant reduction in life expectancy and quality of life, which is significantly influenced by the presence of the above comorbidities and complications. In this article, we discuss the current options for the prevention and treatment of obesity with pharmacotherapy. In particular, we focus on drugs with the highest efficacy based on the principle of stimulation of receptors for glucagon‑like peptide 1 (GLP‑1) and other gastrointestinal hormones (glucose‑dependent insulinotropic peptide, glucagon) which should be introduced to the Czech market in the coming years. However, we also mention antiobesity drugs in earlier stages of clinical development and their position in the context of other obesity treatment options, including bariatric surgery and bariatric endoscopy.
Key words: obesity – diabetes mellitus – GLP‑1R agonists – bariatric surgery – endoscopic treatment – semaglutide – tirzepatide.
Úvod
Obezita se projevuje nadměrným hromaděním tukové tkáně v organismu vedoucím ke zvýšení tělesné hmotnosti nad normální mez. Pro diagnostiku obezity a její další dělení je používán tzv. body mass index (BMI) vypočítaný z poměru tělesné hmotnosti v kilogramech a druhé mocniny tělesné výšky v metrech. Hodnota BMI ≥ 30 kg/m2 je dolní hranicí pro diagnózu obezity. Ta je pak dále rozdělována na obezitu prvního, druhého a třetího stupně (viz tab. 1). Obezita je úzce propojena s řadou metabolických i dalších zdravotních komplikací, jejichž četnost a závažnost významně rostou se zvyšujícím se stupněm obezity. Obezita nebo nadváha představují významný rizikový faktor a zásadní etiopatogenetický mechanismus vzniku diabetes mellitus 2. typu (DM2T) [1]. Snížení hmotnosti může vzniku komorbidit obezity předejít nebo zpomalit jejich progresi, přičemž právě DM2T je změnami hmotnosti ovlivňován nejvíce. Kromě těsného propojení s DM2T obezita významně zkracuje délku dožití primárně v důsledku vzestupu kardiovaskulární (KV) morbidity a mortality, zvyšuje riziko vzniku některých malignit, psychiatrických onemocnění, nemocí kloubů a páteře a také syndromu spánkové apnoe [2]. Souběh obezity, inzulinové rezistence/DM2T, arteriální hypertenze, dyslipidemie a dalších onemocnění označujeme jako syndrom inzulinové rezistence či metabolický syndrom [3], jehož přítomnost několikanásobně zvyšuje KV morbiditu a mortalitu [4]. Nitrobřišní ukládání tuku, tzv. viscerální obezita, je spojeno s vyšším KV rizikem než nadměrné hromadění podkožního tuku, což je dáno mimo jiné i vyšší produkcí prozánětlivých hormonálních faktorů – tzv. adipokinů či adipocytokinů – právě ve viscerálním tuku [5–7].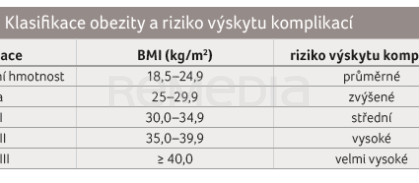
Farmakoterapie obezity prošla v posledním desetiletí překotným vývojem, který vedl k zásadní změně pohledu na optimální léčebný přístup. Zatímco v předchozích obdobích byla v popředí snaha o vyvinutí co nejúčinnějších centrálně působících antiobezitik, současnému léčebnému portfoliu i klinickému vývoji dominují léky založené na principu stimulace receptorů pro GLP‑1 (glucagon‑like peptide 1) a dalších gastrointestinálních hormonů [8]. Výhodou těchto léků proti předchozím přístupům je kromě vyšší účinnosti také jejich přímý pozitivní vliv na řadu metabolických parametrů a komorbidit obezity, jako jsou diabetes, dyslipidemie, KV komplikace, srdeční selhání a řada dalších.
V tomto článku se zaměřujeme na současné možnosti farmakoterapie obezity a zejména na bližší perspektivy antiobezitické léčby na principu agonistů receptoru GLP‑1 (GLP‑1R) nebo kombinovaných agonistů pro receptory gastrointestinálních hormomů. Diskutujeme však také další antiobezitika v časnějších fázích klinického vývoje a jejich postavení v kontextu dalších možností léčby obezity včetně bariatrické chirurgie a bariatrické endoskopie.
Nefarmakologické přístupy v léčbě obezity
Obezita patří spolu s DM2T k onemocněním, jejichž úspěšné dlouhodobé zvládnutí je podmíněno alespoň částečnou compliance pacientů s dietními a režimovými opatřeními. Při opravdu striktní změně životního stylu je možné tělesnou hmotnost výrazně zredukovat a docílit i remise diabetu. Reálně se však toto podaří spíše výjimečně. I přesto jsou však dietní a režimová opatření základním přístupem léčby obezity, který by měl být ideálně kombinován s využitím farmakoterapie a interakce pacienta s multidisciplinárním týmem odborníků léčících obezitu (obezitolog, nutriční terapeut, psycholog atd.) [9,10]. Zvýšení fyzické aktivity náleží (pokud to stav pacienta umožňuje) k mimořádně důležitým opatřením. Typ fyzické aktivity, její trvání a intenzitu je třeba nastavit individuálně podle možností a preferencí pacienta a s respektováním omezení vyplývajících z přítomnosti dalších nemocí.
Dlouhodobé dodržování redukční diety se snížením celkového energetického příjmu (obvykle o 500–700 kcal denně) s omezením příjmu nasycených tuků, u diabetiků i rychle uvolnitelných sacharidů a u hypertoniků také s omezením konzumace soli je nezbytným předpokladem pro snížení hmotnosti. Motivaci pacientů i dlouhodobou compliance s dietním režimem výrazně zlepšují pravidelné konzultace jídelníčku pacienta jak s lékařem, tak s nutričním terapeutem.
Podrobnější popis konkrétních dietních přístupů přesahuje možnosti tohoto článku. Z hlediska dlouhodobého dodržování dietních omezení se jako vhodnější jeví spíše pestré diety bez výraznějších omezení konkrétních makronutrientů. Typickým příkladem může být středomořská dieta při dodržení snížení celkového energetického příjmu. Naopak v poslední době hodně komerčně propagovaná ketogenní dieta má jen minimum důkazů o dlouhodobější úspěšnosti při snížení hmotnosti. Efekty jsou sice poměrně rychlé, ale obvykle pouze dočasné. Intenzivně je v poslední době studován i efekt tzv. přerušovaného hladovění (intermittent fasting), kdy jsou období příjmu potravy střídána obdobími úplného hladovění (například režim 8 hodin jídla, 16 hodin hladovění) [11]. I zde platí, že základem úspěchu je individualizace redukční diety dle možností a preferencí pacienta.
Farmakoterapie obezity
Aktuálně jsou v České republice k dispozici tři léky s prokázaným efektem na snížení hmotnosti, které lze použít u pacientů s obezitou s diabetem i bez diabetu. Perorálně je možné podat orlistat, fixní kombinaci naltrexon/bupropion a subkutánně (s.c.) liraglutid. V používání i pravidlech preskripce dříve oblíbeného centrálně působícího fenterminu došlo v poslední době vzhledem k nežádoucím účinkům a možné návykovosti k výraznému omezení a lze očekávat jeho postupné stažení z trhu.
Primárním mechanismem působení orlistatu je inhibice střevní lipázy, což díky omezení štěpení tuků ve střevě snižuje jejich vstřebávání [12]. Výhodou je omezený průnik do systémového oběhu s minimálním množstvím kontraindikací. Orlistat má zároveň ale poměrně časté nežádoucí účinky (bolesti břicha, nadýmání, průjmy), a to zejména při požití potravy s vyšším obsahem tuků. Podává se obvykle 3× denně v dávce 120 mg. U spolupracujících pacientů a v rámci klinických studií bylo při léčbě tímto přípravkem dosahováno hmotnostních úbytků až 7 kg a v dlouhodobé studii Xendos došlo i ke snížení incidence DM2T [13]. Dlouhodobá efektivita v běžné klinické praxi je však vzhledem k nežádoucím účinkům omezená.
Naltrexon/buprobion je fixní kombinací 8 mg antidepresiva bupropionu a 90 mg opioidního antagonisty naltrexonu. Působením v centrálním nervovém systému snižuje tato kombinace pocit hladu a vede k dlouhodobému poklesu hmotnosti podle provedených studií o 3–8 kg [14]. U diabetiků zlepšuje díky snížení hmotnosti kompenzaci diabetu. Přípravek je indikován jako doplněk k dietě se sníženým obsahem kalorií u dospělých pacientů s BMI ≥ 30 kg/m2 nebo s BMI 27–30 kg/m2 za přítomnosti jedné nebo více přidružených chorob souvisejících s hmotností (DM2T, dyslipidemie, arteriální hypertenze). Opatrnosti je potřeba při podávání u pacientů s antidepresivy.
Nejúčinnějším antiobezitikem dostupným v České republice je liraglutid. Jedná se o agonistu GLP‑1R, který snižuje příjem potravy, zvyšuje sekreci inzulinu a tlumí sekreci glukagonu. Liraglutid je v nižších dávkách (do 1,8 mg denně) používán také jako antidiabetikum. U diabetiků 2. typu s vysokým KV rizikem nebo s anamnézou KV komplikací bylo v rozsáhlé studii LEADER při podávání liraglutidu ve srovnání s placebem prokázáno významné snížení celkové a KV mortality, pokles výskytu KV komplikací a zpomalení progrese diabetického onemocnění ledvin [15].
V rozsáhlém klinickém programu SCALE byla prokázána velmi dobrá účinnost i bezpečnost této léčby při snižování hmotnosti při dávkování až do 3 mg denně [16,17]. Aplikuje se s.c. 1× denně pomocí předplněného pera. Indikace jsou podobné jako u fixní kombinace naltrexon/bupropion (viz výše). Liraglutid je navíc schválen i pro dospívající (≥ 12 let) s obezitou (BMI odpovídající ≥ 30 kg/m² u dospělých) a tělesnou hmotností převyšující 60 kg. Liraglutid je v České republice aktuálně jediným dostupným agonistou GLP‑1R s antiobezitickou indikací bez ohledu na přítomnost či nepřítomnost diabetu.
Chirurgická a endoskopická léčba obezity
Nejúčinnější metodou léčby obezity a jejích metabolických komplikací je bariatrická chirurgie, ačkoliv poklesy hmotnosti při podávání nejnovějších antiobezitik se již začínají účinnosti bariatrie postupně přibližovat (viz níže). Bariatrickou chirurgii je dle aktuálních doporučení možné využít u pacientů s obezitou 2. a vyššího stupně bez komplikací, případně u obezity 1. stupně s přítomnými komplikacemi, jako jsou diabetes, dyslipidemie a další [18]. Nejnovější doporučení IFSO (International Federation for the Surgery of Obesity and Metabolic Disorders) posouvají hranice indikace bariatrické chirurgie ještě níže. Podle těchto doporučení lze zvážit operaci u všech osob s BMI > 35 kg/m2 bez ohledu na přítomnost komorbidit, zatímco při BMI > 30 kg/m2 lze operaci doporučit u osob s DM2T nebo u osob, které nebyly schopny udržet dlouhodobé snížení hmotnosti [19,20].
Na bariatrickou chirurgii je nutné pohlížet jako na velmi mocný nástroj umožňující výrazné snížení hmotnosti, který však bez dobré spolupráce pacienta může v dlouhodobém horizontu také selhat. Dlouhodobé snížení hmotnosti bariatrická chirurgie přináší zejména u pacientů, kteří jsou dobře edukováni a pečlivě sledováni již před provedením výkonu a poté prakticky celoživotně. Pro dlouhodobě udržitelný pokles hmotnosti je nezbytná motivace pacienta k dodržování dietních omezení a ke změně životního stylu po snížení hmotnosti. V současné době je celosvětově nejpoužívanějším výkonem tzv. rukávová resekce žaludku (sleeve gastrectomy) následovaná tzv. gastrickým bypassem a jeho modifikacemi, které kromě zmenšení žaludku zahrnují také vynechání proximální části tenkého střeva z kontaktu s potravou [21].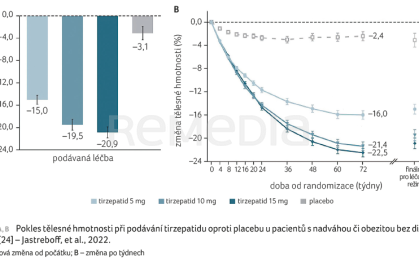
Jedinou v současné době dostupnou endoskopickou metodou v České republice je tzv. endoskopická plikace žaludku, kdy je objem žaludku zmenšen pomocí endoskopického prošití žaludeční stěny [22]. Zájemce o podrobnější popis bariatrické a endoskopické léčby odkazujeme na literaturu zaměřenou na toto téma [18,23]. Za zmínku stojí nepochybně fakt, že i u řady nemocných po bariatrické chirurgii či endoskopii může být k dlouhodobému udržení hmotnostních poklesů také nezbytné podávání antiobezitik.
Nová antiobezitika v klinické praxi ČR dosud nedostupná
Těsně před uvedením na trh v České republice je tirzepatid, duální agonista GLP‑1/GIP (glukózodependentní inzulinotropní polypeptid) receptoru. V 72týdenní studii SURMOUNT‑1 vedlo podávání tirzepatidu v dávkách 5, 10 a 15 mg 1× týdně s.c. u pacientů s nadváhou nebo obezitou bez diabetu k poklesu hmotnosti o 15, 19,5 a 20,9 % ve srovnání se snížením o 3,1 % v placebové skupině při průměrné hmotnosti na počátku studie 104,8 kg [24] (graf 1A, B). Při podávání dávky 15 mg tak dosáhlo nejméně 5% poklesu hmotnosti 91 % pacientů. Ve studii SURMOUNT‑2 byla zkoumána účinnost a bezpečnost tirzepatidu u pacientů s nadváhou či obezitou a DM2T [25]. Podávání tirzepatidu v dávkách 10 a 15 mg vedlo ke snížení hmotnosti o 12,8 a 14,7 % ve srovnání s poklesem o 3,2 % v placebové skupině. Nejméně 5% poklesu hmotnosti dosáhlo ve skupině s 10 mg tirzepatidu 79 % a ve skupině s 15 mg tirzepatidu 83 % pacientů vs. 32 % pacientů v placebové skupině. Výskyt nežádoucích účinků v obou studiích byl vyšší u tirzepatidu než u placeba.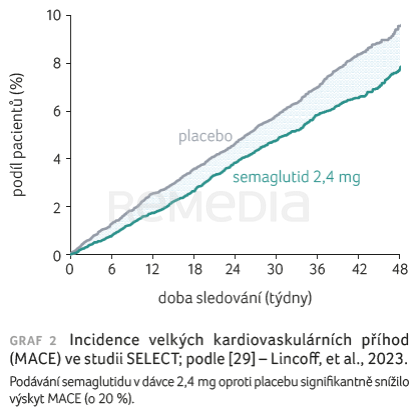
Uvedení na český trh se postupně blíží také agonista GLP‑1R semaglutid v antiobezitické indikaci s dávkováním až 2,4 mg 1× týdně. Zatím je v ČR k dispozici pouze v dávkování maximálně 1 mg 1× týdně v indikaci léčby DM2T. Antiobezitický program semaglutidu 2,4 mg zahrnoval mimo jiné studii STEP 1 provedenou u pacientů s nadváhou nebo obezitou bez diabetu, kde byl semaglutid titrovaný až do dávky 2,4 mg 1× týdně porovnáván s placebem [26]. Po 68 týdnech vedlo podávání semaglutidu k celkovému poklesu hmotnosti o 15,3 kg ve srovnání se snížením o 2,6 kg v placebové skupině. Studie STEP 2 měla podobné uspořádání, ale zahrnula pacienty s obezitou a DM2T, kterým byl podáván semaglutid s titrací dávky na 1 mg 1× týdně, 2,4 mg 1× týdně nebo placebo. Hmotnost poklesla o 6,9 kg a 9,7 kg (7 %, respektive 9,7 % počáteční hmotnosti), zatímco při podávání placeba bylo zaznamenáno snížení o 3,5 kg (3,4 %) [27]. Semaglutid v dávce 2,4 mg měl také významnější vliv na snížení hodnoty glykovaného hemoglobinu (HbA1c) a zlepšení řady dalších kardiometabolických parametrů (výraznější snížení krevního tlaku, hodnoty triglyceridů a koncentrací C‑reaktivního proteinu). Studie STEP 3 zahrnovala podobné spektrum pacientů jako STEP 1 – na jejím počátku však všichni pacienti podstoupili osm týdnů nízkokalorické diety a poté byla po celou dobu studie jak v léčebném, tak placebovém rameni prováděna intenzivní intervence životního stylu [28]. Po 68 týdnech sledování se hmotnost při podávání semaglutidu snížila o 16 % ve srovnání s poklesem o 5,7 % při podávání placeba. Nejméně 5% pokles hmotnosti byl zaznamenán u 86,6 % pacientů s podáváním semaglutidu vs. u 47,6 % s podáváním placeba. Ve studii STEP 4 byli pacienti s obezitou bez diabetu randomizováni k podávání semaglutidu 2,4 mg nebo placeba a po 48 týdnech byla část pacientů léčených semaglutidem převedena na placebo a u části bylo pokračováno v léčbě až do 68. týdne. V léčené podskupině došlo k poklesu hmotnosti o dalších 7,9 %, zatímco u pacientů převedených na placebo se hmotnost naopak o 6,9 % zvýšila.
Do multicentrické dvojitě zaslepené, randomizované, placebem kontrolované kardiovaskulární studie SELECT bylo zařazeno 17 604 pacientů ve věku 45 let a více bez přítomnosti diabetu, kteří měli již existující KV onemocnění a BMI ≥ 27 kg/m2 [29]. Pacienti byli randomizováni k aplikaci s.c. semaglutidu v dávce 2,4 mg jednou týdně nebo placeba. Primárním KV cílovým ukazatelem byla kombinace smrti z KV příčin, nefatálního infarktu myokardu nebo nefatální cévní mozkové příhody. Průměrná délka podávání semaglutidu nebo placeba byla 34,2 ± 13,7 měsíce a průměrná doba sledování byla 39,8 ± 9,4 měsíce. Primární KV příhoda se vyskytla u 569 z 8 803 (6,5 %) pacientů ve skupině se semaglutidem a u 701 z 8 801 (8,0 %) pacientů ve skupině s placebem. U pacientů s podáváním semaglutidu tedy došlo k poklesu výskytu KV příhod o 20 % (graf 2). Nežádoucí příhody vedoucí k trvalému ukončení léčby zkoušeným přípravkem se vyskytly u 1 461 (16,6 %) pacientů ve skupině se semaglutidem a u 718 (8,2 %) pacientů ve skupině s placebem (p < 0,001). Hmotnost při podávání semaglutidu poklesla o 9,39 % ve srovnání se snížením 0,88 % při podávání placeba. Zároveň byla při podávání semaglutidu nižší i celková a KV mortalita a riziko vzniku srdečního selhání. Jde o zcela přelomovou studii, kdy bylo poprvé v historii při podávání jakéhokoliv antiobezitika prokázáno, že kromě efektivního snížení hmotnosti dochází také k poklesu výskytu KV komplikací.
Nová antiobezitika v klinických studiích
Kromě výše uvedených látek jsou v pokročilých fázích klinického hodnocení léčby obezity první nepeptidový perorální agonista GLP‑1R orforglipron (vyvíjený společností Eli Lilly), duální agonista GLP‑1R a receptoru pro glukagon survodutid (Boehringer Ingelheim), kombinace amylinového agonisty cagrilintidu a semaglutidu (CagriSema, Novo Nordisk) a trojitý agonista receptorů pro GLP‑1/GIP a glukagon retatrutid (Eli Lilly). Antiobezitickou studii má rovněž perorální semaglutid v dávkování až 50 mg 1× denně.
U pacientů s nadváhou nebo obezitou bez diabetu v klinické studii fáze III OASIS 1 vedlo podávání upravené formy p.o. semaglutidu s lepší biologickou dostupností v dávce 50 mg denně k poklesu hmotnosti o 15,1 % ve srovnání s poklesem o 2,4 % při podávání placeba. Nejméně 5% poklesu hmotnosti dosáhlo při podávání semaglutidu 85 % pacientů ve srovnání s 26 % při podávání placeba [30]. Tolerance léčby byla srovnatelná s výsledky dalších studií s agonisty GLP‑1R. Zatím není jasné, nakolik bude antiobezitický výzkumný program s vysokodávkovaným perorálním semaglutidem pokračovat s ohledem na fakt, že velmi úspěšně si vede ve stejné indikaci semaglutid 2,4 mg podávaný 1× týdně s.c. (viz výše).
Ve studii fáze II byl hodnocen nepeptidový perorální agonista GLP‑1R orforglipron. Jeho podávání vedlo u pacientů s nadváhou nebo obezitou k poklesu hmotnosti až o 12,6 % po 26 týdnech a o 14,7 % po 36 týdnech ve srovnání s poklesem o 2,0 % v placebové skupině [31]. Výhodou je díky nepeptidové struktuře dobrá biologická dostupnost a absorpce nezávislá na příjmu potravy. To představuje rozdíl oproti výše popsanému perorálnímu semaglutidu, který musí být podáván nalačno (po spolknutí je nutné s podáváním dalších léků či s příjmem potravy 30 minut vyčkat).
Dosud nejlepší účinnost při snížení hmotnosti prokázal trojitý agonista GLP‑1/GIP/glukagonového receptoru retatrutid. Ve dvojitě zaslepené randomizované studii fáze II byl srovnáván jeho efekt při podávání jednou týdně v dávkách 1, 4, 8 mg a 12 mg oproti placebu po dobu 48 týdnů u pacientů s nadváhou či obezitou [32]. Tělesná hmotnost po 24 týdnech se snížila o 7,2 %, 12,0 %, 17,3 % a 17,5 % ve srovnání s poklesem o 1,6 % v placebové skupině. Po 48 týdnech představovaly poklesy hmotnosti 8,7 %, 17,1 %, 22,8 % a 24,2 % vs. 2,1 % v placebové skupině (graf 3). Tvar křivek poklesu hmotnosti navíc zjevně napovídal, že velmi pravděpodobně ještě nebylo po 48 týdnech dosaženo maximálního účinku.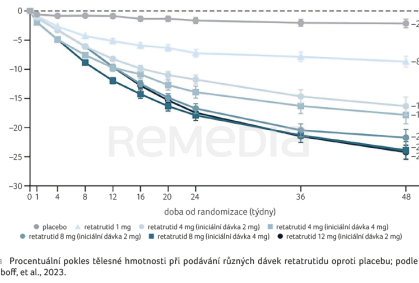
V loňském roce byly také publikovány výsledky studie fáze II hodnotící kombinaci amylinového analogu cagrilintidu a agonisty GLP‑1R semaglutidu v dávkách 2,4 a 2,4 mg s podáváním 1× týdně [33]. Do této 32týdenní studie fáze II byli zařazeni pacienti s DM2T a BMI ≥ 27 kg/m2, kteří užívali metformin s inhibitorem sodíko‑glukózového kotransportéru 2 (SGLT2) nebo bez něj, kteří byli randomizováni k podávání kombinace, semaglutidu nebo cagrilintidu jednou týdně. Hodnota HbA1c poklesla při podávání kombinace o 2,2 %, což bylo významně více než při podávání samotného semaglutidu (–1,8 %) nebo cagrilintidu (–0,9 %). Pokles hmotnosti dosáhl 15,6 % při podávání kombinace ve srovnání se snížením o 5,1 % při podávání semaglutidu a o 8,1 % při podávání cagrilintidu. Pro kontext je nutno zdůraznit, že jde o studii u diabetiků 2. typu a redukce hmotnosti je srovnatelná s dosud nejvyšší účinností u diabetiků zaznamenanou u tirzepatidu ve studii SURMOUNT‑2 [25].
Další zajímavou látkou v pokročilejších fázích klinického hodnocení je duální agonista GLP‑1R a receptoru pro glukagon survodutid. Publikovány byly výsledky studie fáze II srovnávající účinnost a bezpečnost čtyř dávek survodutidu s placebem u pacientů s nadváhou či obezitou bez diabetu [34]. Hmotnost při podávání survodutidu v dávkách 0,6 mg; 2,4 mg; 3,6 mg a 4,8 mg poklesla o 6,2 %, 12,5 %, 13,2 % a 14,9 % ve srovnání se snížením o 2,8 % ve skupině s placebem.
Další pozitivní účinky nových antiobezitik
V tomto článku se primárně zaměřujeme na účinnost a bezpečnost nových antiobezitik z pohledu vlivu na tělesnou hmotnost a podrobněji nepopisujeme jejich antidiabetické efekty, které jsou zejména u semaglutidu a tirzepatidu velmi podrobně prozkoumány a oba léky jsou již rutinně podávány v antidiabetické indikaci – semaglutid v dávkování 1 mg 1× týdně (v některých zemích až 2 mg 1× týdně), případně perorálně 1× denně v maximální dávce 14 mg, a tirzepatid ve stejných dávkách jako v indikaci obezity (maximální dávka 15 mg 1× týdně s.c.). Jde nepochybně o mimořádně účinná antidiabetika s řadou prokázaných pozitivních účinků nad rámec zlepšení kompenzace diabetu a snížení hmotnosti. Prakticky všechny z uvedených látek také vedou k poklesu krevního tlaku a ke zlepšení koncentrací lipidů, přičemž u některých jde vzhledem k časnějším fázím studií zatím jen o předběžné výsledky.
Další velmi intenzivně zkoumanou indikací u řady výše popsaných antiobezitik je MASH (steatohepatitida asociovaná s metabolickou dysfunkcí, dříve označovaná zkratkou NASH). Velmi povzbudivé výsledky s významným snížením míry zánětlivého postižení byly publikovány pro semaglutid [35], tirzepatid [36] i survodutid [37] (graf 4). Lze očekávat, že po dokončení studií fáze III bude využití těchto léků a potenciálně dalších nových antiobezitik i v oblasti léčby MASH.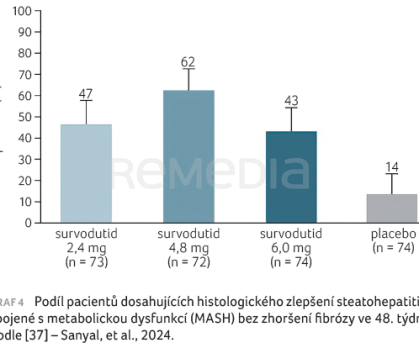
Tirzepatid má zatím jako jediný ukončenou studii primárně zaměřenou na ovlivnění syndromu spánkové apnoe. Podávání tirzepatidu ve srovnání s placebem vedlo kromě očekávaného snížení hmotnosti také k velmi významnému poklesu apnea–hypopnea indexu, který je používán jako základní parametr k určení tíže syndromu spánkové apnoe [38].
Lze očekávat, že s ohledem na výše popsané pozitivní výsledky studie SELECT na snížení výskytu KV komplikací u nemocných s nadváhou či obezitou bez diabetu při podávání semaglutidu 2,4 mg 1× týdně [29] budou následovat podobné studie i s ostatními léky z této skupiny. Žádná další takováto studie však zatím nebyla ukončena.
Nežádoucí účinky a bezpečnost nových antiobezitik
Pokud jde o nežádoucí účinky a bezpečnost nových antiobezitik na principu stimulace receptorů GLP‑1 a dalších hormonů gastrointestinálního traktu, lze konstatovat, že jsou v zásadě podobné jako u agonistů GLP‑1R. Nejčastější nežádoucí účinky při podávání jsou gastrointestinální – nevolnost, průjem, zvracení s frekvencí a tíží srovnatelnými s agonisty GLP‑1R. Uvedené nežádoucí účinky obvykle nevedly k nutnosti vysazení podávané léčby. Pokud jde o účinky na KV systém, typické je mírné zvýšení tepové frekvence o 2–3 tepy/min. Celkový vliv na KV riziko je však velmi pravděpodobně pozitivní (randomizovanou studií zatím prokázán pouze pro semaglutid 2,4 mg 1× týdně ve studii SELECT).
Otevřenou otázkou zůstává, nakolik a u jak vysokého procenta pacientů by významné a rychlé snížení hmotnosti při zásadním omezení příjmu potravy mohlo vést k poklesu jak tukové, tak svalové hmoty. Pojem sarkopenická obezita je v současné době stále častěji používán pro pacienty, u nichž je obezita spojena se sarkopenií a snížením tělesné zdatnosti, které se při dalším razantním poklesu hmotnosti mohou zhoršovat. Je zjevné, že i přes velmi nadějné výsledky bude třeba také získat konkrétnější data právě u subpopulací ohrožených vysokým rizikem sarkopenie, například u starších nemocných, u pacientů s renální insuficiencí atp.
Závěr a perspektivy
V posledních letech je stále více zjevné, že k léčbě obezity a zejména pro dlouhodobé udržení snížené hmotnosti bude podobně jako u jiných chronických onemocnění nutné více využívat farmakoterapii. Aktuálně používaný liraglutid a fixní kombinace naltrexon/bupropion představují účinná a bezpečná antiobezitika, ovšem novější přípravky, jako je semaglutid dávkovaný 2,4 mg 1× týdně nebo tirzepatid, jsou o poznání efektivnější. V přímém srovnání semaglutidu 2,4 mg 1× týdně a liraglutidu 3 mg denně byl u pacientů s nadváhou nebo obezitou pokles hmotnosti –15,8 % při podávání semaglutidu vs. –6,4 % při podávání liraglutidu [39]. Nová antiobezitika tak posouvají možnosti léčby na podstatně vyšší úroveň blížící se některým méně účinným bariatrickým operacím.
Zajímavé efekty na snížení hmotnosti i kardiometabolické parametry mají další antiobezitika na principu stimulace účinků GLP‑1 a dalších gastrointestinálních hormonů: nepeptidový perorální agonista GLP‑1R orforglipron, duální agonista receptoru pro GLP‑1 a glukagon survodutid, kombinace amylinového agonisty cagrilintidu a semaglutidu, trojitý agonista receptoru pro GLP‑1/GIP a glukagon retatrutid, perorální semaglutid v dávkování až 50 mg 1× denně. Dosud nejvyšší popsaný úbytek hmotnosti činil 24 % při podávání nejvyšší dávky retatrutidu ve studii fáze II u nediabetiků [32].
Nastává tedy nepochybně čas na přesnější definování postavení nových antiobezitik v algoritmu léčby obezity tak, aby tato léčba byla nákladově efektivní a zároveň i dlouhodobě financovatelná z veřejného zdravotního pojištění. I přes vysokou efektivitu bude stále u řady pacientů účinnějším přístupem bariatrická chirurgie či endoskopie. I zde však může mít farmakoterapie svůj význam v přípravě před výkonem nebo naopak k dlouhodobému udržení snížené hmotnosti [40].
Základem dlouhodobě úspěšné léčby obezity i přes postupně se zvyšující dostupnost stále účinnějších antiobezitik však stále zůstává dlouhodobé dodržování diety a pravidelná fyzická aktivita k prevenci ztráty svalové hmoty. Úspěšnost léčby výrazně zvyšuje zapojení multidisciplinárního týmu zahrnujícího kromě obezitologa a dalších specializací též nutriční a psychologickou podporu, případně pomoc dalších odborníků a využití telemonitoringu a telemedicíny.
Podpořeno MZ ČR – RVO („Institut klinické a experimentální medicíny – IKEM, IČ 00023001“) a projektem Národní institut pro výzkum metabolických a kardiovaskulárních onemocnění (Program EXCELES, číslo projektu: LX22NPO5104) – Financováno Evropskou unií – Next Generation EU.
Prof. MUDr. Martin Haluzík, DrSc.
Institut klinické a experimentální medicíny
Centrum diabetologie
Vídeňská 1958/9, 140 21 Praha 4
e-mail: martin.haluzik@ikem.cz
Literatura
[1] Chatterjee S, Khunti K, Davies MJ. Type 2 diabetes. Lancet 2017; 389: 2239–2251.
[2] O’Rahilly S. Science, medicine, and the future. Non-insulin dependent diabetes mellitus: the gathering storm. BMJ 1997; 314: 955–959.
[3] Reaven G. Metabolic syndrome: pathophysiology and implications for management of cardiovascular disease. Circulation 2002; 106: 286–288.
[4] Reaven G, Abbasi F, McLaughlin T. Obesity, insulin resistance, and cardiovascular disease. Recent Prog Horm Res 2004; 59: 207–223.
[5] Despres JP. Cardiovascular disease under the influence of excess visceral fat. Crit Pathw Cardiol 2007; 6: 51–59.
[6] Dolinkova M, Dostalova I, Lacinova Z, et al. The endocrine profile of subcutaneous and visceral adipose tissue of obese patients. Mol Cell Endocrinol 2008; 291: 63–70.
[7] Bluher M. Adipose tissue dysfunction in obesity. Exp Clin Endocrinol Diabetes 2009; 117: 241–250.
[8] Le Roux C, Mondoh A. Treatment of obesity with medications binding the glucagon-like peptide 1 receptor: what is the current state of play? Expert Opin Pharmacother 2024; 25: 131–138.
[9] Borghouts LB, Keizer HA. Exercise and insulin sensitivity: a review. Int J Sports Med 2000; 21: 1–12.
[10] Delahanty LM, Halford BN. The role of diet behaviors in achieving improved glycemic control in intensively treated patients in the Diabetes Control and Complications Trial. Diabetes Care 1993; 16: 1453–1458.
[11] Mattson MP, Longo VD, Harvie M. Impact of intermittent fasting on health and disease processes. Ageing Res Rev 2017; 39: 46–58.
[12] Maetzel A, Ruof J, Covington M, Wolf A. Economic evaluation of orlistat in overweight and obese patients with type 2 diabetes mellitus. Pharmacoeconomics 2003; 21: 501–512.
[13] Chiasson JL, Brindisi MC, Rabasa-Lhoret R. The prevention of type 2 diabetes: what is the evidence? Minerva Endocrinol 2005; 30: 179–191.
[14] Saunders KH, Igel LI, Aronne LJ. An Update on Naltrexone/Bupropion Extended-Release in the Treatment of Obesity. Expert Opin Pharmacother 2016; 17: 2235–2242.
[15] Marso SP, Daniels GH, Brown-Frandsen K, et al. Liraglutide and Cardiovascular Outcomes in Type 2 Diabetes. N Engl J Med 2016; 375: 311–322.
[16] Davies MJ, Bergenstal R, Bode B, et al. Efficacy of Liraglutide for Weight Loss Among Patients With Type 2 Diabetes: The SCALE Diabetes Randomized Clinical Trial. JAMA 2015; 314: 687–699.
[17] Pi-Sunyer X, Astrup A, Fujioka K, et al. A Randomized, Controlled Trial of 3.0 mg of Liraglutide in Weight Management. N Engl J Med 2015; 373: 11–22.
[18] Dixon JB, le Roux CW, Rubino F, Zimmet P. Bariatric surgery for type 2 diabetes. Lancet 2012; 379: 2300–2311.
[19] Rubino F, Nathan DM, Eckel RH, et al. Metabolic Surgery in the Treatment Algorithm for Type 2 Diabetes: a Joint Statement by International Diabetes Organizations. Obes Surg 2017; 27: 2–21.
[20] Eisenberg D, Shikora SA, Aarts E, et al. 2022 American Society of Metabolic and Bariatric Surgery (ASMBS) and International Federation for the Surgery of Obesity and Metabolic Disorders (IFSO) Indications for Metabolic and Bariatric Surgery. Obes Surg 2023; 33: 3–14.
[21] Schauer PR, Bhatt DL, Kirwan JP, et al. Bariatric Surgery versus Intensive Medical Therapy for Diabetes – 5-Year Outcomes. N Engl J Med 2017; 376: 641–651.
[22] Gys B, Plaeke P, Lamme B, et al. Endoscopic Gastric Plication for Morbid Obesity: a Systematic Review and Meta-analysis of Published Data over Time. Obes Surg 2019; 29: 3021–3029.
[23] Fried M a kol. Bariatrická a metabolická chirurgie. 1. vydání ed. Praha: Mladá fronta, 2011.
[24] Jastreboff AM, Aronne LJ, Ahmad NN, et al. Tirzepatide Once Weekly for the Treatment of Obesity. N Engl J Med 2022; 387: 205–216.
[25] Garvey WT, Frias JP, Jastreboff AM, et al. Tirzepatide once weekly for the treatment of obesity in people with type 2 diabetes (SURMOUNT-2): a double-blind, randomised, multicentre, placebo-controlled, phase 3 trial. Lancet 2023; 402: 613–626.
[26] Wilding JPH, Batterham RL, Calanna S, et al. Once-Weekly Semaglutide in Adults with Overweight or Obesity. N Engl J Med 2021; 384: 989–1002.
[27] Davies M, Faerch L, Jeppesen OK, et al. Semaglutide 2.4 mg once a week in adults with overweight or obesity, and type 2 diabetes (STEP 2): a randomised, double-blind, double-dummy, placebo-controlled, phase 3 trial. Lancet 2021; 397: 971–984.
[28] Wadden TA, Bailey TS, Billings LK, et al. Effect of Subcutaneous Semaglutide vs Placebo as an Adjunct to Intensive Behavioral Therapy on Body Weight in Adults With Overweight or Obesity: The STEP 3 Randomized Clinical Trial. JAMA 2021; 325: 1403–1413.
[29] Lincoff AM, Brown-Frandsen K, Colhoun HM, et al. Semaglutide and Cardiovascular Outcomes in Obesity without Diabetes. N Engl J Med 2023; 389: 2221–2232.
[30] Knop FK, Aroda VR, do Vale RD, et al. Oral semaglutide 50 mg taken once per day in adults with overweight or obesity (OASIS 1): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet 2023; 402: 705–719.
[31] Wharton S, Blevins T, Connery L, et al. Daily Oral GLP-1 Receptor Agonist Orforglipron for Adults with Obesity. N Engl J Med 2023; 389: 877–888.
[32] Jastreboff AM, Kaplan LM, Frias JP, et al. Triple-Hormone-Receptor Agonist Retatrutide for Obesity – A Phase 2 Trial. N Engl J Med 2023; 389: 514–526.
[33] Frias JP, Deenadayalan S, Erichsen L, et al. Efficacy and safety of co-administered once-weekly cagrilintide 2.4 mg with once-weekly semaglutide 2.4 mg in type 2 diabetes: a multicentre, randomised, double-blind, active-controlled, phase 2 trial. Lancet 2023; 402: 720–730.
[34] le Roux CW, Steen O, Lucas KJ, et al. Glucagon and GLP-1 receptor dual agonist survodutide for obesity: a randomised, double-blind, placebo-controlled, dose-finding phase 2 trial. Lancet Diabetes Endocrinol 2024; 12: 162–173.
[35] Newsome PN, Buchholtz K, Cusi K, et al. A Placebo-Controlled Trial of Subcutaneous Semaglutide in Nonalcoholic Steatohepatitis. N Engl J Med 2021; 384: 1113–1124.
[36] Loomba R, Hartman ML, Lawitz EJ, et al. Tirzepatide for Metabolic Dysfunction-Associated Steatohepatitis with Liver Fibrosis. N Engl J Med 2024; 391: 299–310.
[37] Sanyal AJ, Bedossa P, Fraessdorf M, et al. A Phase 2 Randomized Trial of Survodutide in MASH and Fibrosis. N Engl J Med 2024; 391: 311–319.
[38] Malhotra A, Grunstein RR, Fietze I, et al. Tirzepatide for the Treatment of Obstructive Sleep Apnea and Obesity. N Engl J Med 2024; doi: 10.1056/NEJMoa2404881.
[39] Rubino DM, Greenway FL, Khalid U, et al. Effect of Weekly Subcutaneous Semaglutide vs Daily Liraglutide on Body Weight in Adults With Overweight or Obesity Without Diabetes: The STEP 8 Randomized Clinical Trial. JAMA 2022; 327: 138–150.
[40] Horvath L, Mraz M, Jude EB, Haluzik M. Pharmacotherapy as an Augmentation to Bariatric Surgery for Obesity. Drugs 2024; doi: 10.1007/s40265-024-02029-0.