Léčba atopické dermatitidy pimekrolimem
Souhrn:
Kulmanová L. Léčba atopické dermatitidy pimekrolimem. Remedia 2019; 29: 463–466.
Atopická dermatitida je časté chronické onemocnění kůže, které významně ovlivňuje kvalitu života pacientů. První příznaky se objevují nejčastěji v dětství, ve většině případů pak dochází k postupnému zlepšování s věkem. Pacienti však mohou v následujících letech vyvinout další choroby s atopickým pozadím vzniku, např. bronchiální astma. Včasnou léčbou atopické dermatitidy je možné tento tzv. atopický pochod přerušit. Ke zlatému standardu dosavadní léčby patřily topické kortikosteroidy, které ovšem při dlouhodobém užívání zapříčiňují atrofii kůže, a nehodí se tak k ošetřování citlivých oblastí, jako je např. obličej. Pimekrolimus je topický inhibitor kalcineurinu, který tyto atrofogenní účinky nevykazuje a podle posledních evropských doporučení pro léčbu atopické dermatitidy je vhodný pro ošetřování citlivých oblastí kůže u dětí a dospělých s lehkou až středně těžkou formou onemocnění. Nejčastějším nežádoucím účinkem při léčbě pimekrolimem je pálení a brnění v místě aplikace. Dlouhodobé studie neodhalily žádné vážné nežádoucí účinky doprovázející jeho používání.
Summary:
Kulmanova L. Treatment of atopic dermatitis with pimecrolimus. Remedia 2019; 29: 463–466.
Atopic dermatitis is a common chronic skin disease which significantly deteriorates the quality of life of patients. First symptoms often occur in childhood and the condition tends to improve with age. Some patients may develop other diseases with atopic background with time, such as bronchial asthma. Appropriate therapy of atopic dermatitis can interrupt this so called atopic march. Topical corticosteroids have been the gold standard in the local treatment of atopic dermatitis. However, their long‑term use leads to skin atrophy and thus they are not suitable for treating sensitive skin areas such as face. Pimecrolimus is a topical calcineurin inhibitor which does not show any atrophogenic impact on skin. According to the last European guidelines for treatment of atopic eczema, pimecrolimus is recommended for therapy of sensitive skin areas in children and adults with mild to moderate atopic dermatitis. The most common adverse effect of its use is the sense of local burning. No serious adverse effects connected with pimecrolimus therapy were discovered in long‑term studies so far.
Key words: pimecrolimus ‒ topical calcineurin inhibitors ‒ atopic dermatitis
Atopická dermatitida
Atopická dermatitida (AD) je chronické zánětlivé onemocnění kůže charakterizované střídáním období vzplanutí a následného zklidnění a subjektivně provázené silným svěděním. Častěji postihuje jedince s pozitivní rodinnou anamnézou jiných chorob atopického spektra, jako jsou bronchiální astma, rinitida či konjunktivitida. Prevalence AD v evropské populaci se udává mezi 15‒20 % u dětí a 2‒5 % u dospělých [1]. Onemocnění se vyskytuje ve třech formách, které se od sebe liší dobou výskytu, lokalizací a mnohdy i charakterem projevů. Během života mohou plynule přecházet jedna v druhou nebo může některá úplně chybět. Ačkoliv jsou u většiny pacientů první příznaky přítomny již v raném dětském věku, není výjimkou, že se ekzém poprvé objeví až v dospělosti.
Kojenecká forma začíná během prvních měsíců života nejčastěji na obličeji. Vlivem vnějších i vnitřních faktorů (např. potravinových alergenů, probíhající infekce) může dojít k rozšíření ložisek na krk, trup a do oblastí náchylných k zapářce, jako jsou kožní záhyby či plenková oblast. Nejvýraznější bývají obtíže na konci prvního roku života, postupně pak většinou slábnou.
V předškolním a školním věku popisujeme tzv. dětskou formu atopického ekzému, při které se projevy soustředí do oblastí končetinových flexur, na krk a ruce. Kůže je i v období klidu suchá, zhrubělá, s výraznějším olupováním. Během školního věku se přibližně tři čtvrtiny pacientů zhojí, u zbývajících pak ekzém přetrvává s různou intenzitou do dospělosti.
Dospělá forma ekzému může postihovat stejné lokality jako během dospívání nebo se může projevit jen v omezeném rozsahu, např. na očních víčkách či na rukou. Zhoršení je pak často podmíněno fyzickým či psychickým stresem nebo kontaktem s dráždivými látkami běžně přítomnými v prostředí (detergenty, kosmetika, kovy apod.).
Etiopatogeneze
Atopický ekzém dnes vnímáme jako multifaktoriální onemocnění, k jehož rozvoji je nutná interakce vnímavého vnitřního prostředí a provokujících vnějších vlivů. U většiny pacientů nacházíme tzv. extrinsickou neboli alergickou formu AD, u níž je přítomna vysoká koncentrace imunoglobulinu E (IgE) a onemocnění se zhoršuje kontaktem s alergeny vnějšího prostředí. Právě porucha kožní bariéry se v posledních letech dostala do popředí výzkumu etiopatogeneze AD. Ukazuje se, že mutace v genech kódujících epidermální diferenciaci a podílejících se na tvorbě bariérové funkce kůže mohou být primární příčinou rozvoje choroby. Spolu se zvýšenou prostupností pro vnější alergeny s sebou přinášejí také zvýšenou transepidermální ztrátu vody, která je příčinou typické suchosti kůže atopiků.
Hlavní roli v imunologických pochodech na pozadí atopického ekzému hrají T lymfocyty. Jimi produkované cytokiny vedou ke zvýšené tvorbě IgE a spouštějí kaskádovitou aktivaci dalších buněk, např. keratinocytů, makrofágů a eozinofilů, a udržují tak onemocnění aktivní.
Léčba atopické dermatitidy
Léčba AD je převážně lokální
a režimová. Kromě pravidelného používání emoliencií
patřily v posledních desetiletích mezi léky první volby
topické kortikosteroidy (topic corticosteroids, TCS), které se
vyznačují nespecifickým protizánětlivým, imunosupresivním
a vazokonstrikčním účinkem (tab. 1)
[2]. Tyto jejich vlastnosti zároveň ale přispívají k negativnímu
dopadu na kůži při delším používání, vedou
k její atrofii, tvorbě angiektazií a nelze též
zanedbat jejich možné systémové účinky při delším ošetřování
větších ploch. Z těchto důvodů vidíme mezi pacienty
nárůst tzv. kortikofobie, tedy obav z používání TCS, což
se negativně projevuje na dodržování léčebných
doporučení. Podle studie z roku 2011, která se zabývala
právě problémem kortikofobie, až 80 % pacientů má z TCS
obavy, a třetina z nich je proto nepoužívá podle
doporučení lékaře [3].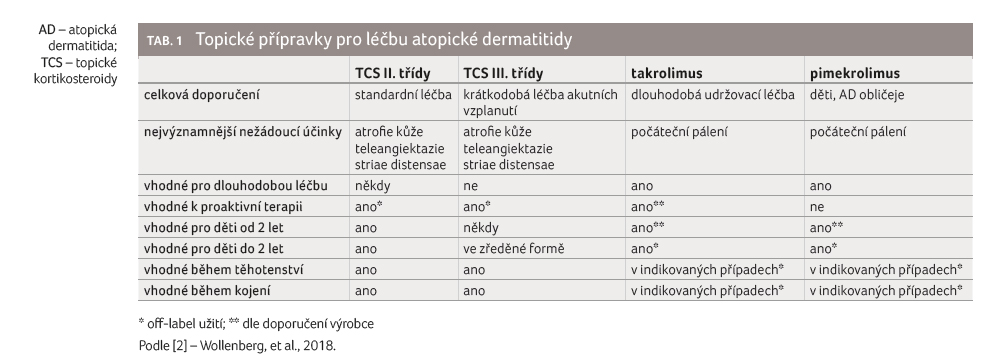
Lokální kortikosteroidy tak stále hrají nezastupitelnou roli ve zvládání akutních exacerbací AD, avšak vzhledem k jejich nežádoucím účinkům při dlouhodobém užívání se rozvinula snaha o zavedení nových léků s lepším bezpečnostním profilem.
Pimekrolimus – topický
inhibitor kalcineurinu
Na přelomu tisíciletí byl na trh uveden pimekrolimus (PIM) ve formě 1% krému jako jeden ze dvou dostupných topických inhibitorů kalcineurinu. Kalcineurin je fosfatáza, tedy enzym odstraňující fosfátovou skupinu. Jeho substrátem je v tomto případě transkripční faktor lokalizovaný v cytoplazmě T lymfocytů, který je po defosforylaci přenesen do jádra a podílí se tam na aktivaci T lymfocytů. Inhibicí kalcineurinu dojde tedy k selektivnímu snížení produkce prozánětlivých cytokinů produkovaných T lymfocyty a žírnými buňkami. Díky tomu PIM efektivně tlumí zánětlivé procesy v kůži, zároveň pak díky velikosti svojí molekuly jen omezeně proniká do oběhu a vykazuje minimální systémové koncentrace [4]. Díky svým vlastnostem – větší selektivitě v mechanismu účinku a omezenému systémovému vstřebávání – byl od začátku nadějnou alternativou TCS.
Zatím nejrozsáhlejším sledováním věnujícím se PIM byla tzv. PETITE studie, která probíhala mezi lety 2004 a 2010 v několika zdravotnických centrech po celém světě [5]. Výjimečná byla jak svým rozsahem, tak věkem sledovaných pacientů. Zúčastnilo se jí 2 418 dětí ve věku od tří do 12 měsíců s lehkým až středně těžkým ekzémem, které byly rozděleny do dvou skupin. Jedna ošetřovala ekzém PIM, druhá slabými až středně silnými TCS a během následujících pěti let se porovnávala bezpečnost a účinnost léčby PIM a TCS, monitorovaly se její nežádoucí účinky a eventuální vliv na vyvíjející se imunitní systém. Ukázalo se, že obě léčiva mají rychlý nástup účinku, více než polovina pacientů v obou skupinách dosáhla léčebného úspěchu už ve třetím týdnu používání. Po pěti letech vykazovalo přibližně 90 % zúčastněných jen minimální známky onemocnění, na což měla vliv pravděpodobně zčásti účinná léčba, zčásti přirozený sklon AD zmírňovat se s věkem. Nejčastěji zmiňovaným nežádoucím účinkem během používání PIM bylo pálení v místě aplikace, což je stav popisovaný u obou dostupných topických inhibitorů kalcineurinu [6]. Ve většině případů během několika dní postupně odeznívá a pouze zřídka je důvodem pro ukončení léčby. Studie prokázala, že používání PIM i TCS v dobách vzplanutí atopického ekzému nemá ani v dlouhodobém horizontu vliv na vyvíjející se imunitní systém. U dětí byla sledována reakce na běžná očkování, četnost výskytu bakteriálních a virových infekcí, růstové křivky a další imunologické parametry. Závěrem studie bylo tedy možno konstatovat, že PIM se dá použít jako lék první volby u lehké a středně těžké AD u dětí a je schopen v těchto případech nahradit TCS. Pimekrolimus dokázal omezit spotřebu TCS, a díky tomu předcházet atrofii kůže, která terapii TCS provází, což je zvlášť přínosné u dětí, kde je již fyziologicky epidermis tenčí, a na citlivých místech těla (oční víčka, kožní záhyby apod.).
Na výzkum případných atrofogenních účinků PIM se soustředila jedna z prvních studií s touto látkou publikovaná v roce 2001 [7]. Porovnávala atrofogenní účinek PIM, středně silného a silného TCS a vehikula. Po čtyřech týdnech používání byla měřena tloušťka kůže jak ultrazvukem, tak ověřena histologicky. Již během osmého dne bylo na ultrazvuku možno pozorovat ztenčení kůže v místech ošetřovaných TCS, během čtyř týdnů pak dosáhlo 10‒15 %. Tloušťka kůže v místech ošetřovaných PIM a vehikulem se během studie nezměnila.
Souběžně se studií PETITE probíhala studie sledující efekt PIM u dětí starších 12 let s AD hlavy a krku [4]. Během 12 týdnů 47 % zúčastněných dosáhlo úplného či téměř úplného zhojení, u 45 % došlo ke zhojení AD na očních víčkách a léčba PIM byla spojena s ústupem kožní atrofie.
Čtyřměsíční multicentrická studie provedená v Německu sledovala účinek a bezpečnost intermitentní dlouhodobé léčby PIM [8]. Zúčastnilo se jí 3 200 pacientů a jejich lékařů, obě skupiny hodnotily spokojenost s léčbou PIM a porovnávaly ji s dosavadní léčbou TCS. Celkem 82 % zúčastněných dosáhlo během čtyř měsíců úplného či zcela úplného zhojení a 74 % ošetřujících lékařů hodnotilo léčbu PIM jako lepší než dosavadní terapii.
Důležitým poznatkem je, že ani rozsáhlé epidemiologické studie provedené během dvaceti let existence lokálních kalcineurinových inhibitorů na trhu nepotvrdily dříve zmiňovaný možný vyšší výskyt lymfomů a kožních nádorů u pacientů užívajících PIM či takrolimus v lokální léčbě AD [9‒11].
Závěr
Topické inhibitory kalcineurinu hrají dnes v léčbě AD nezastupitelnou roli. Naplnily naděje, které do nich byly vkládány, a jsou schopné zastoupit dosud standardně používané TCS v tišení akutních vzplanutí, aniž by negativně ovlivňovaly stav kůže při dlouhodobém používání. Pimekrolimus je doporučován pro léčbu dětí a dospělých s lehkým až středně těžkým atopickým ekzémem, zvlášť pak v místech s tenkou epidermis, jako jsou víčka, periorální a genitální oblast, axily a inguiny. Jeho užívání je spojeno s méně častými nežádoucími účinky, jako je lokální pocit pálení a brnění ihned po aplikaci, dlouhodobé studie nezjistily výskyt závažnějších nežádoucích účinků. Ačkoliv podle oficiálních doporučení je PIM schválen pro použití u dětí starších dvou let, některé studie už doložily jeho bezpečnost i u mladších věkových kategorií [4]. Právě pro tyto skupiny může znamenat největší přínos, protože často se AD poprvé objevuje již během prvních měsíců života, kdy kožní bariéra ještě není plně vyvinutá a je důležité vyhýbat se léčivům, která ji dále oslabují. Včasnou a účinnou terapií se také daří zastavit tzv. atopický pochod, kdy AD postupně přechází v alergickou rinitidu a asthma bronchiale. Můžeme tedy doufat, že další výzkumy podpoří tyto závěry a PIM bude oficiálně uvolněn i pro mladší děti.
Seznam použité literatury
- [1] Hercogová J, et al. Klinická dermatovenerologie. Praha: Mladá fronta, 2019. 1. vyd.
- [2] Wollenberg A, Barbarot S, Bieber T, et al. Consensus‑based European guidelines of atopic eczema in adults and children: part I. J Eur Dermatol Venerol 2018; 32: 657‒682.
- [3] Aubert‑Wastiaux H, Moret l, Le Rhun A, et al. Topical corticosteroid phobia in atopic dermatitis: a study of its nature, origins and frequency. Br J Dermatol 2011; 165: 808‒814.
- [4] Murrell D, Calvieri S, Ortonne J, et al. A randomized controlled trial of pimecrolimus team 1% in adolescents and adults with head and neck atopic dermatitis and intolerant of, or dependent on, topical corticosteroids. Br J Dermatol 2007; 157: 954‒959.
- [5] Sigurgeirsson B, Boznanski A, Todd G, et al. Safety and efficacy of pimecrolimus in atopic dermatitis: 5‑year randomized trial. Pediatrics 2015; 135: 597‒605.
- [6] Bornhovd E, Burgdorf W, Wollenberg A. Immunomodulatory macrolactams for topical treatment of inflammatory skin diseases. Curr Opin Investig Drugs 2002; 3: 708‒712.
- [7] Queille‑Roussel C, Paul C, Duteil L, et al. The new topical ascomycin derivative SDZ ASM 981 does not induce skin atrophy hen applied to normal skin for 4 weeks: a randomized, double‑blind controlled study. Br J Dermatol 2001; 144: 507‒513.
- [8] Gollnick H, Luger T, Freytag S, et al. StabiEL: stabilization of skin condition with Elidel – a patients’ satisfaction observational study addressing the treatment, with pimecrolimus team, of atopic dermatitis pretreated with topical corticosteroid. J Eur Acad Dermatol Venerol 2008; 22: 1319‒1325.
- [9] Sigfried E, Jaworski J, Hebert A. Topical calcineurin inhibitors and lymphoma risk: evidence update with impications for daily practise. Am J Clin Dermatol 2013; 14: 163‒178.
- [10] Arellano F, Wnetworth C, Arana A, et al. Risk of lymphoma following exposure to calcineurin inhibitors and topical steroids in patiens wit atopic dermatitis. J Invest Dermatol 2007; 127: 808‒816.
- [11] Hui R, Lide W, Chan J, et al. Association between exposure to topical tacrolimus or pimecrolimus and cancers. Ann Pharmacother 2009; 43: 1956‒1963.