Postavení opioidů v léčbě bolesti
Souhrn:
Opioidy jsou v léčbě bolesti preferované i zatracované. Opioidy patří do farmakoterapie bolesti, kde zaujímají třetí stupeň analgetického žebříčku. Mnoha pacientům přinášejí úlevu, ale mají také svá rizika, která plynou z jejich povahy, z farmakologických a fyziologických vlastností. Nejobávanější je riziko závislosti, které vzrůstá s rozšiřováním preskripce opioidů, s chybným užíváním a s nesprávnou indikací. K bezpečné preskripci a k včasnému rozpoznání rizika mohou pomoci nová kritéria závislosti Americké psychiatrické asociace DSM‑V z roku 2013. K uspokojivé léčbě vede správná titrace opioidů a pravidelné kontroly jejich účinku.
Key words: non cancer pain – therapy – opioids – risk – efficacy.
Summary:
Opioids are both preferred and condemned in the treatment of pain. They are an important part of the pharmacotherapy of pain and belong to the third degree of the analgesic ladder. They bring relief to many patients but they also have their risks, which are related to their nature, pharmacological and physiological properties. The risk of addiction is the most feared complication, which increases with the expansion of their prescription, incorrect indication, and inappropriate use. The new criteria of addiction according to DSM V published by American Psychiatric Association in 2013 can contribute to the safe prescribing and early detection of risks. The proper titration of opioids and regular checks of their effect result in the satisfactory treatment of pain.
Úvod
Bolest provází člověka od narození, dokonce za uterinního života může plod cítit bolest. Každý člověk někdy v životě bolest zažil. Bolest akutní je jev fyziologický a je signálem faktického nebo potenciálního poškození tkáně nebo orgánu. Bolest ukazuje na místo postižení a na příčinu. Mezi typy akutní bolesti řadíme také bolest pooperační.
Chronická bolest není na rozdíl od akutní bolesti jevem fyziologickým, ale je to syndrom, onemocnění, jehož příčina nemusí být známa, nebo je stabilizovaná, či dokonce vyléčená. Léčení akutní a chronické bolesti se zásadně liší, a to jak ve výběru léků, tak ve způsobu podání.
Za chronickou se považuje bolest trvající déle než tři měsíce. Představuje velký problém z hlediska zdravotnického, sociálního i psychologického. Nemocného invalidizuje, vyžaduje časté návštěvy různých lékařů, narušuje pracovní, společenské i rodinné vztahy. Významně snižuje kvalitu života. Z patofyziologického hlediska dělíme bolest na nociceptivní, neuropatickou, smíšenou a psychickou nebo psychosomatickou. U chronické bolesti je velmi často přítomna i psychická komponenta a komponenta psychosociální. Proto je také chronická bolest označována jako bio‑psycho‑sociální syndrom.
Výskyt chronické bolesti se stále zvyšuje. Je to dáno mnoha faktory jak medicínskými, tak společenskými. Paradoxně pokroky v medicíně, ale také dennodenní stres, prodlužující se věk, méně pohybu, to vše se podílí na vzniku a udržování chronického bolestivého stavu.
Chronická bolest u onkologických pacientů a nenádorová bolest se liší v projevu i v léčení. V tomto sdělení je pozornost věnována chronické nenádorové bolesti (CHNNB). Bolest se u více než 50 % pacientů týká pohybového ústrojí. Tito pacienti trpící chronickou bolestí projdou celou řadou odborných vyšetření i různých léčení, užívají rozličná analgetika, která si i kupují. Nejčastějším výsledkem takového postupu jsou pak nežádoucí účinky a neuspokojivá léčba bolesti. Pokud se pacient dostaví k algeziologovi, je mu zpravidla poskytnuta systematická komplexní léčba chronické nenádorové bolesti multidimenzionálního onemocnění.
Léčba chronické bolesti
Chronická nenádorová bolest by měla být léčena na několika úrovních – algeziologické, rehabilitační, psychologické, případně sociální a ve spolupráci s dalšími specialisty (neurology, ortopedy a dalšími). Ne vždy jsou splněny podmínky pro tuto komplexní péči, přesto systematický přístup vzdělaného algeziologa najde jistě optimální cestu ke zlepšení kvality života a k uspokojivému zmírnění dlouhodobého bolestivého stavu. Cílem je zlepšení kvality života díky snížení míry bolesti, úpravě spánku, díky zlepšení funkční zdatnosti a v nejlepším případě návrat do zaměstnání.
Algeziologický přístup je jednak farmakologický, při nedostatečném účinku intervenční, včetně využití nejmodernějších neuromodulačních metod, které umožní minimalizovat farmakoterapii, zejména opioidy.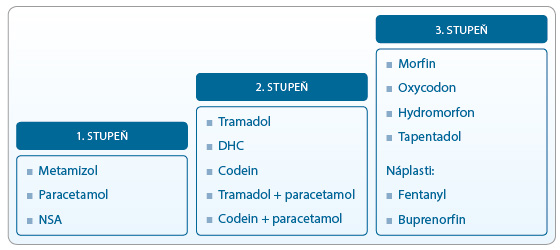
Základem farmakologického postupu je třístupňový analgetický žebříček podle Světové zdravotnické organizace (World Health Organization, WHO), dnes už běžně známý (obr. 1). První stupeň farmakoterapie bolesti představují neopioidní analgetika a nesteroidní antirevmatika (NSA), ve druhém stupni jsou zařazeny slabé opioidy, v první řadě tramadol, dále dihydrocodein a codein, který je účinný v kombinaci s paracetamolem. Stejně tak tramadol je v posledních letech na trhu v kombinaci s paracetamolem. Účinnost takového analgetika se významně zvýší. Podle ukazatele NNT (number needed to treat; počet léčených pacientů, který je nutný k tomu, aby jeden pacient dosáhl 50% úlevy od bolesti) je nejúčinnější paracetamol 1 000 mg + codein 60 mg (NNT 2,2). Paracetamol 650 mg s tramadolem 75 mg dosahují hodnoty NNT 2,6, zatímco tramadol 100 mg má NNT 4,8 a samotný codein 60 mg NNT 16,7 a samotný paracetamol 1 000 mg NNT 3,8 (tab. 1) [1]. Třetí stupeň analgetického žebříčku představují silné 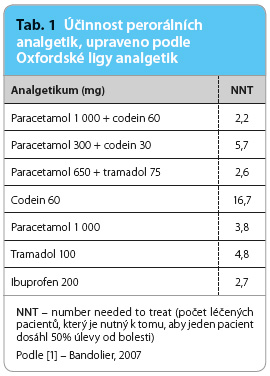 opioidy. Pro chronickou bolest jsou indikované perorální formy s prodlouženým působením nebo formy náplasťové. K perorálním patří morfin, oxycodon, hydromorfon a nejnovější tapentadol. Ve formě náplasti jsou podávány opioidy fentanyl a buprenorfin. Zejména pro nádorovou bolest při průlomové bolesti jsou indikované transmukózní formy fentanylu (sublinguální, bukální, nazální ve spreji a náplasťová bukální forma).
opioidy. Pro chronickou bolest jsou indikované perorální formy s prodlouženým působením nebo formy náplasťové. K perorálním patří morfin, oxycodon, hydromorfon a nejnovější tapentadol. Ve formě náplasti jsou podávány opioidy fentanyl a buprenorfin. Zejména pro nádorovou bolest při průlomové bolesti jsou indikované transmukózní formy fentanylu (sublinguální, bukální, nazální ve spreji a náplasťová bukální forma).
Pro léčbu CHNNB nejsou vhodné injekční formy (pethidin, piritramid, morfin). Mají rychlý nástup účinku s krátkým trváním účinku a invazivní aplikaci, což vše může být u chronické bolesti rizikové z hlediska závislosti nebo nadužívání, a navíc nepřinášejí kontinuální úlevu, jaké je třeba v případě chronické bolesti docílit.
Opioidy lze kombinovat s léčivy prvního stupně analgetického žebříčku, někdy, zvláště pokud je třeba zajistit pomoc při zvýšené bolesti, např. z důvodu zvýšené fyzické námahy apod., lze použít druhý stupeň. V tom případě mají výhodu kombinované přípravky slabých opioidů s paracetamolem. Analgetika prvního až třetího stupně jsou velmi dobře účinná u nociceptivní bolesti, to znamená u bolesti periferní (kosti, svaly, klouby) a viscerální. Nižší účinnosti je dosaženo při ovlivnění neuropatické bolesti, která vzniká porušením nervové tkáně (na jakékoliv úrovni) a je charakterizována typickým vjemem bolesti, poruchou citlivosti a možnou poruchou termického čití (vyjádřena pojmy: pálivá, vystřelující, dysestezie, parestezie, hyperestezie až hyperalgezie, alodynie). V těchto případech jsou podle doporučení Evropské federace neurologických společností (European Federation of Neurological Societies, EFNS) a Společnosti pro studium a léčbu bolesti (SSLB) první léčebnou volbou antiepileptika (gabapentin, pregabalin) a tricyklická antidepresiva (amitriptylin, duloxetin). Opioidy jsou na druhém až třetím místě volby. Lepší účinek u neuropatické bolesti prokazuje tramadol, který má přednost před silnými opioidy.
Součástí léčby CHNNB je podání antidepresivních léčiv (SSRI, SNRI). Selektivní inhibitory zpětného vychytávání serotoninu (selective serotonin reuptake inhibitors, SSRI) nemají analgetický účinek, ale uspokojivě zlepší psychický stav pacienta, který dlouhodobě trpí bolestí; inhibitory zpětného vychytávání serotoninu a noradrenalinu (serotonin and noradrenaline reuptake inhibitors, SNRI) mají mírný analgetický účinek zvláště u neuropatické bolesti. Duloxetin z této skupiny je indikován u bolestivé diabetické polyneuropatie jako lék první volby.
Jak antiepileptika, tak antidepresiva je možno kombinovat s opioidy i s analgetiky užívanými v rámci prvního stupně léčby chronické bolesti. Opatrnosti je třeba u přípravků z druhého stupně v kombinaci s tramadolem, kde dochází k interakci a mohl by se objevit serotoninový syndrom.
Nesteroidní analgetika se pacientům s CHNNB nemohou podávat dlouhodobě, protože mají závažné nežádoucí účinky (krvácení do gastrointestinálního traktu, snížená srážlivost, renální insuficience, interakce s warfarinem či s kortikosteroidy, nevhodné jsou zvláště u seniorů starších 65 let). Při mírné a střední bolesti je zvláště u seniorů vhodný paracetamol, který je ve Spojených státech amerických i v Evropě první volbou mezi neopioidními analgetiky. V kombinaci s codeinem je dobře účinný a bezpečný u seniorů s akutní bolestí, například u osteoartrózy se střední intenzitou bolesti, nebo jako pomocná medikace [2].
Silné opioidy
Opioidy tvoří skupina látek, jež se váží na opioidní receptory, které se nacházejí v mozku, v míše a v periferních tkáních. Dříve byly užívány hlavně pro léčbu nádorové bolesti, v posledních více než dvaceti letech jsou součástí léčby CHNNB. A jejich spotřeba stále vzrůstá. Eriksen [3] uvádí zvýšení preskripce opioidů pro CHNNB během dvaceti let v Dánsku o více než 600 %. U nás nárůst není tak velký, přestože přesná data nejsou k dispozici. Předpis opioidů je u nás omezen receptem s modrým pruhem a může je předepsat každý lékař, pokud tyto recepty vlastní. Opioidy nemají tzv. stropový efekt, tzn., že jejich účinnost není omezena dávkou. Určitě to platí pro nádorovou bolest, ale nenádorová bolest je v mnoha významných aspektech odlišná. Ve většině případů je časově omezena dobou přežití pacienta. To u nenádorové bolesti neplatí, ta spontánně neodezní a může trvat po neomezeně dlouhou dobu. Chronickou bolestí může trpět mladý člověk stejně tak jako starý.
Silné opioidy mají některé přednosti před ostatními léčivy. Indikací k jejich podání je silná nesnesitelná velmi intenzivní bolest, která nereaguje na komplexní léčbu, bez ohledu na původ této bolesti. Výhody silných opioidů spočívají nejen v analgetické účinnosti, ale rovněž v tom, že nepůsobí na sliznici gastrointestinálního traktu a nezpůsobují krvácení jako NSA, neovlivňují parenchymové orgány, je možné je použít u polymorbidních pacientů, dokonce v malých dávkách u starých pacientů. K nežádoucím účinkům opioidů patří nauzea, zvracení, sedace, pruritus, obstipace. S výjimkou obstipace tyto nežádoucí účinky během relativně krátké doby vymizejí, vzniká na ně tolerance. Obstipace přetrvává u více než poloviny pacientů po celou dobu užívání opioidů. Z dlouhodobých nežádoucích účinků se mohou vyvinout kognitivní poruchy, změna nálady, ovlivnění endokrinního systému – androgenní deficit, snížení koncentrace testosteronu může přispět k rozvoji osteoporózy. Dochází ke snížení imunity [4]. Závažným nežádoucím účinkem opioidů je deprese dechového centra. U pacientů s bolestí přetrvávající i při opioidní léčbě se projeví jen vzácně, při užívání vysokých dávek opioidů nebo pokud pacient trpí pokročilou plicní chorobou nebo při užívání v kombinaci s benzodiazepiny či s hypnotiky, při rozvratu vnitřního prostředí, při selhání ledvin apod. Zejména při užití vyšších dávek opioidů může dojít k hyperalgezii – k abnormálnímu čití; k jejímu vzniku přispívají neuroadaptivní změny v mozku, centrální senzibilizace, též jako projev centrální toxicity.
Reakce na opioidy je individuálně velmi rozdílná. Hovoříme o citlivosti k opioidům. Proto musí být dávkování a výběr opioidu přísně individuální.
Terapeutická odpověď na opioidy se u akutní a nádorové bolesti liší od odpovědi u CHNNB, kde je významnější podíl descendentních modulačních systémů.
Důležitými faktory při léčbě silnými opioidy jsou tolerance, fyzická závislost, psychická závislost, pseudozávislost a terapeutická závislost, která se vyskytuje i v jiných případech (opakované obstřiky, injekce atd.). Porozumění těmto faktorům je klíčové pro pochopení opioidní terapie, pro její správnou indikaci, diagnostiku a pro další postup při sledování pacientů užívajících opioidy.
Tolerance vzniká u mnoha léků. U opioidů znamená, že k udržení uspokojivé analgezie je třeba po čase zvýšit dávku, přestože nedošlo ke zhoršení příčiny bolesti. Tolerance je u opioidů užitečná pro odeznění většiny nežádoucích účinků, kromě obstipace.
Fyzická závislost je fyziologický fenomén, který vzniká při delší expozici podávané látce. Projevuje se abstinenčním syndromem (syndromem z odnětí) při náhlém přerušení podávání látky (opioidu) nebo po prudkém snížení dávky. U pacientů s chronickou bolestí se setkáváme se syndromem z odnětí nejčastěji po vysazení opioidů v nemocnici nebo po podání antagonisty μ‑receptorů (naloxon, nalbufin, naltrexon) nebo po prudkém snížení dávky, dále když pacient zapomene užít léky. Fyzická závislost vzniká vysokou aktivitou adrenergního systému v centrálním nervovém systému, když přestane působit tlumivý účinek opioidů. Někteří pacienti však abstinenční syndrom nepocítí ani po přerušení užívání vysoké dávky. Příznaky abstinenčního syndromu se projevují pestře. Patří k nim neklid, bolesti svalů, třesavka, zimnice, pocení, někdy křeče, nevolnost. V menší míře se mohou abstinenční příznaky objevit na konci doby působení dávky. Kromě těchto akutních příznaků je ještě znám protrahovaný abstinenční syndrom, který může trvat od tří do devíti měsíců po vysazení opioidů. Projevuje se diskomfortem, únavou, snížením tlaku, pulsu a teploty [5].
Psychická závislost je bio‑psycho‑sociální fenomén charakterizovaný specifickým způsobem chování. Dominuje touha (bažení) po droze, bez ohledu na rizika zdravotní a sociální, zanedbávání zájmů, povinností, dožadování se dalších a dalších dávek, předstírání ztráty receptů, okradení, půjčování si léků, nedodržování termínů návštěv u lékaře, nedodržování dávkovacího režimu. Takový nemocný často kombinuje předepisované opioidy s jinými látkami, zvláště s benzodiazepiny a s hypnotiky nebo s alkoholem, případně s ilegálními drogami. Předpisované opioidy také prodává.
Psychická závislost je podmíněna stykem s rizikovou látkou při genetické dispozici, sociálním prostředím a případnou psychickou poruchou.
Určitým způsobem se může na této situaci podílet stav bez bolesti, kdy je látka užívána pro euforizující, nikoliv pro analgetický účinek. Z toho důvodu jsou také preferovány pouze rychlé formy, protože libé pocity a euforický stav lépe navodí prudký nárůst koncentrace oproti pomalému uvolňování a vyrovnané koncentraci léku. Proto u dobře vedené opioidní léčby u pacientů s CHNNB psychická závislost nevzniká často.
Pseudozávislost je definována jako abnormální chování jedince v důsledku trvání bolesti při nedostatečné dávce opioidů. Pacient se může razantně dožadovat vyšší dávky, pokud jeho dosavadní dávka nemá uspokojivý účinek. Pak je na lékaři, aby rozhodl, zda byly vyčerpány všechny možnosti, včetně intervenčních, zda není jiná cesta, možnost změny léku či léčebného postupu, nebo je‑li bolest léčena opravdu nedostatečně. Velmi často bývá tato pseudozávislost zaměňována za psychickou závislost.
Terapeutická závislost představuje stav, kdy pacient může být závislý na výkonu, např. na obstřicích, které  opakovaně vyžaduje, nebo na „injekcích“. Kromě vyžadování zákroku se terapeutická závislost může projevit hromaděním léku do zásoby z úzkosti, že by mu lék došel nebo že by se obnovila bolest. Podobná situace je známa např. u diabetiků.
opakovaně vyžaduje, nebo na „injekcích“. Kromě vyžadování zákroku se terapeutická závislost může projevit hromaděním léku do zásoby z úzkosti, že by mu lék došel nebo že by se obnovila bolest. Podobná situace je známa např. u diabetiků.
U pacientů dlouhodobě léčených silnými opioidy může být obtížné odlišit fyzickou a psychickou závislost, zvláště pokud se budeme řídit Mezinárodní statistickou klasifikací nemocí a přidružených zdravotních problémů (MKN‑10) z roku 1994, kde by většina pacientů léčená opioidy splňovala kritéria (tab. 2) závislosti na opioidech vyžadující léčbu. V roce 2013 vydala Americká psychiatrická asociace nová kritéria – pátou edici Diagnostického a statistického manuálu mentálních poruch (Diagnostic and Statistical Manual of Mental Disorders – Fifth Edition, DSM‑V).
Termín závislost zde nahradil výraz onemocnění z užívání návykových látek (substance use disorder) (tab. 3) [6]. V poslední době se v odborném tisku šíří informace o velkém nárůstu nadužívání opioidů, o nezákonném prodeji, dokonce o rostoucím počtu úmrtí, a to zejména v USA. Podíl na tomto stavu mají předepisované opioidy. Ale ve většině případů se to týká opioidů v lékové formě s okamžitým uvolňováním (oxycodon, hydromorfon), které u nás zatím nejsou k dispozici. V těchto zemích je také velmi rozšířená preskripce všemi lékaři, zvláště 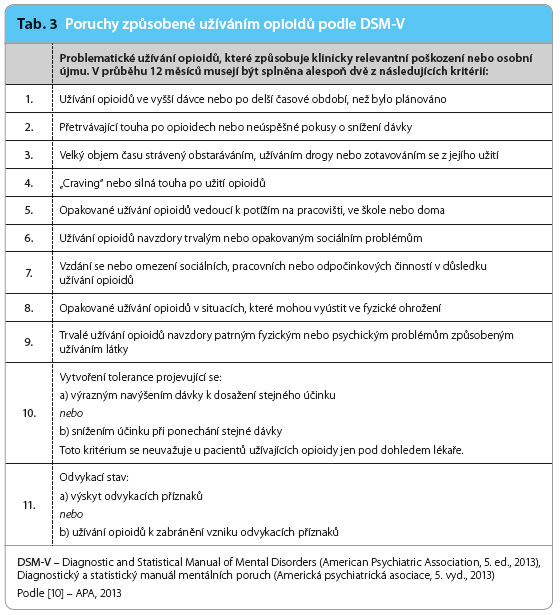 praktickými, a tudíž dobrá dostupnost opioidů.
praktickými, a tudíž dobrá dostupnost opioidů.
Na podobný stav však musíme být připraveni. Znamená to znát rizika opioidů, rozumět prevenci a snažit se bezpečně a účinně léčit. Znamená to také dobře znát jednotlivé opioidy a umět s nimi zacházet. Předvídat reakci pacientů, nežádoucí účinky a rizika.
Přestože opioidy jsou na trhu několik desítek let, stovky studií zkoumajících dlouhodobé užívání jednoznačně nepotvrdily jejich účinnost, bezpečnost a rizika. Málo studií splňuje požadavek na kvalitu, randomizaci a kontrolu v dostatečné délce trvání. Kissin v rozsáhlé metaanalýze z roku 2013 [7] uvádí 53 článků zabývajících se léčbou nenádorové bolesti, kde v randomizovaných kontrolovaných studiích trvalo sledování nejdéle šest měsíců. Závislost byla nejméně desetkrát zvýšena při léčebném užívání opioidů během let 1978–2007, počet úmrtí stoupl v letech 1999–2007 na čtyřnásobek (potvrzeno těmito studiemi).
Odhad frekvence závislosti mezi pacienty s chronickou bolestí se pohybuje podle Højsteda a Sjøgrena při dlouhodobé léčbě v rozmezí 0–50 % u pacientů, kteří netrpí onkologickým onemocněním, a u pacientů s onkologickým onemocněním v rozpětí 0–7 % [8].
Jak předepisovat opioidy
Chronická bolest patří stále k velmi obtížně léčitelným chorobám. Proto jsou opioidy i přes zřejmá rizika nevyhnutelným lékem u pacientů s chronickou bolestí. Znamená to však, že se lékař před rozhodnutím zahájit léčbu opioidy důkladně seznámí s anamnézou nemocného i jeho rodiny (drogové nebo jiné závislosti v rodině), zjistí případná psychická onemocnění, somatoformní poruchu, obeznámí se se sociálním prostředím. Významné jsou i závislosti na tabáku, alkoholu, užívání rekreačních drog. Opioidy by měly být součástí komplexní léčby. Důležité je znát komorbidity a léky, které pacient užívá. Ve spojení s opioidy je současné užívání benzodiazepinů nebo hypnotik. Mohou vést k delirantním stavům nebo k obrazu předávkování, dokonce ke smrti, jak je často zjišťováno v amerických statistikách.
Samozřejmým předpokladem indikace léčby opioidy je intenzivní krutá bolest. Léčba se vždy zahajuje nejnižší možnou dávkou a ta se velmi pomalu zvyšuje do účinné dávky. Titrace může trvat několik týdnů. Pacient musí být i poté pravidelně kontrolován. Sleduje se účinnost, nežádoucí účinky, dodržování dávkovacího režimu. Je dobrým zvykem dát pacientovi před zahájením terapie podepsat podmínky léčby silnými opioidy, toto opatření je nutné zvláště u mladých pacientů. V takovém dokumentu je uvedeno, že léky bude předepisovat jeden lékař, pacient si je bude vyzvedávat v jedné lékárně a že při neúčinnosti mu bude tato léčba přerušena. Pokud pacient recept ztratí nebo jinak znehodnotí, nebude mu vydán nový. Pacient bude seznámen s riziky užívání opioidů, s nežádoucími účinky včetně syndromu z odnětí. Bude upozorněn, že nesmí řídit vozidla, pokud dávka není stabilně nastavena nebo pokud se nachází v době změny léku či dávky.
Ke změně opioidu může dojít při netolerovatelných nežádoucích účincích nebo při nedostatečném účinku dosavadního opioidu. Ačkoliv silné opioidy nemají stropový efekt, nedoporučuje se při CHNNB překračovat denní dávku ekvivalentní 120 mg (180 mg) morfinu. Pro fentanyl TTS (transdermální terapeutický systém) představuje tato hranice 50 µg (75 µg), pro buprenorfin TDS (transdermální systém) 70 µg (105 µg), pro hydromorfon 16 mg (24 mg), pro oxycodon 80 mg (120 mg).
Pokud je pacient tzv. opioid‑senzitivní a užívá relativně nízkou dávku bez nežádoucích účinků, dobře spí a zlepšila se jeho funkční kapacita, pak může být léčen stejnou dávkou a nacházet se v uspokojivém stavu několik let. Zkušenosti jsou např. s geriatrickými pacienty, kde i přes polymorbidity je dlouhodobě účinná malá dávka transdermálního opioidu (např. jedna čtvrtina náplasti s buprenorfinem 35 µg).
Každý pacient léčený opioidy musí být považován za fyzicky závislého a mělo by to být dokumentováno ve zdravotních záznamech. Vhodné je označení takového stavu termínem opioid‑dependentní chronická bolest (nikoliv pacient) [6].
Závěr
Chronická bolest je dlouhodobá, v mnoha případech trvalá. Pacientovi je podávána uspokojivá opioidní terapie, ale jak dlouho má tato léčba trvat? Má ji užívat doživotně? Co se stane při mnohaletém užívání opioidů? V řadě případů pomohou neuromodulační metody, které sníží bolest natolik, že je možné léčbu opioidy ukončit nebo ji snížit na nejnižší dávku. Patří sem míšní stimulace, periferní stimulace, mozková stimulace korová i hluboká, intrathekální podání opioidů a látek (snížení dávky oproti perorálnímu podání opioidu až stonásobné). Patří sem radiofrekvenční metody a vývoj jistě přinese další možnosti. Nicméně vždy zůstane část pacientů, u kterých tyto metody z různých důvodů nebude možno použít nebo nebude dostatek financí k uspokojení všech vhodných pacientů. Prozatím – v blízké, možná i v daleké budoucnosti – budou opioidy patřit do léčby bolesti, jak je tomu od pradávna. Naučit se s nimi pracovat tak, aby byly dobrým sluhou, je v zájmu lékařů i pacientů.
Seznam použité literatury
- [1] Bandolier. Oxford league table of analgesics in acute pain. Bandolier, 2007.
- [2] Murmion BP. Combination analgesics in adults. Aust Prescr 2010; 33: 113–115.
- [3] Eriksen J. Long term/chronic non cancer pain. Epidemiology, health care utilization, socioeconomy and aspects of treatment. University Copenhagen. Thesis 2004.
- [4] Elliot JA, Horton E, Fibuch EE. The endocrine effect of long term oral opioid therapy: A case report and review of the literature. J Opioid Manag 2011; 7: 145–154.
- [5] Mitchell AM, Dewey CM. Chronic pain in patients with substance abuse disorder: general guidelines and approach to treatment. Postgrad Med 2008; 120: 75–79.
- [6] Lejčko J. Chronická bolest, opioidy a závislost – jdeme správným směrem? Bolest 2015; 18: 186–193.
- [7] Kissin I. Long term opioid treatment of chronic nonmalignant pain: unproven efficacy and neglected safety? J Pain Res 2013; 6: 513–529.
- [8] Højsted J, Sjøgren P. Addiction to opioids in chronic pain patients: a literature review. Eur J Pain 2007; 11: 490–518.
- [9] World Health Organization. The ICD 10 Classification of Mental and Behavioural Disorders: Clinical Descriptions and Diagnostic Guidelines. Geneva: World Health Organization, 1992.
- [10] American Psychiatric Association. Diagnostic and Statistical Manual of Mental Disorders, 5th ed. Arlington, VA: American Psychiatric Publishing, 2013.