Zaostřeno Kazuistiky asciminib
Kazuistiky z reálné klinické praxe aneb Příběhy pacientů s chronickou myeloidní leukemií užívajících asciminib
V podvečer 8. dubna 2025 se s podporou společnosti Novartis uskutečnil kazuistický webinář zaměřený na léčbu chronické myeloidní leukemie (CML) a využití terapie asciminibem. Moderování odborného programu i závěrečné diskuse se ujala doc. MUDr. Daniela Žáčková, Ph.D., (Interní hematologická a onkologická klinika, LF MU a FN Brno).
Kolegové z center vysoce specializované hematologické péče napříč Českou republikou prostřednictvím kazuistik konkrétních pacientů přiblížili, jak náročná může být léčba CML v klinické praxi. U prezentovaných pacientů se nedařilo předchozími dvěma anebo více liniemi léčby CML dosáhnout požadované odpovědi nebo pacienti tuto léčbu netolerovali. Léčebnou volbou byl u těchto pacientů asciminib, který nedávno obohatil léčebné možnosti chronické fáze CML.
Asciminib představuje první alosterický inhibitor BCR::ABL kinázové aktivity, který se vyznačuje vysokou specifitou a účinností. Jde o první a zatím jediný inhibitor specificky zaměřený na ABL1 mirystoylové vazebné místo. Je indikován k terapii CML v chronické fázi u pacientů, kteří byli dříve léčeni nejméně dvěma tyrozinkinázovými inhibitory (TKI). Doporučená dávka asciminibu je 40 mg 2× denně zhruba ve 12hodinových intervalech.
Kazuistika pacientky s diagnózou CML ve společné péči lékařů úHKT a Hematologického oddělení v Liberci
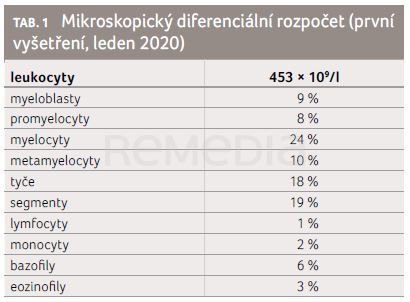 První případ pacientky s CML ve sdílené péči s MUDr. Miroslavem Genským (Oddělení klinické hematologie KNL a.s.) prezentovala MUDr. Dana Srbová (Ústav hematologie a krevní transfuze, ÚHKT, Praha). Jednalo se o 30letou pacientku, která v lednu 2020 přichází na urgentní příjem nemocnice v Liberci pro otoky dolních končetin (DKK) a únavu. Z osobní anamnézy léčena pro hypotyreózu (levothyroxin), subjektivně hmotnostní úbytek zhruba 3 kg za šest měsíců, cítí se unavená, bolestmi nebo dušností netrpí. Objektivně pacientka bez známek krvácení, kachektická, s ascitem, bez anemického syndromu, bez lymfadenopatie, ale splenomegalie hmatná až do malé pánve a lehké otoky DKK. Ve vstupním krevním obraze Leu 453 × 109/l, Hgb 71 g/l, MCV 71,9 fl, Trombo 1 079 × 109/l, biochemicky zvýšená koncentrace kyseliny močové (402 µmol/l), jaterní testy v normě, CRP 12,5 mg/l, LDH 21,2 µkat/l, TSH 10,70 mIU/l. Na ultrazvuku břicha hepatosplenomegalie (slezina 290 mm) s ascitem, známkami portální hypertenze a fluidothorax bilaterálně jako vedlejší nález. V mikroskopickém diferenciálním rozpočtu je vidět výrazný posun doleva a 9 % zachycených myeloblastů (tab. 1).
První případ pacientky s CML ve sdílené péči s MUDr. Miroslavem Genským (Oddělení klinické hematologie KNL a.s.) prezentovala MUDr. Dana Srbová (Ústav hematologie a krevní transfuze, ÚHKT, Praha). Jednalo se o 30letou pacientku, která v lednu 2020 přichází na urgentní příjem nemocnice v Liberci pro otoky dolních končetin (DKK) a únavu. Z osobní anamnézy léčena pro hypotyreózu (levothyroxin), subjektivně hmotnostní úbytek zhruba 3 kg za šest měsíců, cítí se unavená, bolestmi nebo dušností netrpí. Objektivně pacientka bez známek krvácení, kachektická, s ascitem, bez anemického syndromu, bez lymfadenopatie, ale splenomegalie hmatná až do malé pánve a lehké otoky DKK. Ve vstupním krevním obraze Leu 453 × 109/l, Hgb 71 g/l, MCV 71,9 fl, Trombo 1 079 × 109/l, biochemicky zvýšená koncentrace kyseliny močové (402 µmol/l), jaterní testy v normě, CRP 12,5 mg/l, LDH 21,2 µkat/l, TSH 10,70 mIU/l. Na ultrazvuku břicha hepatosplenomegalie (slezina 290 mm) s ascitem, známkami portální hypertenze a fluidothorax bilaterálně jako vedlejší nález. V mikroskopickém diferenciálním rozpočtu je vidět výrazný posun doleva a 9 % zachycených myeloblastů (tab. 1).
Kostní dřeň dle vyšetření středně buněčná až hypercelulární se zachyceným posunem doleva. Dále bylo doplněno vyšetření BCR::ABL z periferní krve, které vyšlo pozitivní. Pacientka byla následně konzultována s ÚHKT a byla zahájena cytoredukční terapie hydroxyureou v dávce 1 500 mg/den, dále alopurinol 600 mg/den, profylaxe nízkomolekulárním heparinem (LMWH) a intravenózní (i.v.) hydratace. Pro postupně se rozvíjející anemický syndrom byla potřeba transfuzní terapie erytrocyty.
Pacientka byla v prvních týdnech hospitalizována, během hospitalizace došlo k několika komplikacím. První byla rozpadová pneumonie s nutností nasazení i.v. antibiotické terapie, dále bilaterální fluidothorax s nutností drenáže a komplikovaný pneumothoraxem. Při zahájení cytoredukce byla zaznamenána výrazná hyperkalemie s nutností přechodné hemodialýzy. Pro soor dutiny ústní byla pacientka léčena antimykotiky (i.v. flukonazol).
Pacientka byla odeslána na ÚHKT 11. srpna 2020, kdy se její stav upravil natolik, že byla schopna zahájení specifické léčby TKI. V té době v krevním obraze Leu 6,85 × 109/l, Hgb 127 g/l, Trombo 291 × 109/l, v diferenciálním rozpočtu posun doleva, se zachycením blastů. V kostní dřeni obraz chronické fáze, bez zmnožení blastů, byla vyslovena suspekce na megakaryocytární subtyp, histologické vyšetření neprovedeno. Dle průtokové cytometrie též obraz chronické fáze se záchytem 1 % blastů. Cytogenetické vyšetření hodnotilo 16 mitóz 46, XX, T/9,22)(q34,q11). BCR::ABL kvantitativně bylo 110 %.
Na základě těchto výsledků byla ukončena stávající léčba hydroxyureou a pro vysoké riziko byla rovnou zahájena terapie TKI 2. generace nilotinibem v plné dávce 300 mg 2× denně. Došlo k přechodné elevaci aktivity jaterních transamináz s postupnou úpravou. V říjnu 2020 bylo dosaženo kompletní hematologické odpovědi, BCR::ABL zůstává vysoké (83 %, v lednu 2021 78 %), v kostní dřeni přetrvává obraz chronické fáze onemocnění, cytogeneticky bylo dosaženo malé cytogenetické odpovědi (Ph+ 55,5 %). Byla doplněna analýza mutací, která byla negativní, za další tři měsíce zůstává BCR::ABL stále vysoké (75 %), mutace byly opět negativní.
Pro neoptimální odpověď na léčbu byla v květnu 2021 léčba změněna na dasatinib v plné dávce 100 mg denně, ale pro významnou hematologickou toxicitu byla dávka redukována na 60 mg denně. Přesto se rozvinula těžká pancytopenie a muselo dojít i k přechodnému přerušení léčby dasatinibem. V listopadu 2021 trvá chronická fáze onemocnění, cytogeneticky stále jen malá cytogenetická odpověď, transkript BCR::ABL sice s poklesem, ale stále zůstává vysoký (43 %…26 %…30 %).
V dubnu 2022 došlo ke změně léčby na ponatinib, ale i při redukované dávce (střídavě 15 a 30 mg denně) opět projevy hematologické toxicity s nutností dočasného přerušování léčby. Hodnoty ACR::ABL klesaly (kvantitativně 46 %…26 %…9,5 %…3,6 %…12 %…4,4 %…7,7 % v září 2023), detekce mutací byla opakovaně negativní. Stále trvá jen malá cytogenetická odpověd (Ph+ 33–65 %), v listopadu 2023 byla detekována translokace t(9,22)(q34,1)(q11,2) v jedné mitóze a 2 % interfázních jader v tetraplodii. Cytologie z kostní dřeně byla pro pancytopenii opakovaně nevýtěžná, trepanobiopsii pacientka opakovaně odmítá.
Po celou dobu léčby se pacientka nacházela ve výborném stavu, subjektivně medikaci TKI toleruje velmi dobře, objektivně ale s opakovanými projevy hematologické toxicity grade 3–4, další nežádoucí účinky nebyly zaznamenány. Vzhledem k mladému věku pacientky a probíhající již 3. linii léčby TKI bez dosažení remise onemocnění byla zvažována opakovaně možnost alogenní transplantace kostní dřeně (mladší bratr), ale této možnosti není pacientka nakloněna. Subjektivně se cítí výborně a transplantaci vidí jako úplně poslední možnost v krajním případě.
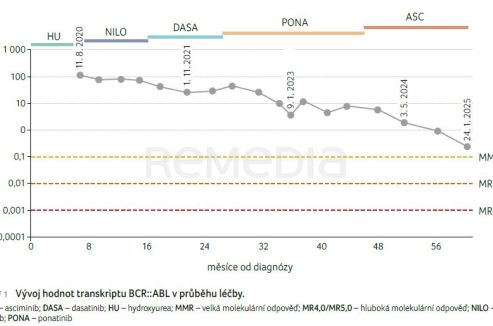 Z tohoto důvodu byl zažádán revizní lékař pojišťovny o schválení léčby v té době nově dostupným TKI asciminibem. Terapie byla schválena, pacientka zahájila léčbu v listopadu 2023 v počáteční redukované dávce 40 mg denně. V krevním obraze došlo postupně k normalizaci hodnot leukocytů, k vymizení neutropenie, postupně i k ústupu trombocytopenie (29..57..83..100 tisíc) a dávka asciminibu byla zvýšena na 80 mg denně. U hodnot transkriptu BCR::ABL bylo dosaženo postupné redukce (5,5 %..1,8 %..0,88 %..0,23 % v lednu 2025). Vývoj hodnot v průběhu času prezentuje graf 1.
Z tohoto důvodu byl zažádán revizní lékař pojišťovny o schválení léčby v té době nově dostupným TKI asciminibem. Terapie byla schválena, pacientka zahájila léčbu v listopadu 2023 v počáteční redukované dávce 40 mg denně. V krevním obraze došlo postupně k normalizaci hodnot leukocytů, k vymizení neutropenie, postupně i k ústupu trombocytopenie (29..57..83..100 tisíc) a dávka asciminibu byla zvýšena na 80 mg denně. U hodnot transkriptu BCR::ABL bylo dosaženo postupné redukce (5,5 %..1,8 %..0,88 %..0,23 % v lednu 2025). Vývoj hodnot v průběhu času prezentuje graf 1.
Kazuistika z Olomouce
Druhý případ představil prof. MUDr. Edgar Faber, CSc., (Hemato‑onkologická klinika, LF UP a FN Olomouc). Jedná se o 69letou pacientku, která se na olomoucké pracoviště dostala poté, co byla 3. listopadu 2023 vyšetřena praktickým lékařem pro vertigo. Zjištěn byl paroxysmus fibrilace síní a dekompenzovaná hypertenze, což vedlo k úpravě zavedené terapie. Vedle toho se pacientka léčila pro autoimunitní tyreoiditidu a diabetes mellitus 2. typu. V laboratorním vyšetření byly zachyceny leukocytóza a trombocytemie, které byly následně řešeny spádovým hematologem. Tyto první výsledky nejsou k dispozici. Počátkem prosince byla potvrzena fúze BCR::ABL1 e13a2. Mutace genu JAK2 a kalretikulin byly negativní, průtokovou cytometrií byla vyloučena lymfoproliferace, sonografické abdominální vyšetření bylo bez abnormalit. První laboratorní výsledky, které byly ze spádové ambulance zaslány do Olomouce, byly až z 12. ledna 2024. V krevním obraze byly následující hodnoty: Leu 15,92 × 109/l, Ery 5,12 × 1012/l, Hgb 143 g/l, Trombo 1 189 × 109/l; diferenciální rozpočet leukocytů vykazoval posun doleva a bazofilii NS 0,69, NT 0,01, Metamyelo 0,03, Myelo 0,01, Lymfo 0,14, Mono 0,05, Eoz 0,01, Baz 0,06.
Pacientka (87 kg, 178 cm) přišla k prvnímu vyšetření 24. ledna 2024 v dobrém stavu (ECOG 0), bez palpovatelné splenomegalie. Dosud nedostávala cytoredukční terapii, proto byly aktuální výsledky krevního obrazu (Leu 20,64 × 109/l, Ery 5,30 × 1012/l, Hgb 152 g/l, Trombo 1 098 × 109/l) a výsledky fyzikálního vyšetření použity pro stanovení prognostického indexu (dle skóre ELTS šlo o nízké riziko). Vyšetření kostní dřeně bylo pro silnou anxietu odloženo. Vzhledem k tomu, že nebyla zaznamenána výrazná leukocytóza, zahájila pacientka další den 1. linii léčby imatinibem ve standardní dávce 400 mg/den.
Při kontrole 31. ledna 2024 byly u pacientky zaznamenány vyšší hodnoty leukocytů (Leu 31,20 × 109/l, Ery 4,63 × 1012/l, Hgb 130 g/l, Trombo 1 102 × 109/l, DIF NS 0,90, NT 0,01, Lymfo 0,05, Mono 0,02, Baz 0,02), nicméně byly patrné známky infekce (CRP 126,1 mg/l). Pacientka si stěžovala na bolesti pravé dolní končetiny (DK) a otok rukou a nohou. K vyloučení infekce byly provedeny kultivační odběry. K imatinibu byla přidána hydroxyurea 1,5 g/den a symptomaticky nimesulid.
Při kontrole 7. února 2024 byly bolesti nohou mírnější, hodnoty CRP poklesly na 26,3 mg/l, infekce nebyla z kultivací potvrzena. Pacientka ale udávala nespavost, nechutenství, únavu a tvorbu velkých hematomů. U pacientky došlo k anemizaci a k vzestupu hodnot krevních destiček: Leu 9,41 × 109/l, Ery 3,78 × 1012/l, Hgb 109 g/l, Trombo 1 477 × 109/l, DIF NS 0,82, Eoz 0,02, Lymfo 0,07, Mono 0,01, Baz 0,08. Léčba hydroxyureou byla ukončena a k imatinibu byl přidán anagrelid v dávce 1 mg/den. Při další kontrole, 21. února 2024, byl patrný efekt anagrelidu: Leu 5,9 × 109/l, Ery 3,94 × 1012/l, Hgb 117 g/l, Trombo 144 × 109/l, DIF NS 0,54, NT 0,01, Eoz 0,20, Lymfo 0,15, Mono 0,07, Baz 0,02, CRP < 4,0 mg/l. Docházelo ale k alergickým projevům (svědivá vyrážka na trupu). Terapie anagrelidem byla ukončena, exantém byl léčen lokálními kortikoidy. Eozinofilie však progredovala (0,14 až 0,55), rozvinul se generalizovaný toxoalergický exantém a při další kontrole (27. 3. 2024) byla proto léčba imatinibem ukončena. Leu 9,15 × 109/l, Ery 3,79 × 1012/l, Hgb 119 g/l, Trombo 133 × 109/l, diferenciální rozpočet v mezidobí svědčil pro hematologickou remisi. Po měsíci terapie došlo k poklesu hladiny transkriptu BCR::ABL1 na 18,9 % (počet kopií BCR::ABL1 57 900, počet kopií ABL 177 000), nicméně pro významné známky alergie nebylo možné v terapii nadále pokračovat.
Prvního dubna 2024 byla zahájena léčba 2. linie dasatinibem v dávce 100 mg/den. Následně byla pacientka ve spádu akutně hospitalizována pro kašel a dušnost. Byl zjištěn bilaterální fluidothorax, paroxysmus fibrilace síní. Echokardiograficky byl potvrzen defekt síňového septa s levo‑pravým tokem, dilatace pravostranných srdečních oddílů a lehká plicní hypertenze. Pacientce byla upravena medikace a byl jí implantován kardiostimulátor. Po telefonické domluvě byla 10. dubna 2024 léčba dasatinibem ukončena. Kontrola 2. května 2024 ukázala výborný efekt dasatinibu, (molekulárněgenetické vyšetření prokázalo pokles hladiny BCR::ABL1 na 1,8 %, počet kopií BCR::ABL1 2 370, počet kopií ABL 105 000). Leu 11,37 × 109/l, Ery 4,69 × 1012/l, Hgb 144 g/l, Trombo 358 × 109/l, DIF NS 0,88, NT 0,01, Eoz 0,03, Lymfo 0,01, Mono 0,05, Baz 0,02.
Od 2. května 2024 byla zahájena 3. linie léčby bosutinibem v redukované dávce 200 mg/den. Nově se objevují bolesti a křeče v břiše a vedle hepatopatie zejména toxická pankreatitida (ALT 2,51 µkat/l, ALP 4,21 µkat/l, GGT 6,73 µkat/l, LDH 6,52 µkat/l, α‑amyláza 4,13 µkat/l, lipáza 19,04 µkat/l, CRP 75 mg/l). Terapie bosutinibem byla proto 15. května ukončena.
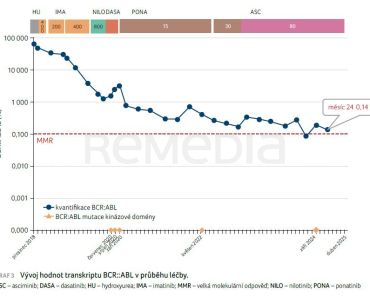
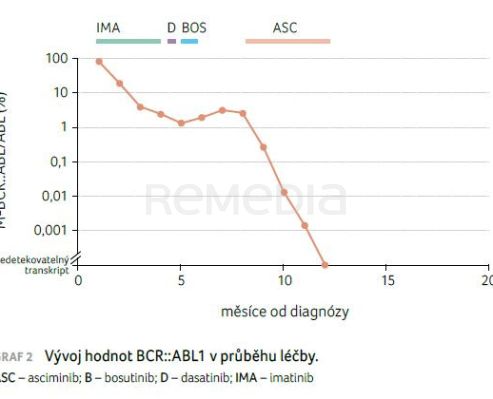 Kvantitativní PCR provedená 18. června 2024 ukázala v důsledku přerušování léčby vzestup transkriptu BCR::ABL na 3,12 % IS, počet kopií BCR::ABL1 4 640, počet kopií ABL 86 000. Byla zahájena 4. linie léčby asciminibem, pro rizikovost pacientky v dávce 20 mg/den, která byla po týdnu navýšena na 40 mg/den, pro prodloužení QTc intervalu na EKG byla po třech měsících léčby dávka opět redukována na 20 mg/den. Pacientka subjektivně léčbu tolerovala dobře, objektivně došlo k časnému ústupu jaterní a pankreatické aktivity. Druhý měsíc léčby bylo dosaženo kompletní cytogenetické odpovědi (BCR::ABL1 0,26 %). Po osmi měsících léčby (5. 2. 2025) byl leukemický transkript již nedetekovatelný (BCR::ABL1/ABL 0,000 %, počet kopií BCR::ABL1 0, počet kopií ABL 121 000). Tolerance léčby je při poslední kontrole pacientky nadále velmi dobrá, aktuální laboratorní výsledky jsou kromě známek incipientní renální insuficience v normě. Vývoj hodnot BCR::ABL1 prezentuje graf 2. Další kontrola je plánována na červen 2025.
Kvantitativní PCR provedená 18. června 2024 ukázala v důsledku přerušování léčby vzestup transkriptu BCR::ABL na 3,12 % IS, počet kopií BCR::ABL1 4 640, počet kopií ABL 86 000. Byla zahájena 4. linie léčby asciminibem, pro rizikovost pacientky v dávce 20 mg/den, která byla po týdnu navýšena na 40 mg/den, pro prodloužení QTc intervalu na EKG byla po třech měsících léčby dávka opět redukována na 20 mg/den. Pacientka subjektivně léčbu tolerovala dobře, objektivně došlo k časnému ústupu jaterní a pankreatické aktivity. Druhý měsíc léčby bylo dosaženo kompletní cytogenetické odpovědi (BCR::ABL1 0,26 %). Po osmi měsících léčby (5. 2. 2025) byl leukemický transkript již nedetekovatelný (BCR::ABL1/ABL 0,000 %, počet kopií BCR::ABL1 0, počet kopií ABL 121 000). Tolerance léčby je při poslední kontrole pacientky nadále velmi dobrá, aktuální laboratorní výsledky jsou kromě známek incipientní renální insuficience v normě. Vývoj hodnot BCR::ABL1 prezentuje graf 2. Další kontrola je plánována na červen 2025.
Z kolečkového křesla zpět na nohy
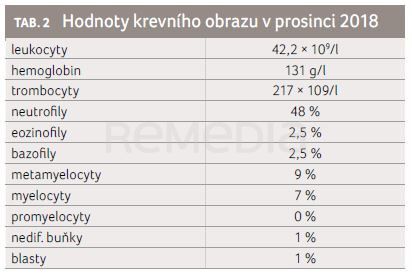 Zajímavým názvem třetí kazuistiky zaujala MUDr. Petra Čičátková (Interní hematologická a onkologická klinika, LF MU a FN Brno). V tomto případě se jednalo o obézního muže, ročník 1972, který byl na hematologické pracoviště referován v prosinci 2018 s neutrofilní leukocytózou (tab. 2). V anamnéze seminom varlete v roce 2016 (orchiektomie, dvě linie chemoterapie, nyní v remisi), dále chronická ezofagitida, tinitus. Aktuálně ho trápí kašel a bolesti hlavy, je bez teplot a nočního pocení, nebyla zaznamenána hepato‑ ani splenomegalie. Byla provedena sternální punkce a zahájena cytoredukce hydroxykarbamidem. Ta byla ale po několika dnech ukončena pro tinitus, který se objevuje již v anamnéze, léčbou se výrazně zhoršil a omezoval pacienta v denních aktivitách.
Zajímavým názvem třetí kazuistiky zaujala MUDr. Petra Čičátková (Interní hematologická a onkologická klinika, LF MU a FN Brno). V tomto případě se jednalo o obézního muže, ročník 1972, který byl na hematologické pracoviště referován v prosinci 2018 s neutrofilní leukocytózou (tab. 2). V anamnéze seminom varlete v roce 2016 (orchiektomie, dvě linie chemoterapie, nyní v remisi), dále chronická ezofagitida, tinitus. Aktuálně ho trápí kašel a bolesti hlavy, je bez teplot a nočního pocení, nebyla zaznamenána hepato‑ ani splenomegalie. Byla provedena sternální punkce a zahájena cytoredukce hydroxykarbamidem. Ta byla ale po několika dnech ukončena pro tinitus, který se objevuje již v anamnéze, léčbou se výrazně zhoršil a omezoval pacienta v denních aktivitách.
V lednu 2019 byla potvrzena diagnóza CML v chronické fázi bez přídatných cytogenetických změn s nízkým rizikovým skóre (Sokal, Hasford, EUTOS). Leukocytóza neprogredovala, z tohoto důvodu nebyla zapotřebí cytoredukční léčba. Z terapeutických možností TKI 1. linie dostupných v roce 2019 byl zvolen imatinib. Během prvních tří měsíců terapie byla došetřována slabost DKK s brněním a mravenčením. Obtíže byly uzavřeny jako těžká polyneuropatie s obrazem chabé paraparézy DKK a byly důvodem k redukci dávky na polovinu (200 mg/den). Obtíže s chůzí přetrvávaly, a přestože se přidávaly v průběhu následujících měsíců další problémy (občasný průjem, dyspepsie, výrazná únava), byla snaha o navýšení dávky (300 mg v 6. měsíci, od 9. měsíce 400 mg denně). Po roce léčby udává pacient slzení a pálení očí, únavu (mimo lůžko méně než polovinu dne), imperativní průjmy, brnění a necitlivost DKK, poruchy zorného pole a zhoršené pískání v uších. Léčba vedla k normalizaci krevního obrazu a k trvalému poklesu transkriptu BCR::ABL (6. měsíc 31 %, 9. měsíc 12 %, 12. měsíc 4 %), nicméně dle terapeutických doporučení se stále jedná o hodnoty svědčící pro selhání léčby. Z důvodu nedostatečné účinnosti i špatné tolerance byla léčba změněna.
V lednu 2020 byla proto zahájena léčba 2. linie nilotinibem v plné dávce 400 mg, která byla po třech měsících navýšena na 800 mg. Efekt léčby byl slibný (pokles BCR::ABL na 1,8 %), pacient byl subjektivně bez obtíží, nicméně ve čtvrtém měsíci se u něj rozvinul diabetes mellitus 2. typu. Přetrvávají vysoké glykemie (> 10 mmol/l) a bolesti levé poloviny břicha.
Na přelomu května/června 2020 byl jako 3. linie léčby nasazen dasatinib ve snížené dávce 80 mg denně. Přednášející se shodli, že dasatinib dobře funguje i při nižších dávkách. Pro bolesti hlavy, únavu a celkovou schvácenost byla ale terapie po prvním měsíci přerušena. K ústupu obtíží nedošlo ani po opětovném zahájení léčby a pro bolest hlavy, tlak v očích, sekreci z očí až světloplachost při dávce 40 mg denně byla po dvou měsících léčba dasatinibem ukončena.
Žádosti o následnou léčbu bosutinibem bohužel nebylo pojišťovnou vyhověno. Jako 4. linie léčby byla zahájena terapie ponatinibem v dávce 15 mg denně (červenec 2020 – prosinec 2022). Po měsíci léčby se objevily úporné bolesti břicha a nekompenzovatelné hyperglykemie, ale v terapii bylo pokračováno. Úvodní kolísání hodnot transkriptu bylo přisuzováno přerušování léčby. Dál byla tolerance léčby uspokojivá bez nových subjektivních nežádoucích účinků, po 20 měsících ale došlo k mírnému vzestupu transkriptu (0,72 %) a dávka byla navýšena na 30 mg denně s rizikem nežádoucích účinků při dlouhodobé léčbě.
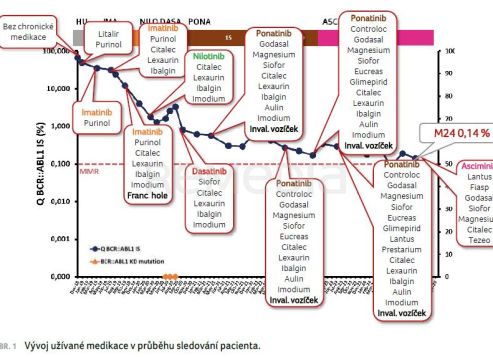 Jak postupovat dál? Pacient, původně bez chronické medikace, byl aktuálně zatížen rozsáhlou medikací (obr. 1) a po používání francouzských holí byl nucen využívat invalidní vozík.
Jak postupovat dál? Pacient, původně bez chronické medikace, byl aktuálně zatížen rozsáhlou medikací (obr. 1) a po používání francouzských holí byl nucen využívat invalidní vozík.
 Využit byl v té době již dostupný specifický léčebný program pro asciminib. Jako 5. linie léčby bylo zahájeno v lednu 2023 jeho podávání v dávce 80 mg. První dny léčby pacient pociťoval „žaludek jako na vodě“, obtíže po 14 dnech ustoupily. Po prvním měsíci terapie se pacient cítil skvěle, hodnoty krevního tlaku a glykemie byly konečně pod kontrolou, ustoupily bolesti hlavy. Kontrola ve 12. měsíci léčby udává pokles hodnoty glykovaného hemoglobinu, zvažováno je vysazení některých antidiabetik. Při kontrole ve 27. měsíci (březen 2025) se pacient se cítí velmi dobře, udává zapomínání, bolesti kloubů a zad, navštěvuje ortopedii a neurologii, souvislost s léčbou asciminibem se nepředpokládá. Co se týče účinnosti, hladina transkriptu setrvale klesá nebo se pohybuje kolem hodnoty velké molekulární odpovědi (MMR; při kontrole ve 24. měsíci 0,14 % graf 3). Z hlediska tolerance léčby se výrazně zúžila podávaná medikace (obr. 1 vpravo) a pacient chodí na kontroly „po svých“, invalidní vozík již nevyužívá.
Využit byl v té době již dostupný specifický léčebný program pro asciminib. Jako 5. linie léčby bylo zahájeno v lednu 2023 jeho podávání v dávce 80 mg. První dny léčby pacient pociťoval „žaludek jako na vodě“, obtíže po 14 dnech ustoupily. Po prvním měsíci terapie se pacient cítil skvěle, hodnoty krevního tlaku a glykemie byly konečně pod kontrolou, ustoupily bolesti hlavy. Kontrola ve 12. měsíci léčby udává pokles hodnoty glykovaného hemoglobinu, zvažováno je vysazení některých antidiabetik. Při kontrole ve 27. měsíci (březen 2025) se pacient se cítí velmi dobře, udává zapomínání, bolesti kloubů a zad, navštěvuje ortopedii a neurologii, souvislost s léčbou asciminibem se nepředpokládá. Co se týče účinnosti, hladina transkriptu setrvale klesá nebo se pohybuje kolem hodnoty velké molekulární odpovědi (MMR; při kontrole ve 24. měsíci 0,14 % graf 3). Z hlediska tolerance léčby se výrazně zúžila podávaná medikace (obr. 1 vpravo) a pacient chodí na kontroly „po svých“, invalidní vozík již nevyužívá.
Pacientka s CML léčená asciminibem po selhání a intoleranci čtyř předchozích inhibitorů tyrozinkináz
Poslední kazuistikou provedl MUDr. Tomáš Procházka (Hematologicko‑onkologické oddělení, FN Plzeň).
Pacientkou je žena, ročník 1959, v anamnéze reaktivní depresivní syndrom, stav po appendektomii a operaci paravaginální píštěle, jinak bez zásadních interních komorbidit. První kontakt s hematoonkologickým pracovištěm proběhl v březnu 2006, kam byla pro leukocytózu odeslána praktickým lékařem. Pacientka dále udávala tři roky trvající subfebrilie a pocity únavy. Vstupní vyšetření ukázala Leu 192 × 109/l, Trombo 536 × 109/l, Hgb 114 g/l, diferenciální rozpočet bez přítomnosti blastů, klinicky splenomegalie +5 cm pod žeberní oblouk. Byla provedena trepanobiopsie, cytologicky CML v chronické fázi, 86% klon BCR::ABL ve variantě major (b2a2), dle prognostické stratifikace nízká rizikovost (Sokalovo skóre 0,68, Hasfordovo skóre 472,7, skóre EUTOS 62, ELTS 1,1277). Zahájena byla 14denní cytoredukce hydroxykarbamidem s velice dobrým efektem.
Následně byla zahájena 1. linie léčby TKI (duben 2006 až duben 2011) imatinibem ve standardní dávce 400 mg/den a začaly se objevovat komplikace. První byla hematologická toxicita – trombocytopenie (květen 2006 – květen 2007), řešena opakovanou redukcí dávky a přerušováním léčby. Druhou komplikací bylo gynekologické krvácení, pacientka absolvovala kyretáž (červen 2006), následně termoablaci endometria (září 2006) a hysterektomii s ponecháním ovarií (duben 2007). Třetí komplikaci léčby představovala suboptimální odpověď se snahou o navýšení dávky na 600 mg/den, která ale nevedla k žádoucí odpovědi v podobě poklesu sledovaných hodnot v rámci molekulární genetiky. V červenci 2010 se u pacientky rozvinula peritonitida na podkladě ruptury divertiklu sigmatu řešená resekcí s přechodnou stomií a jejím následným zanořením v 2. době (březen 2011). V čase všech operačních procedur byla terapie vždy přerušena. Léčba imatinibem byla nakonec pro nedosažení MMR po celé sledované období v dubnu 2011 ukončena.
Poté byla zahájena terapie nilotinibem ve standardní dávce 600 mg/den (duben 2011 – květen 2012). V říjnu 2011 bylo dosaženo první MMR. Komplikací této léčby byla gastrointestinální nesnášenlivost (nauzea, zvracení) s redukcí dávky a následně s nutností terapii ukončit.
Následoval „retreatment“ imatinibem (květen 2012 – červen 2013) v redukované dávce 300 mg/den. Komplikací byl téměř okamžitý vzestup hodnot a selhání léčby z hlediska molekulární genetiky v prosinci 2012. Snaha o navýšení dávky zůstala bez efektu a v červnu 2013 byla terapie ukončena pro její selhání.
U pacientky byla dále nasazena léčba dasatinibem (červen 2013 – květen 2020) ve standardní dávce 90 mg/den. V květnu 2014 bylo dosaženo MMR, v listopadu 2014 hluboká molekulární remise (MR4). Následoval sled komplikací. V únoru 2016 se objevila první v podobě fluidothoraxu. Léčba dasatinibem byla přerušena do května 2016 a znovu zahájena dávkou 70 mg/den. Druhou komplikací byl ileózní stav v květnu 2017, který pravděpodobně nesouvisel s léčbou TKI a odezněl po konzervativních opatřeních. V květnu 2019 se bohužel znovu rozvinul fluidothorax, léčba dasatinibem byla přerušena. Stav si vyžádal opakovaně drenáž, následně v dubnu 2020 i talkáž pleurální dutiny. V květnu 2020 byla léčba dasatinibem z obav z obnovy fluidothoraxu ukončena.
Následoval „retreatment“ nilotinibem (květen 2020 – leden 2024) v redukované dávce 400 mg/den. V lednu 2021 bylo dosaženo MR4. Při navýšení dávky na 800 mg/den se rozvinula hypertenze, byla proto ponechána redukovaná dávka a hypertenze byla farmakologicky kompenzována. V říjnu 2023 se léčba komplikovala periferní neuropatií, po vyloučení jiných příčin neuropatie byla terapie nilotinibem pro toxicitu ukončena. Po jeho vysazení došlo k úpravě stavu.
Jako další linie léčby byl nasazen ponatinib (leden–duben 2024) v redukované dávce 15 mg/den. Od února 2024 byla dávka zvýšena na plných 45 mg/den, bohužel se objevil toxoalergický exantém. Přerušení terapie i restart na redukované dávce bohužel vedly k opakování obtíží a léčba byla v dubnu 2024 ukončena pro alergickou intoleranci.
 V dubnu 2024 byla po schválení zahájena terapie asciminibem v dávce 80 mg/den ve dvou denních dávkách. Konečně byl nalezen TKI, který pacientce „seděl“. V červenci 2024 bylo dosaženo MMR s prohloubením na MR4 v březnu 2025. Léčba dosud probíhá bez komplikací.
V dubnu 2024 byla po schválení zahájena terapie asciminibem v dávce 80 mg/den ve dvou denních dávkách. Konečně byl nalezen TKI, který pacientce „seděl“. V červenci 2024 bylo dosaženo MMR s prohloubením na MR4 v březnu 2025. Léčba dosud probíhá bez komplikací.
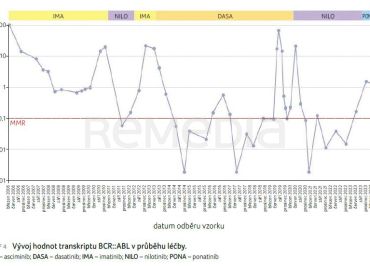
Přednášející v závěru zhodnotil průběh hodnot BCR::ABL během léčby (graf 4).
Závěr
Ačkoliv máme k dispozici cílenou léčbu a přežití pacientů je obdobné jako přežití v celkové populaci, v terapii CML zůstává řada výzev. U významného podílu pacientů je potřeba léčbu (nejednou) měnit, což je pro pacienty nevýhodné z hlediska účinnosti i kumulující se toxicity. Kumulace léčebných linií je spojena s narůstajícím podílem selhání léčby, zhoršuje přežití a může vést ke generování rezistentních mutací, které pak dále komplikují výběr vhodného přípravku. Nezanedbatelná je i zmíněná toxicita, která ve spojení s rizikovými faktory konkrétních pacientů a komorbiditami dále ztěžuje hledání vhodné léčby další linie. Stále je proto žádoucí hledat nové léky splňující obě kritéria účinnosti a bezpečnosti a ideálně je použít v co nejčasnější linii léčby. Asciminib se jeví jako účinný a pacienty dobře snášený lék.
Literatura
SPC Scemblix. Dostupné na https://www.sukl.gov.cz; Datum poslední revize textu 25. 4. 2025
Platná SPC uvedených přípravků dle https://sukl.gov.cz; datum přístupu duben 2025
Laboratorní zkratky souhrnně:
ALP – alkalická fosfatáza; ALT – alaninaminotransferáza; Baz – bazofily; CRP – C‑reaktivní protein; DIF – diferenciální počet leukocytů; Eoz – eozinofily; Ery – erytrocyty; GGT – gamaglutamyltransferáza; Hgb – hemoglobin; LDH – laktátdehydrogenáza; Leu – leukocyty; Lymfo – lymfocyty; Metamyelo – metamyelocyty; Mono – monocyty; Myelo – myelocyty; NS – neutrofilní segmenty; NT – neutrofilní tyče; Trombo – trombocyty; TSH – tyreostimulační hormon