MIBC v roce 2025: Kam se posunuly diagnostika a léčba a jaké otázky se aktuálně řeší?
Jak má dnes vypadat hodnocení, diagnostika a léčba invazivního karcinomu močového měchýře a uroteliálního karcinomu horních močových cest? Jaké poznatky jsou k dispozici u přístupů šetřících močový měchýř? Co pacientům nabízejí neoadjuvantní režimy léčby, pro koho jsou vhodné a co by měly zahrnovat? Může být u pacientů s invazivním karcinomem močového měchýře nápomocná tekutá biopsie? A je optimální současná cesta, kterou musí urazit pacient s karcinomem močového měchýře? Na tyto i další otázky odpověděli přednášející v rámci III. sekce odborného programu kolokvia Bladder Cancer Master Class, zaměřené na svalovinu invadující karcinom močového měchýře.
Staging, diagnostika a endoskopická léčba MIBC a UTUC
 První přednášky se ujal prof. Yann Neuzillet, MD, PhD, z Université de Versailles Saint‑Quentin‑en‑Yvelines ve Francii. Hovořil o stagingu, diagnostice a endoskopické léčbě svalovinu invadujícího karcinomu močového měchýře (muscle‑invasive bladder cancer, MIBC).1
První přednášky se ujal prof. Yann Neuzillet, MD, PhD, z Université de Versailles Saint‑Quentin‑en‑Yvelines ve Francii. Hovořil o stagingu, diagnostice a endoskopické léčbě svalovinu invadujícího karcinomu močového měchýře (muscle‑invasive bladder cancer, MIBC).1
Uroteliální karcinom (urothelial carcinoma, UC) v podstatě tvoří dvě onemocnění – drtivou většinu (95 %) případů představuje karcinom močového měchýře (bladder cancer, BC), zbytek (5 %) uroteliální karcinom horních močových cest (upper tract urothelial carcinoma, UTUC). Světová data o výskytu UC tedy odrážejí především výskyt BC. Karcinom močového měchýře se přitom od UTUC liší. Například kouření je hlavní rizikový faktor BC, ale jen mírně zvyšuje riziko UTUC, za nímž stojí spíše například Lynchův syndrom. Pacienti s UTUC jsou starší než ti s BC. Stejné nejsou ani mutace – BC a UTUC jich sice řadu sdílejí, ale v odlišné frekvenci; u UTUC se častěji vyskytují mutace H‑RAS a FGFR3, u BC mutace RB1, TP53 a ERBB2.2,3 „Celkově lze říci, že ačkoli mají stejný histologický původ, UTUC a BC jsou dvě odlišné nemoci,“ konstatoval přednášející s dovětkem, že existují případy, kdy se BC a UTUC klonálně podobají, protože se šíří do jiné části močového systému.
Rozdíly plynou i z odlišné tloušťky svalové vrstvy močového měchýře a horních močových cest – to ovlivňuje histologickou prognózu i TNM (Tumor–Node–Metastasis) klasifikaci (u BC se u stadií T2 [rozšíření do svaloviny] a T3 [rozšíření do perivezikálních tkání] rozlišují ještě podstadia A a B), u UTUC se ve stadiu T3 zohledňuje lokalizace nádoru v ledvinné pánvičce nebo močovodu (nádory močovodu mají horší prognózu).4
Diagnostika a staging UC
Hlavní nástroj pro detekci a staging BC a UTUC tvoří zobrazovací metody. U BC je přínosnější magnetická rezonance (MR) než výpočetní tomografie (computed tomography, CT). Staging podle multiparametrické MR a klasifikace VI‑RADS má pro MIBC citlivost 83 % a specificitu 90 %.5 „Je to tedy dobré vyšetření pro včasnou detekci nádoru močového měchýře s invazí do svaloviny,“ uvedl přednášející. Výpočetní tomografie je užitečná pro detekci invaze do perivezikální tkáně a přilehlých orgánů. V případě UTUC označil za lepší pro detekci i staging nádoru CT urografii, jejíž citlivost je asi 92 % a specificita 95 %.6
Přednášející ovšem varoval, že staging pomocí zobrazovacího vyšetření není optimální – může podcenit stadium, tj. hloubku invaze, z čehož plyne špatný odhad prognózy pacienta. Hrozí to zejména u nádorů močovodu, stává se to ale i u BC.4,7
Nemalé riziko podcenění stadia nádoru ale existuje i u histologických vzorků. Podle přednášejícího by výsledky pacienta včetně prognózy zlepšil konsenzus ohledně centralizovaného přezkoumávání vzorků odbornými patology. Ten však chybí. Stále tak platí, že léčba se v některých případech může míjet se skutečným stadiem nádoru a není přizpůsobena danému pacientovi. Prof. Neuzillet doplnil, že recentní literatura zmiňuje jako alternativu k endoskopickému odběru vzorků u BC perkutánní biopsii.8,9 Existují sice obavy z šíření nemoci po odběru části BC, bezpečnost tohoto druhu biopsie však byla prokázána. Stále ovšem zbývá definovat pozici perkutánní biopsie v léčbě pacienta.
Endoskopický management
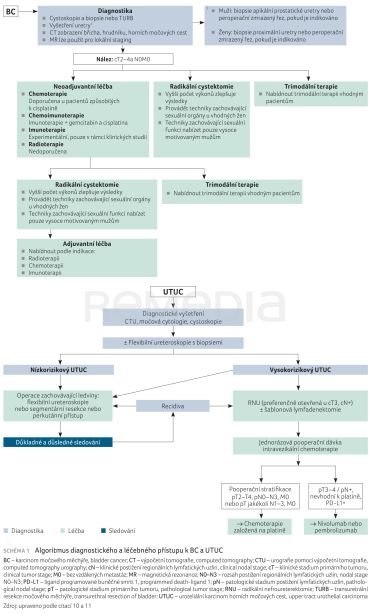 Odborné pokyny pro léčbu pacientů s BC či UTUC upozorňují, že ve vhodných případech má pro pacienty značný význam neoadjuvantní chemoterapie (NAC) na bázi cisplatiny nebo chemoimunoterapie (schéma 1).10 Pro neoadjuvantní režimy u pacientů s UTUC je zde málo prostoru, typ chirurgického zákroku se má zvažovat podle rizika progrese onemocnění, zejména invaze do lymfatických uzlin, a možnosti konzervativní léčby s využitím endoskopie.11
Odborné pokyny pro léčbu pacientů s BC či UTUC upozorňují, že ve vhodných případech má pro pacienty značný význam neoadjuvantní chemoterapie (NAC) na bázi cisplatiny nebo chemoimunoterapie (schéma 1).10 Pro neoadjuvantní režimy u pacientů s UTUC je zde málo prostoru, typ chirurgického zákroku se má zvažovat podle rizika progrese onemocnění, zejména invaze do lymfatických uzlin, a možnosti konzervativní léčby s využitím endoskopie.11
U BC je také podstatné nepodcenit přínosy transuretrální resekce močového měchýře (transurethral resection of bladder tumor, TURB). Nedávná studie prokázala, že u pacientů, kteří po radikální cystektomii (RC) dosáhli pT0, nemělo vliv na prognózu celkového přežití to, zda podstoupili samotnou TURB nebo kombinaci TURB + NAC.12 „Hlavním problémem je, že neexistuje žádný biomarker pro detekci pacientů, kteří mohou profitovat z neoadjuvantní chemoterapie,“ zamyslel se prof. Neuzillet. „Musíme tedy provést co nejlepší resekci. A pokud to není možné, musíme doufat, že pacient bude reagovat na chemoterapii na bázi cisplatiny, aby se zlepšila prognóza.“
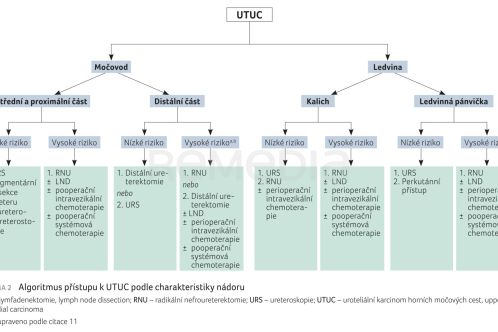 U UTUC je situace velmi odlišná. O operaci se rozhoduje v závislosti na umístění nádoru a riziku daném velikostí, stadiem a počtem nádorů (schéma 2).11 V případě eventuální operace šetřící nefrony je nutná jistota zachování renální funkce, což však u tohoto onemocnění bývá velký problém, protože se obvykle jedná o nejstarší pacienty s komorbiditami a s již narušenou renální funkcí. Hrozí tedy chronické selhání ledvin a nutnost dialýzy, která má podle přednášejícího u komorbidních starších osob vyšší mortalitu než samotný uroteliální karcinom. „U tohoto typu nádoru tedy musíme porovnat riziko dialýzy s konzervativním přístupem,“ upozornil prof. Neuzillet a doplnil, že u BC, a konkrétně MIBC, je důležité odstranit pokud možno celý nádor, zatímco u UTUC tomu tak není.
U UTUC je situace velmi odlišná. O operaci se rozhoduje v závislosti na umístění nádoru a riziku daném velikostí, stadiem a počtem nádorů (schéma 2).11 V případě eventuální operace šetřící nefrony je nutná jistota zachování renální funkce, což však u tohoto onemocnění bývá velký problém, protože se obvykle jedná o nejstarší pacienty s komorbiditami a s již narušenou renální funkcí. Hrozí tedy chronické selhání ledvin a nutnost dialýzy, která má podle přednášejícího u komorbidních starších osob vyšší mortalitu než samotný uroteliální karcinom. „U tohoto typu nádoru tedy musíme porovnat riziko dialýzy s konzervativním přístupem,“ upozornil prof. Neuzillet a doplnil, že u BC, a konkrétně MIBC, je důležité odstranit pokud možno celý nádor, zatímco u UTUC tomu tak není.
Léčba šetřící měchýř: Poznatky, výhody a výzvy
 Kromě radikální cystektomie existuje rovněž několik možností šetřících měchýř (maximální TURB, parciální cystektomie, radioterapie [RT], chemoradioterapie [CRT], chemoterapie [CHT], trimodální terapie [TMT]), mezi lékaři vůči nim ale přetrvává skepse. Data byla dlouho omezená a zůstávaly i zásadní otázky: kdo je vhodný pacient a zda výsledky mohou odpovídat výsledkům chirurgického zákroku. Současné úrovni poznání v této oblasti se věnoval doc. MUDr. Michal Staník, Ph.D., z Oddělení urologické onkologie MOÚ v Brně.13
Kromě radikální cystektomie existuje rovněž několik možností šetřících měchýř (maximální TURB, parciální cystektomie, radioterapie [RT], chemoradioterapie [CRT], chemoterapie [CHT], trimodální terapie [TMT]), mezi lékaři vůči nim ale přetrvává skepse. Data byla dlouho omezená a zůstávaly i zásadní otázky: kdo je vhodný pacient a zda výsledky mohou odpovídat výsledkům chirurgického zákroku. Současné úrovni poznání v této oblasti se věnoval doc. MUDr. Michal Staník, Ph.D., z Oddělení urologické onkologie MOÚ v Brně.13
Vyzdvihl, že pohledy lékařů na chirurgické zákroky a strategie zachovávající močový měchýř se značně liší od pohledu pacientů.14,15 „Odstranění každého močového měchýře není zrovna precizní medicína. Lékaři však vždy mají obavy z rizika rekurence a dopadu na přežití, pokud nebude měchýř odstraněn. Data podporující TMT jsou pořád spíše pro invazivní nádory menšího rozsahu u selektovaných nemocných. Také je nedostatečná multidisciplinární spolupráce,“ uvedl přednášející s tím, že naopak pro pacienty je v mnoha případech zachování močového měchýře hlavním cílem. Nakonec jde tedy o vyvážení – zaměření se na onkologické výsledky versus přání pacientů zachovat močový měchýř.
Většina léčebných možností šetřících měchýř je ale vhodná jen pro určité skupiny pacientů a výsledky v ukazatelích pětileté míry rekurence nebo pětiletého celkového přežití (overall survival, OS) bývají horší než v případě přikročení k RC. Nadějnější je TMT, tedy trojkombinace maximální TURB + CRT ± CHT (neoadjuvantní/adjuvantní). Optimálním pacientem pro ni je osoba s unifokálním tumorem cT2, bez hydronefrózy a multifokálního karcinomu in situ, dobrou funkcí močového měchýře a kompletní TURB.16 „Pokud má pacient po trimodální terapii dobrou odpověď, může být sledován. V opačném případě by dalším krokem byla záchranná cystektomie,“ dodal přednášející.
Radikální cystektomie vs. TMT
Může trimodální terapie dosáhnout stejných výsledků jako chirurgický zákrok? Přímo tyto dva přístupy porovnala pouze jediná randomizovaná kontrolovaná studie fáze III SPARE, která testovala vliv TMT a RC na celkové přežití.17 Bohužel však ve 27 centrech mohlo být randomizováno pouze 45 pacientů, a to především pro non‑compliance k léčbě. Na konci výsledky jasně favorizovaly chirurgický zákrok. První metaanalýza TMT vs. RC byla publikována v roce 2018.18 Zahrnula 57 studií se zhruba 30 000 pacienty, z nichž 3 402 podstoupilo TMT, přičemž desetileté přežití specifické pro daný typ karcinomu (cancer‑specific survival, CSS) rovněž favorizovalo RC.
Nicméně v roce 2023 byla publikována další analýza z hlediska TMT, tentokrát provedená ve dvou významných institucích v Bostonu a Torontu.19 Zahrnuto bylo 722 pacientů s cT2–4N0M0, a to pečlivě vybraných. Většina představovala ideální případy pro TMT – cT2 (90 %), bez karcinomu in situ (79 %), bez hydronefrózy (90 %), po kompletní TURB. Způsobilých pro TMT bylo jen 33 %. Chemoterapii (neoadjuvantní/adjuvantní) podstoupilo 56 vs. 59 % účastníků. Ve skupině s cystektomií mělo 44 % pacientů lokálně pokročilé onemocnění T3 či T4. Analýza neprokázala rozdíl mezi TMT a cystektomií – přežití bez metastáz (metastasis‑free survival, MFS) bylo shodně 74 %, CSS 81 vs. 84 %. „Na základě těchto údajů tedy TMT může u vybraných pacientů přinést srovnatelné výsledky jako chirurgický zákrok,“ shrnul doc. Staník.
Konstatoval, že na základě dosavadních důkazů pro možnosti zachování močového měchýře představuje hlavní skutečnou alternativu k cystektomii trimodální terapie zvolená u vhodně vybraných pacientů.
Co je zapotřebí pro zavedení TMT?
Přednášející připojil rovněž svůj pohled na výhody a výzvy, které je potřeba překonat pro bezpečné zavedení této metody:
- Přijetí TMT v reálné praxi – v současnosti tvoří skutečná cílová skupina maximálně 15 až 20 % (pacienti s klinicky lokalizovaným karcinomem vhodní pro CHT), příchod kombinací konjugátů protilátka–léčivo (antibody–drug conjugate, ADC) (ADC + imunoterapie) ji v blízké budoucnosti může rozšířit na 30–40 %;20
- Infrastruktura a přístup k léčbě– pro reprodukci vynikajících výsledků jsou potřeba odborné znalosti, centralizace a výborná multidisciplinární spolupráce; cesta pacienta je podle přednášejícího velmi složitá a také volbu léčby ovlivňuje mnoho praktických faktorů (třeba vzdálenost bydliště pacienta od onkologického centra);20
- Lepší definování úplné odpovědi – v současné době se spoléhá na cystoskopii a CT; lepší by měly být cirkulující nádorová DNA (circulating tumor DNA, ctDNA) – tady jsou podle doc. Staníka ovšem zapotřebí další studie pro zjištění, jak tyto biomarkery začlenit a využívat;21
- Nutnost pečlivého doživotního sledování (cystoskopie, biopsie a cytologie, zobrazovací vyšetření atd.) pro kontroly funkčnosti močového měchýře; u některých pacientů hrozí chronická radiační toxicita, která se může projevit například jako zmenšení kapacity močového měchýře nebo těžká hemoragická cystitida a nese s sebou riziko ztráty močového měchýře i bez známek onkologického onemocnění;22
- Odpověď na otázku, zda záchranná cystektomie je skutečně záchranná, zní: data jsou omezená, ale slovy přednášejícího pravděpodobně lze pacienty zachránit, pokud byli pečlivě vybráni již na začátku.19
Co by mohlo v nejbližší době přinést změnu?
Jak uvedl doc. Staník, v blízké budoucnosti je očekávána účinnější systémová léčba (ADC + imunoterapie), která přinese vyšší míru dosažení úplné odpovědi, i využití lepších biomarkerů (kinetika ctDNA u pacientů s TMT), které umožní lépe definovat kompletní odpověď i minimální reziduální nemoc. Dodají nám větší jistotu při rozhodování a při volbě strategií deeskalace, které nám možná jednoho dne umožní u části nemocných s invazivními nádory měchýře zcela se vyhnout lokální terapii.
„Všechny tyto pokroky nás pravděpodobně posunou více směrem k personalizovaným možnostem léčby močového měchýře,“ uvedl doc. Staník s tím, že pečlivý výběr pacientů bude naprosto zásadní. „Očekáváme pokroky v oblasti biomarkerů a strategií deeskalace systémové léčby, ale stále budou existovat faktory související s pacienty a institucemi, které budou možná překážkou pro jejich široké zavedení. Potřebujeme i studie, které všechny tyto nové strategie ověří.“
Neoadjuvantní chemoterapie, imunoterapie a ADC
 Své pojednání o aktuální roli NAC, imunoterapie a ADC v léčbě MIBC začal Prof. Dr. med. Jonas Busch z Vivantes Klinikum am Urban v Berlíně‑Kreuzbergu klinickým případem.23
Své pojednání o aktuální roli NAC, imunoterapie a ADC v léčbě MIBC začal Prof. Dr. med. Jonas Busch z Vivantes Klinikum am Urban v Berlíně‑Kreuzbergu klinickým případem.23
Kazuistika pacienta – a co z ní vyplývá
Jedná se o 70letého muže s mírně zhoršeným výkonnostním stavem (performance status, PS) podle Eastern Cooperative Oncology Group (ECOG PS). Trpí retencí moči (od března 2025), má hematurii a zavedený katétr. Anamnéza zahrnuje hypertenzi, diabetes mellitus 2. typu, bolesti zad, cévní mozkovou příhodu; netrpí alergiemi. Cystoskopie odhalila nádor, transuretrální resekce tumoru močového měchýře prokázala multifokální karcinom, MR prokázala nádor cT4 a jednu zasaženou lymfatickou uzlinu. Absolvoval čtyři cykly chemoterapie na bázi gemcitabin–cisplatina s durvalumabem podle studie NIAGARA.24 Během aplikace se neobjevily žádné imunitní nežádoucí účinky, ale ve 4. cyklu došlo k závažné neutropenii. Pacient nakonec podstoupil otevřenou RC, přičemž volba otevřené operace vyšla ze stadia cT4.
Přednášející na tomto příkladu poukázal na některé slabé stránky randomizované kontrolované studie fáze III NIAGARA. V ní jedno rameno užívalo NAC (gemcitabin–cisplatina) + durvalumab a druhé samotnou NAC a po RC první rameno pokračovalo adjuvantní monoterapií durvalumabem a srovnávací rameno zůstalo bez adjuvantní léčby. Řada cílových ukazatelů (přežití bez události [event‑free survival, EFS], míra dosažení úplné odpovědi [complete response, CR], OS, MFS) i analýza podskupin prokázaly výhody přidání durvalumabu. Přednášející se řečnicky otázal, jak by se promítlo do výsledků, kdyby komparátorem v neoadjuvantní fázi byl režim ddMVAC (dose‑dense MVAC [methotrexát, vinblastin, doxorubicin a cisplatina]), kdyby i srovnávací skupina užívala adjuvantní léčbu, například nivolumab, či kolik pacientů je asi nadléčeno adjuvantně durvalumabem, pokud dosáhli patologické CR nebo neodpovídají na inhibitory kontrolních bodů imunity. Zastavil se i u skutečnosti, že studijní soubor měl clearance kreatininu ≥ 40 ml/min – podle přednášejícího je otázka, zda jsme přesvědčeni léčit tuto populaci. Vyjádřil přesvědčení, že pacienti by měli užívat chemoterapii, kdykoli je to možné, a prospěch z ní má i podskupina s mírně zhoršenou renální funkcí.
Dále mimo jiné upozornil, že pacienti, kteří nepodstoupili RC (došlo k odložení), tvořili jen 1 %. „To jsou klasické argumenty chirurgů, jako jsem já, kteří se v minulosti vyhýbali neoadjuvantní chemoterapii. Musíte tyto údaje ukázat chirurgům a pak jim říct: Dobře, neoadjuvantní chemoterapie neodkládá operaci, nezabrání tomu, aby byl váš pacient nakonec operován, pomůže vašemu pacientovi. Tyto údaje jsou tedy důležité, aby přesvědčily chirurgy ohledně chemoterapie,“ apeloval prof. Busch s tím, že chirurgové by také měli znát další možné nežádoucí účinky. Ve studii NIAGARA přidání durvalumabu ke standardní CHT nežádoucí účinky nezměnilo, což označil za dobrou zprávu.
Studie NIAGARA je zatím jediná publikovaná studie fáze III s přesvědčivými výsledky. Probíhá velká diskuse o podávání samotné neoadjuvantní imunoterapie. Určitou účinnost ukázaly studie fáze II s pembrolizumabem a atezolizumabem, ale dosud nebyla publikována studie fáze III. Pokyny tedy v současné době říkají, že samotná neoadjuvantní imunoterapie by měla být pouze ve studiích. „Jsem si však docela jistý, že se tato oblast v budoucnu výrazně změní,“ podotkl.
Na co se čeká
Přednášející rovněž poukázal na několik studií, u nichž je očekáváno zveřejnění v příštích týdnech, měsících a letech:25
- EV‑303 – neoadjuvantně pembrolizumab ± enfortumab vedotin před radikální cystektomií u pacientů, kteří nejsou vhodní pro cisplatinu, a poté adjuvantní fáze;
- EV‑304 – viz EV‑303, ale pro pacienty vhodné pro cisplatinu je pembrolizumab + enfortumab vedotin versus standardní CHT. „Ale i zde po standardní chemoterapii nemáme adjuvantní léčbu, což bude pravděpodobně malý problém při závěrečném vyhodnocení těchto studií, protože adjuvantní imunoterapie je dnes standardem.“
- VOLGA – trojkombinace durvalumab + tremelimumab + enfortumab vedotin vs. durvalumab + enfortumab vedotin vs. cystektomie a adjuvantní terapie – tj. jedna skupina nepodstupuje cystektomii, druhá ano.
- ENERGIZE – NAC + nivolumab ± linrodostat mesylát, pak cystektomie a v adjuvantní fázi nivolumab.
„Nivolumab známe z adjuvantního prostředí,“ uvedl s připomenutím studie CheckMate 274.
„Je tedy důležité připomenout, že kdykoli máte pacienta, který dosud neužíval žádnou neoadjuvantní imunoterapii, měl by ji dostat,“ konstatoval přednášející. Vyjádřil názor, že u nádorů cT2 je zapotřebí diskuse o možnostech v rámci multidisciplinárního tumor boardu – označil to za dobrou interdisciplinární praxi. Chemoterapie by měla být standardem pro všechny pacienty, kteří jsou dostatečně zdravotně způsobilí pro cisplatinu. V současné době je u pacientů vhodných pro cisplatinu novým standardem přidání durvalumabu k CHT. Imunoterapie samotná je zatím pouze experimentální možností. Mimo rámec MIBC lze doplnit, že u UTUC se u vysoce rizikového onemocnění (např. od stadia cT3) diskutuje role neoadjuvantní systémové léčby, a to zejména s ohledem na vysoké riziko mikrometastatického postižení již v době diagnózy. Neoadjuvance je v tomto kontextu chápána jako strategický nástroj časného ovlivnění systémového onemocnění a dosažení downstagingu s prognostickým významem.
„Jsem si docela jistý, že uvidíme obrovské změny,“ prohlásil prof. Busch závěrem.
Role ctDNA
 Významnou roli (nejen) v onkologii mají biomarkery a mezi důležité vyšetřovací možnosti patří tekutá biopsie – tedy možnost identifikovat různé složky tělních tekutin, zejména krve, např. cirkulující nádorové buňky, extracelulární vezikuly, nebo dokonce bezbuněčnou DNA (cell‑free DNA, cfDNA), jež může být uvolňována do krevního systému několika mechanismy, nejčastěji v souvislosti s buněčnou smrtí. U pacientů se zhoubnými nádory stoupá koncentrace z obvyklých < 10 ng/ml až na > 1 000 ng/ml. Podrobněji se jí věnovala dr. Brigida Anna Maiorano z San Raffaele Scientific Institute v Miláně.26
Významnou roli (nejen) v onkologii mají biomarkery a mezi důležité vyšetřovací možnosti patří tekutá biopsie – tedy možnost identifikovat různé složky tělních tekutin, zejména krve, např. cirkulující nádorové buňky, extracelulární vezikuly, nebo dokonce bezbuněčnou DNA (cell‑free DNA, cfDNA), jež může být uvolňována do krevního systému několika mechanismy, nejčastěji v souvislosti s buněčnou smrtí. U pacientů se zhoubnými nádory stoupá koncentrace z obvyklých < 10 ng/ml až na > 1 000 ng/ml. Podrobněji se jí věnovala dr. Brigida Anna Maiorano z San Raffaele Scientific Institute v Miláně.26
Jak uvedla, různé studie prokázaly, že v ctDNA lze nalézt specifické genomické nebo epigenetické změny, které umožňují propojit ji s primárním nádorem. Tekutá biopsie pro analýzu ctDNA je minimálně invazivní a snadno opakovatelná, velmi užitečná u solidních nádorů k monitorování progrese, identifikaci genetických změn a je reprezentativnější pro heterogenitu nádoru v porovnání s tkáňovou biopsií. Používané metody digitální kapkové polymerázové řetězové reakce (droplet digital polymerase chain reaction, ddPCR) a sekvenování nové generace (next‑generation sequencing, NGS) jsou poměrně přesné. Hlavním omezením analýzy tekuté biopsie a jejího zavedení do rutinní praxe zůstává množství ctDNA, které se uvolňuje do krevního řečiště a je ovlivněno různými preklinickými a patofyziologickými parametry.
Důkazů o výhodách tekuté biopsie a analýzy ctDNA u UC, zejména pak MIBC, přibývá. Různé studie se zaměřují na prognostickou stratifikaci UC, možnost definovat tekutou biopsií relaps nebo vyhodnotit minimální reziduální onemocnění, které nelze detekovat současnými zobrazovacími nástroji, stratifikovat odpověď nebo předpovědět rezistenci na léčbu, ale i ji využít k hodnocení v reálném čase během onemocnění či pomoci při rozhodování o různých liniích léčby v rámci kontinua péče.27
Příklad z reálné praxe
Přednášející se podělila o kazuistiku, kterou uvedla slovy, „jak sériové monitorování ctDNA může pomoci při rozhodování o léčbě a hodnocení odpovědi na léčbu a posloužit jako prognostický biomarker“.
Jde o 71letou ženu s MIBC ve stadiu pT3N0M0, která podstoupila radikální cystektomii, po níž měla ctDNA negativní. Zhruba šest měsíců po operaci došlo k nevysvětlitelnému úbytku hmotnosti se zhoršením celkového stavu. Vyšetření CT bylo negativní, ale koncentrace ctDNA začala stoupat a pozitronová emisní tomografie ukázala progresi. Po dalších třech měsících byly hodnoty ctDNA 3× vyšší než výchozí. Pacientka vstoupila do klinické studie fáze II a zahájila léčbu pembrolizumabem. Po zahájení podávání koncentrace ctDNA klesaly. Po třech měsících užívání pembrolizumabu se na CT skenu ukázala progrese, ale byla interpretována jako pseudoprogrese, protože koncentrace ctDNA dále klesaly. Po dalších třech měsících se na CT skenu potvrdila pseudoprogrese. Hodnoty ctDNA se vrátily na nulu.28
ctDNA v rozhodování o léčbě
Pokud jde o biomarkery, u UC přibývají důkazy o prognostické hodnotě mutační nálože nádoru. U MIBC byla prokázána prognostická role ctDNA při monitorování přežití bez známek nemoci. Detekce ctDNA před cystektomií, v okně minimální reziduální nemoci i okně surveillance je u pacientů s BC prognosticky spojena s přežitím bez známek nemoci.
Ve studii IMvigor010 mělo použití atezolizumabu určující vliv na přežití pacientů s pozitivní ctDNA, a proto byla studie IMvigor011 navržena jako studie řízená biomarkery.29,30 V tomto kontextu dr. Maiorano rozdělila studie na dvě generace – za novou označila ty, které používají ctDNA k vedení klinického rozhodnutí o použití adjuvantní terapie (například IMvigor011).
Analýza ctDNA v IMvigor010 potvrdila, že u pacientů s negativní ctDNA není nutné používat adjuvantně atezolizumab, u těch s pozitivní ctDNA však adjuvantní léčba zlepšila přežití bez progrese oproti sledování. „A proto má studie IMvigor011 nový design,“ uvedla přednášející. „Pacienti s negativní ctDNA jsou tedy pouze sledováni, ale pacienti s pozitivní ctDNA randomizováni k adjuvantnímu užívání atezolizumabu oproti placebu.“
Jinými slovy, ctDNA by mohla být užitečná pro zlepšení prognostické stratifikace pacientů u přístupů šetřících močový měchýř či při rozhodování, který pacient by měl pokračovat v udržovací terapii nebo podstoupit intenzifikaci léčby.
V budoucnu by podle dr. Maiorano mohlo být pro personalizovanou léčbu pacientů s UC přínosné, kdyby součástí multidisciplinárních tumor boardů byl i molekulární biolog. Dodala, že před zavedením analýzy ctDNA do rutinní klinické praxe je potřeba standardizovat postup, ale také znát ekonomické náklady. „Myslím si, že v budoucnu budeme analýzu ctDNA používat stále více, a to jak u invazivních, tak metastazujících nádorů,“ uvedla závěrem.
Jak zlepšit péči o pacienty s UC?
V poslední přednášce sekce dr. Jorge Dias z Centro Hospitalar de Vila Nova de Gaia v portugalském Espinhu poukázal na obtížnost cesty pacienta s uroteliálním karcinomem za diagnózou a léčbou.31 Zabýval se přitom rozdílem mezi ideálním světem a realitou v klinické praxi.
„Máme pokyny od všech společností, ať už jde o European Association of Urology (EAU), American Urological Association, National Comprehensive Cancer Network nebo European Society for Medical Oncology, realita je však někdy velmi odlišná,“ konstatoval. Problémy s sebou nesou zpoždění diagnózy i obtížný přístup k léčbě, které odrážejí dopad socioekonomických rozdílů. „Víme, že 75–90 % případů karcinomu močového měchýře se projevuje makrohematurií. Ale pouze 10–15 % diagnostických vyšetření zánětlivého močového ústrojí odhalí nádory. Někdy je tedy stále obtížné to zjistit, zejména u žen.“ Za zpožděním mohou být faktory na straně pacienta (nízké povědomí o tomto onemocnění, nižší socioekonomický status spojený s nezdravým životním stylem, kouření, méně časté screeningové vyšetření na onkologické onemocnění, omezený přístup ke zdravotní péči) i zdravotníků (chybná diagnóza před diagnózou BC, chybné neodeslání k urologovi, dlouhé objednací lhůty – 6 až 12 měsíců je u BC příliš).
Světová koalice pacientů s karcinomem močového měchýře podle slov přednášejícího uvádí, že u 57 % byla před odhalením BC stanovena chybná diagnóza.
Nízké využívání NAC a odklady cystektomie
Přestože NAC zvyšuje pětileté OS až o 8 %, její celkové světové využívání je podle dat z metaanalýzy 13 studií (n = 35 738) publikované v roce 2019 pouze 17 % (!).32 Existují geografické rozdíly – dobrá data mají například v Japonsku a Švédsku, naopak nízká čísla přicházejí například z Nizozemí nebo Kanady. Mezi důvody nevyužívání NAC patří vysoký věk, horší ECOG PS a velká zátěž pacienta komorbiditami, ale také rozdíly ve zdravotnických systémech, doporučeních a v tom, kdy se pacient odesílá na onkologii. European Association of Urology například doporučuje, aby mezi diagnózou BC a cystektomií byl maximálně tříměsíční interval. Většina z 19 studií (n = 17 232) zahrnutých do metaanalýzy a systematického přehledu z roku 2019 ale uváděla zpoždění – mezi důvody patřily stav pacienta (nejsou zdravotně způsobilí pro operaci, tedy nutnost optimalizovat komorbidity), potřeba druhého názoru, socioekonomické faktory (přístup k nemocnicím s nízkou úrovní vybavení, nutnost odeslání do jiných nemocnic) a častěji nižší vzdělání.33 „A musíme být upřímní, cystektomie není procházka růžovým sadem. Je to velmi agresivní operace,“ připomněl přednášející s upřesněním, že úmrtnost po radikální cystektomii může být stále až 3,2 % do 30 dnů a až 8 % do 90 dnů, míra rehospitalizací do 30 dnů dosahuje 25 % a míra komplikací 30–40 %. Minimálně invazivní operace (laparoskopické nebo robotické) snížily potřebu transfuzí a zkrátily hospitalizace, ale v míře komplikací do 90 dnů nebo času do rekurence rozdíl nepřinesly. Roli hraje rovněž počet operací provedených v daném zařízení. Na optimalizaci míry komplikací je podle EAU potřeba alespoň 20 operací ročně v každé nemocnici. „A pokud provádíme tyto operace ve velkých centrech, víme také, že pacientům budeme schopni poskytnout komplexnější péči,“ uvedl dr. Dias s poukázáním, že u kolorektálního karcinomu je již prokázán příznivý vliv multimodálního prehabilitačního programu – zahrnujícího výživu, fyzickou aktivitu, psychickou podporu a zanechání kouření – na snížení výskytu komplikací. Určité výsledky k tomuto přístupu jsou i u BC a v Nizozemí na toto téma probíhá studie ENHANCE.34
Zkoumá se souvislost mezi socioekonomickými nevýhodami, rasou, pokročilostí BC, diagnózou a horšími vyhlídkami na přežití.
Co s tím?
Co se týče zpoždění diagnózy, je podle dr. Diase potřeba vycházet z úspěšných národních osvětových kampaní v oblasti veřejného zdraví, zlepšit své odborné znalosti v oblasti primární péče a diagnostika musí být rychlá. „Tito pacienti nemohou čekat půl roku, než půjdou do nemocnice. Musí být přednostně odesláni a cystoskopie by měla být provedena co nejrychleji.“ Vyzdvihl význam role multidisciplinárního tumor boardu od samého začátku. „Některé studie ukazují, že přehodnocení radiologie a patologie může změnit léčebný plán až u 44 % těchto pacientů.“ Pacienti s vyššími indexy komorbidity měli být léčeni v centrech s vysokými počty výkonů. Rychlé musejí být i léčebné postupy. Důležité jsou také dostupné informace pro pacienty ve srozumitelném jazyce (nejspíše jako konzultace s onkologickými sestrami, pomoc pacientských organizací). „Někdy se pacient ztratí v množství informací a má strach, co se bude dít,“ vysvětlil přednášející. Na mysli je potřeba mít i již zmíněné socioekonomické faktory. Stěžejní je týmová spolupráce ve všech aspektech, které se pacienta s UC dotýkají – tedy společné úsilí urologů, onkologů, sester, fyzioterapeutů, psychologů, případně i sociálních pracovníků.
Klíčové body
- BC a UTUC jsou klinicky i biologicky odlišné jednotky (rizikové faktory, věk, spektrum mutací), což se promítá do odlišného stagingu, prognózy i léčebných algoritmů.
- Staging je primárně pomocí zobrazovacích metod: u MIBC preferujeme multiparametrickou MR s VI‑RADS (dobrá přesnost pro detekci svalové invaze), u UTUC CT urografii; přesto se stadium, tj. hloubka invaze, často podcení, zvláště u nádorů močovodu.
- Variabilita patologie může vést k nesprávné stratifikaci; přínosná by byla centralizovaná revize. Diskutuje se perkutánní biopsie (bezpečnost doložena, indikace a role se vymezují).
- U MIBC je zásadní maximálně kvalitní TURB; chybí robustní biomarker pro predikci profitu z neoadjuvantní léčby, proto se praxe opírá o optimální lokální kontrolu a cisplatinovou neoadjuvantní chemoterapii u způsobilých pacientů.
- UTUC vyžaduje s přihlédnutím k riziku volbu mezi radikálním a konzervativním/endoskopickým postupem; rozhodování je limitováno renální rezervou a u starších komorbidních nemocných může být riziko dialýzy prognosticky dominantní.
- U UTUC se u vysoce rizikového onemocnění (např. od stadia cT3) diskutuje role neoadjuvantní systémové léčby, zejména s ohledem na riziko mikrometastatického postižení a možnost downstagingu; nejde zatím o jednoznačný standard.
- Z přístupů šetřících močový měchýř má nejsilnější důkazy trimodální terapie (TMT: maximální TURB + CHT + CRT) u pečlivě vybraných pacientů (typicky unifokální cT2, bez hydronefrózy a karcinomu in situ, kompletní TURB) se záchrannou cystektomií při nedostatečné odpovědi.
- Data porovnávající radikální cystektomii a TMT jsou heterogenní; při přísné selekci může být TMT onkologicky srovnatelná s chirurgickým řešením za cenu intenzivního celoživotního sledování a rizika chronické radiační toxicity.
- Neoadjuvantní léčba u MIBC se posouvá: výsledky studie NIAGARA podporují přidání durvalumabu k cisplatinové chemoterapii u způsobilých pacientů a tento přístup směřuje k novému standardu perioperační léčby; samotná neoadjuvantní imunoterapie zůstává zatím vyhrazena klinickým studiím.
- Probíhající studie kombinací ADC a imunoterapie (EV‑303/304, VOLGA, ENERGIZE) mohou v budoucnu měnit léčebné standardy; otevřené zůstávají otázky optimální adjuvantní léčby a rizika nadléčení u pacientů s velmi dobrou odpovědí.
- CtDNA se profiluje jako nástroj pro detekci minimálního reziduálního onemocnění, časného relapsu a biomarkerově řízenou adjuvantní léčbu (např. IMvigor011); limitací zůstávají preanalytické faktory a nízké uvolňování ctDNA u části pacientů.
- Slabým místem péče zůstává cesta pacienta: nízké využití neoadjuvantní léčby a odklady cystektomie; klíčové jsou časná multidisciplinární diskuse, centralizace výkonů a prehabilitace.
Literatura
[1] Neuzillet Y. Staging, diagnosis, and endoscopic management and therapy of MIBC and UTUC. Bladder Cancer Master Class, Brno, 24.–26. 9. 2025.
[2] Sfakianos JP, Cha EK, Iyer G, et al. Genetic differences between bladder and upper urinary tract carcinoma: implications for therapy. Eur Urol Oncol 2021; 4: 170–179.
[3] Audenet F, Isharwal S, Cha EK, et al. Clonal relatedness and mutational differences between upper tract and bladder urothelial carcinoma. Clin Cancer Res 2019; 25: 967–976.
[4] Shiga M, Nagumo Y, Kojo K, et al. The correlation between discrepancies in clinical and pathological T stages and overall survival in upper urinary tract urothelial carcinoma: analysis of the hospital‑based cancer registry data in Japan. Int J Urol 2025; 32: 394–400.
[5] Woo S, Panebianco V, Narumi Y, et al. Diagnostic performance of vesical imaging reporting and data system for the prediction of muscle‑invasive bladder cancer: a systematic review and meta‑analysis. Eur Urol Oncol 2020; 3: 306–315.
[6] Janisch F, Abufaraj M, Fajkovic H, et al. Diagnostic performance of multidetector computed tomographic urography in upper tract urothelial carcinoma: a systematic review and meta‑analysis. World J Urol 2020; 38: 1165–1175.
[7] del Giudice F, Rosiello G, Palumbo C, et al. Contemporary trends and predictors of pT0 in radical cystectomy specimens among non‑muscle and muscle‑invasive bladder cancer patients: a propensity score‑matched analysis from a single tertiary centre in the United Kingdom. Cancers 2025; 17: 3110.
[8] Tucker A, Patel N, Allen BC, et al. Safety and diagnostic yield of percutaneous urinary bladder tumor biopsy. Abdom Radiol 2025.
[9] Prost D, Colin P, Rouprêt M, et al. Oncological safety and diagnostic yield of percutaneous needle‑core biopsies in upper tract urothelial carcinoma: the UPERCUT study. Eur Urol Oncol 2025.
[10] van der Heijden AG, Witjes JA, Gakis G, et al. European Association of Urology guidelines on muscle‑invasive and metastatic bladder cancer: summary of the 2025 guidelines. Eur Urol 2025; 87: 582–600.
[11] Masson‑Lecomte A, Colin P, Rouprêt M, et al. European Association of Urology guidelines on upper urinary tract urothelial carcinoma: summary of the 2025 update. Eur Urol 2025; 87: 697–716.
[12] Lavery HJ, Shariat SF, Chang SS, et al. Pathological T0 following radical cystectomy with or without neoadjuvant chemotherapy: a useful surrogate. J Urol 2014; 191: 898–906.
[13] Staník M. Bladder‑sparing treatment – myth, or reality? Bladder Cancer Master Class, Brno, 24.–26. 9. 2025.
[14] Mannion M, O’Neill L, Fitzpatrick JM, et al. Treatment preferences of patients with muscle‑invasive bladder cancer: a discrete choice experiment. BJUI Compass 2024; 5: 1173–1182.
[15] Smith AB, Gore JL, Chisolm S, et al. Muscle‑invasive bladder cancer treatment selection in an emerging treatment era: a patient preference study. Urology 2025.
[16] Hamad J, McKiernan JM, Shah JB, et al. Bladder preservation in muscle‑invasive bladder cancer: a comprehensive review. Int Braz J Urol 2020; 46: 169–184.
[17] Huddart RA, Hall E, Hussain SA, et al. Clinical and patient‑reported outcomes of SPARE – a randomised feasibility study of selective bladder preservation versus radical cystectomy. BJU Int 2017; 120: 639–650.
[18] Williams SB, Huo J, Chamie K, et al. Comparing survival outcomes and costs associated with radical cystectomy and trimodal therapy for older adults with muscle‑invasive bladder cancer. JAMA Surg 2018; 153: 881–889.
[19] Zlotta AR, Fleshner NE, Jewett MAS, et al. Radical cystectomy versus trimodality therapy for muscle‑invasive bladder cancer: a multi‑institutional propensity score matched and weighted analysis. Lancet Oncol 2023; 24: 669–681.
[20] Davies‑Teye BB, Mahal BA, Aizer AA, et al. Treatment patterns and radical cystectomy outcomes in patients diagnosed with urothelial nonmetastatic muscle‑invasive bladder cancer in the United States. Cancer Med 2025; 14: e70644.
[21] Powles T, Assaf ZJ, Davarpanah NN, et al. Circulating tumor DNA in patients with muscle‑invasive bladder cancer who received perioperative durvalumab in NIAGARA. J Clin Oncol 2025; 43 (Suppl).
[22] Kaufmann A, Eapen RS, Rodel C, et al. Follow‑up strategies after trimodal treatment for muscle‑invasive bladder cancer: a systematic review. World J Urol 2024; 42: 527.
[23] Busch J. Neoadjuvant chemo vs IO vs ADCs + case. Bladder Cancer Master Class, Brno, 24.–26. 9. 2025.
[24] Powles T, Assaf ZJ, Davarpanah NN, et al. Perioperative durvalumab with neoadjuvant chemotherapy in operable bladder cancer. N Engl J Med 2024; 391: 1773–1786.
[25] ClinicalTrials.gov. KEYNOTE‑905/EV‑303 (NCT03924895); EV‑304 (NCT04700124); KEYNOTE‑866 (NCT03924856); VOLGA (NCT04960709); ENERGIZE (NCT03661320). Cit. 14. 12. 2025.
[26] Maiorano BA. Role of ctDNA, practical example. Bladder Cancer Master Class, Brno, 24.–26. 9. 2025.
[27] Pantel K, Alix‑Panabières C. Liquid biopsy and minimal residual disease — latest advances and implications for cure. Nat Rev Clin Oncol 2019; 16: 409–424.
[28] Bratman SV, Yang SYC, Iafolla MAJ, et al. Personalized circulating tumor DNA analysis as a predictive biomarker in solid tumor patients treated with pembrolizumab. Nat Cancer 2020; 1: 873–881.
[29] Bellmunt J, Hussain M, Gschwend JE, et al. Adjuvant atezolizumab versus observation in muscle‑invasive urothelial carcinoma (IMvigor010): a multicentre, open‑label, randomised, phase 3 trial. Lancet Oncol 2021; 22: 525–537.
[30] Powles T, Assaf ZJ, Davarpanah NN, et al. CtDNA‑guided adjuvant atezolizumab in muscle‑invasive bladder cancer. N Engl J Med 2025.
[31] Dias J. Patient journey with urothelial carcinoma: “Ideal world versus reality”. Bladder Cancer Master Class, Brno, 24.–26. 9. 2025.
[32] Liu W, Wang Y, Zhang X, et al. The utilization status of neoadjuvant chemotherapy in muscle‑invasive bladder cancer: a systematic review and meta‑analysis. Minerva Urol Nephrol 2021; 73: 144–153.
[33] Russell B, Parekh DJ, Bochner BH, et al. A systematic review and meta‑analysis of delay in radical cystectomy and the effect on survival in bladder cancer patients. Eur Urol Oncol 2020; 3: 239–249.
[34] Akdemir E, van der Heijden MS, Boormans JL, et al. Effectiveness of a multimodal prehabilitation program in patients with bladder cancer undergoing radical cystectomy: protocol of the ENHANCE multicentre randomised controlled trial. BMJ Open 2023; 13: e071304.