Moderní léčba přináší naději na lepší výsledky u pacientů s metastazujícím uroteliálním karcinomem – v klinických studiích i v reálné praxi
Jaký význam dnes mají kritéria způsobilosti pro podávání chemoterapie založené na platině? Jaké poznatky jsou k dispozici o udržovací léčbě metastazujícího uroteliálního karcinomu v 1. linii? Proč je důležité sekvenovat léčbu metastazujícího uroteliálního karcinomu a co to obnáší? Souzní data z klinických studií s daty z reálné praxe? Čím se zabývá aktuální výzkum? Těmito tématy se zabývala IV. sekce odborného programu kolokvia Bladder Cancer Master Class.
Kritéria způsobilosti pacientů s uroteliálními nádory pro systémovou léčbu
 Incidence uroteliálního karcinomu (urothelial carcinoma, UC) v Evropské unii, včetně České republiky, stoupá. Úmrtnost nicméně zůstává poměrně stabilní. Typický průměrný věk pro tuto diagnózu je v České republice kolem 70 let. Podobná data platí i pro 18 zemí, které představovaly domovinu zahraničních hostů kolokvia. Těmito informacemi zahájil svou přednášku prof. MUDr. Alexandr Poprach, Ph.D., z Kliniky komplexní onkologické péče MOÚ v Brně.
Incidence uroteliálního karcinomu (urothelial carcinoma, UC) v Evropské unii, včetně České republiky, stoupá. Úmrtnost nicméně zůstává poměrně stabilní. Typický průměrný věk pro tuto diagnózu je v České republice kolem 70 let. Podobná data platí i pro 18 zemí, které představovaly domovinu zahraničních hostů kolokvia. Těmito informacemi zahájil svou přednášku prof. MUDr. Alexandr Poprach, Ph.D., z Kliniky komplexní onkologické péče MOÚ v Brně.
Kritéria Guptové versus Galského
Pacienti s UC, a zejména s metastazujícím uroteliálním karcinomem (metastatic urothelial carcinoma, mUC), jsou křehcí. Přednášející nicméně přiznal, že ve své praxi nemá časový prostor na používání dotazníků křehkosti. Za užitečný nástroj, který mu pomáhá při rozhodování o léčbě, označil kritéria způsobilosti pro užívání chemoterapie (CHT) založené na platině. Ta zohledňují i velmi silná doporučení European Society for Medical Oncology (ESMO) z let 2022 a 2024 pro léčbu UC, s nimiž se ztotožňují česká doporučení v Modré knize.2,3 Důležité jsou také celkový zdravotní stav pacienta, komorbidity, compliance, motivace k léčbě aj.
Kritéria způsobilosti pro CHT založenou na platině jsou dvojí – podle Guptové a podle Galského.4,5 Přednášející sám podle vlastních slov ve své klinické praxi používá kritéria podle Galského. Připojil svůj názor, že není pochyb o významu ukazatelů, jako je výkonnostní stav (performance status, PS) podle Eastern Cooperative Oncology Group (ECOG PS), funkční třída New York Heart Association (NYHA) a neuropatie, které zahrnují oboje kritéria, za témata k diskusi ovšem považuje ztrátu sluchu a renální insuficienci – Guptové kritéria obsahují clearance kreatininu (creatinine clearance, CrCl) < 30 ml/min a nezmiňují ztrátu sluchu, Galského kritéria uvádějí CrCl < 60 ml/min i ztrátu sluchu.
Přednášející v tomto kontextu připomněl souvislost závažnosti renální insuficience s mortalitou a morbiditou. Hodnoty CrCl v rozmezí 40–60 ml/min označil za šedou zónu a velkou výzvu. Dotkl se též nefrotoxicity vyvolané cisplatinou a upozornil, že nemusí být ireverzibilní – lze jí předcházet hydratací a korekcí hypomagnezémie substitucí hořčíkem. Některé strategie, jak zmírnit nefrotoxicitu, vyplynuly z komplexní práce Jiangové et al.6
Ztráta sluchu z důvodu ototoxicity hrozí hlavně u cisplatiny.7 Přednášející ale zdůraznil potřebu vnímat, co je pro pacienta skutečně důležité. „Když máte pacienta v adjuvantním nebo metastatickém stadiu, myslím, že je potřeba o této potenciální toxicitě diskutovat s pacientem s ohledem na efekty léčby a přežití, jiná je role této toxicity v adjuvantní indikaci ve srovnání s paliativní,“ uvedl přednášející ke kritériu ztráty sluchu.
V současné éře imunoterapie (IT) a konjugátů protilátka–léčivo (antibody–drug conjugates, ADC) se rovněž porovnávají účinky cisplatiny versus karboplatiny, neboť jejich působení na imunitní systém se liší. Přehodnocuje se postavení karboplatiny – řada studií ukázala, že cisplatina u mUC nepřináší signifikantní benefit z hlediska odpovědi na léčbu a přežití v porovnání s karboplatinou.8,9 Přednášející ovšem podle svých zkušeností považuje za účinnější cisplatinu a to obzvláště v éře moderní imunoterapie.
Kritéria EVITA
Výše zmíněná doporučení ESMO mimo jiné zmiňují pro léčbu dosud neléčených pacientů s pokročilým nebo metastazujícím UC (stadium IV) kombinaci pembrolizumabu s enfortumab vedotinem – po progresi při léčbě touto kombinací nebo u osob, pro které není kombinace vhodná či u nichž je kontraindikována, by se měla podávat CHT založená na platině. V České republice v době konání kolokvia tato možnost nebyla schválena. Nabízí dlouhé trvání odpovědi a u některých pacientů je schopna navodit dlouhodobou remisi, má ale „určitou specifickou toxicitu pro pacienta“, jak řekl přednášející, a „finanční toxicitu“ například podle dat ze Spojených států amerických či z Německa.
Pro určení způsobilosti k užívání této kombinace existují kritéria EVITA (EV‑ineligible criteria), byť dosud nebyla validována. Zahrnují následující body:
- hodnota glykovaného hemoglobinu ≥ 8 %,
- senzorická nebo motorická neuropatie stupně ≥ 2,
- jakákoli korneální nebo retinální abnormalita,
- CrCl nebo míra glomerulární filtrace ≤ 45 ml/min,
- ECOG PS ≥ 2.
Přednášející uvedl, že není jejich zastáncem, protože významná část pacientů by podle nich nebyla k užívání pembrolizumabu s enfortumab vedotinem vhodná – při očekávaném profilu toxicity, kam patří i neuropatie nebo kožní choroby, jsou za nevhodné považovány například osoby s komorbiditami, agresivními nádory, nekontrolovaným či nezjištěným diabetem, nadužíváním alkoholu aj.10 „Kritéria představují nástroj, nikoli dogma,“ upozornil přednášející, jak se na kritéria EVITA pohlíží v České republice.
Závěrem svého vystoupení zdůraznil, že základem je individualizace léčby a její přizpůsobení konkrétním pacientům podle podtypu jejich malignity, metastáz, rozsahu onemocnění, komorbidit i specifik různých možností terapie.
Role udržovací léčby u metastazujícího uroteliálního karcinomu
 Skutečnost, že „jedna velikost nepadne každému“, tedy že léčbu je potřeba individualizovat, a že v 1. linii léčby mUC jsou k dispozici různé možnosti, vyzdvihl také prof. Álvaro Pinto, MD, PhD, z Hospital Universitario La Paz ve španělském Madridu.11
Skutečnost, že „jedna velikost nepadne každému“, tedy že léčbu je potřeba individualizovat, a že v 1. linii léčby mUC jsou k dispozici různé možnosti, vyzdvihl také prof. Álvaro Pinto, MD, PhD, z Hospital Universitario La Paz ve španělském Madridu.11
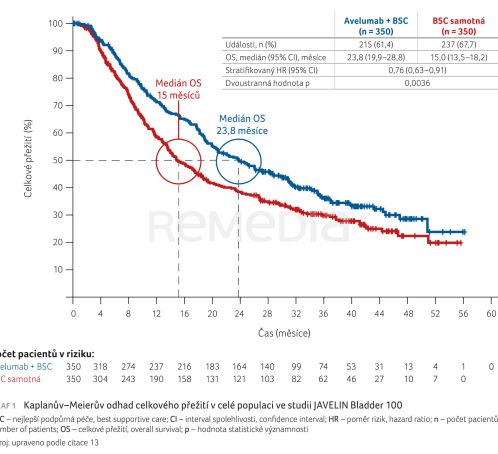 V rámci udržovací léčby v současnosti existuje standard, který zlepšuje celkové přežití (overall survival, OS), a ten vyplynul ze studie JAVELIN Bladder 100 – pacienti, u kterých bylo dosaženo kontroly onemocnění chemoterapií na bázi platiny v 1. linii a byli randomizováni do skupiny s avelumabem plus nejlepší podpůrnou péčí (best supportive care, BSC), dosáhli významného zlepšení OS oproti skupině s BSC samotnou (podle dat z roku 2023 činilo OS 23,8 měsíců vs. 15 měsíců) (graf 1).12,13 Jednalo se o první studii, která u tohoto onemocnění zlepšila OS, včetně léčby platinovými deriváty v 1. linii. „Strategie udržovací léčby se ukázala jako nejúspěšnější,“ uvedl přednášející.
V rámci udržovací léčby v současnosti existuje standard, který zlepšuje celkové přežití (overall survival, OS), a ten vyplynul ze studie JAVELIN Bladder 100 – pacienti, u kterých bylo dosaženo kontroly onemocnění chemoterapií na bázi platiny v 1. linii a byli randomizováni do skupiny s avelumabem plus nejlepší podpůrnou péčí (best supportive care, BSC), dosáhli významného zlepšení OS oproti skupině s BSC samotnou (podle dat z roku 2023 činilo OS 23,8 měsíců vs. 15 měsíců) (graf 1).12,13 Jednalo se o první studii, která u tohoto onemocnění zlepšila OS, včetně léčby platinovými deriváty v 1. linii. „Strategie udržovací léčby se ukázala jako nejúspěšnější,“ uvedl přednášející.
Z analýzy studie JAVELIN Bladder navíc vyplývá, že podávání avelumabu pacientům nemá na organismus žádný negativní dopad. „Takže přidání látky, která zlepšuje přežití, nemá vliv na kvalitu života a bezpečnostní profil,“ vyzdvihl prof. Pinto. „Nepřidáváme žádnou významnou toxicitu a míra imunitních nežádoucích účinků je opravdu nízká, přičemž obvykle se jedná o nežádoucí účinky nízkého stupně.“
Z analýzy podskupin vyplynul přínos udržovací léčby avelumabem bez ohledu na věk, index tělesné hmotnosti (BMI), ale i bez ohledu na volbu předchozí CHT (cisplatina/karboplatina) a odpověď na CHT. „Pokud se jedná o stabilní onemocnění, částečnou odezvu nebo úplnou odezvu nacházíme ve všech těchto podskupinách.“
Jak správně zvolit léčbu 1. linie?
„Je dobré, že máme v 1. linii léčby různé možnosti, ale musíme si vybrat, neboť je to možná poslední linie, kterou pacient podstoupí,“ upozornil prof. Pinto. Připomněl, že sekvenční léčba u karcinomu močového měchýře (bladder cancer, BC) není tak úspěšná jako u karcinomu prostaty, protože pacienti se zhoršují s každou progresí, kterou zažívají.
V různých klinických studiích i studiích z reálné praxe přibližně 80 % pacientů dosáhne odpovědi, případně alespoň stabilizace onemocnění po CHT na bázi platiny – to značí jejich způsobilost k podání udržovací léčby avelumabem v 1. linii. Jelikož studie z reálné praxe mohou být zkreslené, například u BC naznačují nižší míru podávání systémové terapie v 1. linii, přednášející doporučil pohled do studií klinických, v nichž kontrolní skupinu tvořila CHT na bázi platiny.
Například přidání nivolumabu k CHT na bázi cisplatina–gemcitabin progresi onemocnění příliš nezmírnilo.14 Asi u 10 % pacientů dojde k progresi i přes CHT v 1. linii. To ukázala i studie EV‑302/KEYNOTE‑A39 s kombinací pembrolizumab + enfortumab vedotin.15 „Míra progrese onemocnění je většinou stejná, kolem 10 %, ať už podáváte pembrolizumab + enfortumab vedotin, nebo chemoterapii,“ upozornil prof. Pinto. Znamená to ale, že u 85–90 % pacientů dojde alespoň ke stabilizaci onemocnění, a proto budou kandidáty na udržovací léčbu avelumabem.
Podle dat publikovaných v rámci kongresu ESMO v roce 2024 pacienti s udržovací terapií avelumabem mohou dosáhnout dlouhodobé odpovědi. V prezentované studii zhruba 1 ze 3 pacientů užíval avelumab alespoň jeden rok a přibližně 1 z 5 pacientů minimálně dva roky.
Toxicita 1. linie léčby – překážka pro avelumab
Pozor je ovšem potřeba dát na nadměrnou toxicitu některých možností léčby, kvůli nimž pak nebude udržovací terapie avelumabem možná. Ve studii EV‑302/KEYNOTE‑A39 35 % pacientů trvale přerušilo léčbu touto kombinací pro nežádoucí účinky související s léčbou, a tudíž nebudou moci užívat následnou protinádorovou léčbu. Nejvíce znepokojující jsou podle přednášejícího kožní reakce a neuropatie – 15 % pacientů léčených kombinací pembrolizumab + enfortumab vedotin vykazuje kožní toxicitu stupně 3 nebo 4, která je navíc obtížně zvládnutelná, nepředvídatelná a často nevratná. U 42 % pacientů, kteří se potýkají s kožní reakcí vysokého stupně, nedojde k úplnému vymizení. Reziduální neuropatie přetrvává u 89 % pacientů, u kterých se vyskytla.
Prof. Pinto ujasnil, že je při volbě 1. linie léčby třeba u pacienta najít rovnováhu mezi komorbiditami, individualizací léčby a tím, co lze očekávat od její účinnosti i toxicity. Zdůraznil nutnost naslouchat pacientům, zejména v případě většinou nevyléčitelných pacientů s metastazujícím uroteliálním karcinomem.
„Nasloucháme našim pacientům, nebo jen volíme 1. linii léčby a říkáme ‚je to pro vás nejlepší, je to v pořádku´?“ otázal se řečnicky a navázal daty z klinické studie porovnávající preference onkologů versus pacientů na začátku 1. linie léčby mUC. Onkologové nejvíce oceňovali OS, ale pacienti léčebný plán a menší výskyt nežádoucích účinků.16 „Pokud chcete, aby si pacient vybral jednu možnost, víte, jak ho k tomu nasměrovat. Ale pacient musí být alespoň informován o různých možnostech léčby, o tom, co může očekávat z hlediska bezpečnosti a účinnosti, a pak se s ním musíme pokud možno dohodnout.“
Shrnul, že v 1. linii existují tři různé možnosti, přičemž v současné době neexistují údaje, která z nich je lepší, protože nebyly přímo porovnány. Léčba by tedy měla být individualizována na základě klinických faktorů, očekávané toxicity, komorbidit, preferencí pacienta a dostupnosti. „A na závěr bych rád citoval větu, která se mi velmi líbí: ‚Na každý složitý problém existuje jasná, jednoduchá a špatná odpověď.‘ Neexistuje jediná možnost pro všechny naše pacienty,“ uzavřel své vystoupení prof. Pinto.
Udržovací léčba v reálné praxi – čtyři studie včetně českých dat
 Důkazy z reálné praxe navázal doc. MUDr. Jindřich Kopecký, Ph.D., z Kliniky onkologie a radioterapie LF UK a FN Hradec Králové.17 Stejně jako jeho předřečníci připomněl, že UC zůstává onemocněním se špatnou prognózou. Pětileté přežití je horší než u renálního karcinomu nebo karcinomu prostaty.18 Moderní terapie inhibitory kontrolních bodů imunity (immune checkpoint inhibitors, ICI) a ADC ovšem přežití pacientů s UC přece jenom zlepšily. „Posledních deset let přineslo naději pro naše pacienty, ale stále nejsme tam, kde bychom chtěli být, a možná nikdy nebudeme. Ale každý krok, každé zlepšení je dobré,“ podotkl. Koncept udržovací terapie, tedy snaha o dlouhodobé udržení odpovědi méně toxickou léčbou známá z jiných onkologických diagnóz, je u UC nový. Stal se novým standardem, je ale otázka, jak se uplatňuje v praxi.
Důkazy z reálné praxe navázal doc. MUDr. Jindřich Kopecký, Ph.D., z Kliniky onkologie a radioterapie LF UK a FN Hradec Králové.17 Stejně jako jeho předřečníci připomněl, že UC zůstává onemocněním se špatnou prognózou. Pětileté přežití je horší než u renálního karcinomu nebo karcinomu prostaty.18 Moderní terapie inhibitory kontrolních bodů imunity (immune checkpoint inhibitors, ICI) a ADC ovšem přežití pacientů s UC přece jenom zlepšily. „Posledních deset let přineslo naději pro naše pacienty, ale stále nejsme tam, kde bychom chtěli být, a možná nikdy nebudeme. Ale každý krok, každé zlepšení je dobré,“ podotkl. Koncept udržovací terapie, tedy snaha o dlouhodobé udržení odpovědi méně toxickou léčbou známá z jiných onkologických diagnóz, je u UC nový. Stal se novým standardem, je ale otázka, jak se uplatňuje v praxi.
Při získávání důkazů jsou důležitá data z klinických studií i z reálné praxe, protože poskytují odlišné informace. V současné době jsou již k dispozici reálná data hovořící o prospěšnosti udržovací léčby avelumabem v 1. linii u BC. Po celém světě ji zatím užívalo a je řádně registrováno přes 5 000 pacientů s lokálně pokročilým UC nebo mUC, z toho v Evropě přes 2 000 (včetně 107 v České republice).
Přednášející se zaměřil na čtyři studie – AVENANCE (Francie), READY (Itálie), PATRIOT‑II (USA) a data z českého registru (CZECHREG) – a speciálně zmínil data ze svého pracoviště (FN HK).17,19–22 Kritéria zařazení a design se u nich podobají – účastníci museli dříve užívat CHT s určitou odpovědí, nebo alespoň stabilizací. Zdůraznil tři aspekty:
- Podíl cisplatiny vs. karboplatiny v CHT režimech: ve studii AVENANCE, největší z uvedené čtveřice, užívalo cisplatinu jen 28 %, ve studii READY 44,4 %, ve studii PATRIOT‑II 62,5 % a ve studii CZECHREG 51 % (přímo ve FN HK 71 %);
- Lokalizace UC: v klinických studiích je podle přednášejícího obvykle z 20–30 % zastoupen karcinom horních močových cest (upper tract urothelial carcinoma, UTUC) a 70–80 % připadá na BC, čemuž odpovídaly studie AVENANCE i READY, v datech z registru CZECHREG tyto údaje nejsou, přičemž ve FN HK byl podíl pacientů s UTUC vysoký (41 % vs. 59 %);
- Přítomnost viscerálních metastáz: ve studii JAVELIN Bladder se vyskytovaly u 50 % pacientů, v souladu s tím byl soubor pacientů FN HK (53 %), v AVENANCE i READY to ale bylo mnohem více (85 %, resp. 69,2 %).
„Je třeba mít to na paměti, když popisujete nebo chcete interpretovat data z reálné praxe, a nesrovnávat je mezi sebou,“ poznamenal přednášející.
I přes tyto rozdíly v klinických charakteristikách je ale medián po určité době od zahájení léčby avelumabem docela podobný, kolem dvou let, stejně jako v JAVELIN. Přežití bez progrese (progression‑free survival, PFS) je krátké a nejdelší medián PFS byl v České republice (11 měsíců v CZECHREG a 14 měsíců ve FN HK), jak se zamyslel přednášející „možná proto, že jsme měli méně pacientů s viscerálními metastázami“.
Roční OS v reálných údajích dosáhlo 67 % (AVENANCE) až 87 % (FN HK; v CZECHREG 79,3 %), dvouleté OS bylo shodně výrazně nižší – pouze polovina pacientů, kteří přežili první rok, přežije i druhý. Celkové přežití po jednom roce a medián OS jsou v souladu se studií JAVELIN Bladder.
Podle přednášejícího by bylo vysoce žádoucí, kdyby nějaký nástroj pomohl najít pacienty, kteří z avelumabu za dva roky nebudou mít prospěch. „Protože tito pacienti by možná byli kandidáty na jinou agresivnější léčbu. Nicméně byl bych rád, kdybychom takové údaje měli,“ doplnil.
Toxicita v reálném prostředí je podle něj podhodnocena.
Co po avelumabu aneb Je prostor ještě dál?
Data z reálné praxe mohou přinést informace o následné terapii, které „obvykle nezískáme z klinických studií, protože nejsou dostatečně statisticky silné nebo již neshromažďují data z následné terapie“, dodal přednášející. Takto jeho slovy „existují signály“, že po avelumabu je stále ještě prostor pro další linii léčby – ADC a enfortumab vedotin. Z post hoc analýzy studie AVENANCE vyplývá, že účinnost ADC není ovlivněna předchozí linií léčby. Medián OS činil 40,8 měsíce.23 Přednášející uvedl, že se jedná o retrospektivní studii a mnoho výsledků je zkreslených, i data z reálné praxe však podle něj ukazují, že další léčba po avelumabu je stále docela účinná, s trváním odpovědi obvykle kolem jednoho roku. Vyslovil souhlas s prof. Pintem, že „ani prodloužení přežití o jeden rok není špatné a všechno má svou cenu“.
Tristní přežití v České republice
Nakonec se doc. Kopecký věnoval problémům, s nimiž se léčba pacientů s UC potýká v České republice. Mortalita je vysoká (v roce 2022 činila incidence BC 2 352 osob, zemřelo na něj 935 pacientů), pětileté přežití se zvýšilo z 62 na 70 % a podle dat z Národního onkologického registru má Královéhradecký kraj nejhorší míru pětiletého přežití v ČR.24 Vysvětlení je podle přednášejícího několik. Vyzdvihl z nich fakt, že v tuzemsku vázne odesílání pacientů z jiných měst k léčbě do velkých center, kde mohou dostat plnou škálu možností inovativní terapie.
V Královéhradeckém kraji jsou kromě hradeckého komplexního centra čtyři onkologická pracoviště (Jičín, Trutnov, Náchod, Rychnov nad Kněžnou), která mohou poskytovat systémovou léčbu, ale nikoli inovativní. „Nejproblematičtější je dostupnost péče, zejména pro starší pacienty s komorbiditami, kteří nejsou schopni či neměli by po aplikaci onkologické léčby řídit, protože jim během chemoterapie podáváme léky, které mohou narušit jejich koncentraci,“ upozornil doc. Kopecký. Dostat se k nám veřejnou dopravou pak znamená mnoho hodin strávených pouze přesunem a čekáním na léčbu. „Taková je realita, a to nás trápí,“ dodal doc. Kopecký.
Situaci se snaží zlepšit odborníci z celého regionu – urologové, onkologové, kteří si rozdělili zodpovědnost pro předcházení zpoždění (provedení CT, chemoterapie, …). „Máme super inovativní léčbu, ale pokud se nedostane k pacientovi, nemá smysl takovou terapii mít,“ konstatoval přednášející. „Stále máme co zlepšovat a doufáme, že se zlepšíme.“
Závěrem podotkl, že „nejlepší léčbou metastazujícího onemocnění je samozřejmě prevence metastáz“, a vyjádřil naději, že „s novými terapiemi, pokud se pacient dostane do našeho centra, ji může dostat, a nevyvine se u něj metastatické onemocnění“.
Nové údaje z reálného světa v Chorvatsku
O poznatky z chorvatské praxe se podělil doc. dr. Jure Murgić z Klinički bolnički centar Sestre milosrdnice v Záhřebu.25
Do studie bylo zahrnuto 12 chorvatských center, z toho dvě v Záhřebu. V souladu s předchozími řečníky potvrdil, že onkologická péče je poskytována také v menších nemocnicích a vysvětlil, že za účelem analýzy reálných dat vznikla akademická skupina Uro‑Oncology Cooperative Group. Jedním z jejích projektů je slovy přednášejícího „určit výsledky léčby avelumabem v reálné praxi, zejména nyní, kdy je k dispozici velmi účinná terapie 2. linie, a představit klíčové klinické faktory pacientů“. V rámci kolokvia představil data ze 4. analýzy studie léčby avelumabem, shromážděná od července 2022 do března 2025.
Pacientů s UC ve zmíněných 12 centrech přibývá – 4. března 2025 se jednalo o 128 osob. Většina měla dobrý ECOG PS (0 u 64 %, 1 u 35 %), 72 % trpělo BC. Kuřáci představovali 63 %. S lokalizovaným UC se dříve léčilo 51 %. Téměř tři čtvrtiny (73 %) tvořili muži, medián věku činil 69 let, 39 % subjektů podstoupilo radikální operaci, pouze 9 % pacientů užívalo neoadjuvantní chemoterapii, metastázy v době diagnózy mělo 51 % (jen viscerální 37 %, jen v lymfatických uzlinách 27 %, jen v kostech 8 %, s těžkou metastatickou zátěží [≥ 3 lokality] bylo 17 %). Hodnotu CrCl ≥ 60 ml/min mělo 64 %. Jako režim CHT v 1. linii byl nejčastěji volen gemcitabin–cisplatina v 62 % (dále gemcitabin–karboplatina 26 %, ddMVAC 12 %).
Plánem bylo absolvovat čtyři cykly indukční CHT a u pacientů s odpovědí poté přejít na udržovací léčbu avelumabem – tyto čtyři cykly CHT podstoupila většina (72 %) pacientů. Z celkového počtu pacientů, kteří měli kontrolu onemocnění, bylo u 5 % dosaženo úplné odpovědi, 58 % částečné odpovědi a stabilizace onemocnění dosáhlo 36 % pacientů. Medián doby od ukončení CHT do podání avelumabu činil 6 týdnů (rozmezí 2–14). U 41 % (52 ze 128) osob bylo k dispozici komplexní genomové profilování primárního nádoru, analýza mutačního statusu genů a klinických odpovědí na avelumab probíhá a slovy přednášejícího bude představena na dalších konferencích.
Medián doby sledování činil 19 měsíců (15–40), medián doby trvání léčby avelumabem 7 měsíců (0–30), v době konání kolokvia léčbu užívalo 42 %, k přerušení terapie došlo u 57 % (73 osob – 65 z důvodu progrese, 8 pro nežádoucí účinky). Pouze u 5 % nebylo možné provést radiologické vyšetření.
Celková míra odezvy na avelumab (úplná odpověď + částečná odpověď) dosáhla 14 %. Klinický přínos nebo kontrola onemocnění byly zjištěny u 53 % pacientů.
„Pozorovali jsme poměrně velký počet pacientů s výjimečnou odpovědí na avelumab s délkou léčby více než dva roky,“ uvedl přednášející. Medián PFS od podání avelumabu činil 14 měsíců, 12měsíčního PFS dosáhlo 51 %, vyskytlo se 68 případů progrese. Medián OS od podání avelumabu byl 26 měsíců, 12měsíčního OS docílilo 70 %, 45 pacientů zemřelo. Medián PFS od zahájení CHT činil 22 měsíců, 12měsíčního PFS dosáhlo 60 % a medián OS činil 49 měsíců (12měsíční OS 80 %, 24měsíční OS 56 %, 36měsíční OS 52 %). „Myslím, že to ukazuje určitý druh předběžného výběru pacientů, kteří jsou schopni dostat se do našich center, aby podstoupili léčbu. Věříme totiž, že alespoň 30 % pacientů s metastázami by mělo být léčeno chemoterapií a většina z nich by přešla na udržovací léčbu avelumabem,“ uvedl přednášející.
Imunitní nežádoucí účinky související s podáváním avelumabu se vyskytly u 23 %, většinou stupně 2 (nežádoucí účinky související s léčbou stupně 3 tvořily 6 %, stupně 4 pak 2 %), nejčastější se objevily hypotyreóza, trombocytopenie, kolitida, nejhorší byl syndrom podobný myastenii stupně 4 u jednoho pacienta a jaterní toxicita stupně 3 u 2 pacientů. Osm procent pacientů léčbu trvale přerušilo kvůli nežádoucím účinkům.
Po progresi při léčbě avelumabem 41 % (27 z 65 pacientů) podstoupilo další aktivní léčbu:
15 pacientů užívalo enfortumab vedotin, tři pacienti pemigatinib, dva pacienti trastuzumab deruxtecan (TDx) a sedm pacientů paliativní CHT taxany. „Léčba pemigatinibem a TDx byla založena na našem speciálním programu Gratia, který byl zahájen před pěti lety a v rámci kterého můžeme podávat léky schválené European Medicines Agency (EMA) na základě komplexního profilování genomu,“ upřesnil přednášející.
V souboru 15 pacientů, kteří užívali v 2. linii enfortumab vedotin, nebyl dosud dosažen medián PFS ani OS, vyskytly se čtyři progrese onemocnění a tři pacienti zemřeli.
Přednášející uvedl příklad pacienta, u kterého bylo provedeno komplexní genomové profilování, které zjistilo vysokou nádorovou mutační nálož (19 mut/Mb), což může vysvětlit, proč je nyní dva roky při užívání avelumabu s úplnou odpovědí. „Tento pacient má amplifikaci ERBB2, což ho kvalifikuje pro terapii zaměřenou v další linii léčby na HER2, pravděpodobně po enfortumab vedotinu,“ doplnil přednášející.
Shrnul, že OS ve studii bylo podle jeho názoru srovnatelné s jinými studiemi z reálné praxe. Vysoký podíl pacientů vhodných pro cisplatinu naznačuje určitý výběr pacientů. „Celkové přežití je tedy velmi dlouhé, medián OS nebyl dosažen, pokud pacienti užívali enfortumab vedotin. Tyto údaje však nejsou zralé,“ upozornil.
Nakonec vyzval k provádění komplexního genomového profilování, neboť na jeho základě se řadě pacientů otevírají i po avelumabu další možné linie léčby (většinou cílené na lidský receptor 2 epidermálního růstového faktoru [human epidermal growth factor receptor 2, HER2] či na receptor růstového faktoru fibroblastů [fibroblast growth factor receptor, FGFR]).
Sekvenční léčba u karcinomu močového měchýře
Klíčová pro maximalizaci OS při zachování kvality života u UC je sekvenční léčba, která je již u této diagnózy také možná. „V minulosti to tak nebylo, protože jsme měli jako účinnou možnost pouze chemoterapii na bázi platiny. Takže vše, co jsme měli k dispozici, jsme použili jako 1. linii,“ uvedl doc. Jakub Kucharz, MD, PhD, z Narodowy Instytut Onkologii im. Marii Skłodowskiej‑Curie v Polsku.26 „Údaje potvrzují účinnost sekvenční léčby v rutinní klinické praxi, ale je třeba vybrat správného pacienta pro správný přístup, resp. správný přístup pro správného pacienta. A personalizovaná léčba zohledňující prognostické faktory, profil toxicity a preference pacienta je základním pilířem optimální léčby,“ konstatoval. Svou přednášku zaměřil právě na sekvenování léčby.
Předeslal, že pro správnou volbu sekvenční terapie je důležitá biologie nádoru. U pacientů s metastazujícími nádory, malignitami s velmi agresivním chováním a rychlým průběhem však není dobré o ní uvažovat. Pacient musí být v dobrém celkovém stavu s dobrým ECOG PS a s adekvátní funkcí orgánů. Mezi výhody sekvenční léčby obecně patří maximalizace OS, protože účinek několika účinných látek podávaných v průběhu času se kumuluje (viz např. u kolorektálního karcinomu, renálního karcinomu či karcinomu prsu). Mezi další výhody patří lepší snášenlivost, protože v rámci sekvencí se používají méně intenzivní režimy, i lepší prostor pro personalizaci léčby, protože přístup se přizpůsobuje reakci, toxicitě a klinickému scénáři, a dále nižší toxicita. Pokyny Polské společnosti klinické onkologie podle přednášejícího kladou důraz na klinickou stránku – první rozhodnutí o léčbě metastatického onemocnění by mělo být založeno na kontraindikacích, preferencích pacienta minimalizovat toxicitu nebo maximalizovat výsledek, na symptomech, přítomnosti jaterních metastáz, potřebě rychlé léčebné odpovědi aj.27
Možnosti v 1. linii léčby
V 1. linii mUC se uplatňuje CHT na bázi platiny. U pacientů nevhodných pro cisplatinu se volí karboplatina. „Známe data, víme, že cisplatina se zdá být o něco účinnější a obecně se upřednostňuje, a opravdu se mi líbí režimy rozdělených dávek, protože nám umožňují použít cisplatinu,“ uvedl doc. Kucharz. V udržovací léčbě se zahajuje imunoterapie po dosažení kontroly onemocnění chemoterapií a současný standard tvoří podle studie JAVELIN Bladder 100 avelumab u pacientů vhodných i nevhodných pro cisplatinu. „Podle mého názoru je nesmírně důležité, jak zmínil docent Kopecký, že pracujeme s daty, která nám poskytují jistotu výsledků,“ uvedl s připomenutím studií JAVELIN Bladder i AVENANCE.
Různé kombinace CHT + imunoterapie v 1. linii v různých studiích neměly jednotné výsledky v ukazatelích PFS a OS – některé vyšly pozitivně, jiné negativně. Ve studii IMvigor130 se ukázala role cisplatiny – u pacientů, kterým byla podána karboplatina, neměl atezolizumab přínos, zatímco ve skupině s cisplatinou se projevily některé signály účinnosti.28 Naopak ve studii CheckMate 901, kde v rameni s kombinací CHT založené na platině + nivolumab nebyla karboplatina, vyšly pozitivně PFS i OS.29
„Kdybychom od samého začátku pozorovali synergii mezi chemoterapií a ICI, měli bychom méně pacientů s progresivním onemocněním jako první reakcí,“ doplnil.
Kombinace ADC + imunoterapie, konkrétně pembrolizumab + enfortumab vedotin, byla úspěšná ve studii EV‑302/KEYNOTE‑A39 – pacienti po celou dobu studie užívali enfortumab vedotin a maximálně dva roky pembrolizumab.30 Mediány PFS i OS byly v rameni léčeném touto kombinací téměř dvojnásobné než v rameni se samotnou CHT. Do PFS se podle přednášejícího promítlo podávání enfortumab vedotinu až do progrese, do OS zase skutečnost, že v rameni se samotnou CHT pouze 30 % nemocných užívalo udržovací léčbu. Další možnost léčby po kombinaci pembrolizumab + enfortumab vedotin může změnit případná periferní neuropatie.
Co o kombinaci pembrolizumab + enfortumab vedotin říkají data z reálné praxe? Přednášející upozornil na studii z Mayo Clinic, které se účastnilo 120 pacientů (98 s mUC, 22 s lokálně pokročilým UC), v níž pacienti dosáhli stejné odpovědi i PFS jako ve studii EV‑302/KEYNOTE‑A39, ale krátkého OS (25 měsíců). „Pokud se podíváte na koncept sekvenční léčby a celkové přežití je tak nízké, znamená to, že po progresi se něco děje,“ upozornil doc. Kucharz. „Domnívám se, že to může být špatný celkový stav nebo absence účinné látky, kterou lze použít. Zdá se tedy, že 2. linie léčby u těchto pacientů není účinná, nebo nejsou v dostatečně dobré kondici, aby mohli podstoupit další léčbu,“ dodal s poznámkou, že studie sice byla malá, ale spodní hranice intervalu spolehlivosti (confidence interval, CI) byla o 10 měsíců kratší než ve studii EV‑302/KEYNOTE‑A39.
Co dělat po selhání 1. linie léčby?
Pokud u pacienta, který dosud neužíval imunoterapii, selže CHT, použije se imunoterapie (podle studie z roku 2017 pembrolizumab).31
Selže‑li CHT + imunoterapie, lze podle studie EV‑301 použít enfortumab vedotin. „A víme, že je to vysoce účinný postup se 40% mírou odezvy u pacientů, kteří již podstoupili intenzivní léčbu,“ poznamenal přednášející. V reálné praxi ukázala databáze UNITE u pacientů, kteří užívali udržovací léčbu, stejné výsledky jako ve studii EV‑301.
Jak postupovat u mutace FGFR
Pro pacienty s mutací FGFR platí úhrada erdafitinibu, jenž se osvědčil ve studii THOR.32 Představuje u nich možnou 3. linii léčby. Přednášející ho označil za velmi dobrou možnost, u níž je ale potřeba mít na paměti specifickou toxicitu, zejména oční.
Enfortumab vedotin a erdafitinib je podle analýzy lepší podávat v sekvenci, přičemž nebylo zřejmé, který z nich by měl být zvolen jako první.33
Po dočasné progresi při užívání enfortumab vedotinu je podle odborných názorů prostor pro pokračování v CHT.
Studie kombinované terapie u UC:
co je nového?
Z pacientů s nově diagnostikovaným pokročilým nebo metastazujícím UC se k 1. linii léčby dostane jen 48 % pacientů a do každé další linie postoupí opět jen necelá polovina pacientů. „A proto se musíme zaměřit především na 1. linii, protože šanci se do ní dostat má nejvíce pacientů,“ konstatoval prof. Dr. med. Friedemann Zengerling z Universitätsklinikums Ulm.34 Ve své přednášce se zaměřil na nová data o kombinacích zavedených léků.
Imunoterapie + imunoterapie
Boj ICI s nádory podle přednášejícího připomíná Davida s Goliášem. Na imunoterapii v monoterapii odpovídá ne více než 30 % pacientů. Možnosti imunoterapie se často kombinují do duální inhibice kontrolních bodů imunity. Podle přednášejícího tudy cesta ke zlepšení výsledků pacientů s UC nepovede. Zmínil přitom nejvýznamnější studie pro kombinaci nivolumab + ipilimumab.30,35 Neosvědčila se ani kombinace pembrolizumab + epacadostat (molekula, která obnovuje vyšší reaktivitu T lymfocytů), při jejíž užívání nebyl zaznamenán žádný rozdíl; účinky vyvolával pouze pembrolizumab. Tento koncept byl tedy opuštěn, a i když se jednalo o rozsáhlou studii fáze III, byla předčasně ukončena.
Imunoterapie + inhibitor FGFR
Ve studii fáze II byla u pacientů s FGFR pozitivitou zkoumána kombinace erdafitinibu s protilátkou anti‑PD‑1 cetrelimabem. Průběžná analýza přinášela povzbudivá data, kdy celková četnost odpovědí činila 68 %, tj. více než dvojnásobek oproti monoterapii erdafitinibem, ale v pozdější analýze prezentované v abstraktu na kongresu už výsledky nebyly tak výrazné, rozdíl činil pouze 10 %. „Tato kombinace má podle mě také slibné výsledky, ale nestojí za to se jí dále zabývat,“ konstatoval přednášející.
Imunoterapie + chemoterapie
Co se týče kombinace imunoterapie + CHT, máme dnes k dispozici dva schválené režimy, a to nivolumab + CHT podle studie CheckMate 901 a pro léčbu svalovinu invadujícího karcinomu močového měchýře (muscle‑invasive bladder cancer, MIBC) nově durvalumab + CHT podle studie NIAGARA. V tomto případě přednášející uvedl, že účinky imunoterapie + CHT jsou omezené, ale zejména spolu s cisplatinou funguje kombinace docela dobře.
Imunoterapie + ADC
Budoucnost ovšem přednášející spatřuje spíše v kombinaci imunoterapie + ADC. Mechanismy se podobají kombinaci CHT + imunoterapie, fragment Fc v molekule protilátky má ale specifické imunitní účinky – aktivizuje imunitní buňky, což by mohl být rozdíl oproti CHT. Mezi ADC a ICI také existuje synergie, což umožňuje hlubší odpověď a vytvoření systémové imunitní paměti. Dobrou reakci pacientů prokázala studie EV‑302/KEYNOTE‑A39 (pembrolizumab + enfortumab vedotin). Celkové přežití při užívání kombinace pembrolizumab + enfortumab vedotin bylo významně lepší než při CHT, přičemž dlouhodobého OS dosáhlo o 20 % více osob.
Zkoumány jsou i další ADC. Zajímavě se jeví kombinace disitamab vedotin + ICI – s pembrolizumabem i toripalimabem je celková četnost odpovědí 75 %, OS u kombinace disitamab vedotin + toripalimab 33 měsíců, u kombinace disitamab vedotin + pembrolizumab zatím nebylo dosaženo mediánu OS.
Sacituzumab govitekan byl testován v kombinaci s avelumabem jako udržovací léčba ve studii JAVELIN Bladder Medley, která navazovala na JAVELIN Bladder 100.36 Ukázalo se, že kombinace sacituzumab govitekan + avelumab prodloužila PFS oproti monoterapii avelumabem (12 vs. 3 měsíce). „Přidání sacituzumab govitekanu tedy činí udržovací léčbu v 1. linii ještě atraktivnější,“ poznamenal přednášející. Údaje o OS jsou numericky lepší, ale nejsou ještě zralé, medián OS ještě nebyl dosažen. Významně lepší byla i objektivní míra odpovědi (24,3 vs 2,7 %). Problémem sacituzumab govitekanu je toxicita, což činí tento přístup méně atraktivním kvůli nežádoucím účinkům souvisejícím s léčbou. „Účinek avelumabu byl tedy potvrzen. Kombinace má dobré PFS. Myslím, že musíme počkat na OS, aby se tato terapie stala pro nás skutečně možností,“ podělil se o svůj názor přednášející.
Lze jít ještě dál?
V současnosti probíhá také výzkum trojkombinací. Neosvědčila se ADC (sacituzumab govitekan) + ICI (nivolumab) + ICI (ipilimumab) – tento režim byl velmi toxický a studie musela být ukončena. Nábor aktuálně probíhá do čtyř studií, které mají testovat ADC (enfortumab vedotin) + ADC (sacituzumab govitekan nebo sacituzumab tirumotekan nebo datopotamab deruxtekan) + ICI (pembrolizumab nebo zimberelimab).
Pokračují studie fáze III VOLGA, KEYNOTE 905/EV‑303 a KEYNOTE‑B15/EV‑304 zaměřené na léčbu MIBC. U svalovinu neinvadujícího BC (NMIBC) se hodnotí ve studiích fáze I až II kombinace ADC + imunoterapie či například ADC + BCG (Bacillus Calmette–Guérin), intravezikální podávání sacituzumabu tirumotekanu a další možnosti.
„Myslím, že se objevuje mnoho slibných režimů,“ uvedl přednášející. Dodal, že je zapotřebí lépe vybírat pacienty a v neposlední řadě přenést aktualizace pokynů do klinické praxe.
Klíčové body
- Epidemiologie mUC: incidence UC v EU/ČR roste při relativně stabilní mortalitě; typický věk kolem 70 let znamená vysoký podíl křehkých pacientů a nutnost pragmatické stratifikace již v 1. linii.
- Způsobilost k užívání platiny jako klíčové rozhodovací kritérium: v praxi se používají zejména kritéria Galského vs. Guptové; problematická zůstává „šedá zóna“ CrCl 40–60 ml/min a ototoxicita, rozhodnutí má vždy reflektovat cíl léčby a preference pacienta.
- Cisplatina vs. karboplatina v éře imunoterapie a ADC: část dat naznačuje srovnatelné výsledky, klinická zkušenost však často favorizuje cisplatinu; zásadní je prevence nefrotoxicity (hydratace, korekce Mg) a individualizace dávkování.
- Pembrolizumab + enfortumab vedotin a kritéria EVITA: existují zatím nevalidovaná kritéria „EV‑ineligible“, která jsou v českém prostředí vnímána jako orientační pomůcka, nikoli rigidní selekce.
- Udržovací léčba avelumabem po 1. linii platinové CHT je standardem s prodloužením OS: studie JAVELIN Bladder 100 prokázala prodloužení OS po dosažení kontroly onemocnění při nízké imunitně zprostředkované toxicitě a bez zhoršení kvality života; přínos byl napříč podskupinami včetně režimu s cisplatinou i karboplatinou.
- Volba 1. linie musí zachovat možnost udržovací léčby: nadměrná toxicita může znemožnit navázání léčbou avelumabem; u kombinace pembrolizumab + enfortumab vedotin je nutné počítat s vyšším podílem přerušení léčby pro kožní toxicitu a periferní neuropatii.
- Reálná praxe potvrzuje účinnost avelumabu, ale registry (AVENANCE, READY, PATRIOT‑II, CZECHREG) jsou klinicky nehomogenní, což limituje přímé srovnávání; výsledky jsou však konzistentní se studií JAVELIN Bladder 100.
- Po ukončení udržovací léčby avelumabem existuje prostor pro další systémovou terapii: u pacientů s progresí onemocnění se uplatní ADC (enfortumab vedotin) nebo cílená léčba při přítomnosti mutace FGFR; klíčové je plánování sekvence léčby a zachování kvality života.
- Systémové limity: dostupnost inovativní léčby závisí na dosažitelnosti center, přičemž logistika regionální péče může významně ovlivnit reálné přežití.
- Největší potenciál ve výzkumu mají kombinace imunoterapie + ADC (včetně intenzifikace udržovací léčby) a výběr pacientů pomocí komplexního genomového profilování (HER2, FGFR3).
Literatura
[1] Poprach A. Eligibility criteria for patients with urothelial tumors. Bladder Cancer Master Class, Brno, 24.–26. 9. 2025.
[2] Powles T, Bellmunt J, Comperat E, et al. Bladder cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow‑up. Ann Oncol 2022; 33: 244–258.
[3] Powles T, Bellmunt J, Comperat E, et al., et al. ESMO Clinical Practice Guideline interim update on first‑line therapy in advanced urothelial carcinoma. Ann Oncol 2024.
[4] Gupta S. Defining platinum‑ineligible patients with metastatic urothelial cancer (mUC). ASCO Annual Meeting 2022.
[5] Galsky MD. Defining cisplatin‑ineligible patients with metastatic bladder cancer. ASCO Annual Meeting 2011.
[6] Jiang Y, Wang J, Li Y, et al. Natural products: Potential treatments for cisplatin‑induced nephrotoxicity. Acta Pharmacol Sin 2021; 42: 1951–1969.
[7] Dillard LK, McMahon CM, Austin DF, et al. Global burden of ototoxic hearing loss associated with platinum‑based cancer treatment: A systematic review and meta‑analysis. Cancer Epidemiol 2022; 79: 102203.
[8] Mori K, Pradere B, Quhal F, et al. Reassessment of the efficacy of carboplatin for metastatic urothelial carcinoma in the era of immunotherapy: A systematic review and meta‑analysis. Eur Urol Focus 2022; 8: 1687–1695.
[9] Galsky MD, Stensland KD, Sfakianos JP, et al. Immunomodulatory effects and improved outcomes with cisplatin‑ versus carboplatin‑based chemotherapy plus atezolizumab in urothelial cancer. Cell Rep Med 2024; 5: 101393.
[10] Grande E, Pérez‑Valderrama B, Gupta S, et al. Re: Powles T, Pérez‑Valderrama B, Gupta S, et al. Enfortumab vedotin and pembrolizumab in untreated advanced urothelial cancer. Letter to the editor. N Engl J Med 2024; 390: 875–888.
[11] Pinto Á. The role of maintenance in the treatment of metastatic urothelial cancer. Bladder Cancer Master Class, Brno, 24.–26. 9. 2025.
[12] Powles T, Park SH, Voog E, et al. Avelumab maintenance therapy for advanced or metastatic urothelial carcinoma. N Engl J Med 2020; 383: 1218–1230.
[13] Powles T, Park SH, Voog E, et al. Avelumab first‑line maintenance for advanced urothelial carcinoma: Results from the JAVELIN Bladder 100 trial after ≥ 2 years of follow‑up. J Clin Oncol 2023; 41: 3486–3492.
[14] van der Heijden M, Loriot Y, Durán I, et al. Nivolumab plus gemcitabine–cisplatin in advanced urothelial carcinoma. N Engl J Med 2023; 389: 1778–1789.
[15] Powles T, Rosenberg JE, Sonpavde GP, et al. Enfortumab vedotin and pembrolizumab in untreated advanced urothelial cancer. N Engl J Med 2024; 390: 875–888.
[16] Grivas P, Monk BJ, Petrylak DP, et al. Preferences for first‑line treatment of advanced urothelial carcinoma among US practicing oncologists and patients. Future Oncol 2023; 19: 369–383.
[17] Kopecký J. Summary of real‑world evidence in urothelial carcinoma treatment with maintenance strategies: How the standard of care has evolved. Bladder Cancer Master Class, Brno, 24.–26. 9. 2025.
[18] ÚZIS ČR. Novotvary 2019–2021 v ČR. Dostupné z: https://www.uzis.cz/res/f/008447/novotvary2019‑2021.pdf [cit. 7. 1. 2025].
[19] Barthelemy P, Loriot Y, Massard C, et al. Full analysis from AVENANCE: A real‑world study of avelumab first‑line maintenance treatment in patients with advanced urothelial carcinoma. J Clin Oncol 2023; 41: 471.
[20] Antonuzzo L, Galli L, Fontana A, et al. READY: Real‑world data from an Italian compassionate use program of avelumab first‑line maintenance treatment for locally advanced or metastatic urothelial carcinoma. J Clin Oncol 2023; 41: 469.
[21] Grivas P, Plimack ER, Bilen MA, et al. Avelumab first‑line maintenance for locally advanced or metastatic urothelial carcinoma: Results from the real‑world US PATRIOT‑II study. Clin Genitourin Cancer 2024; 22: 102238.
[22] Zemánková A, Kopecký J, Poprach A, et al. Avelumab first‑line maintenance in patients with locally advanced or metastatic urothelial carcinoma in the Czech Republic: Interim real‑world results from a national reimbursement registry. J Clin Oncol 2024; 42: 557.
[23] Barthélémy P, Loriot Y, Massard C, et al. Real‑world study of avelumab first‑line maintenance treatment in patients with advanced urothelial carcinoma in France: Results from the AVENANCE study. Eur Urol Oncol 2025; 8: 407–416.
[24] Národní onkologický registr, ÚZIS ČR. Analýza periody 2020–2022.
[25] Murgić J. Avelumab as maintenance therapy in advanced urothelial carcinoma – new real‑world data from Croatia. Bladder Cancer Master Class, Brno, 24.–26. 9. 2025.
[26] Kucharz J. Sequence treatments: Current approaches in bladder cancer. Bladder Cancer Master Class, Brno, 24.–26. 9. 2025.
[27] Wysocki PJ, Rutkowski P, Krzakowski M, et al. Optimization of systemic treatment in patients with bladder, ureter and renal pelvis cancer – expert opinion of the Polish Society of Clinical Oncology. Oncol Clin Pract 2025; 21: 177–192.
[28] Bamias A, van der Heijden MS, Necchi A, et al. Atezolizumab monotherapy versus chemotherapy in untreated locally advanced or metastatic urothelial carcinoma (IMvigor130): Final overall survival analysis. Lancet Oncol 2024; 25: 46–61.
[29] van der Heijden M, Galsky MD, Retz M, et al. Nivolumab plus ipilimumab versus gemcitabine–carboplatin in cisplatin‑ineligible patients with metastatic urothelial carcinoma: Final results of CheckMate 901. ASCO Annual Meeting 2025, abstr. 4500.
[30] Powles T, Rosenberg JE, Sonpavde GP, et al. EV‑302/KEYNOTE‑A39: Enfortumab vedotin plus pembrolizumab versus chemotherapy in untreated locally advanced or metastatic urothelial carcinoma. Ann Oncol 2023; 34 (Suppl): S1340.
[31] Bellmunt J, de Wit R, Vaughn DJ, et al. Pembrolizumab as second‑line therapy for advanced urothelial carcinoma. N Engl J Med 2017; 376: 1015–1026.
[32] Loriot Y, Necchi A, Park SH, et al. Phase III THOR study: Erdafitinib versus chemotherapy in patients with FGFR‑altered advanced urothelial carcinoma. J Clin Oncol 2023; 41: LBA4619.
[33] Jiang CY, Lee JL, Li CC, et al. Sequencing of erdafitinib and enfortumab vedotin in FGFR2/3‑altered advanced urothelial carcinoma: UNITE database analysis. J Clin Oncol 2024; 42 (Suppl): 616.
[34] Zengerling F. New combination studies in urothelial cancer. Bladder Cancer Master Class, Brno, 24.–26. 9. 2025.
[35] Sharma P, Retz M, Siefker‑Radtke A, et al. Nivolumab alone or in combination with ipilimumab in platinum‑pretreated metastatic urothelial carcinoma: Extended follow‑up from CheckMate 032. Ann Oncol 2024; 31 (Suppl): S582–S583.
[36] Hoffmann‑Censits J, Grivas P, Petrylak DP, et al. Avelumab plus sacituzumab govitecan versus avelumab monotherapy as first‑line maintenance treatment in advanced urothelial carcinoma: JAVELIN Bladder Medley interim analysis. Ann Oncol 2025; 36: 1088–1095.