Boj proti infekci virem HIV – současný stav klinického testování mikrobicidních přípravků
Rostoucí počet infekcí virem HIV a onemocnění AIDS se stal v posledních letech hrozbou pro celý svět. Doposud nebyla vyvinuta účinná
terapie a světový boj proti HIV/AIDS stojí na třech základních pilířích: použití kondomů, vyvinutí vakcíny a vyvinutí účinných mikro-
bicidů – látek, které se lokálně aplikují na vaginální nebo rektální sliznici a zabraňují přenosu viru HIV. Do přípravků s obsahem mikrobicidů
byla vkládána velká naděje. Cílovou skupinou měly být zejména ženy zemí třetího světa, které by aplikací tohoto přípravku mohly samy rozhodovat o své ochraně a nepotřebovaly by tak souhlas partnera. Tento příspěvek se zabývá rozdělením mikrobicidních přípravků do tří základních skupin a shrnuje jejich jednotlivé zástupce. Hlavní část je věnována hodnocení současného stavu vývoje a klinického testování mikrobicidů a posouzení úspěšnosti této strategie.
Úvod
Virus HIV, způsobující onemocnění AIDS, se stal v posledních letech hrozbou pro celý svět. Údaje o počtu nakažených jsou alarmující. V roce 2009 označila Světová zdravotnická organizace (WHO) AIDS za celosvětově nejčastější onemocnění a příčinu úmrtí žen v reprodukčním věku. V roce 2011 bylo evidováno 34 milionů HIV-pozitivních jedinců, z toho v Evropě bylo odhadováno 2,3 milionu HIV-pozitivních – 1,4 milionu takto postižených žilo ve východní Evropě. Toto číslo bylo v porovnání s rokem 2000 trojnásobné [1]. Nepříznivá je i situace v České republice. V roce 2010 bylo diagnostikováno 180 nových případů infekce virem HIV. Tento rekordní nárůst byl největší od roku 1986, kdy se výskyt onemocnění začal monitorovat [2, 3].
Rok 2011 byl o něco příznivější. Celkem přibylo 141 nově infikovaných jedinců. Podle tajemníka České společnosti AIDS však nižší počet diagnostikovaných případů pravděpodobně nesouvisí s tím, že by se podařilo snížit šíření infekce, ale je způsoben poklesem množství provedených testů na HIV. Asi 60 % nakažených tvoří homosexuálové/bisexuálové. ![Graf 1 Počet infikovaných osob, dospělých a žen v letech 1990–2011; podle [4] – UNAIDS Report on the Global AIDS Epidemic, 2012.](https://www.remedia.cz/photo-a-29385---.jpg)
V celosvětovém měřítku ze všech nakažených lidí (34 milionů HIV-pozitivních) tvořili dospělí 30,7 milionu, z nich 16,7 milionu byly ženy (graf 1) [4]. Zbylé 3,3 milionu infikovaných představovaly děti mladší 15 let. V roce 2011 bylo evidováno 2,5 milionu nově infikovaných jedinců (graf 2), z toho 2,2 milionu byli dospělí, tedy 7000 nových infekcí den![Graf 2 Počet zemřelých a nově infikovaných osob v letech 1990–2011; podle [4] – UNAIDS Report on the Global AIDS Epidemic, 2012.](https://www.remedia.cz/photo-a-29386---.jpg) ně. Na onemocnění AIDS zemřelo v roce 2011 asi 1,7 milionu lidí, z toho 1,5 milionu dospělých [5].
ně. Na onemocnění AIDS zemřelo v roce 2011 asi 1,7 milionu lidí, z toho 1,5 milionu dospělých [5].
Doposud stále neexistuje účinná vakcína proti HIV/AIDS, i když se mnoho kandidátů nachází ve fázi výzkumu nebo klinického testování. Vzhledem k tomu, že žádná virová epidemie nebyla zastavena bez očkování, je vývoj účinné vakcíny největší nadějí, jak šíření smrtelného onemocnění zabránit [6–8].
Světový boj proti HIV/AIDS stojí na třech základních pilířích, a to na používání ochranných prostředků před zahájením pohlavního styku (mužský a ženský kondom), na vývoji selektivní vakcíny a na vyvinutí účinných mikrobicidů. Ty představují různorodou skupinu látek, které se aplikují lokálně před pohlavním stykem na vaginální sliznici a chrání před nákazou virem HIV a jinými sexuálně přenosnými chorobami [9, 10]. Původně byly mikrobicidy zamýšleny k ochraně proti širokému spektru pohlavně přenosných chorob [11]. Myšlenka začít je používat proti přenosu viru HIV se objevila přibližně před dvaceti lety, intenzivní klinický výzkum mikrobicidů začal teprve před deseti lety [12]. Novější profylaxi představuje preventivní podávání antiretrovirotik.
Do přípravků s obsahem mikrobicidů byla vkládána velká naděje. Cílovou skupinou měly být zejména ženy zemí třetího světa, které by aplikací těchto přípravků mohly samy rozhodovat o své ochraně a nepotřebovaly by tak souhlas partnera.
Tento příspěvek je věnován hodnocení současného stavu vývoje a klinického testování mikrobicidů a posouzení úspěšnosti této strategie.
Rozdělení mikrobicidů a jejich zástupci
Mikrobicidy vykazují různou míru specifity a na základě této skutečnosti se rozdělují do tří hlavních skupin. Nespecifické a částečně specifické mikrobicidy jsou účinné proti širšímu spektru sexuálně přenosných chorob, často působí také spermicidně [13]. Patří do skupiny mikrobicidů první generace [14]. Specifické mikrobicidy naopak působí výhradně proti viru HIV [13]. Jedná se o mikrobicidy druhé generace [14].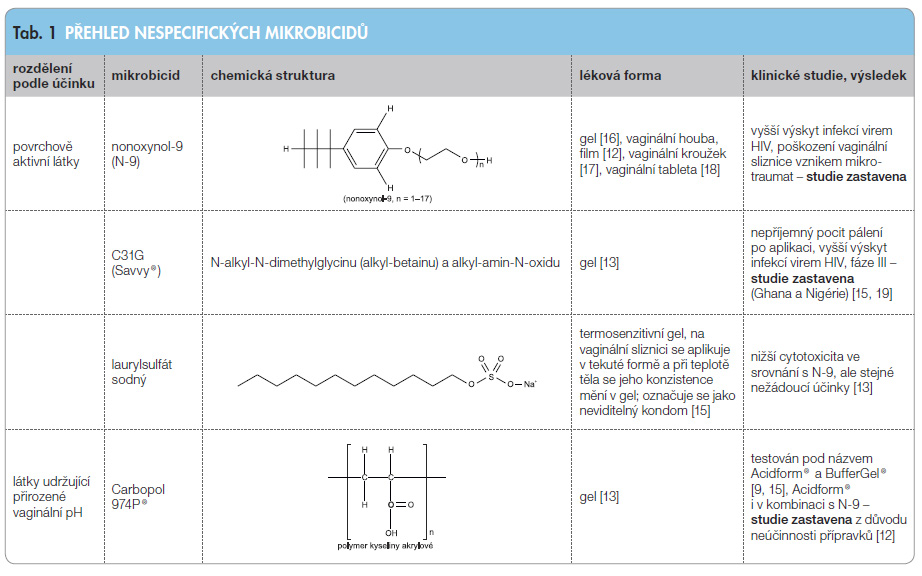
Výhodou mikrobicidů první generace je nízká cena, širokospektrá aktivita, omezená systémová absorpce a schopnost některých mikrobicidů působit kontracepčně. Nevýhodou je závislost na pohlavním styku, snížená nebo chybějící aktivita proti virům využívajícím koreceptor CCR5 a dále těžko odhadnutelná lokalizace mikrobicidu [14].
U mikrobic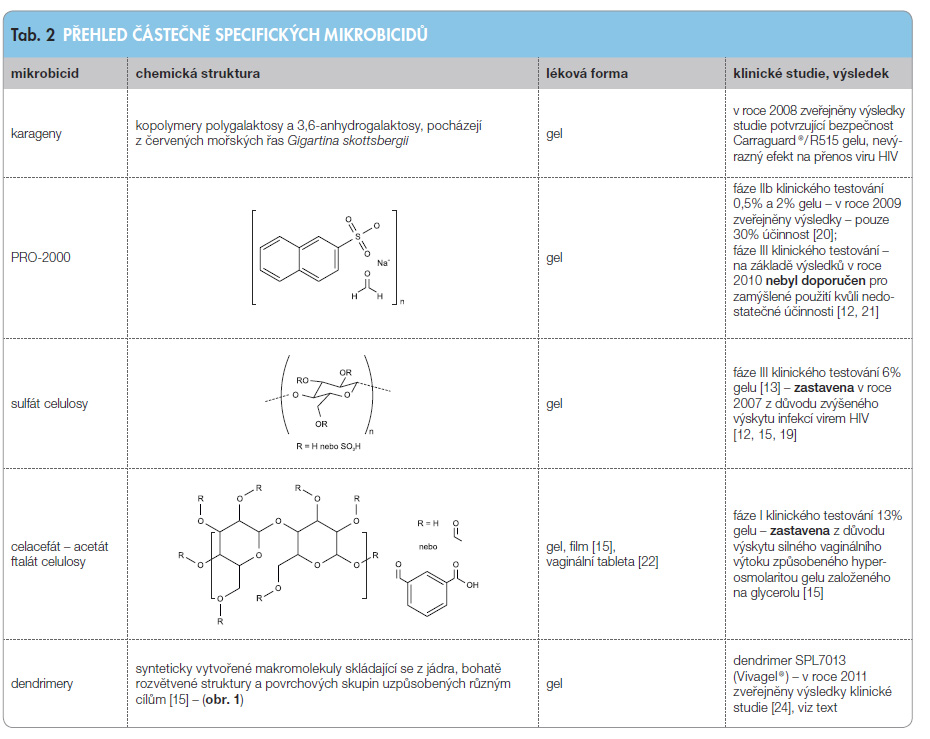 idů druhé generace patří mezi výhody vysoká specifita, bezpečnost, účinnost (zpravidla již zdokumentovaná při použití v jiné formě aplikace) a možnost využití lékové formy poskytující dlouhodobou ochranu (vaginální kroužky, mukoadhezivní gely). Nevýhodou je riziko vzniku rezistence a neúčinnost proti dalším sexuálně přenosným chorobám [14].
idů druhé generace patří mezi výhody vysoká specifita, bezpečnost, účinnost (zpravidla již zdokumentovaná při použití v jiné formě aplikace) a možnost využití lékové formy poskytující dlouhodobou ochranu (vaginální kroužky, mukoadhezivní gely). Nevýhodou je riziko vzniku rezistence a neúčinnost proti dalším sexuálně přenosným chorobám [14].
Vzhledem k tomu, že mikrobicidy brání přenosu viru HIV různými cestami [13], byly dále ještě rozděleny do skupin podle mechanismu účinku [15]. Informace týkající se účinku mikrobicidů, jejich struktury, použité lékové formy a stavu klinických studií uvádí tab. 1 pro nespecifické mikrobicidy, tab. 2 pro částečně specifické a tab. 3 pro specifické mi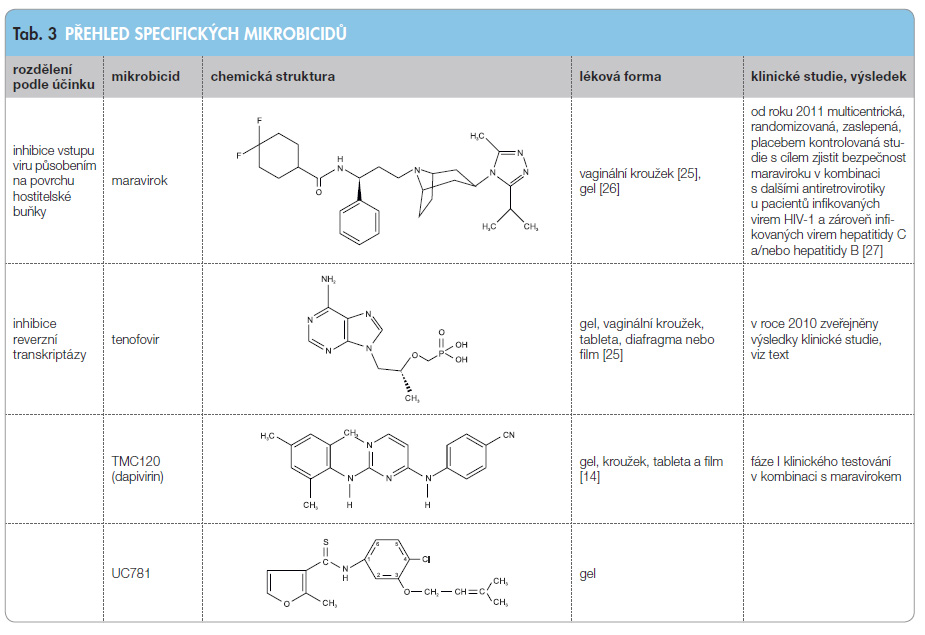 krobicidy.
krobicidy.
Nespecifické mikrobicidy
Mezi nespecifické mikrobicidy se řadí povrchově aktivní látky (tenzidy) a pufrovací systémy (látky udržující přirozené kyselé vaginální pH). Zatímco povrchově aktivní látky narušují obal patogenů rozpouštěním membránových proteinů, pufrovací systémy zajišťují udržení stálého kyselého prostředí ve vaginální oblasti, které přirozeně brání přenosu sexuálně přenosných chorob [13]. Jednotliví zástupci jsou uvedeni v tab. 1 spolu s jejich mechanismem účinku, strukturou, použitou lékovou formou a stavem klinických studií.
Částečně specifické mikrobicidy
Do této skupiny řadíme aniontové polymery, které zasahují do fáze adsorpce nebo fúze viru s hostitelskou buňkou a vstup viru do buňky tak blokují. Polymery se vážou na virový obal díky svým povrchovým negativním skupinám, které interagují s pozitivně nabitými bílkovinami gp120 na povrchu virové částice a zasahují tak do vazby mezi HIV a buňkami CD4 [15]. Aby se zabránilo infikování zdravých buněk, musí však být mikrobicid tohoto typu přítomen ve vysoké koncentraci.
Nižší celková toxicita umožňuje širší terapeutické využití těchto aniontových polymerů, než je tomu v případě tenzidů. Navíc se ukazuje, že by mohly být účinné nejen proti viru HIV, ale díky vazbě na virový obal by mohly působit i proti jiným obaleným virům, jako je například herpetický virus HSV-2.
Antivirová aktivita zástupců této skupiny se liší v závislosti na jejich molekulové hmotnosti a rozložení náboje v molekule. Vnímavost viru k inhibiční aktivitě těchto mikrobicidů je závislá na tom, zda virus využívá povrchový koreceptor CXCR4, nebo koreceptor CCR5. Jsou polymery, které inaktivují viry používající oba koreceptory, některé polymery inaktivují pouze jeden typ virů [13].
Jednotliví zástupci jsou uvedeni v tab. 2 spolu s jejich strukturou, použitou lékovou formou a stavem klinických studií.
Specifické mikrobicidy
Skupina specifických mikrobicidů by měla mít schopnost zablokovat virus HIV dříve, než zabuduje svou DNA do genetické informace hostitelské buňky. Potenciálních míst, kde může mikrobicid zasáhnout, je několik; může být blokována adsorpce viru a fúze s hostitelskou buňkou, odpláštění viru, reverzní transkripce nebo zabudování virové genetické informace do chromozomu hostitelské buňky.
Specifické mikrobicidy blokující vstup HIV do hostitelské buňky můžeme rozdělit podle místa působení na dvě skupiny; mikrobicidy, které inhibují vstup v místě buněčné stěny hostitelské buňky, a mikrobicidy, které inhibují vstup v místě virového obalu. Další významnou skupinou jsou inhibitory reverzní transkriptázy a inhibitory virové integrázy. Tato skupina je velice rozsáhlá a velká většina jejích zástupců se nachází pouze ve fázi preklinického výzkumu. Některé ze specifických mikrobicidů však postoupily do klinického testování a jsou uvedeny v tab. 3 spolu s jejich mechanismem účinku, strukturou, použitou lékovou formou a stavem klinických studií.
Stav klinického testování mikrobicidních přípravků
Ve fázi I a II klinického hodnocení je testováno dávkování, bezpečnost a tolerance mikrobicidního přípravku, následně ve fázi III pak jeho účinnost [15].
V![Obr. 1 Struktura dendrimeru; podle [23] – http://www.uochb.cas.cz, 6. 12. 2011.](https://www.remedia.cz/photo-a-29390---.jpg) letech 1987–2009 byly v klinických studiích testovány mikrobicidy s nespecifickým nebo částečně specifickým účinkem. Jednalo se zpravidla o přípravky levné, snadno dostupné, nenápadné po aplikaci, nejčastěji ve formě vaginálního gelu. Ani jeden z testovaných preparátů však nezaznamenal úspěch a nedostal se do klinické praxe [28]. Mikrobicidy nonoxynol-9 (ve formě houby, filmu a gelu) a Savvy vedly dokonce k nárůstu počtu infekcí virem HIV ve srovnání s kontrolní skupinou. Přípravky Carraguard, PRO-2000 nebo BufferGel byly z dalšího testování vyřazeny z důvodu nízké účinnosti. Kvůli tomuto neúspěchu je klinické testování soustředěno na specifické mikrobicidní přípravky, a to tenofovir, dapivirin, maravirok, UC781 aj.; ze skupiny částečně specifických mikrobicidů zůstal v klinickém testování pouze Vivagel na bázi dendrimerů (obr. 1) [12, 25, 29].
letech 1987–2009 byly v klinických studiích testovány mikrobicidy s nespecifickým nebo částečně specifickým účinkem. Jednalo se zpravidla o přípravky levné, snadno dostupné, nenápadné po aplikaci, nejčastěji ve formě vaginálního gelu. Ani jeden z testovaných preparátů však nezaznamenal úspěch a nedostal se do klinické praxe [28]. Mikrobicidy nonoxynol-9 (ve formě houby, filmu a gelu) a Savvy vedly dokonce k nárůstu počtu infekcí virem HIV ve srovnání s kontrolní skupinou. Přípravky Carraguard, PRO-2000 nebo BufferGel byly z dalšího testování vyřazeny z důvodu nízké účinnosti. Kvůli tomuto neúspěchu je klinické testování soustředěno na specifické mikrobicidní přípravky, a to tenofovir, dapivirin, maravirok, UC781 aj.; ze skupiny částečně specifických mikrobicidů zůstal v klinickém testování pouze Vivagel na bázi dendrimerů (obr. 1) [12, 25, 29].
Významnou studií probíhající v letech 2007–2010 v Jižní Africe byla klinická studie CAPRISA 004 (fáze II), která testovala gel tenofoviru v 1% koncentraci. Do této studie byly zařazeny sexuálně aktivní ženy ve věku 18–40 let [28]. Gel ženy aplikovaly na vaginální sliznici před stykem a po styku. Výsledky studie ukázaly, že účinnost gelu s obsahem tenofoviru byla ve srovnání s placebem o 39 % vyšší [30]. Byl také zaznamenán snížený výskyt infekce virem HSV-2 [31]. Na studii CAPRISA 004 navázala v říjnu 2011 klinická studie FACTS 001, fáze III [28, 30]. Tato studie testuje totožný 1% tenofovirový gel aplikovaný před stykem a po styku. Zahrnuto bylo asi 2200 sexuálně aktivních žen ve věku 18–30 let. Jejím úkolem je potvrdit účinnost tenofovirového gelu v prevenci nákazy virem HIV a HSV-2 a poskytnout další data potřebná k registraci přípravku [31]. FACTS 001 je multicentrická randomizovaná studie probíhající taktéž v Jižní Africe [28, 30]. Předpokládané dokončení studie by mělo být v roce 2014 [30].
Další klinickou studií, která testuje mikrobicid tenofovir, je VOICE [28]. V této studii, která probíhá v Jižní Africe od roku 2009, jsou zahrnuty tři přípravky – gel s tenofovirem, perorální tableta s obsahem tenofoviru (známá pod obchodním názvem Viread) a perorální tableta s obsahem tenofoviru a emtricitabinu (obchodní název Truvada). Vzhledem k tomu, že tenofovir gel i tableta s obsahem tenofoviru ve studii prokázaly bezpečnost, avšak účinnost v prevenci přenosu viru HIV byla nedostatečná, pokračuje další klinické sledování pouze s kombinovanou perorální tabletou Truvada [30, 32]. Do studie, která se nyní nachází ve fázi IIb [28], bylo zařazeno více než 5000 sexuálně aktivních žen ve věku 18–45 let [28, 32]. Výsledky studie, které by měly být dostupné v roce 2013, by mohly osvětlit, proč gel a perorální tableta s obsahem tenofoviru nebyly účinné [32].
Ve fázi I se nachází vaginální kroužky s obsahem maraviroku a kombinace maraviroku s dapivirinem. Je studována jejich bezpečnost a farmakokinetika.V blízké budoucnosti se plánuje fáze I klinické studie vaginálního kroužku s obsahem tenofoviru. Další potenciálně vhodné lékové formy (vaginální tablety a filmy) jsou stále ve fázi preklinického výzkumu.Další plánovanou studií je randomizovaná klinická studie kontrolovaná placebem, která má ověřit účinnost a bezpečnost při dlouhodobém používání vaginálního kroužku s obsahem emtricitabinu. Do studie, která bude probíhat v Subsaharské Africe, má být zahrnuto 5000 žen. V plánu je také studie bezpečnosti u dospívajících, premenopauzálních a postmenopauzálních žen [25].Většina klinických studií mikrobicidů se týká přípravků, které jsou určeny k aplikaci na vaginální sliznici. Přípravky určené k rektální aplikaci jsou zatím v časných fázích klinického výzkumu. Tenofovirový gel aplikovaný rektálně byl v roce 2012 shledán v I. fázi testování bezpečným [33].
Závěry klinického testování
Graf 3![Graf 3 Počet kandidátů ve výzkumu mikrobicidů v letech 1994–2010; podle [12] – Stone, Harrison, 2010.](https://www.remedia.cz/photo-a-29391---.jpg) zachycuje počty mikrobicidů v preklinickém a klinickém testování v letech 1994 až 2010. Z grafu je zřejmé, že ačkoliv kandidátů ve fázi preklinického testování je velké množství, do klinického testování se jich dostane jen velmi málo [12]. Počet kandidátů v klinických studiích má od roku 2000 sestupnou tendenci, přičemž do klinické praxe nebyl zaveden žádný mikrobicidní přípravek.
zachycuje počty mikrobicidů v preklinickém a klinickém testování v letech 1994 až 2010. Z grafu je zřejmé, že ačkoliv kandidátů ve fázi preklinického testování je velké množství, do klinického testování se jich dostane jen velmi málo [12]. Počet kandidátů v klinických studiích má od roku 2000 sestupnou tendenci, přičemž do klinické praxe nebyl zaveden žádný mikrobicidní přípravek.
Výrazným způsobem se změnily také investice, které jsou na výzkum mikrobicidů vynakládány. V roce 2008 bylo do výzkumu mikrobicidů celosvětově investováno 244 milionů dolarů. Tato suma byla téměř čtyřnásobná oproti roku 2000, kdy do výzkumu mikrobicidů bylo celosvětově investováno 65 milionů dolarů [12].Na obr. 2 je zachyceno zastoupení jednotlivých skupin mikrobicidů v klinickém testování v roce 2010. Po neúspěchu téměř mizí mikrobicidy s nespecifickým mechanismem účinku [12], naopak převažují sp![Obr. 2 Zastoupení jednotlivých skupin mikrobicidů v klinickém výzkumu v roce 2010; podle [12] – Stone, Harrison, 2010.](https://www.remedia.cz/photo-a-29392---.jpg) ecifické mikrobicidní preparáty. Dalším trendem současnosti je snaha mikrobicidy navzájem kombinovat. Výhody kombinace spočívají ve zvýšení účinnosti proti rezistentním virům, v možnosti synergického působení látek, a tím snížení spotřeby léku a pokrytí více cest, kterými k přenosu viru dochází. Mezi nevýhody takových kombinací patří možné obtíže s formulací přípravku, zvýšení toxicity, možnost navýšení ceny přípravku a nebezpečí uzavírání smluv mezi institucemi a společnostmi [14].
ecifické mikrobicidní preparáty. Dalším trendem současnosti je snaha mikrobicidy navzájem kombinovat. Výhody kombinace spočívají ve zvýšení účinnosti proti rezistentním virům, v možnosti synergického působení látek, a tím snížení spotřeby léku a pokrytí více cest, kterými k přenosu viru dochází. Mezi nevýhody takových kombinací patří možné obtíže s formulací přípravku, zvýšení toxicity, možnost navýšení ceny přípravku a nebezpečí uzavírání smluv mezi institucemi a společnostmi [14].
I přes intenzivní výzkum v posledních letech se stále nepodařilo vyvinout účinný a bezpečný mikrobicid. Nejčastější lékovou formou mikrobicidů, které jsou nyní předmětem klinického výzkumu, jsou gely a vaginální kroužky.
Podle původních předpokladů měl být mikrobicid s účinností 70–90 % vyvinut do roku 2012 [33]. Tento cíl se splnit nepodařilo. V klinických studiích byla doposud prokázána nejvyšší účinnost u gelu s obsahem tenofoviru, a to 39 %.
Seznam použité literatury
- [1] WHO: European action plan for HIV/AIDS 2012–2015, http://www.euro.who.int, 27. 11. 2011.
- [2] Koubek J. Rok 2011 smutně rekordní – 180 nových případů HIV!, http://www.colourplanet.cz, 7. 1. 2012.
- [3] Zpráva o výskytu a šíření HIV/AIDS za rok 2011, http://www.szu.cz, 21. 3. 2012.
- [4] UNAIDS Report on the Global AIDS Epidemic, http://www.unaids.org, 21. 4. 2012.
- [5] http://www.unaids.org/en/resources/campaigns/, 20. 11. 2012.
- [6] AIDS vaccines in perspective, http://www.iavi.org, 25. 11. 2011.
- [7] Alcamí J, Munné JJ, Muñoz-Fernández M, et al. Current situation in the development of a preventive HIV vaccine. Enfermedadez infecciosas y microbiología clínica 2009; 146: 15–24.
- [8] Esparza J, Chang M, Widdus R, et al. Estimation of “needs” and “probable uptake” for HIV/AIDS preventive vaccines based on possible policies and likely acceptance (a WHO/UNAIDS/IAVI study). Vaccine 2003; 21: 2032–2041.
- [9] Mcgowan I. Microbicides: A new frontier in HIV prevention. Biologicals 2006; 34: 241–255.
- [10] Dvořáčková K, Rabišková M. Vaginální aplikace léčiv – nové směry. Prakt Lékáren 2006; 2: 93–97.
- [11] Omar RF, Bergeron MG. The future of microbicides. Int J Infect Dis 2011; 15: 656–660.
- [12] Stone A, Harrison PF. Microbicides: Ways forward. Alliance for microbicide development 2010, 1–40.
- [13] Balzarini J, Van Damme L. Microbicide drug candidates to prevent HIV infection. Lancet 2007; 369: 787–797.
- [14] Rosenberg ZF. Microbicide products in the pipeline, http://www.global-campaign.org, 15. 1. 2012.
- [15] Cutler B, Justman J. Vaginal microbicides and the prevention of HIV transmission. Lancet 2008; 8: 685–697.
- [16] Amaral E, Perdigao A, Souza MH, et al. Vaginal safety after use of a bioadhesive, acid-buffering, microbicidal contraceptive gel (ACIDFORM) and a 2% nonoxynol-9 product. Contraception 2006; 73: 542–547.
- [17] Malcolm K, Woolfson D, Russell J, et al. In vitro release of nonoxynol-9 from silicone matrix intravaginal rings. J Control Rel 2003; 91: 355–364.
- [18] Chompootaweep S, Dusitsin N. A comparative study of safety, effectiveness and acceptability of two foaming vaginal tablets (nonoxynol-9 versus menfegol) in Thai women. Contraception 1990; 41: 507–617.
- [19] Rogowska-Szadkowska D, Chlabicz S. Microbicides in HIV infection prophylaxis – not only ethical challenges. HIV & AIDS Review 2008; 7: 5–12.
- [20] Hillier S. Microbicide research (2009), http://www.global-campaign.org, 15. 1. 2012.
- [21] Mccormack S, Ramjee G, Kamali A, et al. PRO2000 vaginal gel for prevention of HIV-1 infection (Microbicides development programme 301): a phase 3, randomised, double-blind, parallel-group trial. Lancet 2010; 376: 1329–1337.
- [22] Buckheit Jr. RW, Watson KM, Morrow KM, et al. Development of topical microbicides to prevent the sexual transmission of HIV. Antiviral Research 2010; 85: 142–158.
- [23] Struktura dendrimeru, http://www.uochb.cas.cz, 6. 12. 2011.
- [24] Telwatte S, Moore K, Johnson A, et al. Virucidal activity of the dendrimer microbicide SPL7013 against HIV-1. Antiviral Research 2011; 90: 195–199.
- [25] Rosenberg ZF, Devlin B. Future strategies in microbicide development. Best Pract Res Clin Obstet Gynaecol 2012; 26: 503–513.
- [26] Forbes CJ, Lowry D, Geer L, et al. Non-aqueous silicone elastomer gels as a vaginal microbicide delivery system for the HIV-1 entry inhibitor maraviroc. J Control Rel 2011; 156: 161–169.
- [27] AIDS research alliance: Clinical trials, http://aids-research.org, 4. 2. 2012.
- [28] Sibeko S, Cohen GM, Moodley J. Contraception and pregnancy in microbicide trials. Best Pract Res Clin Obstet Gynaecol 2012; 26: 473–486.
- [29] Global campaign for microbicides: Current trials, http://www.global-campaign.org, 8. 1. 2012.
- [30] Microbicide trials network statement on decision to discontinue use of tenofovir gel in VOICE, a major HIV prevention study in women, http://www.mtnstopshiv.org, 19. 3. 2012.
- [31] FACTS 001 study, http://www.facts-consortium.com, 21. 3. 2012.
- [32] The VOICE study: Vaginal and oral interventions to control the epidemic, http://www.mtnstops-hiv.org, 21. 3. 2012.
- [33] Rectal formulation of tenofovir gel found safe and acceptable in early phase clinical study, www.mtnstopshiv.org, 21. 3. 2012.
- [34] Jedlička, J. Mikrobicidy – stručná informace o nově vyvíjených látkách. CEM/Pracoviště manažera Národního programu HIV/AIDS, http://paveldanko.com/, 30. 3. 2012.