Agomelatin – antidepresivum, jež obnovuje cirkadiánní rytmy
Agomelatin je antidepresivum s novým mechanismem účinku. Působí jako agonista melatoninergních receptorů (MT1 , MT2 ) a jako antagonista serotoninergních receptorů 5-HT2C . Působením na tyto receptory resynchronizuje cirkadiánní rytmy a vykazuje antidepresivní účinky. Účinnost a bezpečnost agomelatinu byla hodnocena v řadě klinických studií, kde byl srovnáván s placebem i s aktivními komparátory. Antidepresivní účinnost byla prokázána ve studiích s placebem a při všech přímých porovnáních s jinými antidepresivy (venlafaxin, sertralin, fluoxetin, escitalopram), a to i u závažné deprese. Z klinických studií vyplynula také anxiolytická účinnost agomelatinu a příznivý vliv na kvalitu spánku. Významným přínosem agomelatinu je rychlý nástup účinku, pozorovaný již v prvních 2 týdnech léčby, a vynikající profil snášenlivosti bez nárůstu tělesné hmotnosti a bez poruch sexuálních funkcí. Agomelatin je účinný i při dlouhodobém podávání, kdy vykazuje vysoký podíl adherentních pacientů.
Evropská léková agentura (EMA) registrovala agomelatin pro použití v zemích Evropského společenství v únoru 2009. Je indikován k léčbě depresivních epizod u dospělých, v dávce 25 mg podávané jednou denně před spaním. Doporučená délka léčby, tak jako u všech antidepresiv, je alespoň 6 měsíců. Agomelatin se vyznačuje velmi dobrou snášenlivostí a nízkou mírou nežádoucích účinků. Ukončování léčby agomelatinem není provázeno příznaky z odnětí, a proto nevyžaduje postupné vysazování dávky. Agomelatin se nesmí podávat u závažného poškození funkce jater a v průběhu léčby všech pacientů je doporučeno sledovat jaterní funkce. Léčba agomelatinem musí být ukončena, pokud aktivita aminotransferáz stoupne na více než trojnásobek horního limitu normálního rozmezí. Agomelatin je možné bezpečně kombinovat s jinými léky s výjimkou fluvoxaminu a ciprofloxacinu. U kojících matek je třeba zastavit kojení. V posledních letech potvrdilo účinnost a bezpečnost agomelatinu v běžné klinické praxi několik rozsáhlých observačních studií. Dosud užívalo agomelatin okolo 2 milionů pacientů po celém světě.
Farmakologická skupina
Farmakologický profil agomelatinu se liší od ostatních antidepresiv, a patří tedy do samostatné skupiny agonistů melatoninu a selektivních serotoninergních antagonistů (MASSA – Melatonin Agonist and Selective Serotonin Antagonist).
Mechanismus účinku, farmakodynamika
Agomelatin, N-[2-(7-methoxy-1-naftyl)ethyl]-acetamid, je prvním a zatím jediným zástupcem nové skupiny antidepresiv (MASSA) založené na inovativním mechanismu účinku. Tento derivát melatoninu působí jako agonista melatoninových receptorů MT1 a MT2 a jako antagonista serotoninových receptorů 5-HT2C [1–4]. Melatoninové receptory jsou nejvíce zastoupeny v nucleus suprachiasmaticus a jejich exprese podléhá cirkadiánním rytmům s maximem večer. Účinek agomelatinu na melatoninergní receptory je podobný melatoninu, jeho afinita k nim je však vyšší a jejich aktivace dlouhodobější. Blokáda receptorů 5-HT2C zvyšuje koncentraci noradrenalinu a dopaminu ve frontálním kortexu a v hipokampu; jsou jí přisuzovány jak antidepresivní a anxiolytické účinky, tak podpora pomalovlnného spánku (SWS). Blokádou receptorů 5-HT2C se agomelatin liší od melatoninu, který takové účinky nemá. Svým působením na receptory MT1, MT2 a 5-HT2C zasahuje agomelatin do patogeneze deprese na buněčné úrovni a vede tak ke zmírnění příznaků deprese jak prostředni![Obr. 1 Schéma mechanismu účinku agomelatinu; volně podle [53] – Racagni, et al., 2011. ARC – activity-regulated cytoskeleton-associated protein; BDNF – mozkový neurotrofický faktor (Brain Derived Neurotrophic Factor)](https://www.remedia.cz/photo-a-28939---.jpg) ctvím synchronizace cirkadiánních rytmů, tak posílením dopaminergní a noradrenergní stimulace frontální mozkové kůry (obr. 1). Agomelatin nemá účinek na zpětné vychytávání monoaminů, nevykazuje afinitu k α-adrenergním, β-adrenergním, histaminergním, cholinergním, dopaminergním či benzodiazepinovým receptorům, neovlivňuje počet serotoninergních receptorů a nemá vliv na extracelulární hladinu serotoninu. Podle některých zpráv agomelatin omezuje uvolňování glutamátu v hipokampu potkanů [5]. Redukce uvolňování glutamátu by mohla vysvětlovat jeho neuroprotektivní působení a stimulaci neurogeneze v animálních studiích [6–8]. Jde tedy o unikátní
ctvím synchronizace cirkadiánních rytmů, tak posílením dopaminergní a noradrenergní stimulace frontální mozkové kůry (obr. 1). Agomelatin nemá účinek na zpětné vychytávání monoaminů, nevykazuje afinitu k α-adrenergním, β-adrenergním, histaminergním, cholinergním, dopaminergním či benzodiazepinovým receptorům, neovlivňuje počet serotoninergních receptorů a nemá vliv na extracelulární hladinu serotoninu. Podle některých zpráv agomelatin omezuje uvolňování glutamátu v hipokampu potkanů [5]. Redukce uvolňování glutamátu by mohla vysvětlovat jeho neuroprotektivní působení a stimulaci neurogeneze v animálních studiích [6–8]. Jde tedy o unikátní 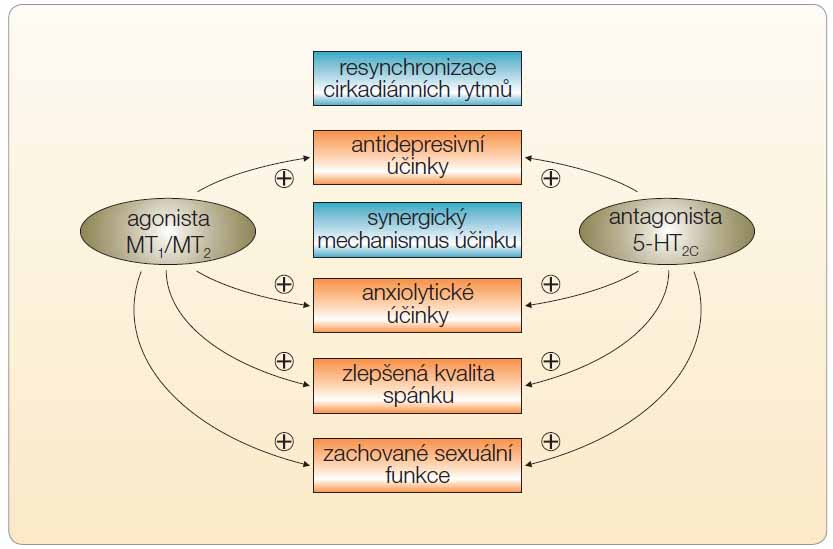 mechanismus účinku, který příznivě ovlivňuje nejen náladu, ale i spánek a fungování během dne (obr. 2) [9, 10].
mechanismus účinku, který příznivě ovlivňuje nejen náladu, ale i spánek a fungování během dne (obr. 2) [9, 10].
Koncepce resynchronizace cirkadiánních rytmů v léčbě deprese vychází ze zjištěných změn některých biologických parametrů v rámci 24hodinového cyklu dne u pacientů s depresí (graf 1) [11]. Při depresi dochází ke změnám cirkadiánních rytmů tělesné teploty, plazmatických hladin některých hormonů a neurotransmiterů. Výrazně změněn je spánkový cyklus s narušenou architekturou spánku (střídání a délka fází REM spánku a SWS spánku) a s dopadem na fungování, kognitivní výkonnost a náladu během dne. Cirkadiánnímu kolísání podléhá také nálada. Příkladem jsou tzv. ranní pessima – převažující horší nálada u pacientů s depresí v ranních hodinách. Byla prokázána korelace mezi závažností deprese a poruchami cirkadiánních rytmů. ![Graf 1 Změny cirkadiánních rytmů tělesné teploty, sekrece kortizolu a melatoninu u pacientů s depresí; podle [11] – Höschl, 1989.](https://www.remedia.cz/photo-a-28941---.jpg) U pacientů s depresivní poruchou bylo vyšší skóre Hamiltonovy škály pro depresi (HAM-D17) spojeno s větším opožděním fáze začátku sekrece melatoninu po setmění [12].
U pacientů s depresivní poruchou bylo vyšší skóre Hamiltonovy škály pro depresi (HAM-D17) spojeno s větším opožděním fáze začátku sekrece melatoninu po setmění [12].
Farmakokinetika
Po perorálním podání se vstřebává 80 % podané dávky agomelatinu. Maximální plazmatické koncentrace je dosaženo za 45 až 90 minut. Biologická dostupnost je relativně nízká (< 5 %), o něco vyšší je u žen než u mužů, zvyšuje se při užívání perorálních kontraceptiv. Příjem potravy biologickou dostupnost ani rychlost absorpce nemění. Distribuční objem agomelatinu je cca 35 litrů, na plazmatické bílkoviny se váže 95 % účinné látky. Agomelatin je metabolizován v játrech cytochromovým systémem CYP1A2. Hlavní metabolity jsou inaktivní a rychle se vylučují ledvinami. Poločas eliminace agomelatinu je 1 až 2 hodiny, clearance je převážně metabolická. Močí se vyloučí 80 % agomelatinu, z velké části ve formě metabolitů. Farmakokinetika se při opakovaném podání nemění. Významné změny farmakokinetických parametrů nebyly zjištěny ani u pacientů se závažnou renální poruchou, klinické údaje jsou však u tohoto typu pacientů omezené. Při chronické mírné až středně závažné poruše funkce jater byla u cirhotických pacientů hladina agomelatinu významně zvýšena, aniž by byl zvýšen počet nebo závažnost nežádoucích účinků [1].
Klinické zkušenosti
Vlastnosti agomelatinu byly hodnoceny v řadě preklinických a klinických studií. Jeho účinnost a bezpečnost byla v klinických studiích porovnávána s placebem i aktivními komparátory u téměř 8000 pacientů a více než 10 000 pacientů bylo sledováno v observačních studiích.
Obnova cirkadiánních rytmů
V prvních fázích vývoje byl agomelatin testován na zvířecích modelech deprese a u poruch cirkadiánních rytmů. U validovaného modelu deprese vedl agomelatin k obnově původní amplitudy kolísání tělesné teploty u samečků tany vystavených stresu [13]. V další experimentální studii došlo u potkanů vystavených stálé tmě k opoždění fáze aktivity, jež přetrvávalo i po návratu do prostředí s normálním střídáním světla a tmy. Podávání agomelatinu vedlo u těchto zvířat k přesunu fáze aktivity zpět do normálu, což potvrzuje obnovu cirkadiánních rytmů [14]. Resynchronizace cirkadiánních rytmů byla prokázána také v humánních klinických studiích. V mezinárodní randomizované, dvojitě zaslepené studii [15] byl agomelatin (25–50 mg/den) porovnáván se sertralinem (50–100 mg/den) u pacientů s depresivní poruchou. Kromě vyšší antidepresivní účinnosti agomelatinu od 2. do 6. týdne bylo prokázáno i zvětšení amplitudy cyklu aktivity a klidu, která je u pacientů s depresí, stejně jako řada dalších cirkadiánních výkyvů, oploštělá. Tento cyklus byl měřen v každodenních podmínkách aktigraficky pomocí přístroje umístěného na zápěstí, který zaznamenával pohyby pacienta během dne. U pacientů léčených agomelatinem navíc došlo ke zkrácení spánkové latence a ke zvýšení spánkové účinnosti. Příznivé účinky na spánek byly zjištěny také v další studii [16, 17] u pacientů s depresivní poruchou, u nichž byly provedeny polysomnografické záznamy 7., 14. a 42. den léčby. Agomelatin v dávce 25 mg/den zlepšil spánkovou účinnost, prodloužil dobu do prvního probuzení, zvýšil celkové množství SWS spánku a resynchronizoval jeho cykly v průběhu noci. Neovlivnil REM fázi spánku. V randomizované, dvojitě zaslepené dlouhodobé studii s venlafaxinem jako aktivním komparátorem bylo prokázáno zlepšení kvality spánku a fungování během dne již od prvního týdne léčby agomelatinem [18].
Porovnání s placebem
Účinnost agomelatinu byla porovnávána s placebem v 9 randomizovaných, dvojitě zaslepených studiích. Zařazováni byli dospělí muži i ženy, hospitalizovaní i ambulantní, se středně těžkou až těžkou depresí. V 5 z těchto studií [19–23] byla prokázána statisticky významně vyšší účinnost agomelatinu v porovnání s placebem z hlediska snížení celkového skóre na škále Montgomeryho a Åsbergové pro posuzování deprese (MADRS) nebo na Hamiltonově škále pro depresi (HAM-D) nebo z hlediska počtu respondérů (odpověď na léčbu = pokles celkového skóre HAM-D/MADRS ≥ 50 %). V hromadné analýze 3 z těchto studií [24] byl počet respondérů při léčbě agomelatinem 56 % a při podávání placeba 39 %. Zajímavým parametrem je NNT (number needed to treat), který udává počet pacientů, jež je třeba léčit, aby bylo dosaženo jednoho léčebného výsledku navíc. Klinický význam má NNT při hodnotách nižších než 10. V 5 studiích s agomelatinem, kde byla prokázána jeho účinnost proti placebu, se hodnota NNT pohybovala od 6 do 9. Ve studiích, kde nebyla prokázána účinnost proti placebu (snížení celkového skóre na škále HAM-D/MADRS, počet respondérů), byl použit aktivní komparátor [9]. V jedné ze tří nepublikovaných studií (CL3-022, CL3-023, CL3-024) se účinnost agomelatinu ani paroxetinu nelišila od placeba. Příčinou byla vysoká míra odpovědi na placebo (47–58 %) v této studii. V další studii nebyl agomelatin účinnější než placebo, zatímco fluoxetin ano. Ve třetí studii nebyla prokázána statisticky významně větší účinnost agomelatinu ani fluoxetinu oproti placebu, jak se již v poslední době stalo i u jiných psychofarmak. Příčinou může být nízké vstupní skóre použitých škál nebo další faktory.
V kombinované analýze 3 studií [25, 26], jež prokázaly účinnost agomelatinu, byl pozorován rychlý nástup jeho účinku, a to již od 2. týdne léčby. V této analýze byla zjištěna i anxiolytická účinnost agomelatinu s příznivým ovlivněním somatické i psychické složky úzkosti. Účinnost agomelatinu stoupala se zvyšující se závažností deprese a nebyla závislá na pohlaví, věku ani tělesné hmotnosti.
Anxiolytické účinky
Anxiolytická účinnost agomelatinu byla hodnocena v 6 studiích [27]: ve třech kontrolovaných placebem a ve třech v porovnání s jinými antidepresivy (fluoxetin, sertralin, venlafaxin). Ze všech těchto studií vyplynuly 3 hlavní závěry: (i) čím vyšší je intenzita úzkosti, tím silnější je anxiolytická účinnost agomelatinu, (ii) agomelatin snižuje míru úzkosti již v prvních dvou týdnech léčby, a to nezávisle na závažnosti úzkosti a (iii) anxiolytická účinnost agomelatinu je větší v porovnání se selektivními inhibitory zpětného vychytávání serotoninu (SSRI) a inhibitory zpětného vychytávání serotoninu a noradrenalinu (SNRI). Podle výsledků pilotní studie je agomelatin účinný i v léčbě generalizované úzkostné poruchy [28].
Rychlost nástupu účinku
Rychlý nástup účinku je jednou z výhod agomelatinu, jež byla opakovaně prokázána v klinických studiích. Nástup účinku aktivní léčby po prvním týdnu podávání agomelatinu byl prokázán ve studii srovnávající agomelatin s placebem [22]. Již po 1. týdnu léčby agomelatinem bylo zjištěno statisticky významné snížení celkového skóre na škále HAM-D oproti vstupní hodnotě (p = 0,005), které přetrvávalo při všech hodnoceních včetně posledního vyšetření po 8 týdnech (p = 0,010). V jiné mezinárodní randomizované, dvojitě zaslepené studii [18] dosáhli pacienti léčení agomelatinem (n = 165, 25–50 mg/den) rychlejšího klinického zlepšení podle škály CGI-I (Clinical Global Impression) v porovnání s pacienty léčenými venlafaxinem (n = 165, 75–150 mg/den), a to již po jednom týdnu podávání (p = 0,0001). Nástup účinku agomelatinu v 1. týdnu léčby potvrdil i vyšší počet (19 %) respondérů (CGI-I skóre ≤ 2) než u venlafaxinu (11 %; p = 0,010). Rovněž při porovnání se sertralinem [15] vedla léčba agomelatinem k dvojnásobnému počtu respondérů po 2 týdnech léčby. Téměř 20 % pacientů s depresivní poruchou dosáhlo ve 2. týdnu snížení skóre na škále HAM-D o více než 50 % (definováno jako respondéři).
![Graf 2 Zlepšování stavu pacientů léčených agomelatinem je lineární a průběžné na rozdíl od efektu stávajících generací antidepresiv; podle [29] – Gorwood, 2010. SSRI – inhibitory zpětného vychytávání serotoninu; SNRI – inhibitory zpětného vychytávání serotoninu a noradrenalinu](https://www.remedia.cz/photo-a-28942---.jpg) Zlepšení stavu se u pacientů, kteří zareagovali na léčbu, dostavilo v průměru po 1–3 týdnech léčby. Toto zlepšování bylo u pacientů léčených agomelatinem spíše lineární a průběžné, na rozdíl od efektu dosavadních generací antidepresiv [29] (graf 2).
Zlepšení stavu se u pacientů, kteří zareagovali na léčbu, dostavilo v průměru po 1–3 týdnech léčby. Toto zlepšování bylo u pacientů léčených agomelatinem spíše lineární a průběžné, na rozdíl od efektu dosavadních generací antidepresiv [29] (graf 2).
Dlouhodobá účinnost v prevenci relapsů
Dvě ze studií s agomelatinem byly věnovány speciálně prevenci relapsů [30]. Dlouhodobá studie s agomelatinem zaměřená na prevenci relapsů zahrnovala 339 pacientů, již byli nejprve 8–10 týdnů za otevřených podmínek léčeni agomelatinem a poté 6 měsíců v randomizovaném, dvojitě zaslepeném uspořádání dostávali agomelatin (25–50 mg/den) nebo placebo. Relaps byl definován jako zvýšení skóre HAM-D o více než 15 bodů, předčasné přerušení léčby nebo pokus o sebevraždu. Kromě významného zlepšení primárního sledovaného parametru, kterým byl pokles skóre na škále HAM-D, byl zjištěn dvojnásobně nižší výskyt relapsů u pacientů léčených agomelatinem (22 %) v porovnání s placebem (47 %) v průběhu studie (p = 0,0001). Kontrolované prodloužení studie navíc ukázalo, že tento přínos přetrvává i po 10 měsících léčby (24 % vs. 50 %; p < 0,0001) jak u celé zahrnuté populace, tak u podskupiny pacientů se závažnější depresivní poruchou [31]. V jiné studii, jež zahrnovala 367 pacientů a trvala 34 týdnů, se přínos agomelatinu oproti placebu nepodařilo prokázat především z důvodu nízkého počtu relapsů ve skupině s placebem (26 % placebo vs. 24 % agomelatin) [9].
Dlouhodobou účinnost agomelatinu potvrdily výsledky studií s aktivními komparátory. Studie, která porovnávala agomelatin se sertralinem, ukázala o 12 % vyšší podíl respondérů ve skupině s agomelatinem po 6 měsících léčby (p = 0,05) [15]. Šestiměsíční porovnání s escitalopramem prokázalo přetrvávající antidepresivní účinnost na konci studie s počtem respondérů 82,6 % ve skupině s agomelatinem a 81,3 % ve skupině s escitalopramem [32].
Zařazení do současné palety léčiv
![Graf 3 Účinnost agomelatinu na zmírnění symptomů deprese oproti placebu v týdnu 6/8; podle [27] – Demyttenaere, 2011](https://www.remedia.cz/photo-a-28943---.jpg) Antidepresivní účinnost agomelatinu vede k významnému zmírnění všech stěžejních symptomů deprese (graf 3).
Antidepresivní účinnost agomelatinu vede k významnému zmírnění všech stěžejních symptomů deprese (graf 3).
Srovnání s jinými antidepresivy
Bylo provedeno několik randomizovaných, dvojitě zaslepených studií fáze III, jež porovnávaly agomelatin s jinými antidepresivy (venlafaxin, sertralin, fluoxetin, escitalopram, paroxetin). Při všech přímých porovnáních agomelatinu s aktivním komparátorem byla prokázána minimálně stejná antidepresivní účinnost agomelatinu [33].
![Graf 4 Procento respondérů po 6–8 týdnech v hromadné analýze studií s agomelatinem a aktivním komparátorem; podle [24] – Kasper, et al., 2010.SSRI - nhibitory zpětného vychytávání serotoninu; SNRI – inhibitory zpětného vychytávání serotoninu a noradrenalinu](https://www.remedia.cz/photo-a-28944---.jpg) Hromadná analýza studií s agomelatinem a aktivním komparátorem, zahrnující celkem 630 pacientů léčených agomelatinem a 637 pacientů léčených escitalopramem, sertralinem, fluoxetinem a venlafaxinem [24], ukázala vyšší podíl respondérů po 6 nebo 8 týdnech léčby agomelatinem (71,7 % vs. 64,5 %; p = 0,005), graf 4. Léčba agomelatinem byla také spojena s větším poklesem celkového skóre na škále HAM-D po 6 nebo 8 týdnech léčby oproti vstupní hodnotě, a to v porovnání s jakýmkoliv komparátorem. Za zmínku stojí, že agomelatin byl účinný u celého spektra pacientů včetně pacientů s nejzávažnější depresí [34, 35]. Podstatnou skutečností v porovnání s ostatními antidepresivy je rychlý nástup účinku, zaznamenaný již ve 2. týdnu léčby v podobě většího počtu respondérů či většího symptomatického zlepšení.
Hromadná analýza studií s agomelatinem a aktivním komparátorem, zahrnující celkem 630 pacientů léčených agomelatinem a 637 pacientů léčených escitalopramem, sertralinem, fluoxetinem a venlafaxinem [24], ukázala vyšší podíl respondérů po 6 nebo 8 týdnech léčby agomelatinem (71,7 % vs. 64,5 %; p = 0,005), graf 4. Léčba agomelatinem byla také spojena s větším poklesem celkového skóre na škále HAM-D po 6 nebo 8 týdnech léčby oproti vstupní hodnotě, a to v porovnání s jakýmkoliv komparátorem. Za zmínku stojí, že agomelatin byl účinný u celého spektra pacientů včetně pacientů s nejzávažnější depresí [34, 35]. Podstatnou skutečností v porovnání s ostatními antidepresivy je rychlý nástup účinku, zaznamenaný již ve 2. týdnu léčby v podobě většího počtu respondérů či většího symptomatického zlepšení.
Mezinárodní randomizovaná, dvojitě zaslepená studie [36] porovnávala účinnost agomelatinu (25–50 mg/den) a escitalopramu (10–20 mg/den) u 138 pacientů s velkou depresivní poruchou a délkou léčby až 24 týdnů. Antidepresivní účinnost obou preparátů byla srovnatelná z hlediska snížení skóre na škále HAM-D, počtu respondérů i podílu pacientů s remisí. U agomelatinu byl prokázán příznivější vliv na kvalitu spánku v porovnání s escitalopramem (zkrácení spánkové latence, méně ospalosti během dne, zachování latence REM spánku, zachování počtu spánkových cyklů). V další randomizované, dvojitě zaslepené dlouhodobé studii, jež porovnávala agomelatin s escitalopramem u pacientů s depresivní poruchou, bylo prokázáno, že při léčbě agomelatinem došlo k obnově intenzity emocí u významně vyššího počtu pacientů než při podávání escitalopramu [32]. Otázka emočního oploštění, které zatím nebylo u pacientů s depresivní poruchou nijak zvlášť zdůrazňováno, nabývá s příchodem agomelatinu na významu. Zdá se totiž, že agomelatin kromě úpravy oploštělých emocí také příznivě ovlivňuje rozpoznávání negativních emocí ve tvářích a zvyšuje „recall“ pozitivních (oproti negativním) slovních podnětů v porovnání s placebem [37]. Další studie řeknou i o tomto jistě více.
Observační studie
Agomelatin se v řadě zemí používá již několik let. Proto byl jeho přínos hodnocen v každodenní lékařské praxi v několika observačních studiích.
V Německu proběhla studie VIVALDI [38], jež hodnotila účinnost a snášenlivost agomelatinu u 3317 ambulantních pacientů s depresivní poruchou po dobu 12 týdnů. V této studii bylo zjištěno zmírnění závažnosti depresivních příznaků podle škály MADRS ze 30,6 na začátku studie na 12,8 po 12 týdnech léčby agomelatinem. Remise dosáhlo 54,8 % pacientů. Významně se snížil podíl pacientů s poruchami spánku, u 78,2 % pacientů došlo oproti začátku studie ke zmírnění únavy během dne. Snášenlivost agomelatinu byla hodnocena jako velmi dobrá nebo dobrá, nežádoucí účinky se vyskytovaly u 10 % pacientů.
Ruská observační studie CHRONOS [39] zahrnovala přes 6000 pacientů s depresivní poruchou. Prokázala rychlý nástup účinku agomelatinu s významným snížením celkového skóre HAM-D již v prvním týdnu léčby. Počet respondérů (pokles celkového skóre HAM-D ≥ 50 %) činil po 4 týdnech léčby agomelatinem 51 %, po 6 týdnech 72 % a po 8 týdnech 81 %.
V Itálii proběhla 8týdenní studie [40], v níž byla u pacientů s depresí hodnocena účinnost agomelatinu v dávce 25–50 mg/den. Hodnoceny byly příznaky deprese (Hamilton Depression Scale, HAM-D), úzkosti (Hamilton Anxiety Scale, HAM-A), anhedonie – neschopnosti prožít radost (Snaith Hamilton Rating Scale, SHAPS) a kvalita spánku (Leeds Sleep Evaluation Questionnaire, LSEQ) u 24 pacientů. Významné zlepšení bylo zjištěno u HAM-D (p < 0,05), HAM-A (p < 0,01), SHAPS (p < 0,05) i LSEQ (p < 0,05). Po jednom týdnu léčby agomelatinem dosáhlo 30 % pacientů odpovědi na léčbu a 17 % remise. Na konci studie bylo v remisi 60 % účastníků. Bezpečnost léčby byla velmi dobrá. Tato studie potvrdila rychlý nástup účinku agomelatinu a poprvé i jeho účinnost při zmírnění anhedonie.
V 8týdenní otevřené studii se 111 ambulantními pacienty s depresivní poruchou, jež proběhla na Slovensku [41], bylo zjištěno snížení průměrného celkového skóre na škále MADRS z 28,7 na 9,8.
Pokles byl statisticky významný již po 1. týdnu léčby. Podíl respondérů (pokles MADRS ≥ 50 %) po 1., 2., 4. a 8. týdnu léčby byl 0,9 %, 17 %, 48,1 %, resp. 74,5 %. Došlo také ke zlepšení všech složek fungování během dne podle Sheehan Disability Scale a ke zlepšení kvality spánku. Rovněž tato studie potvrdila dobrou antidepresivní účinnost agomelatinu s rychlým nástupem účinku a dobrou bezpečností léčby.
Indikace
Agomelatin je indikován k léčbě depresivních epizod u dospělých. Kromě toho byla jeho účinnost hodnocena v léčbě bipolární deprese [42], sezonní afektivní poruchy [43], generalizované úzkostné poruchy [28] a Alzheimerovy demence. Byly také provedeny studie využití agomelatinu v léčbě insomnií a poruch spánkového rytmu. V těchto indikacích nebyla léčba agomelatinem zatím schválena
.Kontraindikace
Agomelatin je kontraindikován u pacientů s poruchou funkce jater, při současném podávání silných inhibitorů cytochromu P450 1A2 (zejména fluvoxaminu, ciprofloxacinu) a při přecitlivělosti na účinnou nebo některou pomocnou látku přípravku [1]. Vzhledem k tomu, že dostupný preparát obsahuje laktózu, neměli by jej užívat pacienti s intolerancí galaktózy nebo glukózo-galaktózovým malabsorpčním syndromem.
Nežádoucí účinky
Velmi příznivých výsledků bylo s agomelatinem dosaženo při hodnocení snášenlivosti. Dobrá snášenlivost je přitom rozhodujícím parametrem pro úspěšné zahájení léčby a dlouhodobou adherenci. Příznivý bezpečnostní profil agomelatinu je patrný již v krátkodobých studiích, kde se výskyt nežádoucích účinků spojených s léčbou agomelatinem téměř nelišil od placeba [1, 19–23]. V 6měsíčních sledováních porovnávajících agomelatin s placebem byly jediným statisticky významným nežádoucím účinkem spojeným s podáváním agomelatinu v porovnání s placebem závratě (5,9 %, resp. 3,5 %; p < 0,01) [30]. Metaanalýza výsledků studií s aktivními komparátory ukázala, že proporce pacientů s depresivní poruchou, kteří dokončili 6 měsíců léčby, byla statisticky významně vyšší při podávání agomelatinu (69,4 %) než při léčbě jinými antidepresivy (61,5 %; p = 0,012) [44]. Jedním z důvodů dobré adherence k léčbě agomelatinem může být i jeho výborná gastrointestinální snášenlivost a absence nárůstu tělesné hmotnosti a sexuálních dysfunkcí, jež jsou zmíněny i v SPC [1].
Sexuální dysfunkce
Vzhledem k tomu, že podstatným nežádoucím účinkem antidepresiv jsou sexuální dysfunkce, byla u agomelatinu věnována značná pozornost také tomuto aspektu léčby. V souhrnné analýze všech studií s agomelatinem byla zjištěna sexuální dysfunkce u 0,7 % mužů léčených agomelatinem, u 1,2 % mužů, kteří dostávali placebo, u 2,4 % mužů léčených SSRI (fluoxetin, sertralin, paroxetin) a u 1 % mužů s venlafaxinem. Specificky byly ovlivnění sexuálních funkcí věnovány dvě studie s agomelatinem. V první z nich [45] byl agomelatin porovnáván s venlafaxinem. Zhoršení sexuálních funkcí hodnocené podle dotazníku SFQ (Sexual Functioning Questionnaire) bylo zaznamenáno u 4,1 % žen léčených agomelatinem a u 15,3 % léčených venlafaxinem (p = 0,002). Ve druhé studii [46] byl agomelatin porovnáván s paroxetinem u 98 zdravých mužů. Sexuální dysfunkce byla zjištěna u 4,5 % mužů léčených agomelatinem, u 4,3 % mužů s placebem a u 61,9 % mužů s paroxetinem (p < 0,0001 pro rozdíl mezi agomelatinem a paroxetinem). U pacientů převedených z léčby jiným antidepresivem na léčbu agomelatinem byly sexuální funkce sledovány dotazníkem CSFQ (Changes in Sexual Functions Questionnaire). Po 6 týdnech léčby bylo zjištěno statisticky významné zlepšení ve všech složkách sexuálního cyklu [47].
Jaterní funkce
Při podávání agomelatinu byly zaznamenány případy reverzibilního zvýšení aktivity aminotransferáz (ALT/AST) v prvních měsících léčby převážně při dávce 50 mg denně (1,1 % celkově u všech dávek agomelatinu vs. 0,7 % u placeba) [1]. Proto EMA doporučuje provedení jaterních testů jako preventivní opatření při zahájení léčby agomelatinem a následně vyšetření jaterních funkcí po přibližně 3, 6, 12 a 24 týdnech léčby a dále v případě potřeby. Léčba agomelatinem musí být ukončena, pokud aktivita aminotransferáz stoupne na více než trojnásobek horního limitu normálního rozmezí. Při cirhóze nebo aktivním onemocnění jater je podávání agomelatinu kontraindikováno.
Syndrom z vysazení
Výskyt případných příznaků z vysazení léčby byl hodnocen ve speciální placebem kontrolované studii [48] po 12 týdnech léčby agomelatinem nebo paroxetinem. U 192 pacientů léčených pro depresi bylo po dosažení remise nadále podáváno stávající antidepresivum nebo bylo nahrazeno placebem. Ve 13. a 14. týdnu nebyly u pacientů po vysazení agomelatinu zjištěny příznaky z vysazení podle škály DESS (Discontinuation-Emergent Signs and Symptoms); tyto příznaky byly významně častější ve skupině po vysazení paroxetinu (p < 0,001). Ve srovnávací studii agomelatinu s placebem u generalizované úzkostné poruchy [28] byl počet nemocných s více než jedním příznakem na škále DESS po vysazení agomelatinu dokonce nižší než po vysazení placeba (39,5 % vs. 43,8 %). Zatím se tedy zdá, že náhlé ukončení léčby agomelatinem není provázeno rizikem výskytu syndromu z vysazení.
Tělesná hmotnost
Agomelatin se v krátkodobých studiích neodlišoval co do ovlivnění hmotnosti ani od placeba, ani od paroxetinu či venlafaxinu. Podle souhrnné analýzy dlouhodobých 6měsíčních studií se tělesná hmotnost po podávání agomelatinu zvýšila v průměru o 0,23 kg ve srovnání s 0,24 kg po podávání placeba, 0,51 kg po SSRI a 0,29 kg po venlafaxinu. Počet nemocných se zvýšením hmotnosti o více než 7 % iniciální hodnoty činil po agomelatinu 5 % ve srovnání s 5,7 % po placebu, 8,8 % po SSRI a 5,4 % po venlafaxinu (přehled viz např. Švestka a Mohr [9]). Dosavadní zkušenost tedy nasvědčuje tomu, že agomelatin je k tělesné hmotnosti neutrální.
Kardiovaskulární funkce
Agomelatin podle všeho neovlivňuje krevní tlak a tepovou frekvenci více než placebo. Agomelatin neprodlužoval QTc interval ve studii specificky zaměřené na kardiovaskulární systém (přehled viz [9]).
Věk pacienta
Agomelatin dosud nebyl klinicky testován v populaci mladší 18 let, takže se vzhledem k nedostatku údajů jeho podávání dětem a dospívajícím nedoporučuje. Souhrn údajů o přípravku také nabádá k opatrnosti při podávání agomelatinu pacientům starším 65 let [1]. Nicméně s ohledem na mechanismus účinku jde o lék, jenž by mohl být pro část starších pacientů vhodný. V retrospektivním vyhodnocení vzorku starších pacientů byl agomelatin dobře tolerován a byla potvrzena jeho antidepresivní účinnost jak v monoterapii, tak v kombinaci s jinými antidepresivy. Bylo zaznamenáno zlepšení i u pacientů prokazatelně farmakorezistentních [49].
Agomelatin v těhotenství a laktaci
Dosud nejsou k dispozici klinické údaje o podávání agomelatinu v těhotenství. Animální studie však nenaznačují teratogenní či škodlivé účinky na průběh těhotenství, porod nebo postnatální vývoj. Není také známo, zda se agomelatin vylučuje do mateřského mléka u člověka. Agomelatin nebo jeho metabolity se však během laktace vylučují do mléka potkanů. Potenciální účinky agomelatinu na kojené dítě nebyly dosud stanoveny. Pokud je léčba agomelatinem nezbytná, mělo by být kojení ukončeno [1].
Lékové interakce
Agomelatin je metabolizován cestou cytochromu P-450, izoenzymu 1A2. Léky, jež inhibují CYP1A2, zvyšují koncentraci agomelatinu. Současné podávání agomelatinu se silnými inhibitory CYP1A2 (fluvoxamin, ciprofloxacin) je kontraindikováno. U středně silných inhibitorů CYP1A2 (estrogeny, propranolol, grepafloxacin, enoxacin, moklobemid, cimetidin, tiklodipin, fluorochinolony) je při kombinaci s agomelatinem doporučeno opatrné podávání. Při léčbě touto kombinací dochází k několikanásobnému zvýšení expozice agomelatinu, ale u 800 pacientů léčených kombinací estrogenů a agomelatinu nebyly zjištěny z hlediska bezpečnosti žádné změny. Naopak paroxetin (středně silný inhibitor CYP1A2) a flukonazol (silný inhibitor CYP1A2) koncentrace agomelatinu téměř neovlivňují. Rovněž nebyly zjištěny farmakokinetické ani farmakodynamické interakce s dalšími léky, jež by mohly být předepisovány spolu s agomelatinem, jako jsou benzodiazepiny, lithium a theofylin. Agomelatin sám CYP1A neinhibuje ani neindukuje, a proto významněji neovlivňuje expozici lékům touto cestou metabolizovaným. Klinické zkušenosti se současným podáním agomelatinu a elektrokonvulzivní léčby chybějí, nicméně vzhledem k výsledkům experimentálních studií jsou klinické dopady této kombinace považovány za nepravděpodobné. Při léčbě agomelatinem se nedoporučuje konzumace alkoholu [1].
Dávkování
Agomelatin je k dispozici ve formě potahovaných tablet s obsahem účinné látky 25 mg. Užívá se perorálně jednou denně před spaním. Léčba se zahajuje dávkou 25 mg denně bez potřeby titrace. Pokud po 2 týdnech léčby nedojde ke zmírnění příznaků, je možné zvýšit dávku na 50 mg; i tato dávka (2 tablety) se podává najednou před spaním. Dávkování vychází z dvojitě zaslepených studií u pacientů s depresivní poruchou [1, 19]. Účinnost byla hodnocena pomocí škál MADRS a HAMD-17. Agomelatin je možno užívat nezávisle na jídle. Pro dosažení stabilní remise by léčba měla trvat nejméně 6 měsíců i po odeznění depresivní epizody. Pro ukončení léčby není nutné postupné vysazování dávky. U pacientů s poruchou funkce ledvin je doporučena opatrnost z důvodu nedostatku údajů o jeho použití u těchto populací. U pacientů s poškozením funkce jater je agomelatin kontraindikován [1].
Shrnutí
Agomelatin je svým novým mechanismem účinku prvním reprezentantem skupiny antidepresiv MASSA (Melatonin Agonist and Selective Serotonin Antagonist). Vykazuje vyšší afinitu k melatoninovým než k serotoninovým receptorům a z melatoninových pak vyšší afinitu k podtypům MT1 než MT2. Blokáda serotoninových receptorů 5-HT2C, která má též za následek uvolnění noradrenalinu a dopaminu v prefrontální kůře, se patrně podílí rozhodujícím způsobem na antidepresivním a anxiolytickém účinku a je pravděpodobně i na pozadí zvýšené hustoty pomalovlnného spánku, jež vede k lepší konsolidaci paměti [50, 51]. Nicméně podání specifických antagonistů receptorů 5-HT2C samo o sobě nevedlo ve zvířecích modelech k antidepresivní aktivitě, takže se zdá, že k antidepresivnímu působení agomelatinu je nezbytné kombinované ovlivnění serotoninových i melatoninových receptorů. Stimulace receptorů MT1 navozuje spánek a aktivace receptorů MT2 resynchronizuje cirkadiánní rytmus spánku a bdění. Obojí pak zvyšuje sekreci melatoninu. Všechny tyto parametry jsou u depresivní poruchy narušeny.
Ve většině studií vykazoval agomelatin v porovnání s placebem do dvou týdnů významný účinek na depresi (i těžkou) a úzkost. V porovnání s aktivními komparátory nebyl inferiorní co do účinku, byl velmi dobře snášen, nevedl k únavě přes den ani k sexuálním dysfunkcím, měl příznivý vliv na spánek a nedocházelo po jeho vysazení k syndromu z odnětí. Agomelatin byl neutrální k tělesné hmotnosti, neprodlužoval QT interval a při jeho podávání nedocházelo ke zvyšování tolerance. Diskuse k několika negativním studiím s akcentovaným účinkem placeba je podrobněji rozvedena v přehledu Švestky a Mohra [9].
Snášenlivost agomelatinu je velmi dobrá (z nežádoucích účinků byl pouze výskyt závratí vyšší než při podávání placeba), nicméně EMA na základě pozorovaného zvýšení sérových hladin aminostransferáz u přibližně 1 % léčených doporučila monitorovat jaterní testy (EMA, 2009 [1, 52]). Jako substrát CYP450 1A2 nesmí být kombinován se silnými inhibitory tohoto izoenzymu.
Další studie agomelatinu budou třeba k mapování účinnosti a hlavně bezpečnosti ve speciálních populacích (děti a dospívající, starší nemocní, pacienti s rezistentní depresí, s depresí s psychotickými příznaky, nemocní s narušením kognitivních funkcí aj.). To může dále rozšířit cílovou populaci nemocných, pro něž nové antidepresivum již nyní znamená přínos.
Seznam použité literatury
- [1] Valdoxan. Souhrn údajů o přípravku 03/2012, dostupné na http://www.ema.europa.eu
- [2] Audinot V, Mailliet F, Lahaye-Brasseur C, et al. New selective ligands of human cloned melatonin MT1 and MT2 receptors. Naunyn-Schmiedeberg’s Arch Pharmacol 2003; 367: 553–561.
- [3] Millan MJ, Gobert A, Lejeune F, et al. The novel melatonin agonist agomelatine (S20098) is an antagonist at 5-hydroxytryptamine 2c receptors, blockade of which enhances the activity of frontocortical dopaminergic and adrenergic pathways. J Pharmacol Exp Ther 2003; 306: 954–964.
- [4] Racagni G, Riva MA, Molteni R, et al. Mode of action of agomelatine: synergy between melatonergic and 5-HT(2C) receptors. World J Biol Psychiatry 2011; 12: 574–587.
- [5] Barbiero VS, Zappettini S, Mocaër E, et al. The novel antidepressant agomelatine reduces release of glutamate and related presynaptic mechanism in rat hippocampus (Abstract). Eur Neuropsychopharmacol 2007; 17 (Suppl. 4): 365.
- [6] Banasr M, Soumier A, Hery M, et al. Agomelatine, a new antidepressant, induces regional changes in hippocampal neurogenesis. Biol Psychiatry 2006; 59: 1087–1096.
- [7] Soumier A, Banasr M, Lortet S, et al. Mechanisms contributing to the phase-dependent regulation of neurogenesis by the novel antidepressant agomelatine, in the adult rat hippocampus. Neuropsychopharmacol 2009; 34: 2390–2403.
- [8] Paizanis E, Kelaï S, Renoir T, et al. Life-long hippocampal neurogenesis: environmental, pharmacological and neurochemical modulations. Neurochem Res 2007; 32 : 1762–1771.
- [9] Švestka J, Mohr P. Agomelatin – antidepresivum s novým mechanizmem působení. Psychiatrie 2010; 14: 98–108.
- [10] Švestka J. Agomelatin – nové melatonergní a serotonergní antidepresivum. Psychiatrie 2005; 9: 307–310.
- [11] Höschl C. Chronobiologie v lékařství. Bratisl Lek Listy 1989; 90: 300–308.
- [12] Emens J, Lewy A, Kinzie JM, et al. Circadian misalignment in major depressive disorder. Psychiatry Res 2009; 168: 259–261.
- [13] Corbach S, Schmelting B, Fuchs E, et al. Comparison of agomelatine and melatonin for effects in chronically stressed tree shrews, an animal model of depression. Eur Neuropsychopharmacol 2007; 17 (suppl 4): S364–S365.
- [14] Armstrong SM, MacNulty OM, Guardiola-Lemaitre B, et al. Successful use of S20098 and melatonin in an animal model of delayed sleep-phase syndrome (DSPS). Pharmacol Biochem Behav 1993; 46: 45–49.
- [15] Kasper S, Hajak G, Wulff K. Efficacy of the novel antidepressant agomelatine on the circadian rest-activity cycle and depressive and anxiety symptoms in patients with major depressive disorder: A randomized, double-blind comparison with sertraline. J Clin Psychiatry 2010; 71: 109–120.
- [16] Quera-Salva MA, Vanier B, Laredo J, et al. Major depressive disorder, sleep EGG and agomelatine: an open-label study. Int J Neuropsychopharmacol 2007; 10: 691–696.
- [17] Quera-Salva MA, Lemoine P, Guilleminault C. Impact of the novel antidepressant agomelatine on disturbed slep-wake cycles in depressed patients. Hum Psychopharmacol Clin Exp 2010; 25: 222–229.
- [18] Lemoine P, Guilleminault C, Alvarez E. Improvement in subjective sleep in major depressive disorder with a novel antidepressant, agomelatine: randomized, double-blind comparison with venlafaxine. J Clin Psychiatry 2007; 68: 1723–1732.
- [19] Loo H, Hale A, D´Haenen H, et al. Determination of the dose of agomelatine, a melatonergic agonist and selective 5-HT2C antagonist, in the treatment of major depressive disorder: a placebo-controlled dose range study. Int Clin Psychopharmacol 2002; 17: 239–247.
- [20] Kennedy SH, Emsley R. Placebo-controlled trial of agomelatine in the treatment of major depressive disorder. Eur Neuropsychopharmacol 2006; 16: 93–100.
- [21] Olie JP, Kasper S. Efficacy of agomelatine, a MT1/MT2 receptor agonist with 5-HT2C antagonistic properties, in major depressive disorder. Int J Neuropsychopharmacol 2007; 10: 661–673.
- [22] Stahl SM, Fava M, Trivedi MH, et al. Agomelatine in the treatment of major depressive disorder: an 8-week, multicenter, randomized, placebo-controlled trial. J Clin Psychiatry 2010; 71: 616–626.
- [23] Zajecka J, Schatzberg A, Stahl S, et. al. Efficacy and safety of agomelatine in the treatment of major depressive disorder: a multicenter, randomized, double-blind, placebo-controlled trial. J Clin Psychopharmacol 2010; 30: 135–144.
- [24] Kasper S, Hale A, Lemoine P, et al. Superior efficacy results of agomelatine in a pooled analysis versus SSRI/SNRI. Eur Neuropsychopharmacol 2010; 20: S348–S349.
- [25] Kennedy S, Loo H, Olié JP. The antidepressant efficacy of agomelatine is independent of gender, age, body mass index and use of concomitant anxiolytics: combined analysis of three placebo-controlled studies (Abstract). Int J Neuropsychopharmacol 2008b; 11 (Suppl. 1): 193.
- [26] Kennedy SH, Loo H, Olié JP, Montgomery SA. The efficacy of agomelatine accross distinct clinical populations of depressive patients (Abstract). World Psychiatry 2009; 8 (Suppl. 1): 182.
- [27] Demyttenaere K. Agomelatine: a narrative review. Eur Neuropsychopharmacol 2011; 21 (suppl 4): S703–709.
- [28] Stein DJ, Ahokas AA, de Bodinat C. Efficacy of Agomelatine in Generalized Anxiety Disorder. A Randomized, Double-Blind, Placebo-Controlled Study. J Clin Psychopharmacol 2008; 28: 561–566.
- [29] Gorwood P. Restoring circadian rhythms: a new way to successfully manage depression. J Psychopharmacol 2010; 24: 15–19.
- [30] Goodwin G, Emsley R, Rouillon F. Agomelatine prevents relapse in patients with Major Depressive Disorder without evidence of a discontinuation syndrome: A 24-week randomized, double-blind, placebo-controlled trial. J Clin Psychiatry 2009; 70: 1128–1137.
- [31] Goodwin GM, Rouillon F, Emsley R et al. Long-term treatment with agomelatine: prevention of relapse in patients with major depressive disorder over 10 months. Eur Neuropsychopharmacol 2008; 18 (suppl 4): S338.
- [32] Corruble E, Bélaidi C, Goodwin GM. Agomelatine versus escitalopram in major depressive disorders: a randomized double-blind, long term study focusing on sleep satisfaction and emotional blunting. Eur Psychiatry 2011; 26: P02–P24.
- [33] de Bodinat C, Guardiola-Lemaitre B, Mocaër E, et al. Agomelatine, the first melatonergic antidepressant: discovery, characterization and development. Nat Rev Drug Discov 2010; 9: 628–642.
- [34] Montgomery SA, Kasper S. Severe depression and antidepressants: focus on a pooled analysis of placebo-controlled studies on agomelatine. Int Clin Psychopharmacol 2007; 22: 283–291.
- [35] Hale A, Corral RM, Mencacci C, et al. Superior antidepressant efficacy results of agomelatine versus fluoxetine in severe MDD patients: a randomized, double-blind study. Int Clin Psychopharmacol 2010; 25: 305–314.
- [36] Quera-Salva MA, Hajak G, Philip P, et al. Comparison of agomelatine and escitalopram on nighttime sleep and daytime condition and efficacy in major depressive disorder patients. Int Clin Psychopharmacol 2011; 26: 252–262.
- [37] Harmer CJ, de Bodinat C, Dawson GR, et al. Agomelatine facilitates positive versus negative affective processing in healthy volunteer models. J Psychopharmacol 2011; 25: 1159–1167.
- [38] Laux G. Antidepressive Therapie mit Agomelatin der Farachspraxis. Psychopharmakotherapie 2011; 18: 18–26.
- [39] Ivanov SV, Samuchia MA. Agomelatine (Valdoxan) in clinical practice: Results from the Russian observational program CHRONOS. Int J Psychiatry Clin Pract 2011; 15 (S2): 15–42, P29.
- [40] Di Giannantonio M, Di Iorio G, Guglielmo R, et al. Major depressive disorder, anhedonia and agomelatine: an open-label study. J Biol Regul Homeostatic Agents 2011; 25: 109–114.
- [41] Novotny V, Pecenak J. Agomelatine in depression treatment, a multicentre study in Slovakia. Int J Psychiatry Clin Pract 2011; 15 (suppl 2): 33–34.
- [42] Calabrese JR, Guelfi JD, Perdrizet-Chevallier C; Agomelatine Bipolar Study Group. Agomelatine adjunctive therapy for acute bipolar depression: preliminary open data. Bipolar Disord 2007; 9: 628–635.
- [43] Pjrek E, Winkler D, Konstantinidis A, et al. Agomelatine in the treatment of seasonal affective disorder. Psychopharmacology (Berl) 2007; 190: 575–579.
- [44] Kennedy S, Rizvi S. Agomelatine in the treatment of major depressive disorder: Potential for clinical effectiveness. CNS Drugs 2010; 24: 479–499.
- [45] Kennedy SH, Rizvi S, Fulton K, Rasmussen J. A double-blind comparison of sexual functioning, antidepressant efficacy, and tolerability between agomelatine and venlafaxine-XR. J Clin Psychopharmacol 2008; 28: 329–333.
- [46] Montejo AL, Prieto N, Terleira A, et al. Better sexual acceptability of agomelatine (25 and 50 mg) compared with paroxetine (20 mg) in healthy male volunteers. An 8-week, placebo-controlled study using the PRSEXDQ-SALSEX scale. J Psychopharmacol 2010; 24: 111–120.
- [47] Žourková A. Sexuální funkce při léčbě depresivní poruchy agomelatinem. Psych pro praxi 2012; 13: 32–34.
- [48] Montgomery SA, Kennedy SH, Burrows GD, et al. Absence of discontinuation symptoms with agomelatine and occurrence of discontinuation symptoms with paroxetine: a randomized, double-blind, placebo-controlled discontinuation study. Int Clin Psychopharmacol 2004; 19: 271–280.
- [49] Krombholz R, Drástová H. Agomelatin – klinické zkušenosti u starších pacientů. Psychiatrie 2011; 15: 151–153.
- [50] Van Laar M, Volkerts E, Verbaten M. Subchronic effects of the GABA-agonist lorazepam and 5-HT2A/2C antagonist on driving performance, slow wave sleep and daytime sleepiness in healthy volunteers. Psychopharmacology 2001; 154: 189–197.
- [51] Walker MP. The role of slow wave sleep in memory processing. J Clin Sleep Medicine 2009; 5 (Suppl): 20–26.
- [52] EMEA-CHMP Assessment Report for Valdoxan; Procedure No. EMEA/H/C/000915; www.emea.europa.eu.
- [53] Racagni, G, Riva MA, Molteni R, et al. Mode of action of agomelatine: Synergy between melatonergic and 5-HT2C receptors. World J Biol Psychiatr 2011; 12: 574–587.