Sitagliptin
Sitagliptin, inhibitor dipeptidyl peptidázy 4, patří mezi nová antidiabetika. Má incidenci nežádoucích účinků shodnou s placebem, snížení glykémie dosahuje znovunastolením fyziologických poměrů v organismu. Účinnost sitagliptinu je srovnatelná s ostatními perorálními antidiabetiky. Právě pro tyto vlastnosti se sitagliptin řadí mezi farmaka s vysokým terapeutickým potenciálem. Ideálním místem v léčbě je kombinace s metforminem, je možné jej použít i v kombinaci s glitazony nebo s deriváty sulfonylurey. Registrován je i pro použití v trojkombinaci s derivátem sulfonylurey a metforminem.
Farmakologická skupina
Sitagliptin je perorální antidiabetikum. Je určen k farmakologické léčbě diabetes mellitus 2. typu. Je zařazen mezi inhibitory DPP-4, ATC kód je A10BH01.
Chemické a fyzikální vlastnosti
Sitagliptin je chemicky 7-[(3R)-3-amino-1-oxo-4-(2,4,5-trifluorophenyl)butyl]-5,6,7,8-tetrahydro-3-(trifluoromethyl)-1,2,4-triazolo[4,3-a]pyrazin fosfát (1 : 1) monohydrát (obr. 1) [20]. V léčivém přípravku se vyskytuje ve formě monohydrátu sitagliptinfosfátu.
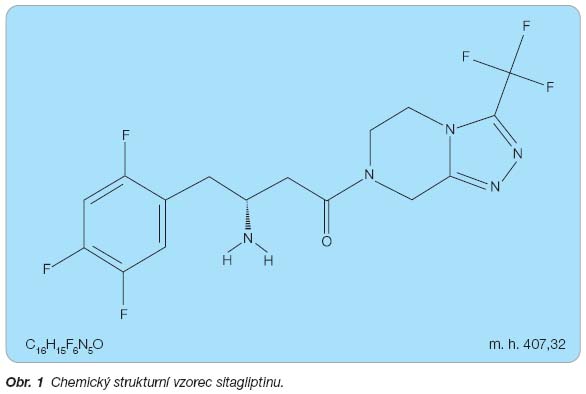 Sumární vzorec:
Sumární vzorec:
sitagliptin: C16H15F6N5O
monohydrát sitagliptinfosfátu: C16H18F6N5O5P . H2O
Molekulová hmotnost:
sitagliptin: 407,32
monohydrát sitagliptinfosfátu: 523,33  Sitagliptin je bílý nebo téměř bílý prášek. Sitagliptin je řazen do 3. kategorie klasifikačního systému BCS – jeho rozpustnost ve vodě je vysoká, avšak pronikání přes střevní stěnu je relativně pomalé. Sitagliptin je dobře rozpustný ve vodě (míra rozpustnosti závisí na pH), v ethanolu, acetonu, mírně rozpustný v methanolu, velmi těžce rozpustný v isopropanolu. Molekula obsahuje jedno chirální centrum, v přípravku je přítomen pouze R-enantiomer
Sitagliptin je bílý nebo téměř bílý prášek. Sitagliptin je řazen do 3. kategorie klasifikačního systému BCS – jeho rozpustnost ve vodě je vysoká, avšak pronikání přes střevní stěnu je relativně pomalé. Sitagliptin je dobře rozpustný ve vodě (míra rozpustnosti závisí na pH), v ethanolu, acetonu, mírně rozpustný v methanolu, velmi těžce rozpustný v isopropanolu. Molekula obsahuje jedno chirální centrum, v přípravku je přítomen pouze R-enantiomer
Mechanismus účinku a farmakodynamika
Inkretiny jsou hormony secernované střevními buňkami. Sekreci vyvolává prandiální podnět. Inkretiny jsou polypeptidy, jsou velmi rychle degradovány, a proto mají velmi krátký poločas. Hlavními mechanismy, kterými ovlivňují homeostázu glukózy, jsou: ovlivnění sekrece inzulinu závislé na glykémii, postprandiální suprese sekrece glukagonu a ovlivnění evakuace žaludku (obr. 2). Inkretiny však vykazují i celou řadu dalších pozitivních účinků, jejichž klinický význam je předmětem výzkumu. Z hlediska terapeutického využití pro léčbu diabetu je nejdůležitějším inkretinem glukagonu podobný peptid 1 (glucagon-like peptide-1, GLP-1) [1, 2].
Za bazálních podmínek je koncentrace GLP-1 v krvi relativně nízká, rychle vzrůstá po požití potravy. Vzestup hladiny je zprostředkován neuroendokrinně a současně přímým stimulačním účinkem potravy na buňky střevní sliznice [3].
U pacientů s diabetem 2. typu je typicky koncentrace GLP-1 snížená, nicméně jeho účinek je zachován [4]. U pacientů s diabetem 2. typu je snížená odpověď b-buněk na zvyšující se glykémii, tato porucha se upravuje po farmakologických dávkách GLP-1 [5]. O citlivosti a-buněk (secernují glukagon) pacientů s diabetem 2. typu na GLP-1 nejsou dostatečné zprávy.
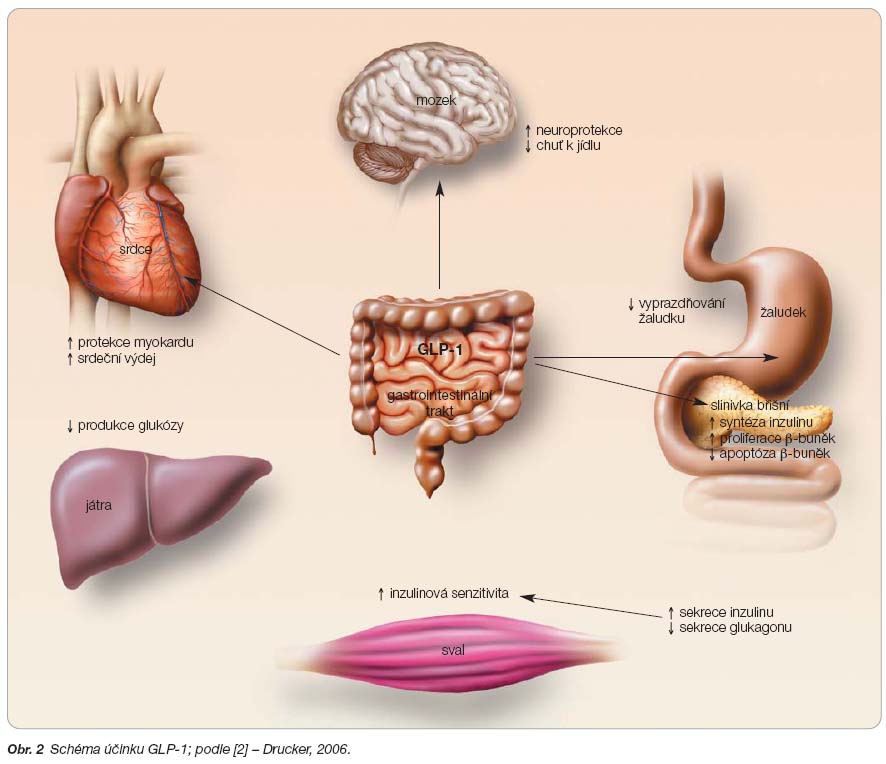 GLP-1 zpomaluje vyprazdňování žaludku, zvyšuje citlivost b-buněk k sekrečním podnětům, upravuje kvalitu sekrece inzulinu (obnovuje první fázi inzulinové sekrece) a snižuje sekreci glukagonu (účinek glukagonostatický), tím snižuje výdej glukózy hepatocyty. Byl prokázán příznivý efekt na b-buňky. Inhibuje apoptózu, zvyšuje proliferaci a diferenciaci z buněk duktulů. GLP-1 také snižuje chuť k jídlu. Svým komplexním účinkem ovlivňuje významněji postprandiální glykémii než glykémii nalačno. Účinek na sekreci inzulinu je tzv. glukózo-dependentní. To znamená, že se neprojevuje při normální nebo snížené glykémii, taktéž ustává při poklesu postprandiální glykémie na normální hodnotu. Z hlediska jeho případného terapeutického užití je nevýhodou velmi krátký poločas působení (minuty). Jsou studovány účinky GLP-1 na kardiovaskulární systém, zdá se, že protektivně působí na myokard při ischémii, zlepšuje funkci myokardu u pacientů se srdečním selháním [6, 7].
GLP-1 zpomaluje vyprazdňování žaludku, zvyšuje citlivost b-buněk k sekrečním podnětům, upravuje kvalitu sekrece inzulinu (obnovuje první fázi inzulinové sekrece) a snižuje sekreci glukagonu (účinek glukagonostatický), tím snižuje výdej glukózy hepatocyty. Byl prokázán příznivý efekt na b-buňky. Inhibuje apoptózu, zvyšuje proliferaci a diferenciaci z buněk duktulů. GLP-1 také snižuje chuť k jídlu. Svým komplexním účinkem ovlivňuje významněji postprandiální glykémii než glykémii nalačno. Účinek na sekreci inzulinu je tzv. glukózo-dependentní. To znamená, že se neprojevuje při normální nebo snížené glykémii, taktéž ustává při poklesu postprandiální glykémie na normální hodnotu. Z hlediska jeho případného terapeutického užití je nevýhodou velmi krátký poločas působení (minuty). Jsou studovány účinky GLP-1 na kardiovaskulární systém, zdá se, že protektivně působí na myokard při ischémii, zlepšuje funkci myokardu u pacientů se srdečním selháním [6, 7].
GLP-1 se váže na specifické receptory, po jejich aktivaci se zvyšuje obsah cAMP v buňce. K tomu, aby se zvýšila sekrece inzulinu z b-buněk, je zapotřebí glukózy. GLP-1 tak můžeme považovat za „senzitizér“, neboť zvyšuje stimulační účinek glukózy na sekreci inzulinu.
GLP-1 je degradován ubikviterně přítomným enzymen s názvem dipeptidyl peptidáza 4 (DPP-4), což je aminopeptidáza odštěpující dipeptidy z N-konce peptidů a proteinů. Tento enzym degraduje vedle inkretinů ještě celou řadu dalších substancí, nicméně, a to je z hlediska klinického velmi důležité, mimo inkretiny jsou ostatní peptidy a proteiny deaktivovány ještě ostatními typy dipeptidyl peptidáz. DPP-4 je shodná s T-lymfocytárním membránovým proteinem CD 26 [8].
Látky, které blokují aktivní místo uvedené aminopeptidázy, se nazývají inhibitory DPP-4, zkráceně gliptiny. Dovedou zablokovat aktivitu enzymu, následně je zastaveno odbourávání jeho přirozeného substrátu GLP-1, jehož plazmatická koncentrace se proto významně zvýší (a prodlouží se poločas).
Vlastní účinek sitagliptinu – inhibitoru DPP-4 – tedy spočívá v prodloužení biologického poločasu GLP-1 cestou inhibice jeho degradace. Akutním efektem sitagliptinu je snížení glykémie zprostředkované zvýšením sekrece inzulinu. Prokazatelný je vliv nejen na glykémii nalačno, ale také na výšku postprandiální glykémie. Dalším významným efektem sitagliptinu je jeho schopnost znovu nastavit normální citlivost b-buněk Langerhansových ostrůvků, a tak obnovit první fázi inzulinové sekrece.
Podstatná se jeví skutečnost, že snížení glykémie po léčbě sitagliptinem je důsledkem nejen ovlivnění sekrece inzulinu, ale také přímým důsledkem snížené sekrece glukagonu. Pokles glukagonémie snižuje zejména produkci glukózy v játrech. Bylo prokázáno, že právě snížení sekrece glukagonu se podílí významně na snížení postprandiální exkurze glykémie [9].
Sitagliptin je selektivní pro DPP-4 a in vitro neinhibuje aktivitu DPP-8 ani DPP-9 při koncentraci blížící se koncentraci terapeutických dávek podaných in vivo.
V terapeutických dávkách sitagliptin zablokuje aktivitu DPP-4 na dobu 24 hodin. To vede ke dvoj- až trojnásobnému zvýšení koncentrací aktivního GLP-1, snížení koncentrace glukagonu, zvýšení odezvy uvolnění inzulinu na sekreční podnět.
Účinky GLP-1 a GIP (na glukóze závislý inzulinotropní peptid) jsou závislé na glukóze, a to tak, že při nízkých koncentracích glukózy v krvi není stimulace uvolňování inzulinu ani potlačování sekrece glukagonu ze strany GLP-1 pozorováno. Pro GLP-1 i GIP platí, že stimulace uvolňování inzulinu je zesílena při vzestupu glukózy nad normální koncentrace. Dále platí, že GLP-1 neovlivňuje negativně normální odpověď glukagonu na hypoglykémii. U nemocných diabetiků 2. typu nehraje GIP vlivem poruchy na intracelulární úrovni tak významnou roli jako GLP-1. Glukózo-dependentní mechanismus sitagliptinu je odlišný od mechanismu účinku derivátů sulfonylurey, které zvyšují sekreci inzulinu i při nízké koncentraci glukózy, a mohou tak u pacientů s diabetem mellitem 2. typu a u zdravých jedinců způsobovat hypoglykémii.
Sitagliptin má tedy glukózo-dependentní efekt. To znamená, že sitagliptin nezvyšuje sekreci inzulinu při normální hladině glykémie. Proto u zdravých osob sitagliptin nevede k hypoglykémii, u pacientů s diabetem nezvyšuje riziko hypoglykémie.
Farmakokinetické vlastnosti
Absorpce
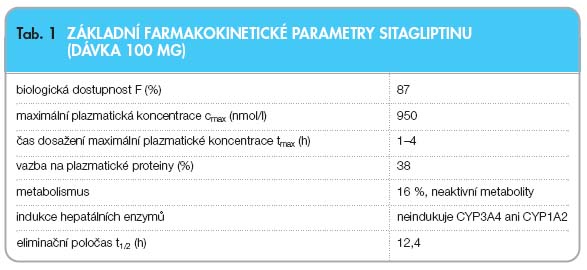 Následně po jednorázovém perorálním podání dávky 100 mg zdravým dobrovolníkům byl sitagliptin rychle vstřebán, s vrcholem plazmatické koncentrace (medián tmax) 1–4 hodiny po podání, cmax byla 950 nmol/l (tab. 1). Absolutní biologická dostupnost sitagliptinu je přibližně 87 %. Protože současná konzumace vysoce tučného jídla a sitagliptinu nemá vliv na farmakokinetiku, lze uvedený přípravek užívat spolu s jídlem nebo bez něj.
Následně po jednorázovém perorálním podání dávky 100 mg zdravým dobrovolníkům byl sitagliptin rychle vstřebán, s vrcholem plazmatické koncentrace (medián tmax) 1–4 hodiny po podání, cmax byla 950 nmol/l (tab. 1). Absolutní biologická dostupnost sitagliptinu je přibližně 87 %. Protože současná konzumace vysoce tučného jídla a sitagliptinu nemá vliv na farmakokinetiku, lze uvedený přípravek užívat spolu s jídlem nebo bez něj.
Distribuce
Průměrný distribuční objem v ustáleném stavu po jediné intravenózní dávce 100 mg sitagliptinu zdravým dobrovolníkům je přibližně 198 litrů. Podíl sitagliptinu reverzibilně vázaného na bílkoviny v plazmě je nízký (38 %).
Metabolismus
Sitagliptin se vylučuje v nezměněné podobě převážně močí (79 %) a metabolismus představuje méně důležitou cestu. Přibližně 16 % sitagliptinu se vylučuje ve formě metabolitů, nepředpokládá se, že by přispívaly k inhibičnímu účinku sitagliptinu na DPP-4 v plazmě. Studie in vitro prokázaly, že hlavním enzymem odpovídajícím za omezený metabolismus sitagliptinu je CYP3A4 s přispěním CYP2C8 [10].
Eliminace
Po podání perorální dávky radioaktivně značeného (14C)sitagliptinu zdravým dobrovolníkům se přibližně 100 % podaného přípravku během jednoho týdne vyloučilo stolicí (13 %) nebo močí (87 %). Sitagliptin se tedy vylučuje převážně ledvinami, a to aktivní tubulární sekrecí [10]. Biologický poločas sitagliptinu byl 12,4 hod.
Speciální populace
U pacientů s mírnou renální nedostatečností nedošlo ve srovnání s normálními zdravými kontrolními jedinci ke klinicky významnému vzestupu plazmatické koncentrace sitagliptinu. Ve srovnání s normálními zdravými kontrolními jedinci bylo přibližně dvojnásobné zvýšení hodnoty AUC sitagliptinu v plazmě pozorováno u pacientů se středně těžkou renální nedostatečností a přibližně čtyřnásobné zvýšení u pacientů s těžkou renální nedostatečností a u hemodialyzovaných pacientů s ESRD. Sitagliptin se v menší míře odstraňoval z organismu hemodialýzou (13,5 % během 3–4hodinové hemodialýzy zahájené 4 hodiny po podání dávky). Sitagliptin se proto nedoporučuje používat u pacientů se středně těžkou nebo těžkou renální nedostatečností včetně pacientů s ESRD, protože zkušenosti se sitagliptinem v léčbě těchto pacientů jsou příliš omezené [10].
U pacientů s mírnou až středně těžkou jaterní nedostatečností (Childovo-Pughovo skóre ≤ 9) není nutno dávkování sitagliptinu upravovat. U pacientů s těžkou jaterní nedostatečností (Childovo-Pughovo skóre > 9) nejsou k dispozici žádné klinické zkušenosti. Protože se však sitagliptin vylučuje převážně ledvinami, nepředpokládá se, že by těžká jaterní nedostatečnost farmakokinetiku sitagliptinu nějak ovlivňovala [10]. Podle farmakokinetických studií není nutná úprava dávky ve vztahu k body mass indexu, pohlaví ani primárně podle věku [10]. Nebyly provedeny žádné studie se sitagliptinem u dětských pacientů. Intraindividuální a interindividuální variabilita parametrů farmakokinetiky je velmi nízká.
Klinické zkušenosti
Sitagliptin byl testován standardním procesem klinických studií. Doposud byly zveřejněny výsledky studií, do nichž byly zahrnuty téměř 4000 pacientů s diabetem 2. typu. Byla hodnocena zejména účinnost, bezpečnost, vliv na funkci b-buněk. Sitagliptin byl testován jako lék první volby v monoterapii u pacientů neúspěšně léčených pouze režimovými opatřeními, dále jako lék přidaný do dvojkombinace po selhání základní léčby metforminem nebo v iniciální léčbě dvojkombinací s metforminem. Poslední uveřejněné výsledky ukazují dobrý efekt sitagliptinu použitého v trojkombinaci s metforminem a sulfonylureou. V roce 2007 byla uveřejněna metaanalýza, která hodnotila klinickou účinnost a bezpečnost léčby založené na inkretinech [11]. I když bylo v této metaanalýze hodnocení souhrnné pro oba inhibitory DPP-4, potvrdila dobrou účinnost nového způsobu léčby diabetu 2. typu.
Klinické studie potvrzují dobrou klinickou účinnost sitagliptinu v monoterapii i v kombinované léčbě, účinnost je srovnatelná s potenciálem ostatních standardně používaných perorálních antidiabetik. Při léčbě v kombinaci s metforminem je konečné zlepšení kompenzace větší než pouhý součet účinků obou látek samostatně (synergický efekt, viz dále). Z klinického pohledu je velmi významné, že sitagliptin nezvyšuje v naprosté většině všech studií riziko hypoglykémie, dále že má neutrální efekt na hmotnost pacientů. Účinek sitagliptinu se zvyšuje s horší kompenzací diabetu na začátku léčby. Právě tyto vlastnosti jej budou stavět na místo první volby, zejména u pacientů s diabetem 2. typu, který netrvá ještě dlouho.
Sitagliptin v monoterapii
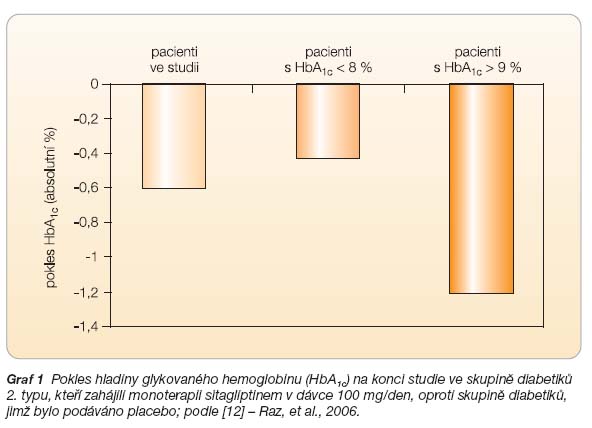 Účinnost sitagliptinu hodnotila prospektivní, randomizovaná, placebem kontrolovaná studie trvající 18 týdnů, v níž byl sitagliptin použit jako iniciální monoterapie u pacientů s diabetem 2. typu nedostatečně kompenzovaných režimovými opatřeními (n = 521). Primárním cílem bylo prokázat účinnost a bezpečnost sitagliptinu v dávce 100 mg a 200 mg denně oproti placebu. Bylo dosaženo statisticky významného průměrného poklesu o 0,6 % HbA1c (100 mg sitagliptinu) proti placebu. U osob s velmi špatnou vstupní kompenzací (HbA1c > 9 % dle DCCT) poklesla hladina glykohemoglobinu během užívání 100 mg sitagliptinu denně v průměru až o 1,2 % (graf 1). U pacientů léčených sitagliptinem se prokazatelně zlepšila funkce b-buněk. Ve studii nebyly zaznamenány žádné závažné nežádoucí příhody ve vztahu k aktivní léčbě sitagliptinem. Po léčbě sitagliptinem došlo ke snížení hmotnosti, které se však nelišilo statisticky významně od změn hmotnosti po podávání placeba. Nebyla zaznamenána vyšší incidence hypoglykémií ani nežádoucích gastrointestinálních účinků. Účinek sitagliptinu byl zřetelně vyšší u pacientů, u nichž diabetes netrval dlouho [12].
Účinnost sitagliptinu hodnotila prospektivní, randomizovaná, placebem kontrolovaná studie trvající 18 týdnů, v níž byl sitagliptin použit jako iniciální monoterapie u pacientů s diabetem 2. typu nedostatečně kompenzovaných režimovými opatřeními (n = 521). Primárním cílem bylo prokázat účinnost a bezpečnost sitagliptinu v dávce 100 mg a 200 mg denně oproti placebu. Bylo dosaženo statisticky významného průměrného poklesu o 0,6 % HbA1c (100 mg sitagliptinu) proti placebu. U osob s velmi špatnou vstupní kompenzací (HbA1c > 9 % dle DCCT) poklesla hladina glykohemoglobinu během užívání 100 mg sitagliptinu denně v průměru až o 1,2 % (graf 1). U pacientů léčených sitagliptinem se prokazatelně zlepšila funkce b-buněk. Ve studii nebyly zaznamenány žádné závažné nežádoucí příhody ve vztahu k aktivní léčbě sitagliptinem. Po léčbě sitagliptinem došlo ke snížení hmotnosti, které se však nelišilo statisticky významně od změn hmotnosti po podávání placeba. Nebyla zaznamenána vyšší incidence hypoglykémií ani nežádoucích gastrointestinálních účinků. Účinek sitagliptinu byl zřetelně vyšší u pacientů, u nichž diabetes netrval dlouho [12].
Také další prospektivní, randomizovaná kontrolovaná klinická studie v délce 24 týdnů hodnotila účinnost a bezpečnost sitagliptinu v dávkách 100 mg a 200 mg podávaných jednou denně ve srovnání s placebem. Výsledný pokles glykovaného hemoglobinu byl statisticky významný, činil průměrně 0,79 % HbA1c po léčbě dávkou 100 mg/den a 0,94 % po podávání dávky 200 mg/den sitagliptinu. Opět u pacientů se špatnou vstupní kompenzací (HbA1c > 9 % dle DCCT) poklesla hladina glykovaného hemoglobinu po dávkování 100 mg/den sitagliptinu v průměru až o 1,52 % proti placebu. Efekt dávky 100 mg/den a 200 mg/den sitagliptinu byl velmi blízký. Postprandiální glykémie ve 120. minutě po definovaném jídle se snížila o 2,6 mmol/l po léčbě sitagliptinem v dávce 100 mg/den a o 3,0 mmol/l po léčbě sitagliptinem v dávce 200 mg/den. U pacientů léčených sitagliptinem se prokazatelně zlepšila funkce b-buněk. Po léčbě sitagliptinem nebyla zaznamenána vyšší incidence hypoglykémií [13].
Sitagliptin v kombinované léčbě
Cílem 24týdenní, prospektivní, randomizované studie kontrolované placebem bylo prokázat klinickou efektivitu a tolerabilitu sitagliptinu přidaného k léčbě pioglitazonem a podávaného v dávce 100 mg jednou denně (po vymývací periodě byla jeho dávka 30 mg nebo 45 mg pro die) u pacientů s diabetem 2. typu [14]. Celkový počet pacientů, kteří vstoupili do studie, byl 175. Zlepšení proti placebové větvi činilo průměrně 0,7 % HbA1c. Po léčbě sitagliptinem se zlepšil poměr proinzulin/inzulin a snížila se koncentrace proinzulinu v plazmě. Ve studii nebyla incidence hypoglykémií v aktivní větvi statisticky významně vyšší ve srovnání se skupinou placeba. Stejně tak vliv na hmotnost byl shodný s placebem. S ohledem na mechanismus účinku je vhodná i kombinace sitagliptinu s metforminem, jak prokázala 24týdenní prospektivní, randomizovaná a placebem kontrolovaná klinická studie, v níž bylo 100 mg/den sitagliptinu přidáno ke stávající léčbě metforminem [15]. Dávka metforminu byla stabilní, 1500 mg 1krát denně nebo více. Cílem studie bylo prokázat účinnost a bezpečnost léčby sitagliptinem. Intervenovaný soubor byl tvořen 701 pacienty s diabetem 2. typu nedostatečně kompenzovanými monoterapií metforminem. Výsledný pokles HbA1c o průměrných 0,65 % proti placebu byl statisticky významný. Ve studii bylo po léčbě sitagliptinem zjištěno statisticky významné zlepšení parametrů popisujících funkci b-buněk. Nebylo zaznamenáno zvýšené riziko hypoglykémií, nežádoucích gastrointestinálních účinků a pokles hmotnosti byl stejný jako v placebové větvi.
V případě, že je léčba sitagliptinem zahájena společně s metforminem, je možno očekávat ještě vyšší účinnost. V prospektivní randomizované studii kontrolované placebem byl hodnocen efekt léčby kombinací sitagliptinu s metforminem [16]. Cílem bylo zjistit účinnost a bezpečnost této kombinace. Ve studii trvající 24 týdnů bylo randomizováno 1091 pacientů s diabetem 2. typu nedostatečně kompenzovaných režimovými opatřeními. Kohorta byla rozdělena do šesti větví, v nichž byly užity následující intervence: kombinace sitagliptin 100 mg/den + 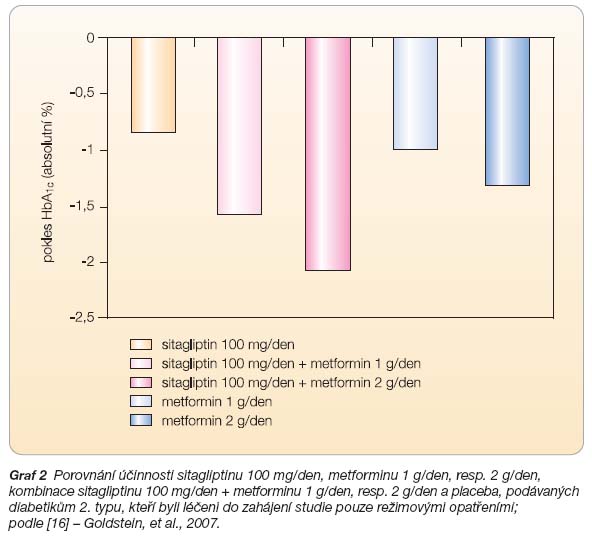 metformin 1000 mg, resp. 2000 mg/den, dále samostatně metformin 1000 mg/den, resp. 2000 mg/den, samostatně podávaný sitagliptin 100 mg/den a placebo. Na konci sledování bylo dosaženo nejhlubšího poklesu glykovaného hemoglobinu průměrně o 2,07 % oproti placebu (vyjádřeno v absolutní hodnotě) ve skupině léčené kombinací 100 mg sitagliptinu a 2 g metforminu (graf 2). Ve skupině 79 pacientů, kteří byli zahrnuti do otevřené kohorty a dokončili sledování (vstupní HbA1c 11,2 %), byl absolutní pokles HbA1c o 3,5 %! Riziko hypoglykémie po léčbě sitagliptinem nebylo zvýšeno oproti aktivnímu komparátoru, stejně tak nebyla významně vyšší incidence ostatních nežádoucích účinků. Tyto příznivé výsledky vedly k podrobnějšímu výzkumu. Bylo prokázáno, že metformin působí se sitagliptinem komplementárně, neboť metformin zvyšuje hladiny endogenního GLP-1, a to jak celkového, tak i jeho aktivní složky [17]. Hovoříme tedy o výsledném synergickém účinku, což znamená, že při současné léčbě oběma farmaky je zlepšení kompenzace větší než prostý součet potenciálního efektu obou léčiv užitých samostatně.
metformin 1000 mg, resp. 2000 mg/den, dále samostatně metformin 1000 mg/den, resp. 2000 mg/den, samostatně podávaný sitagliptin 100 mg/den a placebo. Na konci sledování bylo dosaženo nejhlubšího poklesu glykovaného hemoglobinu průměrně o 2,07 % oproti placebu (vyjádřeno v absolutní hodnotě) ve skupině léčené kombinací 100 mg sitagliptinu a 2 g metforminu (graf 2). Ve skupině 79 pacientů, kteří byli zahrnuti do otevřené kohorty a dokončili sledování (vstupní HbA1c 11,2 %), byl absolutní pokles HbA1c o 3,5 %! Riziko hypoglykémie po léčbě sitagliptinem nebylo zvýšeno oproti aktivnímu komparátoru, stejně tak nebyla významně vyšší incidence ostatních nežádoucích účinků. Tyto příznivé výsledky vedly k podrobnějšímu výzkumu. Bylo prokázáno, že metformin působí se sitagliptinem komplementárně, neboť metformin zvyšuje hladiny endogenního GLP-1, a to jak celkového, tak i jeho aktivní složky [17]. Hovoříme tedy o výsledném synergickém účinku, což znamená, že při současné léčbě oběma farmaky je zlepšení kompenzace větší než prostý součet potenciálního efektu obou léčiv užitých samostatně.
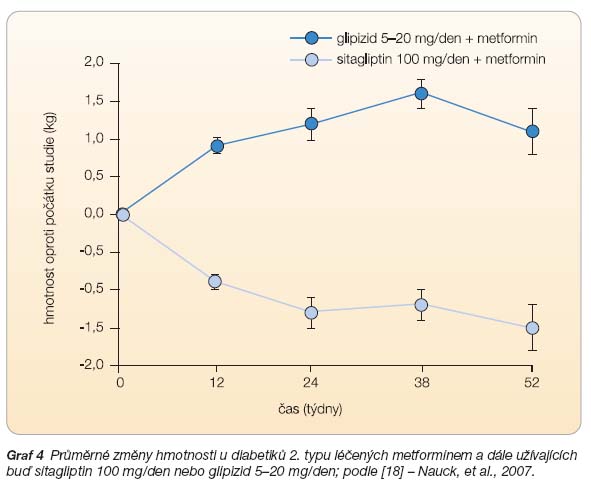
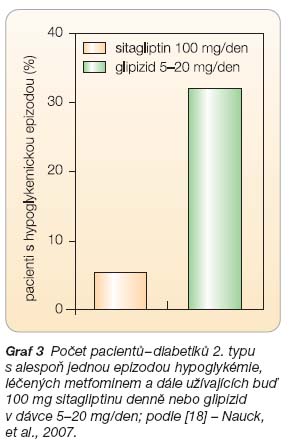 V roce 2007 byly uveřejněny výsledky 52týdenní prospektivní, dvojitě slepé studie kontrolované placebem [18], která porovnávala účinnost a bezpečnost léčby sitagliptinem (100 mg/den) oproti glipizidu (byl titrován v dávkách od 5 do 20 mg). Studie byla koncipována jako non-inferiorní. Ve studii bylo randomizováno 1172 pacientů s nedostatečně kompenzovaným diabetem 2. typu léčených stabilní dávkou metfominu (nejméně 1500 mg denně). Snížení glykovaného hemoglobinu bylo na konci studie shodné v obou větvích (průměrný pokles o 0,67 %). Pouze 5 % pacientů, kteří byli léčeni sitagliptinem, mělo epizodu hypoglykémie, což je významně méně oproti 32 % pacientů léčených glipizidem (graf 3). Stejně tak ve prospěch sitagliptinu hovoří výsledný pokles hmotnosti (průměrné snížení o 1,5 kg), osoby léčené glipizidem v průměru zvýšily tělesnou hmotnost o 1,1 kg (graf 4). Tato non-inferiorní studie potvrdila klinicky velmi dobrou účinnost sitagliptinu, plně srovnatelnou s efektem klasického derivátu sulfonylurey, a to současně při minimálním riziku hypoglykémie.
V roce 2007 byly uveřejněny výsledky 52týdenní prospektivní, dvojitě slepé studie kontrolované placebem [18], která porovnávala účinnost a bezpečnost léčby sitagliptinem (100 mg/den) oproti glipizidu (byl titrován v dávkách od 5 do 20 mg). Studie byla koncipována jako non-inferiorní. Ve studii bylo randomizováno 1172 pacientů s nedostatečně kompenzovaným diabetem 2. typu léčených stabilní dávkou metfominu (nejméně 1500 mg denně). Snížení glykovaného hemoglobinu bylo na konci studie shodné v obou větvích (průměrný pokles o 0,67 %). Pouze 5 % pacientů, kteří byli léčeni sitagliptinem, mělo epizodu hypoglykémie, což je významně méně oproti 32 % pacientů léčených glipizidem (graf 3). Stejně tak ve prospěch sitagliptinu hovoří výsledný pokles hmotnosti (průměrné snížení o 1,5 kg), osoby léčené glipizidem v průměru zvýšily tělesnou hmotnost o 1,1 kg (graf 4). Tato non-inferiorní studie potvrdila klinicky velmi dobrou účinnost sitagliptinu, plně srovnatelnou s efektem klasického derivátu sulfonylurey, a to současně při minimálním riziku hypoglykémie.
 Cílem následující 24týdenní, prospektivní, randomizované, dvojitě zaslepené a placebem kontrolované studie bylo vyhodnocení účinnosti a bezpečnosti sitagliptinu v léčbě pacientů nedostatečně kompenzovaných terapií glimepiridem samotným nebo v kombinaci s metforminem [19]. Ve studii bylo randomizováno 441 pacientů s diabetem 2. typu. Sitagliptin (100 mg/den) nebo placebo byly přidány k léčbě samotným glimepiridem (4 mg a více denně) nebo kombinací glimepiridu a metforminu (1500 mg denně a více). Po léčbě sitagliptinem došlo k průměrnému snížení glykovaného hemoglobinu o 0,74 % (absolutní hodnota) proti placebu, ve skupině léčené dvojkombinací glimepirid plus metformin snížilo přidání 100 mg sitagliptinu glykovaný hemoglobin dále o průměrných 0,89 % ve srovnání s placebem. V této jediné klinické studii byla nalezena vyšší incidence hypoglykémií proti placebové skupině. Při léčbě diabetu obecně platí, že čím více se léčivy snižuje cílová průměrná hodnota glykémie (resp. glykovaného hemoglobinu), tím více se zvyšuje riziko hypoglykémie. Sitagliptin má však glukózo-dependentní účinek, což znamená, že po normalizaci glykémie přestává působit, a proto je riziko při léčbě sitagliptinem samotným či v kombinaci s metforminem nebo s glitazony shodné s rizikem po podávání placeba. Při snížení průměrné glykémie kombinovanou léčbou sitagliptinem s deriváty sulfonylurey je riziko hypoglykémie nutně zvýšeno, za toto zvýšení je však zodpovědný účinek vlastní glimepiridu. Sitagliptin přidaný ke glimepiridu snížil významně průměrnou glykémii, proto se tito nemocní dostali do vyššího rizika hypoglykémie ve srovnání s placebovou skupinou. Při okamžitém poklesu glykémie u těchto nemocných na normální hodnotu přestane sitagliptin účinkovat, nicméně efekt glimepiridu, “tvrdého“ inzulinového sekretagoga, trvá dále. Tuto tezi potvrzuje srovnání s výsledky studie GUIDE [20]. Celková incidence hypoglykémií ve výše uvedené studii je blízká incidenci hypoglykemických příhod při monoterapii glimepiridem ve studii GUIDE, přičemž výsledná úroveň dosažené kompenzace je srovnatelná.
Cílem následující 24týdenní, prospektivní, randomizované, dvojitě zaslepené a placebem kontrolované studie bylo vyhodnocení účinnosti a bezpečnosti sitagliptinu v léčbě pacientů nedostatečně kompenzovaných terapií glimepiridem samotným nebo v kombinaci s metforminem [19]. Ve studii bylo randomizováno 441 pacientů s diabetem 2. typu. Sitagliptin (100 mg/den) nebo placebo byly přidány k léčbě samotným glimepiridem (4 mg a více denně) nebo kombinací glimepiridu a metforminu (1500 mg denně a více). Po léčbě sitagliptinem došlo k průměrnému snížení glykovaného hemoglobinu o 0,74 % (absolutní hodnota) proti placebu, ve skupině léčené dvojkombinací glimepirid plus metformin snížilo přidání 100 mg sitagliptinu glykovaný hemoglobin dále o průměrných 0,89 % ve srovnání s placebem. V této jediné klinické studii byla nalezena vyšší incidence hypoglykémií proti placebové skupině. Při léčbě diabetu obecně platí, že čím více se léčivy snižuje cílová průměrná hodnota glykémie (resp. glykovaného hemoglobinu), tím více se zvyšuje riziko hypoglykémie. Sitagliptin má však glukózo-dependentní účinek, což znamená, že po normalizaci glykémie přestává působit, a proto je riziko při léčbě sitagliptinem samotným či v kombinaci s metforminem nebo s glitazony shodné s rizikem po podávání placeba. Při snížení průměrné glykémie kombinovanou léčbou sitagliptinem s deriváty sulfonylurey je riziko hypoglykémie nutně zvýšeno, za toto zvýšení je však zodpovědný účinek vlastní glimepiridu. Sitagliptin přidaný ke glimepiridu snížil významně průměrnou glykémii, proto se tito nemocní dostali do vyššího rizika hypoglykémie ve srovnání s placebovou skupinou. Při okamžitém poklesu glykémie u těchto nemocných na normální hodnotu přestane sitagliptin účinkovat, nicméně efekt glimepiridu, “tvrdého“ inzulinového sekretagoga, trvá dále. Tuto tezi potvrzuje srovnání s výsledky studie GUIDE [20]. Celková incidence hypoglykémií ve výše uvedené studii je blízká incidenci hypoglykemických příhod při monoterapii glimepiridem ve studii GUIDE, přičemž výsledná úroveň dosažené kompenzace je srovnatelná.
Zařazení do současné palety léčiv
Sitagliptin je představitelem nejnovějšího způsobu léčby diabetu 2. typu, která je založena na inkretinovém efektu. Tato léčba je velkým příslibem, neboť dle současných výsledků klinického výzkumu je provázena velmi nízkým rizikem nežádoucích účinků. Riziko vzniku hypoglykémie (vyjma kombinace s deriváty sulfonylurey) je stejné jako po podávání placeba. Vliv na hmotnost je prakticky neutrální, v některých studiích dokonce s tendencí snižování tělesné hmotnosti. Toto vše při vlastní antihyperglykemické účinnosti srovnatelné s ostatními perorálními antidiabetiky. Můžeme oprávněně předpokládat, že u vhodně zvolených indikací bude v reálné praxi léčba sitaglitinem velmi úspěšná, neboť právě nežádoucí účinky často snižují compliance pacientů. Typicky opakované, byť jenom lehké hypoglykémie po léčbě deriváty sulfonylurey inspirují nemocné k přejídání se, což vede ke zvyšování hmotnosti. Část potenciálu léčby se tak „spotřebuje“ na vyrovnání zvýšené inzulinové rezistence v důsledku přírůstku hmotnosti.
Sitagliptin je také představitelem nové terapie, která je založena na rozpoznání fyziologie a patofyziologie diabetu 2. typu. Obecně je takováto léčba šetrnější a bezpečnější, což sitagliptin zatím jednoznačně naplňuje.
Podle výsledků klinických studií a s ohledem na platná omezení SPC bude asi nejvhodnější poloha sitagliptinu v klinické praxi následující: ideální lék druhé volby u pacientů nedostatečně kompenzovaných režimovými opatřeními a léčbou metforminem. Dále, lék druhé volby v kombinaci s deriváty sulfonylurey nebo s glitazony při nesnášenlivosti léčby metforminem. Jako třetí lék do kombinace s metforminem a deriváty sulfonylurey při nedostatečném efektu režimových opatření a dvojkombinace. Speciální indikací může být situace, kdy u nemocných pacientů potřebujeme minimalizovat riziko hypoglykémie. Sitagliptin nemá smysl podávat jako náhradu jiného perorálního antidiabetika, ale naopak jako další zintenzivnění stávající léčby (výjimkou může být náhrada deriváty sulfonyurey k zamezení hypoglykémií). Toto je poznatek zásadní důležitosti pro praxi, neboť potenciál sitagliptinu snížit glykémii je přibližně shodný s ostatními perorálními antidiabetiky, a tak, pokud zaměníme jedno za druhé, nelze v naprosté většině případů očekávat zlepšení kompenzace diabetu.
Pozornost si zaslouží ještě dva aspekty. S ohledem na synergický účinek je velmi výhodná kombinace s metforminem, proto je připravována tableta s fixní kombinací obou látek. Předmětem dlouhodobého výzkumu jsou další, potenciálně velmi výhodné vlastnosti. Zatím víme, že v krátkodobých a střednědobých studiích sitagliptin zlepšuje funkci b-buněk. Otázkou zůstává, jak se tento vliv projeví po více letech léčby (ve vztahu ke známé skutečnosti, že právě úbytek sekreční kapacity b-buněk zodpovídá za postupné zhoršování diabetu 2. typu).
Indikace
Sitagliptin je nejčastěji podáván jako lék druhé volby u pacientů nedostatečně kompenzovaných režimovými opatřeními a metforminem. Dále jako lék druhé volby v kombinaci s deriváty sulfonylurey nebo s glitazony při nesnášenlivosti metforminu. Rovněž se podává jako třetí látka do kombinace s metforminem a deriváty sulfonylurey při nedostatečném efektu režimových opatření a dvojkombinace. Podán může být také pacientům, u nichž je nutno minimalizovat riziko hypoglykémie.
Kontraindikace
Přecitlivělost na účinnou látku nebo na pomocné látky obsažené v přípravku.
Nežádoucí účinky
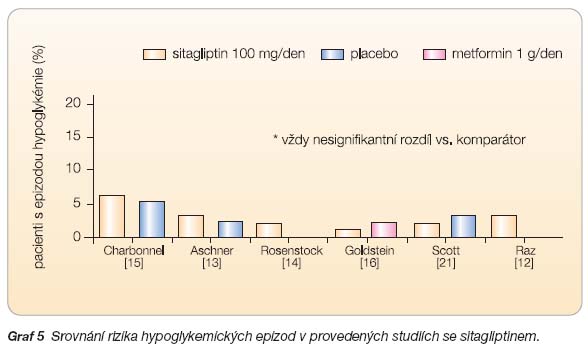 Běžné nežádoucí účinky zaznamenané v klinických studiích mají incidenci shodnou s placebem. Byla zaznamenána mírně zvýšená incidence nazofaryngitid a infekcí horních cest dýchacích [10]. V provedené metaanalýze, kde však byly zahrnuty oba registrované inhibitory DPP-4, byla navíc zvýšená incidence infekcí uropoetického aparátu [11]. Vyšší incidence v porovnání s placebem je také v případě bolestí hlavy. Vliv na tělesnou hmotnost je prakticky neutrální, což je zásadní rozdíl proti doposud běžně užívaným perorálním antidiabetikům, jejichž podávání obvykle vede ke zvýšení tělesné hmotnosti pacientů s diabetem. Zásadní význam má velmi nízké riziko hypoglykémie. V jednotlivých studiích je shodné s rizikem hypoglykémie po užívání placeba (graf 5). Výjimka v kombinaci s deriváty sulfonylurey je diskutována v kapitole Klinické studie.
Běžné nežádoucí účinky zaznamenané v klinických studiích mají incidenci shodnou s placebem. Byla zaznamenána mírně zvýšená incidence nazofaryngitid a infekcí horních cest dýchacích [10]. V provedené metaanalýze, kde však byly zahrnuty oba registrované inhibitory DPP-4, byla navíc zvýšená incidence infekcí uropoetického aparátu [11]. Vyšší incidence v porovnání s placebem je také v případě bolestí hlavy. Vliv na tělesnou hmotnost je prakticky neutrální, což je zásadní rozdíl proti doposud běžně užívaným perorálním antidiabetikům, jejichž podávání obvykle vede ke zvýšení tělesné hmotnosti pacientů s diabetem. Zásadní význam má velmi nízké riziko hypoglykémie. V jednotlivých studiích je shodné s rizikem hypoglykémie po užívání placeba (graf 5). Výjimka v kombinaci s deriváty sulfonylurey je diskutována v kapitole Klinické studie.
Lékové interakce
Při společném podávání digoxinu se 100 mg sitagliptinu po dobu 10 dní došlo k mírnému nárůstu v oblasti pod křivkou (AUC, o 11 %) a střední špičky koncentrace léku (cmax, o 18 %). Pacienti užívající digoxin musí být náležitě sledováni. Nedoporučuje se žádná úprava dávkování digoxinu nebo sitagliptinu [10].
Těhotenství a kojení
Vzhledem k nedostatku údajů týkajících se použití u člověka se sitagliptin nesmí během těhotenství užívat. Není známo, zda se sitagliptin vylučuje do mateřského mléka u člověka, protože však studie se zvířaty vylučování do mateřského mléka prokázaly, nesmí se během kojení sitagliptin užívat.
Dávkování
Obvykle se podává 100 mg sitagliptinu jednou denně per os. Zvyšování dávky nepřináší žádný relevantní klinický efekt.
Balení
Balení obsahuje 28 nebo 98 tablet, jedna tableta obsahuje 100 mg sitagliptinu (tab. 2).
Seznam použité literatury
- [1] Ahrén B. Gut peptides and type 2 diabetes mellitus treatment. Curr Diab Rep 2003; 3: 365–372.
- [2] Drucker DJ. The biology of incretin hormones. Cell Metabolism 2006; 3: 153–165.
- [3] D Alessio DA, Vahl TP. Glucagon-like peptid 1: evolution of an incretin into a treatment for diabetes. Am J Physiol Endocrinol Metab 2004; 286: E882–E890.
- [4] Nauck MA, Stöckmann F, Ebert R, et al. Reduced incretin effect in Type 2 (non-insulin-dependent) diabetes. Diabetologia 1986; 29: 46–52.
- [5] Kjems LL, Holst JJ, Vo/ lund A, Madsbad S. The influence of GLP-1 on glucose-stimulated insulin secretion: effects on beta-cell sensitivity in type 2 and nondiabetic subjects. Diabetes 2003; 52: 380–386.
- [6] Bose AK, Mocanu MM, Carr RD, et al. Glucagon-like peptide 1 can directly protect the heart against ischemia/reperfusion injury. Diabetes 2005; 54: 146–151.
- [7] Sokos GG, Nikolaidis LA, Mankad S, et al. Glucagon-like peptide-1 infusion improves left ventricular ejection fraction and functional status in patients with chronic heart failure. J Card Fail 2006; 12: 694–699.
- [8] Demuth HU, McIntosh CH, Pederson RA. Type 2 diabetes–therapy with dipeptidyl peptidase IV inhibitors. Biochim Biophys Acta 2005; 1751: 33–44.
- [9] Kvapil M, Perušičová J. Postprandiální glykémie. Praha, Triton 2006.
- [10] Souhrn údajů o přípravku Januvia (2008).
- [11] Amori RE, Lau J, Pittas AG. Efficacy and safety of incretin therapy in type 2 diabetes: systematic review and meta-analysis. JAMA 2007; 298: 194–206.
- [12] Raz I, Hanefeld M, Xu L, et al.; Sitagliptin Study 023 Group. Efficacy and safety of the dipeptidyl peptidase-4 inhibitor sitagliptin as monotherapy in patients with type 2 diabetes mellitus. Diabetologia 2006; 49: 2564–2571.
- [13] Aschner P, Kipnes MS, Lunceford JK, et al.; Sitagliptin Study 021 Group. Effect of the dipeptidyl peptidase-4 inhibitor sitagliptin as monotherapy on glycemic control in patients with type 2 diabetes. Diabetes Care 2006; 29: 2632–2637.
- [14] Rosenstock J, Brazg R, Andryuk PJ, et al.; Sitagliptin Study 019 Group. Efficacy and safety of the dipeptidyl peptidase-4 inhibitor sitagliptin added to ongoing pioglitazone therapy in patients with type 2 diabetes: a 24-week, multicenter, randomized, double-blind, placebo-controlled, parallel-group study. Clin Ther 2006; 28: 1556–1568.
- [15] Charbonnel B, Karasik A, Liu J, et al.; Sitagliptin Study 020 Group. Efficacy and safety of the dipeptidyl peptidase-4 inhibitor sitagliptin added to ongoing metformin therapy in patients with type 2 diabetes inadequately controlled with metformin alone. Diabetes Care 2006; 29: 2638–2643.
- [16] Goldstein BJ, Feinglos MN, Lunceford JK, et al.; Sitagliptin 036 Study Group. Effect of initial combination therapy with sitagliptin, a dipeptidyl peptidase-4 inhibitor, and metformin on glycemic control in patients with type 2 diabetes. Diabetes Care 2007; 30: 1979–1987.
- [17] Migoya E. Sitagliptin, a selective DPP-4 inhibitor, and metformin have complementary effects to increase active GLP-1 concentrations. Oral presentations at 67th ADA scientifict sessions, Chicago 2007.
- [18] Nauck MA, Meininger G, Sheng D, Terranella L, Stein PP; Sitagliptin Study 024 Group. Efficacy and safety of the dipeptidyl peptidase-4 inhibitor, sitagliptin, compared with the sulfonylurea, glipizide, in patients with type 2 diabetes inadequately controlled on metformin alone: a randomized, double-blind, non-inferiority trial. Diabetes Obes Metab 2007; 9: 194–205.
- [19] Hermansen K, Kipnes M, Luo E, et al.; Sitagliptin Study 035 Group. Efficacy and safety of the dipeptidyl peptidase-4 inhibitor, sitagliptin, in patients with type 2 diabetes mellitus inadequately controlled on glimepiride alone or on glimepiride and metformin. Diabetes Obes Metab 2007; 9: 733–745.
- [20] Schernthaner G, Grimaldi A, Di Mario U, Kvapil M, et al. GUIDE study: double blind comparison of once-daily gliclazide MR and glimepride in type 2 diabetic patients. Eur J Clin Invest 2004; 34: 535–542.
- [21] Scott R, Wu M, Sanchez M, Stein P. Efficacy and tolerability of the dipeptidyl peptidase-4 inhibitor sitagliptin as monotherapy over 12 weeks in patients with type 2 diabetes. Int J Clin Pract 2007; 61: 171–180.