Tiotropium
Tiotropium bromid je inhalační anticholinergikum, selektivní, kompetitivní, reverzibilní antagonista cholinergních receptorů M1 a M3 s 24hodinovým působením. Ročními a šestiměsíčními studiemi s tiotropiem bylo opakovaně prokázáno, že tiotropium zlepšuje funkci plic, dušnost, kvalitu života vztaženou ke zdraví, snižuje počet exacerbací a snižuje plicní hyperinflaci. Tato farmakologická volumová redukce souvisí s příznivým vlivem tiotropia na zlepšení ponámahové dušnosti a na zlepšení tolerance fyzické zátěže. Retrospektivní data z roční placebem kontrolované klinické studie zvýšila pravděpodobnost příznivého vlivu tiotropia na roční deklinaci funkce plic. Tiotropium je indikováno pro dlouhodobou udržovací léčbu chronické obstrukční plicní nemoci od středně těžkého stadia (stadium II) v jedné denní dávce 18 mikro gramů. Tiotropium může být současně užíváno s ostatními léky určenými k léčbě CHOPN (sympatomimetika, methylxanthiny, systémové nebo inhalační kortikosteroidy), ale není doporučeno jeho dlouhodobé podávání s ipratropiem. Hlavním nežádoucím účinkem tiotropia je suchost v ústech. Podávání tiotropia je kontraindikováno u pacientů s anamnestickou hypersenzitivitou k atropinu nebo k jeho derivátům. Opatrnosti je třeba při léčbě tiotropiem u pacientů s glaukomem s úzkým úhlem, s hyperplazií prostaty a s obstrukcí hrdla močového měchýře. Zvýšené opatrnosti je též třeba u nemocných se středně těžkým až těžkým postižením funkce ledvin (clearance kreatininu pod 50 ml/min). Pro inhalační aplikaci tiotropia byl speciálně vyvinut dechem aktivovaný inhalační systém HandiHaler.
Farmakologická skupina
Tiotropium je inhalační anticholinergikum. Tiotropium je inhalační, selektivní, kompetitivní, reverzibilní antagonista M1 a M3 cholinergních receptorů s dlouhodobým 24hodinovým účinkem. Tiotropium patří společně s ipratropiem (ipratropium bromid) mezi inhalační bronchodilatancia, která jsou odvozena od atropinu. Tiotropium se řadí do anatomicko-terapeuticko-chemické skupiny léčiv k terapii onemocnění spojených s obstrukcí dýchacích cest (R03), kde má přidělený kód R03BB04.
Chemické a fyzikální vlastnosti
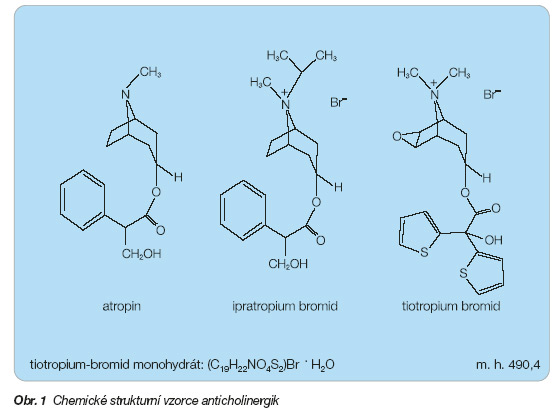
Tiotropium bromid (obr. 1) je chemicky 3b-[bis(2-thienyl)hydroxyacetoxy]-6b,7b-epoxy-8-methyl-1aH,5aH-tropan-8-ium-bromid. V léčivém přípravku je obsažen ve formě monohydrátu.
Sumární vzorec: (C19H22NO4S2)Br . H2O
Molekulová hmotnost: 490,4
Tiotropium bromid je achirální (opticky inaktivní) kvarterní amoniová sůl. Tiotropium bromid monohydrát je bílý nebo nažloutlý krystalický nezapáchající prášek, mírně rozpustný ve vodě, dobře rozpustný v methanolu a prakticky nerozpustný v dichlormethanu.
Mechanismus účinku
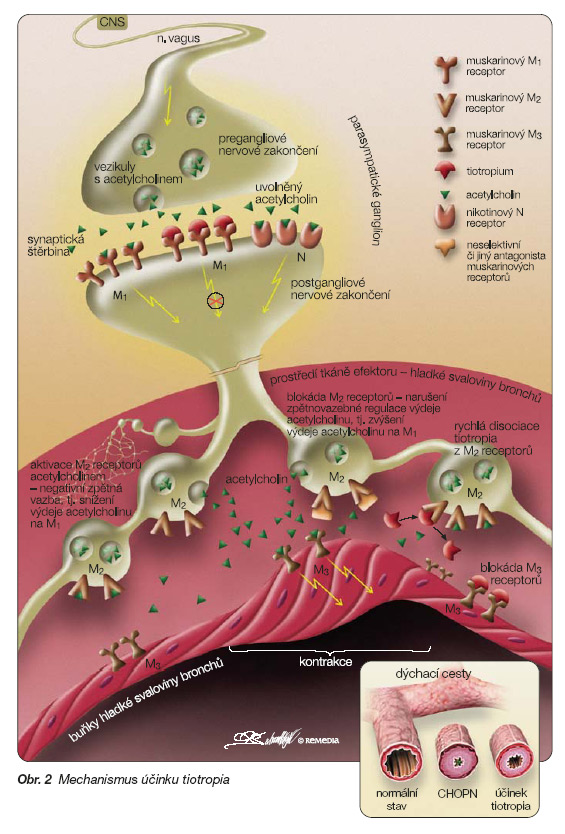
Cholinergní teorie bronchiální obstrukce je známa 200 let, ale přírodní anticholinergika byla v léčbě dušnosti užívána již před 2 000 lety [1]. Dnes je u nemocných s CHOPN prokázáno, že pouze cholinergní mechanismus bronchokonstrikce je plně reverzibilní [2]. U lidí byly v plicích identifikovány tři subtypy muskarinových receptorů (M1, M2 a M3) s odlišnými fyziologickými funkcemi [3] (obr. 2).
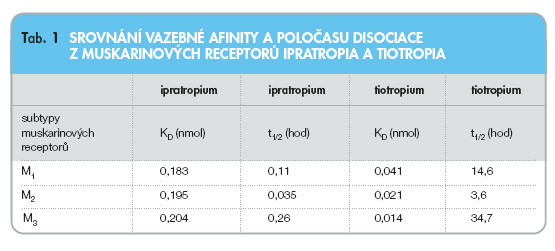
Muskarinové receptory M1, které jsou lokalizovány v parasympatických gangliích, usnadňují neurotransmisi acetylcholinu. Jejich aktivace usnadňuje cholinergní přenos, jejich blokáda neurotransmisi zastavuje. Muskarinové receptory M2, které byly nalezeny v myokardu a v hladkých svalech, působí negativní zpětnou vazbou na uvolňování acetylcholinu. Jejich aktivace tlumí uvolňování acetylcholinu, jejich blokáda způsobuje zvýšení produkce acetylcholinu v dýchacích cestách, což má za následek pěti- až osminásobné zvýšení bronchokonstrikce navozené vagem. Aktivace muskarinových receptorů M3 v dýchacích cestách navozuje konstrikci hladkých svalů a zvýšení sekrece hlenových žlázek. Blokádou tohoto výkonného receptoru dojde ke snížení vagového tonu v dýchacích cestách. V humánních průduškách byl ještě identifikován muskarinový receptor M4, ale jeho funkce dosud není známa. Ideální anticholinergikum pro léčbu CHOPN bude preferenčně antagonizovat činnost receptoru M1 a M3, či pouze činnost receptoru M3 a současně bude mít minimální afinitu k receptoru M2 [3]. V léčbě CHOPN je široce používaným inhalačním anticholinergikem ipratropium bromid, který je neselektivním antagonistou všech muskarinových receptorů, což přináší interferenci bronchodilatačního účinku se zvýšeným uvolňováním acetylcholinu z receptorů M2. Účinek ipratropia trvá maximálně 6 hodin, proto je nutno podávat je 4x denně. Inhalační cestou podávaný tiotropium bromid je selektivní kompetitivní reverzibilní antagonista receptorů M1 a M3 s 24hodinovým působením. Tiotropium má stejnou vazebnou afinitu ke všem typům muskarinových receptorů (disociační konstanta je 0,014–0,041 nmol/l), ale jeho disociace z receptoru M2 je rychlá (t1/2– poločas disociace je 3,6 h), kdežto z receptorů M1 a M3 je disociace pomalá (t1/2 pro M1 je 14,6 hod a pro M3 je 34,7 hod). Tiotropium je tedy kineticky selektivní [3, 4] (viz tab. 1), což přináší ve srovnání s ipratropiem větší a prolongovanější účinek umožňující jeho podávání 1x za 24 hodin.
Farmakodynamické vlastnosti
K farmakodynamickým vlastnostem tiotropia [5] patří bronchodilatační účinek verifikovaný zlepšením hodnoty FEV1 (usilovně vydechnutý objem za 1 sekundu a FVC (usilovná vitální kapacita). Vrcholu zlepšení FEV1 je dosaženo za 1–4 hodiny po aplikaci jedné dávky 18 mg tiotropia, účinek přetrvává 24 hodin a rovnovážného stavu hodnoty FEV1 před podáním další dávky tiotropia (trough FEV1 – průměrná hodnota FEV1 změřená 55 a 5 minut před podáním další dávky léku) je dosaženo přibližně za 48 hodin. Nebyl prokázán na dávce závislý účinek při aplikaci 4,5–36 mg tiotropia. Při podávání tiotropia byl medián trough FEV1 signifikantně lepší (p < 0,05) ve srovnání s podáváním ipratropia, salmeterolu nebo formoterolu. Rovnovážného stavu hodnoty FVC bylo dosaženo po 8 dnech. Nebyl prokázán rebound fenomén bronchokonstrikce po ukončení léčby tiotropiem.
Bronchodilatační účinek nebyl závislý na denní době podávání tiotropia. Bronchodilatancia mají u CHOPN jen malý vliv na ukazatele míry obstrukce, kterou je postbronchodilatační hodnota FEV1 a FEV1/FVC %. Větší a významnější změny jsou však zaznamenány v plicních objemech, kde dochází k redukci funkční reziduální kapacity (FRC) a k recipročnímu zvýšení inspirační kapacity (IC) a k oddálení začátku dynamické hyperinflace během fyzické zátěže. Tyto změny plicních objemů jsou mnohem důležitější, neboť snižují percepci námahové dušnosti a zvyšují toleranci fyzické zátěže [6, 7].
Tiotropium, díky svému účinku na snížení statické a dynamické plicní hyperinflace, zlepšuje dyspnoi, zlepšuje toleranci fyzické námahy a snižuje desaturaci kyslíkem v krvi během REM fáze spánku [5]. Při léčbě tiotropiem byl prokázán vrchol zvýšení IC již za 3 hodiny po podání léku a zvýšení hodnoty trough IC dokumentuje farmakologickou volumovou redukci přetrvávající po 24 hodin [8, 9].
Dnes je prokázáno, že poměr inspirační kapacity k celkové plicní kapacitě (IC/TLC) představuje nezávislý prediktivní faktor mortality pacientů s CHOPN [10], proto jakékoliv zvýšení tohoto poměru signalizující snížení plicní hyperinflace snižuje riziko úmrtí pacientů na CHOPN.
Farmakokinetické vlastnosti
Tiotropium se podává ve formě prášku k inhalaci v tvrdých tobolkách, které obsahují 5,5 mg krystalické laktózy. Pro inhalaci tiotropia byl vyvinut nový inhalační systém HandiHaler, jehož výhodou je velmi nízký vnitřní odpor, jenž umožňuje dosáhnout optimální inhalace léku i při nízkých hodnotách inspiračního průtoku (PIF) již nad 25 l/min. Studiemi in vitro je prokázáno, že dodaná dávka tiotropia přestavuje kolem 60 % nominální dávky s podílem respirabilní frakce (FPF) kolem 20 % nominální dávky. Maximum dodané dávky tiotropia je deponováno do gastrointestinálního traktu a menší část do průduškového stromu. Tiotropium se špatně vstřebává z gastrointestinálního traktu, celková biologická dostupnost zkoumaná na zdravých dobrovolnících představuje pouze 2–3 % z perorálně podaného roztoku. Díky tomu se dá se říci, že tiotropium je bronchotopicky selektivní. Absolutní biologická dostupnost 19,5 % po inhalaci prášku tiotropia u mladých zdravých dobrovolníků naznačuje, že podíl, který se dostává do plic, má vysokou biologickou dostupnost. Maximální plazmatické koncentrace tiotropia 17–19 pg/ml je dosaženo za 5 min. po inhalaci 18 mg léku. Absorpce tiotropia není ovlivnitelná potravou. Tiotropium je ze 72 % vázáno na plazmatické proteiny a jeho distribuční objem je 32 l/kg. Tiotropium neproniká hematoencefalickou bariérou. Rozsah biotransformace tiotropia je nízký, po intravenózním podání mladým zdravým dobrovolníkům je 74 % podané dávky v nezměněné podobě vylučováno močí. Ester tiotropia je neenzymaticky štěpen na N-methylscopin a na kyselinu dithienylglykolovou. Oba produkty biotransformace jsou biologicky inaktivní a již dále nepůsobí na muskarinové receptory. Méně než 20 % intravenózně podané dávky tiotropia je metabolizováno oxidací závislou na cytochromu P-450 a následnou konjugací s glutathionem na metabolity II. řádu. Tuto enzymatickou cestu lze inhibovat inhibitory CYP 2D6 a 3A4, jako je chinidin, ketoconazol a gestoden. Celková clearance tiotropia po intravenózním podání mladým zdravým dobrovolníkům je 880 ml/min. s 22% interindividuální variabilitou.
Terminální eliminační poločas tiotropia nastává mezi 5.–6. dnem po inhalaci. Po inhalačním podání tiotropia je močí vyloučeno 14 % dávky, zbytek představující nevstřebaný lék ze střeva je vyloučen stolicí. U pacientů s CHOPN je farmakokinetického rovnovážného stavu dosaženo za 2–3 týdny bez jeho další kumulace. Vylučování tiotropia močí je sníženo u pacientů s CHOPN v seniorském věku, avšak beze změny jeho plazmatických koncentrací. Proti tomu u pacientů se středně těžkou až těžkou poruchou renálních funkcí (clearance kreatininu pod 50 ml/min.) dochází po intravenózním i po inhalačním podání tiotropia až ke zdvojnásobení plazmatických koncentrací léku. Jaterní insuficience nemá významný vliv na farmakokinetiku tiotropia [11].
Klinické zkušenosti
V prvních klinických studiích, ve kterých byl zkoumán u nemocných s astmatem účinek tiotropia v závislosti na dávce, byl prokázán bronchodilatační a protektivní účinek tiotropia v dávce 10, 40 a 80 mg proti metacholinem navozené bronchokonstrikci. Bronchodilatační účinek tiotropia nastupuje do 30 minut po podání první dávky, bronchoprotektivní účinek před metacholinem nastupuje za 2 hodiny po podání dávky a přetrvává nejméně 24 hodin [12]. Další dvojitě zaslepená placebem kontrolovaná zkřížená studie u nemocných s CHOPN prokázala, že maximálního účinku tiotropia je dosaženo za 4 hodiny po jeho aplikaci a účinek byl přítomen i po 72 hodinách po podání [13]. V jiné studii byl srovnáván bronchodilatační účinek tiotropia v dávkách 9–36 mg [14]. Závěry studie vedly k doporučení používat dávku 18 mg tiotropia pro další studie. Do 92denní randomizované dvojitě zaslepené klinické studie, ve které byla primární proměnnou změna FEV1 měřená za 24 hod. po podání dávky léku (trough FEV1), bylo zařazeno 470 pacientů s CHOPN. Studie prokázala signifikantní zlepšení trough FEV1 u pacientů léčených tiotropiem ve srovnání s placebem [15]. Do dvou identických randomizovaných dvojitě zaslepených placebem kontrolovaných studií trvajících 1 rok bylo zařazeno celkem 921 pacientů se stabilizovanou středně těžkou CHOPN. Bylo prokázáno, že tiotropium je schopno výrazně zpomalit progresi obstrukce u CHOPN, díky snížení hyperinflace plic zlepšuje toleranci fyzické zátěže, snižuje četnost a tíži exacerbací CHOPN a zlepšuje kvalitu života nemocných [16, 17, 30]. Do 13týdenní randomizované dvojitě zaslepené studie srovnávající účinnost a bezpečnost tiotropia s ipratropiem bylo zařazeno 288 pacientů s CHOPN [18]. Výsledky studie prokázaly signifikantní zlepšení výchozích hodnot FEV1 a snížení dávek salbutamolu, který byl podáván jako záchranný inhalační lék, u pacientů dostávajících tiotropium ve srovnání s pacienty dostávajícími ipratropium. Četnost exacerbací i četnost výskytu nejčastějšího nežádoucího účinku, kterým je suchost v ústech, byly u obou skupin stejné. Pacienti zařazení do výše zmíněné studie pokračovali ve studii v celkové délce 1 rok a výsledky byly kombinovány s výsledky další studie se stejným uspořádáním srovnávající účinnost tiotropia podávaného 356 pacientům v dávce 18 mg /den a ipratropia podávaného179 pacientům v dávce 40 mg 4x denně. Roční podávání tiotropia vedlo ve srovnání s podáváním ipratropia k signifikantnímu zlepšení dušnosti hodnocené indexem přechodné dušnosti (TDI), ke zlepšení kvality života a ke snížení pravděpodobnosti další exacerbace [19]. Účinnost tiotropia byla srovnávána v šestiměsíční placebem kontrolované studii se salmeterolem, do které bylo randomizováno 623 pacientů se středně těžkou až těžkou CHOPN [20, 21]. Tiotropium bylo podáváno v dávce 18 mg/den, salmeterol v dávce 50 mg 2x denně pomocí aerosolového dávkovače. Po šestiměsíční léčbě byla ve skupině dostávající tiotropium hodnota trough FEV1 signifikantně větší než ve skupině dostávající salmeterol. Zlepšení skóre dušnosti přineslo podávání tiotropia, ne však podávání salmeterolu. Rovněž signifikantně větší zlepšení hodnoty večerní PEF a signifikantně větší zlepšení kvality života bylo prokázáno ve skupině dostávající tiotropium ve srovnání se skupinou dostávající salmeterol. Při dlouhodobém podávání tiotropia nedochází k vývoji tolerance na jeho účinky. Vývoj tolerance je však prokázán u dlouhodobé léčby salmeterolem pacientů s CHOPN [22]. Předběžná data z 6týdenní studie u 78 nemocných s CHOPN ukazují, že tiotropium podávané samostatně nebo v kombinaci s formoterolem aplikovaným v dávce12 mg jednou denně má větší bronchodilatační účinek než formoterol podávaný samostatně v dávce 12 mg 2x denně [23]. Dalšími studiemi je nutno potvrdit, že kombinace tiotropia a LABA je účinnější než jejich samostatné podávání; je pravděpodobné, že se prokáže stejný aditivní účinek, jako byl zaznamenán při kombinaci ipratropium-salbutamol nebo ipratropium-salmeterol [24]. Výsledky probíhajících klinických studií srovnávajících účinek tiotropia s fixními kombinacemi (LABA/ IKS) nejsou zatím známy. Zajímavé výsledky přinesou i studie srovnávající léčebnou kombinaci tiotropium plus fixní kombinace. Zde však bude limitující velká cena této léčby.
Klinicky prokázaný příznivý účinek tiotropia na snížení počtu exacerbací i na prevenci dalších exacerbací [17, 19, 21] pozitivně zasahuje i do farmakoekonomického pohledu na léčbu tiotropiem. Je prokázáno, že 50–75 % ročních přímých nákladů na léčbu CHOPN se spotřebuje na léčbu exacerbací [6]. Publikovaná data z reálného života byla získána z databáze US Veterans Administration Medical System [25]. V šestiměsíční placebem kontrolované dvojitě zaslepené studii, do které bylo zařazeno 1 826 pacientů s CHOPN, bylo prokázáno, že tiotropium ve srovnání s placebem signifikantně snižuje frekvenci a trvání exacerbací, prodlužuje čas do první exacerbace a snižuje nároky na zdravotní péči. Podobné výsledky přinesla i roční studie MISTRAL provedená ve 177 centrech ve Francii, do které bylo zařazeno 1 010 pacientů s CHOPN [26, 27]. Tiotropium ve srovnání s placebem signifikantně snížilo, bez ohledu na stávající léčbu IKS, počet (-35 %) a tíži exacerbací vyjádřenou počtem dnů léčby exacerbace (-37 %), počtem dnů s podáváním antibiotik (-34 %) a počtem dnů s podáváním systémových kortikosteroidů (-28 %). Obecně lze konstatovat, že tiotropium snižuje přímé náklady spojené s léčbou CHOPN [28] díky snížení počtu hospitalizací, což je důsledek poklesu počtu a tíže exacerbací. Roční studie v USA prokázala snížení nákladů na 1 pacienta s CHOPN léčeného tiotropiem (1 738 US$) o 1 055 US$ ve srovnání s placebem (2 993 US$). Do kalkulace nebyla zahrnuta cena tiotropia. Nizozemská studie prokázala, že roční rozdíl za cenu samotného léku tiotropium versus ipratropium představuje nárůst o 180 †, který je parciálně vyvážen snížením nákladů za hospitalizace během exacerbací [29].
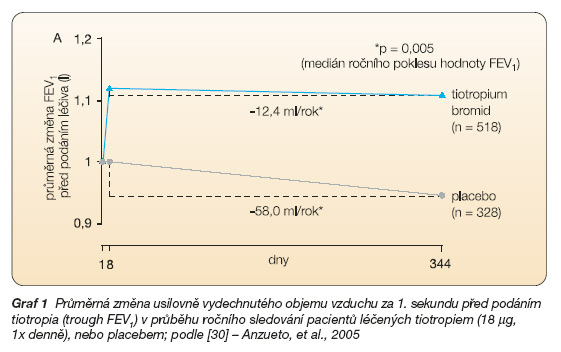
Výsledky krátkodobých klinických studií (trvajících 28, resp. 42 dní) potvrzují, že tiotropium v dávce 18 mg/den ve srovnání s placebem redukuje statickou i dynamickou plicní hyperinflaci a zlepšuje toleranci fyzické zátěže [8, 9]. Recentně publikovaná placebem kontrolovaná klinická studie analyzující vliv ročního podávání tiotropia na deklinaci plicní funkce u 921 pacientů s CHOPN prokázala, že medián ročního poklesu hodnoty FEV1 před podáním další medikace (trough FEV1) byl mezi 8.–344., resp. 50.–344. dnem studie 58 ml, resp. 59 ml ve skupině dostávající placebo a 12 ml, resp. 19 ml ve skupině dostávající tiotropium (graf 1) [30].
Tato retrospektivní analýza potvrdila, že léčba tiotropiem je schopna zpomalit roční deklinaci FEV1.
Kritický přehled 9 randomizovaných klinických studií s tiotropiem, do kterých bylo zařazeno 6 584 pacientů s CHOPN, uvádí, že tiotropium ve srovnání s placebem i ipratropiem snižuje riziko exacerbací (OR = 0,74) a k nim vztažené riziko hospitalizací (OR = 0,64). Při bazálním ročním 45% riziku exacerbace a 10% riziku hospitalizace je nutno k prevenci 1 exacerbace za rok léčit tiotropiem 14 pacientů (NNT = 14) a k prevenci 1 hospitalizace za rok je nutno léčit tiotropiem 30 pacientů (NTT = 30) ve srovnání s placebem či ipratropiem [31]. Srovnání rozdílů těchto výsledných proměnných u pacientů léčených tiotropiem a LABA není statisticky signifikantní. Tiotropium rovněž zlepšuje kvalitu života vztaženou ke zdraví, zlepšuje příznakové skóre u pacientů se středně těžkým až těžkým stadiem CHOPN a zpomaluje roční deklinaci hodnoty FEV1 [31]. Tiotropium významně zlepšuje toleranci fyzické zátěže. Z těchto důvodů tiotropium v reálném životě nemocných s CHOPN zásadním způsobem redukuje progresi jejich celoživotní nemoci, a tím přispívá ke snížení invalidizace handicapovaných nemocných s CHOPN [32].
Zařazení do současné palety léčiv
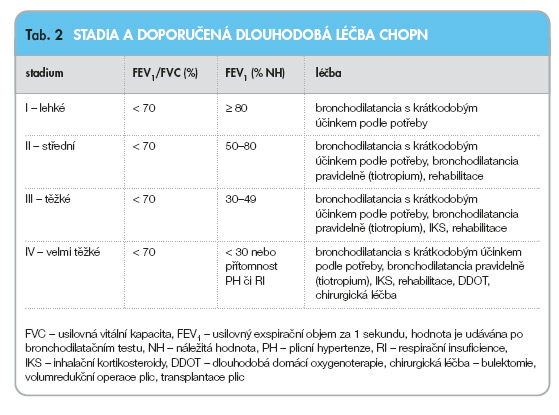
CHOPN se dělí na lehké stadium – I, střední stadium – II, těžké stadium – III a velmi těžké stadium – IV. GOLD (Global Initiative for Chronic Obstructive Lung Disease) uvádí ještě rizikové stadium – označované 0, kdy se ještě v pravém slova smyslu nejedná o CHOPN, ale o chronickou bronchitidu s příznaky, jako je kašel a vykašlávání sputa. Klasifikace CHOPN do stadií umožňuje jednotný léčebný přístup (viz tab. 2) [6, 33–38].
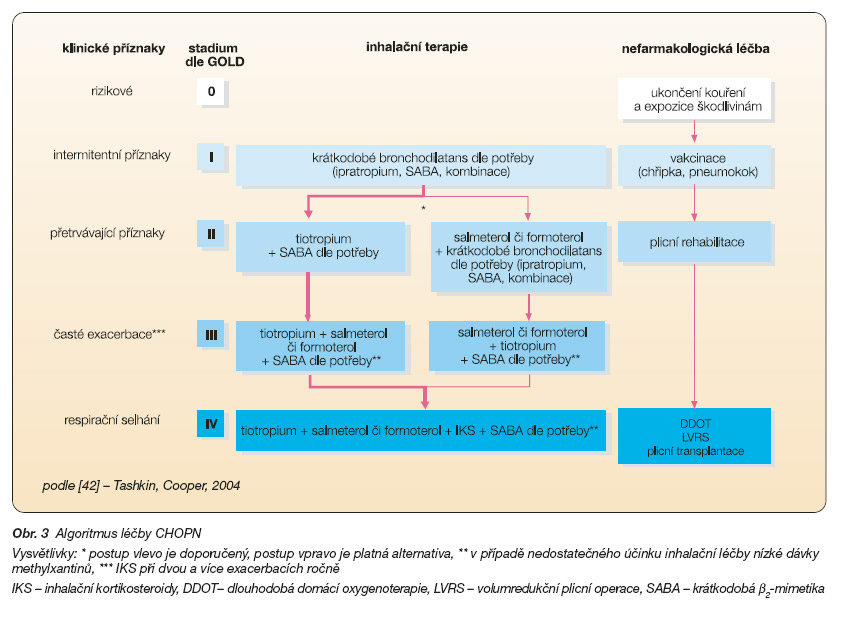
Lékem první volby pro léčbu CHOPN všech stadií jsou bronchodilatancia. Přednost je dávána inhalačním bronchodilatanciím, pokud tato nejsou k dispozici nebo nemocný dobře nezvládá inhalační techniku, je nutno perorálně podávat methylxantiny (theofyliny) s prodlouženým účinkem. Inhalační bronchodilatancia s krátkodobým účinkem, tj. b2-mimetika (fenoterol, salbutamol, terbutalin) a anticholinergikum (ipratropium bromid), se podávají jako úlevový lék podle potřeby pro všechna stadia CHOPN. Pokud přetrvávají příznaky, jako je kašel, pískání na hrudníku či dušnost spojená s fyzickou námahou, je nutno bronchodilatancia podávat pravidelně, což v případě bronchodilatancií s krátkodobým účinkem znamená 4x denně, neboť doba jejich účinku je 4, resp. 6 hodin. Klinickými studiemi bylo prokázáno, že podávání inhalačních bronchodilatancií s dlouhodobým účinkem, kam se řadí inhalační b2-mimetika s dlouhodobým účinkem (LABA, tj. formoterol a salmeterol) a nové inhalační anticholinergikum s dlouhodobým účinkem (tiotropium), je efektivnější. Od stadia III – těžká CHOPN – se ke stávající léčbě bronchodilatancii přidávají inhalační kortikosteroidy /IKS/, zvláště pokud jsou exacerbace časté, tj. dvě a více exacerbací ročně [37]. Kombinace IKS a LABA podávaná v jednom inhalátoru, tzv. fixní kombinace, je efektivnější než podávání obou komponent odděleně [39–41]. Od stadia II (středně těžká CHOPN) je doporučována komplexní rehabilitace. Dlouhodobá domácí oxygenoterapie a eventuální chirurgická léčba jsou určeny pro stadium IV – velmi těžká CHOPN. Pro všechna stadia CHOPN je základní a imperativní podmínkou efektivní léčby zanechání kouření tabáku. Jeden z algoritmů léčby CHOPN viz obr. 3 [42].
Příslušnou vyhláškou (vyhl. MZ ČR č. 589/2004 Sb. o úhradách léčiv a potravin pro zvláštní lékařské účely) je od 1. 1. 2005 v ČR legalizována léčba CHOPN inhalačními bronchodilatancii s dlouhodobým účinkem (LABA a tiotropium), což si vyžádalo mj. i upřesnění podmínek jejich preskripce. LABA i tiotropium pro léčbu CHOPN může předepisovat pouze pneumolog (odborník pro léčbu tuberkulózy a respiračních onemocnění – TRN) pacientům s CHOPN od středně těžkého stadia (stadium II). Základní podmínkou preskripce je, aby nemocný zanechal kouření. Umožnění léčby tiotropiem pacientům se středně těžkou CHOPN příznivě ovlivní průběh nemoci u nemocných, kteří jsou většinou ještě v produktivním věku.
Ve světě se tiotropium po svém uvedení na trh rychle rozšířilo do více než 40 zemí a nyní je již považováno za lék první volby pro léčbu všech stadií CHOPN [5, 24].
Indikace
Tiotropium je indikováno jako bronchodilatační lék k udržovací léčbě dospělých pacientů od 18 let věku se všemi formami CHOPN.
V České republice má v současné době tiotropium preskripční omezení. Léčbu tiotropiem indikuje pneumolog (TRN) u nemocných s diagnózou CHOPN stadia II, III, IV, kteří dodržují léčebný režim včetně zákazu kouření.
Nežádoucí účinky
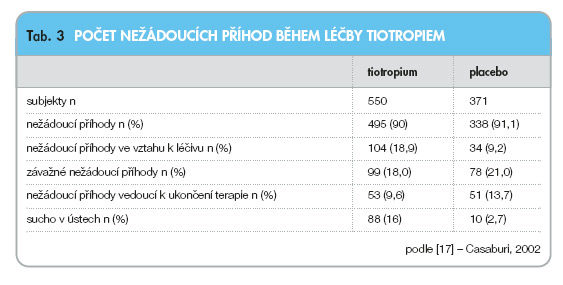
Inhalačně podané tiotropium má minimální nežádoucí účinky typické pro všechna inhalační anticholinergika. Nejčastějším nežádoucím účinkem je suchost v ústech, která se vyskytovala zejména v průběhu 3.–5. týdne léčby u 14 % pacientů zařazených do klinických studií a byla hojnější u žen [11, 31]. Suchost v ústech byla většinou mírná a často vymizela v průběhu léčby. Mezi časté nežádoucí účinky patří zácpa, kandidóza, faryngitida a sinusitida. Jako vzácný nežádoucí účinek se vyskytla supraventrikulární tachykardie a fibrilace síní, obtíže při močení a retence moči postihující starší muže s dispozičními faktory, jako je hyperplazie prostaty. Profil nežádoucích příhod ve studii trvající jeden rok udává tab. 3 [17].
Kontraindikace
Léčba tiotropiem je kontraindikována u pacientů s hypersenzitivitou k atropinu a jeho derivátům, jako je ipratropium nebo oxitropium, nebo k ostatním komponentám tohoto léku. Jako inertní substance k přenosu tiotropia je použita krystalická laktóza, která může být vzácnou příčinou intolerance inhalační aplikace tiotropia.
Zvláštní upozornění a bezpečnostní varování
Tiotropium není určeno pro léčbu akutního bronchospasmu. Jakýkoliv inhalačně podaný lék může vyvolat paradoxní bronchospasmus. Opatrnosti je třeba u nemocných s těžkým postižením funkce ledvin (clearance kreatininu pod 50 ml/min). Jako při léčbě ostatními anticholinergiky je třeba při léčbě tiotropiem zvláštní opatrnosti u pacientů s glaukomem s úzkým úhlem, s hyperplazií prostaty a s obstrukcí hrdla močového měchýře. Nemocný musí být poučen o správné inhalační technice a o zacházení s kapslemi obsahujícími tiotropium. Prášek tiotropia se nesmí dostat do oka, kde by mohl vyvolat akutní glaukomový záchvat.
Lékové interakce
Tiotropium nemá nežádoucí interakce s ostatními léky podávanými při léčbě CHOPN nebo u komorbidit. Při léčbě tiotropiem však není vhodné pravidelné podávání jiných preparátů s inhalačními anticholinergiky, i když i toto doporučení je v poslední době zpochybňováno. Omezení současného podávání tiotropia a ipratropia se netýká léčby exacerbace CHOPN.
Těhotenství a laktace
Pro tiotropium nejsou dostupná klinická data týkající se jeho podávání během gravidity. Studie prováděné na zvířatech ukázaly reprodukční toxicitu, která je spojena s mateřskou toxicitou.
Klinické údaje týkající se kojících žen vystavených účinkům tiotropia též nejsou k dispozici. Ze studií prováděných na hlodavcích v laktačním období vyplynulo, že malé množství tiotropia je vylučováno do mateřského mléka. Z těchto důvodů nesmí být tiotropium podáváno těhotným a kojícím ženám, pokud očekávaný přínos léčby nepřeváží případná rizika pro plod či kojence.
Řízení motorových vozidel a práce vyžadující zvýšenou pozornost
Studie zkoumající vliv tiotropia na schopnost řídit motorová vozidla a obsluhovat stroje nebyly provedeny. Nicméně na základě farmakodynamických vlastností a zaznamenaných nežádoucích účinků při užívání tiotropia v doporučených dávkách neexistují údaje svědčící o případném nežádoucím ovlivnění schopnosti řídit motorová vozidla a obsluhovat stroje.
Předávkování
Vysoké dávky tiotropia mohou vyvolat anticholinergní příznaky a projevy. U zdravých dobrovolníků, kterým byla podávána jednotlivá inhalační dávka až 340 mg tiotropia, nebyly zaznamenány žádné nežádoucí systémové účinky. Kromě suchosti v ústech a s tím spojené bilaterální konjunktivitidy nebyly po sedmidenním inhalačním podávání dávek až 170 mg tiotropia zdravým dobrovolníkům zaznamenány žádné významné nežádoucí účinky. Ve studii s opakovaným podáváním u pacientů s CHOPN s maximální dávkou 43 mg tiotropia po dobu čtyř týdnů nebyl pozorován žádný závažný nežádoucí účinek. Akutní intoxikace po náhodném perorálním požití tobolek tiotropia je nepravděpodobná vzhledem k nízké perorální biologické dostupnosti.
Dávkování
Je doporučeno inhalovat obsah jedné tobolky s odměřenou dávkou 18 mg tiotropia 1x denně vždy ve stejnou denní dobu pomocí inhalační pomůcky HandiHaler. Uvolněná dávka tiotropia je 10 mg.
Pro používání inhalačního systému HandiHaler je třeba nemocného naučit správné inhalační technice a tuto techniku opakovaně kontrolovat. Některým pacientům může dělat problém i manipulace s tobolkou léku, zvláště její vyjmutí z blistru, které je snadné, pokud je zcela dodržován návod. Tobolka se nedá přes blistr protlačit silou, je nutno správným směrem odstranit ochrannou fólii a tobolku vyjmout. HandiHaler je nutno jedenkrát měsíčně čistit. Čištění se provádí opláchnutím teplou vodou po otevření inhalátoru a mechanickém odstranění zbytků prášku. Čištění inhalátoru je nutno provést ihned po jejím použití, protože vysychá až 24 hodin.
Balení
viz tab. 4
Seznam použité literatury
- [1] Vondra V. Bronchodilatancia v terapii chronické obstrukční plicní nemoci a bronchiálního astmatu – I. část: Anticholinergika. Remedia 1998; 8: 279–287.
- [2] Barnes PJ, Belvisi MG, Mak JCW, et al. Tiotropium bromide (Ba 679 Br), a novel long-acting muscarinic antagonist for treatment of obstructive airway disease. Life Sci 1995; 56: 853–859.
- [3] Barnes PJ. Novel approaches and targets for treatment of chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1999; 160: S72–79.
- [4] Panning CA, DeBisschop M. Tiotropium: An inhaled, long-acting anticholinergic drug for chronic obstructive pulmonary disease. Pharmacotherapy; 2003: 23: 183–189.
- [5] Keam SJ, Keating GM. Tiotropium bromide. A review of its use as maintenance therapy in patients with COPD. Treat Respir Med 2004; 3: 247–268.
- [6] Celli BR, MacNee W, and committee members. Standards for diagnosis and treatment of patiens with COPD: a summary of the ATS/ERS position paper. Eur Respir J 2004; 23: 932–946.
- [7] O´Donnel DE, Lam M, Webb KA. Spirometric correlates of improvement in exercise perfomance after anticholinergic therapy in chronic obstructive pulmonary disease. Am J Respir Crit Care Med 1999; 160: 542–549.
- [8] Celli B, ZuWallack R, Wang S, Kesten S. Improvement in resting inspiratory capacity and hyper-inflation with tiotropium in COPD patients with increased static lung volumes. Chest 2003; 124: 1743–1748.
- [9] O´Donnell, Flüge T, Gerken F, et al. Effect of tiotropium an lung hyperinflation, dyspnea and exercise tolerance in COPD. Eur Respir J 2004; 23: 832–840.
- [10] Casanova C, Cote C, de Torres JP, et al. Inspiratory-to-total lung capacity ratio predicsts mortality in patients with chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2005; 171: 591–597.
- [11] Spiriva® (tiotropium). Monografie o přípravku, Boehringer Ingelheim International GmbH 2003; 45 s.
- [12] O´Connor BJ, Towse LJ, Barnes PJ. Prolonget effect of tiotropium bromide on metacholine-induced bronchoconstriction in asthma. Am J Respir Crit Care Med 1996; 154: 876–880.
- [13] Maesen FPV, Smeets JJ, Sledsen TJH, et al. on behalf of the Dutsch Study Group. Tiotropium bromide, a new long-acting antimuscarinic bronchodilatator: a pharmacodynamic study in patients with chronic obstructive pulmonary disease. Eur Respir J 1995; 8: 1506–1513.
- [14] Littner MR, Ilowite JS, Tashkin DP, et al. Long-acting bronchodilation with once-daily dosing of tiotropium (Spiriva) in stable chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2000; 161: 1136–1142.
- [15] Casaburi R, Briggs DD Jr, Donohue JF, et al., fort he U.S. Tiotropium Study Group. The spirometric efficacy of once daily dosing with tiotropium in stable COPD. Chest 2000; 118: 1294–1302.
- [16] Rees PJ. Tiotropium in the management of chronic obstructive pulmonary disease. Eur Respir J 2002; 19: 205–206.
- [17] Casaburi R, Mahler DA, Jones PW, et al. A long term evaluation of once-daily inhaled tiotropium in chronic obstructive pulmonary disease. Eur Respir J 2002; 19: 217–224.
- [18] van Noord JA, Bantje ThA, Eland ME, et al. A randomised controlled comparison of ipratropium in the treatment of chronic obstructive pulmonary disease. Thorax 2000; 55: 289–294.
- [19] Vincken W, van Noord JA, Greefhorst APM, et al. Improved health outcomes in patients with COPD during 1 yr´s treatment with tiotropium. Eur Respir J 2002; 19: 209–216.
- [20] Donohue JF, van Noord JA, Bateman ED, et al. A 6-month placebo-controlled study comparing lung function and health status changes in COPD patients treated with tiotropium or salmeterol. Chest 2002; 122: 47–55.
- [21] Brusasco V, Hodder R, Miravitles M, et al. Health outcomes in 6-month placebo controlled trial of once-daily tiotropium compared with twice-daily salmeterol in patients with COPD. Thorax 2003; 58: 399–404.
- [22] Donohue JF, Menjoge S, Kesten S. Tolerance to bronchodilating effect of salmeterol in COPD. Respir Med 2003; 97: 1014–1020.
- [23] van Noor J, Aumann J, Jansens E, et al. Comparison of once daily tiotropium, twice daily formoterol and the free combination, once daily, in patients with COPD. Respir Crit Care Med 2003; A320.
- [24] ZuWallack AR, ZuWallack RL. Tiotropium bromide, a new once-daily inhaled anticholinergic bronchodilatator for chronic obstructive pulmonary disease. Expert Opin Pharmacother 2004; 5: 1827–1835.
- [25] Niewoehner D, Rice K, Cote C, et al. Reduced COPD exacerbations and associated health care utilization with once-daily tiotropium (TIO) in the VA medical system. Am J Respir Crit Care Med 2004; 169: A207.
- [26] Dusser D, Bravo ML, Iacono P, et al. Tiotropium reduced COPD exacerbations: The MISTRAL study. Annual Congress ERS, Glasgow 2004; P323.
- [27] Dusser D, Bravo ML, Iacono P, et al. Tiotropium reduced health resource utilization associated with COPD exacerbations: The MISTRAL study. Annual Congress ERS, Glasgow 2004; P324.
- [28] Friedman M, Menjoge SS, Anton S, et al. Healhtcare costs with tiotropium plus usual care versus usual care along following 1 year of treatment in patients with chronic obstructive pulmonary disorder (COPD). Pharmacoeconomics 2004; 22: 741–749.
- [29] Ostenbrink JB, Rutten-van Mölken MPMH, et al. One-year cost-effectiveness of tiotropium versus ipratropium to treat chronic obstructive pulmonary disease. Eur Respir J 2004; 23: 241–249.
- [30] Anzueto A, Tashkin D, Menjoge S, Kesten S. One-year analysis of longitudinal changes in spirometry in patients with COPD receiving tiotropium. Pulmonary Pharmacology and Therapeutics 2005; 18: 75–81.
- [31] Barr RG, Bourbeau J, Camargo CA, Ram FSF. Inhaled tiotropium for stable chronic obstructive pulmonary disease. The Cochrane Database of Systematic Reviews 2005; Issue 2, Art. No.: CD002876.pub2.
- [32] Mahler DA. Impacting lifestyle: real word benefits of tiotropium in COPD. Eur Respir Rev 2004; 13: 89: 45–49.
- [33] Fabri LM, Hurd SS. Global Strategy for the Diagnosis, Management and Prevention of COPD: 2003 update. Eur Respir J 2003; 22: 1–2.
- [34] Musil J, Balý J, Kos S, Salajka F, Vondra V. Změny ve strategii diagnostiky, léčby a prevence chronické obstrukční plicní nemoci (CHOPN). Stud Pneumol Phtiseol 2003; 63: 195–196.
- [35] Kašák V. Novinky v léčbě CHOPN. Medicína po promoci 2004; 5; 2: 52–57.
- [36] Vondra V. Moderní inhalační terapie stabilizované chronické obstrukční plicní nemoci (CHOPN). Respirace 2004; 10: 13–21.
- [37] NICE Guideline – COPD 2004. www.nice.org.uk/ pdf/CG012_niceguideline.pdf
- [38] Sutherland RE, Cherniack RM. Management of chronic obstructive pulmonary disease. N Engl J Med 2004; 350: 2689–2697.
- [39] Calverley PM, Pauwels R, Vesbo J, et al. Combined salmeterol and fluticasone in the treatment of chronic obstructive pulmonary disease: a randomised controlled trial. Lancet 2003; 361: 449–456.
- [40] Calverley PM, Boonsawat W, Czeke Z, et al. Maintenance therapy with budesonide and formoterol in chronic obstructive pulmonary disease. Eur Respir J 2003; 22: 912–919.
- [41] Szafranski W, Cukier A, Ramirez A, et al. Efficacy and safety of budesonide/formoterol in the management of chronic obstructive pulmonary disease. Eur Respir J 2003; 21: 74–81.
- [42] Tashkin DP, Cooper CB. The role of long-acting bronchodilators in the management of stable COPD. Chest 2004; 125: 249–259.