Pacient s těžkou formou psoriázy a psoriatické artritidy úspěšně léčený guselkumabem
Souhrn:
Nováková M. Pacient s těžkou formou psoriázy a psoriatické artritidy úspěšně léčený guselkumabem. Remedia 2022; 32: 28–32.
Psoriáza je chronické geneticky podmíněné imunitně mediované systémové zánětlivé onemocnění, které je kromě postižení kůže spojeno i s jinými systémovými chorobami (tzv. komorbidity) a s negativním dopadem na kvalitu života pacientů. Mezi nejčastější komorbidity patří psoriatická artritida, kardiovaskulární onemocnění, metabolický syndrom a jeho komponenty, zánětlivé onemocnění střev a deprese. Včasné rozpoznání a správná diagnostika těchto komorbidit by měly vést k dřívějšímu zahájení léčby, zlepšení dlouhodobé prognózy a předcházení vzniku dalších komplikací. Psoriatická artritida je chronické heterogenní systémové zánětlivé onemocnění, potenciálně progresivní a erozivní, které postihuje přibližně 30 % pacientů s psoriázou. Jednotlivé typy kloubního (artikulárního) i mimokloubního (extraartikulárního) postižení se mezi sebou mohou vzájemně překrývat a v průběhu času se měnit. Našim pacientům bychom měli nabídnout adekvátní, ověřenou a dlouhodobě účinnou léčbu. Vždy je třeba individuální přístup k léčbě konkrétního pacienta. V kazuistice je prezentován případ 41letého pacienta s těžkou formou psoriasis vulgaris et arthropatica, který je od února 2020 úspěšně léčen guselkumabem.
Summary:
Novakova M. Patient with a severe form of psoriasis and psoriatic arthritis successfully treated with guselkumab. Remedia 2022; 32: 28–32.
Psoriasis is a chronic, genetically determined immune‑mediated systemic inflammatory disease that is, aside from skin damage, also associated with other systemic disorders (so‑called comorbidities) and negatively impacts the patients' quality of life. The most common comorbidities include psoriatic arthritis, cardiovascular disease, metabolic syndrome and its components, inflammatory bowel disease and depression. Early detection and correct diagnosis of these comorbidities should lead to timely treatment initiation, better long‑term prognosis and prevention of other complications. Psoriatic arthritis is a chronic, heterogenic systemic inflammatory disease, potentially progressive and erosive, affecting approximately 30% of patients with psoriasis. Individual types of articular and extra‑articular damage can overlap and change with time. We should offer adequate and verified treatment with proven long‑term efficacy to our patients. An individual approach to the treatment of each patient is always needed. This case study presents successful treatment with guselkumab of a 41‑year‑old patient with a severe form of psoriasis vulgaris et arthropatica.
Key words: psoriasis, psoriatic arthritis, comorbidities, biologic treatment, guselkumab
Úvod
Psoriáza je
chronické geneticky podmíněné imunitně mediované systémové
zánětlivé onemocnění, které je kromě postižení kůže
spojeno i s jinými systémovými chorobami (tzv.
komorbidity) a s negativním dopadem na kvalitu života
pacientů [1]. Psoriáza postihuje přibližně 2-3 %
celosvětové populace [2]. Komorbidity
psoriázy lze zjednodušeně klasifikovat jako 1. klasické,
2. související s chronickým systémovým zánětem,
3. související s životním stylem a 4. související
s léčbou (viz tab. 1) [3]. Mezi
nejčastější komorbidity patří psoriatická artritida,
kardiovaskulární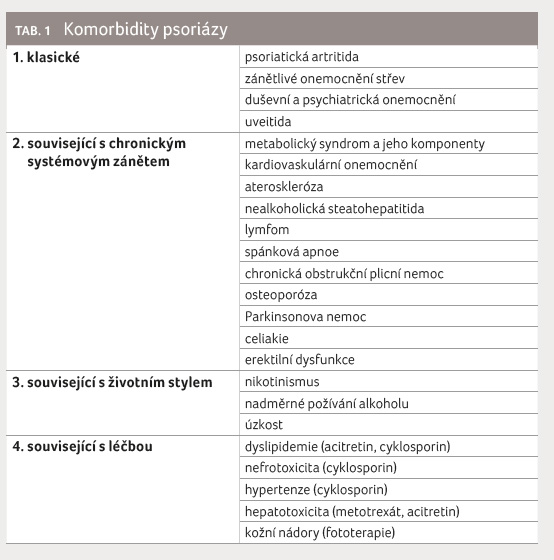 onemocnění, metabolický syndrom a jeho
komponenty, zánětlivé onemocnění střev a deprese
[4]. Včasné rozpoznání a správná diagnostika těchto
komorbidit by měly vést k dřívějšímu zahájení léčby,
zlepšení dlouhodobé prognózy a předcházení vzniku dalších
komplikací [5]. Psoriatická artritida
(PsA) je chronické heterogenní systémové zánětlivé onemocnění,
potenciálně progresivní a erozivní, které postihuje
přibližně 30 % pacientů s psoriázou [6].
Psoriatická artritida postihuje ve stejné míře muže
i ženy a obvykle se rozvíjí ve třetí až páté
dekádě života [7]. Sdílí mnoho
klinických, radiologických a sérologických rysů s jinými
spondyloartropatiemi a také s revmatoidní artritidou.
Obvykle je séronegativní, ale malé procento pacientů může mít
pozitivní revmatoidní faktor a přítomnost protilátek proti
cyklickému citrulinovanému peptidu [8,9]. Těžká
forma psoriázy, psoriáza nehtů a obezita jsou spojeny
s vyšším rizikem rozvoje PsA [5].
Psoriatická artritida je mnohotvárné onemocnění
charakterizované zánětem periferních kloubů (distální,
oligoartikulární a polyartikulární forma), entezí,
axiálního skeletu, daktylitidami a změnami kůže a nehtů,
které mohou být přítomny buď samostatně, nebo se vzájemně
kombinovat [7,10].
Klinický obraz PsA je heterogenní, protože jednotlivé typy
kloubního (artikulárního) i mimokloubního
(extraartikulárního) postižení se mezi sebou mohou vzájemně
překrývat a v průběhu času se měnit [8].
onemocnění, metabolický syndrom a jeho
komponenty, zánětlivé onemocnění střev a deprese
[4]. Včasné rozpoznání a správná diagnostika těchto
komorbidit by měly vést k dřívějšímu zahájení léčby,
zlepšení dlouhodobé prognózy a předcházení vzniku dalších
komplikací [5]. Psoriatická artritida
(PsA) je chronické heterogenní systémové zánětlivé onemocnění,
potenciálně progresivní a erozivní, které postihuje
přibližně 30 % pacientů s psoriázou [6].
Psoriatická artritida postihuje ve stejné míře muže
i ženy a obvykle se rozvíjí ve třetí až páté
dekádě života [7]. Sdílí mnoho
klinických, radiologických a sérologických rysů s jinými
spondyloartropatiemi a také s revmatoidní artritidou.
Obvykle je séronegativní, ale malé procento pacientů může mít
pozitivní revmatoidní faktor a přítomnost protilátek proti
cyklickému citrulinovanému peptidu [8,9]. Těžká
forma psoriázy, psoriáza nehtů a obezita jsou spojeny
s vyšším rizikem rozvoje PsA [5].
Psoriatická artritida je mnohotvárné onemocnění
charakterizované zánětem periferních kloubů (distální,
oligoartikulární a polyartikulární forma), entezí,
axiálního skeletu, daktylitidami a změnami kůže a nehtů,
které mohou být přítomny buď samostatně, nebo se vzájemně
kombinovat [7,10].
Klinický obraz PsA je heterogenní, protože jednotlivé typy
kloubního (artikulárního) i mimokloubního
(extraartikulárního) postižení se mezi sebou mohou vzájemně
překrývat a v průběhu času se měnit [8].
Artikulární/periartikulární projevy PsA zahrnují:
- Periferní artritidu (distální, oligoartikulární a polyartikulární forma).
- Periartikulární onemocnění včetně entezitidy (zánět v oblasti úponu šlachy, vazu nebo kloubního pouzdra na kost), daktylitidy (zánět kloubů s otokem celého prstu na rukou nebo nohou – tzv. sausage fingers) a tenosynovitidy (zánět synoviální výstelky a šlachové pochvy).
- Axiální formu – sakroiliitida postihující sakroiliakální klouby, obvykle asymetricky, a spondylitida s diskontinuálním postižením a vznikem syndesmofytů. Axiální forma se vyskytuje u 25-70 % pacientů s PsA.
- Extraartikulární projevy PsA zahrnují:
- Kožní projevy, které obvykle předcházejí vzniku PsA, ale mohou se objevit i současně nebo se zpožděním. Závažnost kožních projevů nekoreluje se závažností kloubního postižení.
- Psoriáza nehtů, která se projevuje buď na nehtové matrix jako leukonychie, červené skvrny na nehtech, dolíčkování, drolení, nebo na nehtovém lůžku jako olejové skvrny, třískovité hemoragie, subunguální hyperkeratóza či onycholýza. Postižení nehtů koreluje se závažností onemocnění a je významným prediktorem rozvoje PsA. Psoriáza nehtů je přítomna u 80-90 % pacientů s PsA a je spojena též s postižením distálních interfalangeálních kloubů.
- Oční onemocnění ve formě uveitidy, která je obvykle bilaterální, chronická a závažná. Manifestuje se bolestí, začervenáním, slzením a světloplachostí [7,8,11,12].
Nejstarší klasifikace podle Molla a Wrighta dělí PsA do pěti podtypů: 1. asymetrická oligoartritida, 2. symetrická polyartritida, 3. distální artritida, 4. mutilující artritida a 5. axiální spondyloartritida [8].
Přesná etiopatogeneze PsA není známa. Předpokládá se, že PsA sdílí společné etiopatogenetické mechanismy s psoriázou [13]. Regulační osa interleukin (IL) 23/IL 17 má klíčovou roli ve vzniku poškozujícího zánětu u pacientů s psoriázou a PsA. Genetickými a histologickými studiemi porovnávajícími kůži a synovii byly ovšem zjištěny tkáňově specifické rozdíly v aktivaci a expresi této dráhy [14]. Současná strategie farmakologické léčby psoriázy a PsA se opírá zejména o aktualizovaná doporučení Evropského dermatologického fóra (European Dermatology Forum, EDF) a Evropské ligy proti revmatismu (European League Against Rheumatism, EULAR) k systémové léčbě těchto onemocnění [15–17].
Kazuistika
Jednačtyřicetiletý pacient (ročník 1981) s těžkou formou psoriasis vulgaris et arthropatica je v péči naší Dermatovenerologické kliniky od března 2018.
Anamnéza
Rodinná anamnéza je nevýznamná, pacient neguje výskyt psoriázy v rodině. V osobní anamnéze jsou kromě výše zmiňované psoriasis vulgaris et arthropatica nejdůležitějšími diagnózami hypertenze, dyslipidemie a obezita III. stupně (hmotnost 140 kg, výška 187 cm, index tělesné hmotnosti [BMI] 40,04). Pacient během svého života neprodělal žádné operační výkony, alergie neudává. Chronická medikace nemocného zahrnuje antihypertenziva – amlodipin, perindopril, rilmenidin a rosuvastatin. Pacient je kuřák (30 cigaret denně), alkohol nepije, pracuje jako řidič a žije s partnerkou. Muž absolvuje pravidelné dispenzární kontroly na dermatologii, revmatologii, pneumologii a u praktického lékaře.
Nynější onemocnění
Pacient trpí psoriázou od 27 let (rok 2008). Vznik prvních ložisek psoriázy v oblasti stehen a bérců dává pacient do souvislosti se zvýšeným stresem. V průběhu dalších měsíců došlo k postupné progresi onemocnění na trup, horní končetiny a kštici. U nemocného byla ambulantně zahájena lokální terapie (kortikosteroidy, keratolytika) a komorová UVB fototerapie (20 sezení). Odpověď na zavedenou terapii byla vždy pouze s přechodným efektem. V roce 2017 začal mít pacient kloubní obtíže – bolesti drobných kloubů rukou, bolesti v oblasti Achillovy šlachy a intermit
entní bolesti
kolenních a loketních kloubů. V péči naší
Dermatovenerologické kliniky je muž od března 2018, kdy u něj
vzhledem k těžké formě psoriázy –
erytematoskvamózním plakům v oblasti loktů, kolen
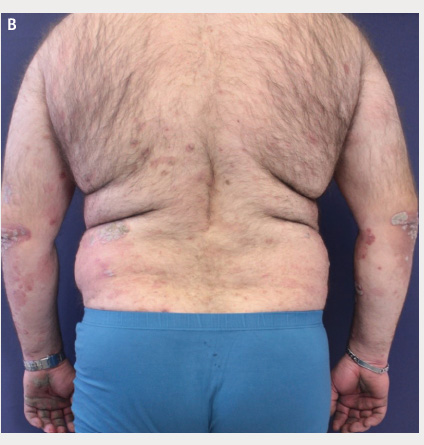
a trupu - a výsevu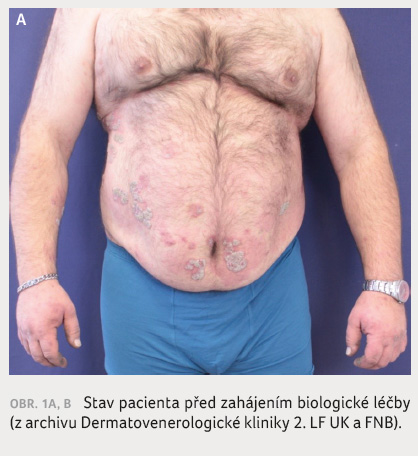 kapkovitých (gutátních) ložisek diseminovaně po celém těle
(index Body Surface Area [BSA] 17, Psoriasis Area and Severity Index
[PASI] 19), obrá
kapkovitých (gutátních) ložisek diseminovaně po celém těle
(index Body Surface Area [BSA] 17, Psoriasis Area and Severity Index
[PASI] 19), obrá
iniciálně podávána s dostatečným efektem na kožní (BSA 5, PASI 6) i kloubní postižení. V průběhu léčby došlo ke ztrátě jeho účinnosti (BSA 15, PASI 17, bolest kloubů a entezí), proto byl MTX v prosinci 2019 vysazen a byla zvažována jiná konvenční systémová léčba psoriázy. Léčba acitretinem byla kontraindikována vzhledem k dyslipidemii a mírné elevaci hodnot jaterních testů. Léčba cyklosporinem byla kontraindikována vzhledem k dekompenzované hypertenzi.
zek 1A, B, a suspekci na PsA byla zahájena systémová terapie metotrexátem (MTX) v iniciální dávce 7,5 mg týdně s postupnou titrací na 20 mg týdně, kterou pacient užíval bez nežádoucích účinků.
Revmatologické vyšetření v dubnu 2018 potvrdilo diagnózu PsA – oligoartikulární a entezopatická forma. Revmatologem bylo doporučeno pokračovat v zavedené terapii MTX jak z kožní, tak i z kloubní indikace. Diagnóza psoriázy byla histopatologicky verifikována v květnu 2018. Terapie MTX byla
 Pacient absolvoval v únoru 2020
revmatologické vyšetření se závěrem progrese PsA
a s doporučením zahájení biologické terapie. Od února
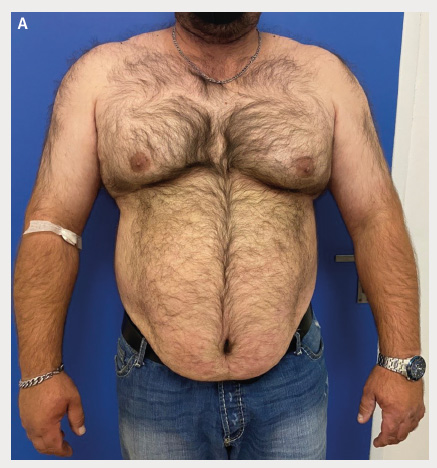
2020 jsme vzhledem k progresi psoriázy (kožního i kloubního
postižení) zahájili terapii guselkumabem, při níž došlo
postupně k plné regresi kožních projevů (BSA 0, PASI 0), obrázek 2A, B. Poslední revmatologické vyšetření v září
2021 bylo se závěrem remi
Pacient absolvoval v únoru 2020
revmatologické vyšetření se závěrem progrese PsA
a s doporučením zahájení biologické terapie. Od února
2020 jsme vzhledem k progresi psoriázy (kožního i kloubního
postižení) zahájili terapii guselkumabem, při níž došlo
postupně k plné regresi kožních projevů (BSA 0, PASI 0), obrázek 2A, B. Poslední revmatologické vyšetření v září
2021 bylo se závěrem remi
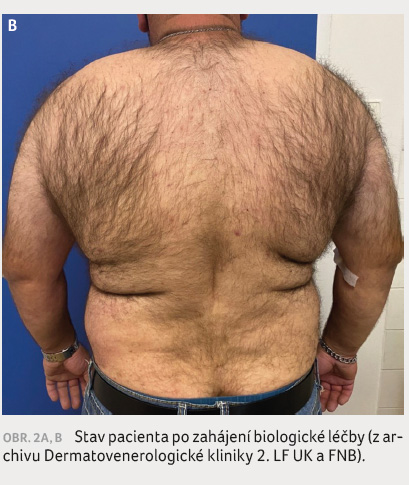
se PsA a s doporučením pravidelných revmatologických kontrol. Pacient je se zavedenou biologickou léčbou velmi spokojen, aplikace zvládá bez obtíží, terapii toleruje bez nežádoucích účinků. Přetrvává dlouhodobá remise psoriázy i PsA.
Diskuse
Psoriatická artritida může mít větší vliv na snížení kvality života pacientů než samostatná psoriáza. Taktéž výskyt komorbidit může být u pacientů s PsA vyšší než u pacientů pouze s kožním postižením, což je dáno zvýšenou systémovou zánětlivou zátěží souběžným onemocněním kůže a kloubů [18].
Obezita je důležitou komorbiditou u pacientů s psoriázou a PsA. Obezita zvyšuje riziko vzniku PsA, pravděpodobně v souvislosti s vyšší hodnotou prozánětlivých mediátorů. Tuková tkáň je metabolicky aktivní a u obézních jedinců se rozvíjí chronický zánět nízkého stupně. U pacientů s vyšším BMI je méně pravděpodobné, že dosáhnou minimální aktivity onemocnění. Bylo prokázáno, že redukce hmotnosti vede ke snižování aktivity onemocnění spolu s příznivým ovlivněním diabetes mellitus, hypertenze a ischemické choroby srdeční [19].
Proaktivní screening PsA u pacientů
s psoriázou (mírnou, středně těžkou, těžkou formou) je
klíčem ke včasné diagnóze a intervenci. Dermatologové
mohou pro včasné odhalení příznaků PsA použít krátký
pacientský dotazník PEST (Psoriasis Epidemiology Screening Tool)
obsahující pět jednoduchých otázek (tab. 2). Každá
kladná odpověď je hodnocena jedním bodem. Zisk tří a více
bodů znamená pravděpodobnou PsA a pacient by měl být
odeslán k revmatologickému vyšetření [7]. Dotazník PEST je
užitečným nástrojem k identifikaci PsA u nemocných
s psoriázou [20]. Při fyzikálním vyšetření bychom se měli
zaměřit na prsty rukou a nohou (daktylitida), Achillovy
šlachy (entezitida), sakroiliakální a velké klouby (kolena,
lokty), kůži a nehty [4]. Včasná terapeutická intervence je
důležitá pro prevenci trvalého strukturálního poškození
a ztráty funkčnosti kloubů [7].
Guselkumab, plně humánní monoklonální protilátka proti podjednotce p19 IL 23, blokuje signální dráhu prozánětlivých cytokinů IL 23/IL 17, která se ukazuje jako klíčová pro patogenezi psoriázy a PsA. Guselkumab je schválen k léčbě dospělých pacientů se středně těžkou až těžkou psoriázou a aktivní PsA. Doporučená dávka je 100 mg podávaných subkutánně pomocí předplněného pera či injekce v nultém a čtvrtém týdnu, následuje udržovací aplikace jednou za osm týdnů. Nízká frekvence aplikací je výhodou guselkumabu a může zlepšit adherenci pacientů k léčbě. V klinických studiích byl profil nežádoucích účinků guselkumabu podobný jako u placeba. Reich a kol. publikovali pětiletá data o účinnosti a bezpečnosti guselkumabu v léčbě pacientů se středně těžkou až těžkou psoriázou. Více než 80 % nemocných si po pěti letech udrželo PASI 90 (90% zlepšení indexu plochy postižení a závažnosti psoriázy) a více než 50 % nemocných PASI 100 (kompletní remise). I po pěti letech léčby pokračuje v terapii guselkumabem více než 80 % nemocných. McInnes a kol. publikovali dvouletá data o účinnosti a bezpečnosti guselkumabu v léčbě pacientů s aktivní PsA [21-24].
Závěr
Psoriatická artritida je heterogenní rychle se rozvíjející onemocnění, které je spojeno s potenciálním rizikem závažného průběhu a strukturální progrese a obvykle se objevuje až po vzniku kožních projevů, přibližně do 10 let, tj. ve třetí až páté dekádě života. Dermatologové mohou včasným rozpoznáním PsA u pacientů s psoriázou a zahájením adekvátní terapie ve spolupráci s revmatology zabránit progresi onemocnění a trvalé invaliditě [4,6]. Cílem současné léčby PsA je dosažení a udržení remise nebo případně nízké aktivity onemocnění a zlepšení kvality života pacientů [17]. Guselkumab, subkutánně podávaná plně humánní monoklonální protilátka proti podjednotce p19 IL 23, blokuje signální dráhu prozánětlivých cytokinů IL 23/IL 17, která se ukazuje jako klíčová pro patogenezi psoriázy a PsA. Guselkumab představuje ověřenou a dlouhodobě účinnou léčbu psoriázy a PsA, což potvrzují i publikovaná data z klinických studií [21-24].
Seznam použité literatury
- [1] Torales J, Echeverría C, Barrios I, et al. Psychodermatological mechanisms of psoriasis. Dermatol Ther 2020; 33: e13827.
- [2] Ghoreschi K, Balato A, Enerbäck C, Sabat R. Therapeutics targeting the IL‑23 and IL‑17 pathway in psoriasis. Lancet 2021; 397: 754−766.
- [3] Oliveira Mde F, Rocha Bde O, Duarte GV. Psoriasis: classical and emerging comorbidities. An Bras Dermatol 2015; 90: 9−20.
- [4] Menter MA, Armstrong AW, Gordon KB, Wu JJ. Common and Not‑So‑Common Comorbidities of Psoriasis. Semin Cutan Med Surg 2018; 37(2S): S48−S51.
- [5] Kovitwanichkanont T, Chong AH, Foley P. Beyond skin deep: addressing comorbidities in psoriasis. Med J Aust 2020; 212: 528−534.
- [6] Gottlieb A, Merola JF. Psoriatic arthritis for dermatologists. J Dermatolog Treat 2020; 31: 662−679.
- [7] Gottlieb AB, Merola JF. Axial psoriatic arthritis: An update for dermatologists. J Am Acad Dermatol 2021; 84: 92−101.
- [8] Tiwari V, Brent LH. Psoriatic Arthritis. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2022 Jan. 2021 Aug 11. Dostupné na: https://www.ncbi.nlm.nih.gov/books/NBK547710/
- [9] Peluso R, Iervolino S, Vitiello M, et al. Extra‑articular manifestations in psoriatic arthritis patients. Clin Rheumatol 2015; 34: 745−753.
- [10] Gladman DD, Ye JY, Chandran V, et al. Oligoarticular vs Polyarticular Psoriatic Arthritis: A Longitudinal Study Showing Similar Characteristics. J Rheumatol 2021; 48: 1824−1829.
- [11] Schons KR, Knob CF, Murussi N, et al. Nail psoriasis: a review of the literature. An Bras Dermatol 2014; 89: 312−317.
- [12] Fotiadou C, Lazaridou E. Psoriasis and uveitis: links and risks. Psoriasis (Auckl) 2019; 9: 91−96.
- [13] de Vlam K, Gottlieb AB, Mease PJ. Current concepts in psoriatic arthritis: pathogenesis and management. Acta Derm Venereol 2014; 94: 627−634.
- [14] Boutet MA, Nerviani A, Gallo Afflitto G, Pitzalis C. Role of the IL‑23/IL‑17 Axis in Psoriasis and Psoriatic Arthritis: The Clinical Importance of Its Divergence in Skin and Joints. Int J Mol Sci 2018; 19: 530.
- [15] Nast A, Smith C, Spuls PI, et al. EuroGuiDerm Guideline on the systemic treatment of Psoriasis vulgaris − Part 1: treatment and monitoring recommendations. J Eur Acad Dermatol Venereol 2020; 34: 2461−2498.
- [16] Nast A, Smith C, Spuls PI, et al. EuroGuiDerm Guideline on the systemic treatment of Psoriasis vulgaris − Part 2: specific clinical and comorbid situations. J Eur Acad Dermatol Venereol 2021; 35: 281−317.
- [17] Gossec L, Baraliakos X, Kerschbaumer A, et al. EULAR recommendations for the management of psoriatic arthritis with pharmacological therapies: 2019 update. Ann Rheum Dis 2020; 79: 700−712.
- [18] Skornicki M, Prince P, Suruki R, et al. Clinical Burden of Concomitant Joint Disease in Psoriasis: A US‑Linked Claims and Electronic Health Records Database Analysis. Adv Ther 2021; 38: 2458−2471.
- [19] Kumthekar A, Ogdie A. Obesity and Psoriatic Arthritis: A Narrative Review. Rheumatol Ther 2020; 7: 447−456.
- [20] Setoyama A, Sawada Y, Saito‑Sasaki N, et al. Psoriasis epidemiology screening tool (PEST) is useful for the detection of psoriatic arthritis in the Japanese population. Sci Rep 2021; 11: 16146.
- [21] Schinocca C, Rizzo C, Fasano S, et al. Role of the IL‑23/IL‑17 Pathway in Rheumatic Diseases: An Overview. Front Immunol 2021; 12: 637829.
- [22] Reich K, Gordon KB, Strober BE, et al. Five‑year maintenance of clinical response and health‑related quality of life improvements in patients with moderate‑to‑severe psoriasis treated with guselkumab: results from VOYAGE 1 and VOYAGE 2. Br J Dermatol 2021; 185: 1146−1159.
- [23] McInnes IB, Rahman P, Gottlieb AB, et al. Efficacy and Safety of Guselkumab, an Interleukin‑23p19‑Specific Monoclonal Antibody, Through One Year in Biologic‑Naive Patients With Psoriatic Arthritis. Arthritis Rheumatol 2021; 73: 604−616.
- [24] McInnes IB, Rahman P, Gottlieb AB, et al. Long‑Term Efficacy and Safety of Guselkumab, a Monoclonal Antibody Specific to the p19 Subunit of Interleukin‑23, Through Two Years: Results From a Phase III, Randomized, Double‑Blind, Placebo‑Controlled Study Conducted in Biologic‑Naive Patients With Active Psoriatic Arthritis. Arthritis Rheumatol 2021 Nov 1; doi: 10.1002/art.42010 [online ahead of print].