Hidradenitis suppurativa
Souhrn
Cerovská Z, Kysilka Z, Slonková V, Stuchlík D. Hidradenitis suppurativa. Remedia 2024; 34: 184–192.
Hidradenitis suppurativa (HS) je chronické onemocnění terminálních pilosebaceózních žláz primárně se projevující bolestivými zánětlivými recidivujícími noduly a abscesy, které opakovaně praskají, a vedou tak k tvorbě píštělí a jizev. Projevy HS lze rozdělit na dvě formy – zánětlivou a nezánětlivou –, které pak určují způsob léčby pacienta. Hidradenitis suppurativa je spojena s četnými komorbiditami, jako jsou např. obezita, kouření, deprese, idiopatické střevní záněty, axiální spondyloartritida aj., proto je klíčová multioborová spolupráce.
Klíčová slova: hidradenitis suppurativa – Hurleyho skóre – IHS4 – léčba – komorbidity.
Summary
Cerovska Z, Kysilka Z, Slonkova V, Stuchlik D. Hidradenitis suppurativa. Remedia 2024; 34: 184–192.
Hidradenitis suppurativa (HS) is a chronic disease of the terminal pilosebaceous glands, manifesting primarily by recurrent painful inflammatory nodules and abscesses that tend to rupture and thus form fistulas and scars. Two distinct forms of HS – inflammatory and non‑inflammatory – require different clinical approach. HS is associated with multiple comorbidities including obesity, smoking, depression, inflammatory bowel disease, axial spondylarthritis, etc. Cooperation of various specialists in the management of patients suffering from HS is mandatory.
Key words: hidradenitis suppurativa – Hurley score – IHS4 – treatment – comorbidities.
Úvod
Hidradenitis suppurativa (HS) dle Mezinárodní klasifikace nemocí (MKN‑10) označená kódem L73.2 – dříve nazývaná také acne inversa – je chronické onemocnění terminálních pilosebaceózních žláz primárně se projevující bolestivými zánětlivými recidivujícími noduly a abscesy, které opakovaně praskají, a vedou tak k tvorbě sinusových traktů/tunelů a jizvení. Projevy se typicky vyskytují v predilekčních lokalizacích v apokrinních žlázových oblastech těla (axilárně, submammárně, inguinálně, gluteálně a genitálně), a ačkoliv lze klinickou diagnózu stanovit s 97% přesností, je toto onemocnění stále málo známé. To potvrzuje zpoždění ve stanovení klinické diagnózy, které činí např. v Německu 10 ± 9,6 roku [1].
Patogeneze
Vznik onemocnění je vysvětlován dvěma procesy – abnormální diferenciací keratinocytů terminální části pilosebaceózních žláz a následným masivním zánětem (obr. 1) [2]. Podobně jako u akné také u HS hyperkeratóza způsobí okluzi horní části vlasového folikulu. Na rozdíl od acne vulgaris nehraje v patogenezi HS úlohu nadprodukce mazu nebo změna jeho složení. Dilatace a prasknutí vlasového folikulu způsobují smíšenou zánětlivou reakci, jizvení a tvorbu píštělí. Zánětu se účastní více populací imunitních buněk, zejména aktivované B lymfocyty, plazmocyty, dendritické buňky, neutrofilní granulocyty a osa Th1/Th17. Ke spouštěcím faktorům onemocnění řadíme kouření, obezitu, mechanické dráždění, bateriální kolonizaci a genetickou predispozici [1]. Při větším tělesném povrchu vznikají větší intertriginózní plochy – místa mechanického dráždění – způsobující kožní mikropoškození, které uvolňuje tzv. molekulární vzorce asociované s poškozením (damage‑associated molecular patterns, DAMPs) a podporuje vstup těchto molekul do kůže, čímž spouští další zánětlivou reakci. Obezita taktéž podněcuje subklinický zánět v tukové tkáni a sekreci dalších proinflamatorních cytokinů [2,3]. Nikotin stimuluje acetylcholinové receptory, což vede k epidermální hyperplazii v infundibulu mazové žlázy a k její okluzi [1]. U pacientů trpících HS bylo pozorováno dysbiotické prostředí a oportunní bakteriální flóra v místech zánětu. Nacházíme také vyšší frekvenci anaerobních bakterií ve srovnání se zdravými jedinci. Otázkou zůstává, jestli je dysbióza vyvolávajícím faktorem, nebo důsledkem zánětlivé reakce [1].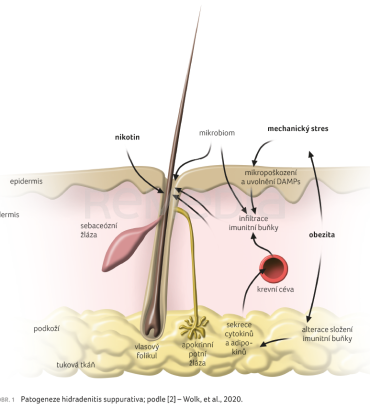
Klinický obraz
Klinicky se HS projevuje jako zánětlivé noduly, abscesy, píštěle, které se hojí jizvami. Jsou provázeny bolestivostí, zápachem a hnisavou sekrecí [3]. Predilekční lokalizací jsou axily, třísla, vnitřní strany stehen, hýždě, oblast pubis, skrota, vulvy a konečníku. Rovněž se projevy mohou vyskytovat na hrudníku, ve kštici a retroaurikulárně. K dalším znakům onemocnění patří chronicita a relapsy [4].
Dle klinických projevů můžeme HS rozdělit na fenotyp zánětlivý (aktivní) a predominantně nezánětlivý (neaktivní). Typickými znaky zánětlivého fenotypu jsou papuly, pustuly, zánětlivé noduly a abscesy. Tvorba píštělí, sinusů a jizev je charakteristická pro neaktivní fenotyp [1].
Diferenciální diagnostika
Do diferenciálně diagnostické úvahy patří acne vulgaris, folikulitida, pilonidální cysta, kožní projevy Crohnovy choroby, granuloma inguinale, neoplazie a další. Od acne vulgaris odlišují HS predilekční lokalizace, hloubka lézí, píštěle a provazcovité jizvy. Na rozdíl od HS folikulitida po vhodné antibiotické terapii rychle regreduje, nepozorujeme komedony, perzistující píštěle nebo hypertrofické jizvy [1,3]. Někteří autoři uvádějí, že pilonidální cysta by mohla být fenotypovou variantou lokalizované formy HS [5]. Granuloma inguinale se vyskytuje především v tropických oblastech, patří mezi klasické venerické choroby, je způsobena bakterií Klebsiella granulomatis a klinicky se projevuje jako zvětšující se vřed s hypertrofickou spodinou [3].
Skórovací systémy
K monitorování pacienta a hodnocení rozsahu onemocnění bylo vytvořeno několik hodnoticích skóre. Nejstarší klasifikací je Hurleyho skóre, které je doposud i nejpoužívanějším. Rozděluje pacienty do tří stadií: I. – izolované abscesy, bez píštělí a bez jizvení; II. – izolované a/nebo mnohočetné recidivující abscesy s tvorbou píštělí a jizvením s postižením větší plochy kůže; III. – rozsáhlé difuzní postižení pospojovaných píštělí a abscesů. Nicméně je to statická klasifikace, a proto není vhodná ke sledování účinnosti léčby pacienta.
Od roku 2017 je k dispozici mezinárodní skórovací systém IHS4 (International Hidradenitis Suppurativa Severity Scoring System), jenž jednoduchým způsobem počítá množství nodulů, abscesů a píštělí a je vhodnější k hodnocení dynamiky a progrese onemocnění (tab. 1) [6]. Vzhledem k psychologickému dopadu na život nemocného je rovněž vhodné pravidelně vyhodnocovat stav prostřednictvím indexu kvality života (Dermatology Life Quality Index, DLQI) a vizuální analogové škály bolesti (Visual Analogue Scale, VAS) k celkovému náhledu na potíže pacienta a jeho omezení v každodenním životě [1,6,7].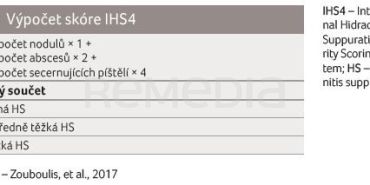
V České republice pacienty s těžkými projevy HS, kteří jsou léčeni biologiky, monitorujeme a údaje zadáváme do registru BIOREP, do něhož jsou zapojena všechna centra biologické léčby.
Souhrn nových doporučení, nové guidelines
Vzhledem k chronicitě onemocnění a jeho dopadu na kvalitu života pacienta je včasná diagnostika HS a volba vhodného léčebného postupu zásadní k minimalizaci mutilace nemocného [1,8].
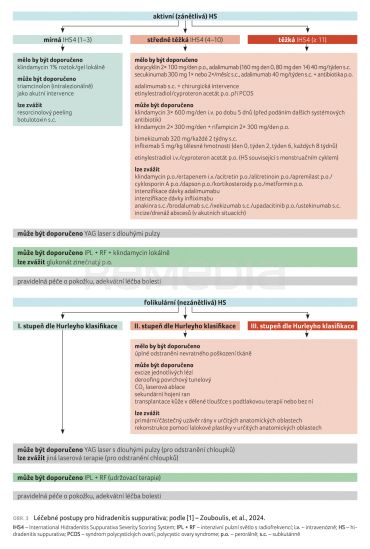
Dle nejnovějších publikací a také doporučení Evropské nadace pro hidradenitis suppurativa (European Hidradenitis Suppurativa Foundation, EHSF) z roku 2024 se u HS rozlišuje podle aktivity onemocnění aktivní, zánětlivá a neaktivní, převážně nezánětlivá forma [1]. Léčba zánětlivé formy HS se dělí pomocí klasifikace IHS4 na lehkou, střední a těžkou formu a opírá se o konzervativní medikamentózní léčbu, která zahrnuje nejen terapii lokální a systémovou, ale též cílenou. Naproti tomu nezánětlivá forma HS se dle Hurleyho klasifikace dělí na I., II., a III. stupeň a léčí se převážně chirurgickými postupy [1].
Léčba onemocnění
Terapie zánětlivé (aktivní) formy choroby
Jak již bylo zmíněno, nejnovější terapeutická doporučení u zánětlivé formy HS se opírají o konzervativní léčbu. Řadíme sem lokální léčbu, systémovou antibiotickou terapii a cílenou terapii. Včasné zahájení farmakoterapeutické intervence je důležité i pro tzv. okno příležitosti, tedy vliv léčby na stav onemocnění v čase, kdy je tento efekt při terapii nodulů a abscesů nejzřetelnější [1].
Lokální terapie
V případě mírné HS (IHS4 1–3) můžeme volit topickou terapii – klindamycin 1% gel/roztok či krém v použití dvakrát denně, který se dle studií ukazuje účinnější než jeho perorální forma. Dále můžeme volit také resorcinolový 15% gel, opět v použití dvakrát denně, který má navíc keratolytický, antipruriginózní a antiseptický účinek [9]. V úvahu přichází rovněž 15% resorcinolový peeling u pacientů s mírnou až středně těžkou HS [1].
V léčbě dále přichází v úvahu aplikace kortikosteroidů intralezionálně (triamcinolon) ke zmírnění akutního zánětu. Mezi další lokální léčebné metody lze zařadit botulotoxin aplikovaný subkutánně [1], tato léčba však není v ČR hrazena ze zdravotního pojištění.
Systémová antibiotická terapie
Systémová terapie je určena pro středně těžké (IHS4 4–10) a závažné formy HS (IHS4 ≥ 11), nově je doporučováno systémové podávání perorálních tetracyklinů (doxycyklin nebo minocyklin) v dávce 100 mg dvakrát denně, ev. 50 mg dvakrát denně, kdy je jejich použití srovnatelné s účinností kombinace klindamycin 300 mg dvakrát denně a rifampicin 300 mg dvakrát denně. Zkrácení doby tohoto typu léčby lze dosáhnout intravenózní systémovou antibiotickou terapií klindamycinem (600 mg intravenózně třikrát denně) podávanou po dobu pěti dnů před další systémovou léčbou [1]. V případě průjmů se pak doporučuje záměna této terapie za minocyklin 100 mg/den. Dle doporučení z roku 2024 by léčba tetracykliny navíc měla být superiorní u pacientů, kteří současně trpí akné, nebo u pacientů se superficiálními lézemi (folikuly, papuly, pustuly) [1].
Systémovou antibiotickou terapii lze podávat po dobu 12 týdnů, která se jeví jako optimální v managementu inflamatorních procesů. Kratší nebo delší systémová antibiotická terapie pravděpodobně nepřináší větší prospěch, tedy nejpozději po třech měsících léčby systémovými antibiotiky je nutné vyhodnotit efekt léčby a v případě nedostatečného účinku přejít na jinou formu terapie [1].
Léčba systémovými kortikosteroidy
Tato léčba je vyhrazena pro akutní vzplanutí HS nebo k přemostění dlouhodobé terapie, kdy používáme krátkodobé pulzy kortikosteroidů 0,5–1 mg/kg/den [1].
Biologická terapie
Inhibitor tumor nekrotizujícího faktoru alfa (TNFα – adalimumab) a inhibitor interleukinu (IL) 17A (secukinumab) představují v současné době jediná schválená léčiva pro farmakologickou léčbu HS. Adalimumab je určen pro léčbu středně těžké až těžké HS u pacientů ve věku od 12 let, kteří nedostatečně reagovali na systémovou konvenční terapii (tj. nepřetržitou systémovou antibiotickou terapii po dobu 12 týdnů).
Dále lze dle nejnovějších poznatků zvážit další inhibitory IL‑17 (bimekizumab, brodalumab, ixekizumab), inhibitor IL‑1 (anakinra), inhibitory IL‑12/23 (ustekinumab), léčbu inhibitory Janusovy kinázy (JAK – upadacitinib) [1].
Terapie nezánětlivé (neaktivní) formy choroby
K léčbě nezánětlivé formy HS volíme zvláště chirurgické přístupy, neboť zánětlivé změny vedly u pacienta k nevratné destrukci tkáně, která tak nereaguje adekvátně na farmakologickou léčbu. Chirurgické přístupy zahrnují incize a drenáž, tzv. mini‑unroofing, standardní deroofing nebo širokou excizi. Cílem chirurgické léčby je odstranění veškeré nevratně poškozené tkáně. Chirurgický zákrok musí být kombinován se systémovou protizánětlivou léčbou, aby bylo dosaženo co nejvyšší léčebné odpovědi [1].
Jako alternativu ke konvenčním chirurgickým zákrokům lze zvolit také ablaci lézí CO2 laserem [10].
Chirurgická léčba
Incizi a drenáž používáme na zánětlivé a hnisavé léze, solitární projevy, avšak tyto přístupy nepředstavují dlouhodobou terapii HS vzhledem k téměř 100% míře recidivy [11,12]. Po tomto akutním řešení následuje antibiotická terapie.
Standardní deroofing („odstranění střechy“) je užíván u HS II. stupně podle Hurleyho klasifikace k odstranění svrchní části povrchové léze abscesu, nodulu nebo sinusového traktu nůžkami, elektrokauterem nebo CO2 laserem s ponecháním epitelu tzv. dna. Postup umožňuje zacelení bez vzniku dalšího hnisavého obsahu (obr. 2A, B). Tato technika se provádí převážně v lokální anestezii a míra recidivy u ní činí asi 17 % [12]. Mini‑unroofing slouží k odstranění malé akutní nebo subakutní zánětlivé léze použitím 8mm punch biopsie (minibiopsie).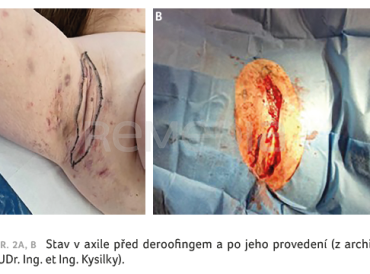
Široká excize v případě HS III. stupně dle Hurleyho klasifikace slouží k odstranění veškeré postižené oblasti až do zdravé tukové tkáně (tj. 1–2 cm od viditelných hranic), u hlubokých nebo rozsáhlých projevů, při přítomnosti hypertrofických nebo fibrotických jizev. Tunely a jizevnatá tkáň v okrajové oblasti by měly být intraoperačně vizualizovány a kompletně odstraněny, k jejich vizualizaci lze použít intraoperační injekci barviva (např. toluidinovou modř) nebo termografii [1]. Podle nejnovějších guidelines EHSF 2024 jsou doporučené okraje pro axilu, tříslo a genitál 2 cm, pro trup a krk 3 cm a pro gluteální oblast 4 cm [1]. Primární uzávěr volíme pro lokální excizi jednotlivých uzlin a abscesů u HS II. stupně dle Hurleyho, sekundární hojení ran pak po kompletní chirurgické excizi nevratně poškozené tkáně [1,12].
Uzavření defektu sekundárním hojením představuje standardní možnost po radikální operaci, kdy toto hojení trvá v závislosti na velikosti rány i 2–3 měsíce. V rámci pooperační péče je nutné pacienta edukovat o zvýšené nutnosti hygienických opatření a vyhnutí se znehybnění rány, aby se předešlo omezení pohybu v důsledku jizvení [12].
Anestezie
Lokální anestezii volíme u incizí a drenáží, mini‑unroofingu nebo deroofingu, kdy začínáme aplikovat anestetikum z periferie, tj. z nepostižené (zdravé) oblasti do postižených míst. Tumescentní lokální anestezie je dle EHSF 2024 doporučena jako první volba u většiny HS I.–II. stadia a u některých HS III. stadia [1]. K celkové či spinální anestezii bychom měli přistupovat vždy u rozsáhlých oblastí HS III. stadia, u HS v perianální oblasti či v případě úzkostných pacientů.
Ultrasonografie
Ultrasonografie by měla být dle nejnovějších doporučení nedílnou součástí předoperačního vyšetření s cílem ozřejmení traktů a sinů a vhodné volby chirurgického přístupu. V této souvislosti se používá dopplerovský monitoring, který umožňuje sledovat a hodnotit aktivitu onemocnění [13].
Jiné metody léčby
Podle výsledků dosavadních studií mají pacienti trpící HS nižší koncentraci zinku v krvi [14], proto lze u mírné až středně těžké HS zvážit perorální systémovou léčbu glukonátem zinečnatým v dávkovacím schématu 90 mg/den po dobu tří měsíců [10].
Intralezionální aplikace kortikosteroidů (infiltrace triamcinolon acetonidem 10 mg/ml – 0,5–1,0 ml v kombinaci s lokálními anestetiky) volíme při léčbě akutních zánětlivých lézí k dosažení procesu hojení (klinická odpověď nastává po 48–72 hodinách). Tuto léčbu je možné pacientům nabídnout jako monoterapii i jako doplňkovou léčbu lézí u HS I. stupně dle Hurleyho klasifikace [1].
Na základě nejnovějších doporučení lze ke snížení celkového počtu lézí a zlepšení kvality života použít také terapii botulotoxinem (50 U/ml) 0,05–0,1 ml intradermálně ve vzdálenosti 1–1,5 cm mezi místy vpichu v postižené oblasti a perilezionálně (o maximální celkové dávce 4 000 U každé tři měsíce) [1]. Uvedenou léčbu si však v ČR musí hradit pacient sám, neboť není začleněna do úhrady z prostředků veřejného zdravotního pojištění.
 Kombinovanou léčbu intenzivním pulzním světlem (IPL) s radiofrekvencí (RF) a lokálním klindamycinem je možné použít jako alternativu k lokální monoterapii klindamycinem u mírných a středně těžkých forem HS, monoterapii IPL + RF volíme jako udržovací terapii [1]. Dále lze jako alternativní protizánětlivou terapii u pacientů s mírnou až středně těžkou HS doporučit použití pulzujícího neodymového YAG laseru, který má využití i při destrukci vlasových folikulů ve smyslu sekundární prevence HS [12].
Kombinovanou léčbu intenzivním pulzním světlem (IPL) s radiofrekvencí (RF) a lokálním klindamycinem je možné použít jako alternativu k lokální monoterapii klindamycinem u mírných a středně těžkých forem HS, monoterapii IPL + RF volíme jako udržovací terapii [1]. Dále lze jako alternativní protizánětlivou terapii u pacientů s mírnou až středně těžkou HS doporučit použití pulzujícího neodymového YAG laseru, který má využití i při destrukci vlasových folikulů ve smyslu sekundární prevence HS [12].
Léčebné postupy pro HS znázorňuje obrázek 3 [1].
Management bolesti
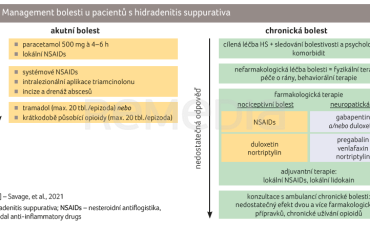 Jedním z významných faktorů snížení kvality života pacientů trpících HS je bolestivost, a to jak chronická, tak akutní, při vzplanutí onemocnění. Chronická bolestivost se pak podílí na vzniku anxiózních a depresivních poruch. Bolest u pacientů s HS rozdělujeme na nociceptivní a neuropatickou. Nociceptivní bolest vzniká dysfunkcí somatosenzorického systému na podkladě poškození tkáně. Neuropatická bolest je výsledkem chronického zánětu, který způsobuje změny na periferní i centrální senzitivní dráze. Tabulka 2 shrnuje doporučený postup terapie bolesti u pacientů s HS [15].
Jedním z významných faktorů snížení kvality života pacientů trpících HS je bolestivost, a to jak chronická, tak akutní, při vzplanutí onemocnění. Chronická bolestivost se pak podílí na vzniku anxiózních a depresivních poruch. Bolest u pacientů s HS rozdělujeme na nociceptivní a neuropatickou. Nociceptivní bolest vzniká dysfunkcí somatosenzorického systému na podkladě poškození tkáně. Neuropatická bolest je výsledkem chronického zánětu, který způsobuje změny na periferní i centrální senzitivní dráze. Tabulka 2 shrnuje doporučený postup terapie bolesti u pacientů s HS [15].
Komorbidity a jejich management
Obezita
Metabolický syndrom pravděpodobně přispívá k rozvoji HS. Některé studie rovněž prokázaly pozitivní korelaci mezi závažností HS a hodnotou indexu tělesné hmotnosti (BMI). Při větším tělesném povrchu vznikají větší intertriginózní plochy, místa mechanického dráždění, čímž se zvyšuje možnost folikulární okluze [3]. Velmi nízkokalorická ketodieta může zmírňovat zánět a oxidativní stres v organismu, a tím projevy HS [16].
Kouření
Nikotin stimuluje acetylcholinové receptory, což vede k epidermální hyperplazii v infundibulu mazové žlázy a k její okluzi [1]. Incidence HS je u kuřáků dvakrát vyšší [17]. Aktivní kuřáci mají větší počet postižených míst na těle než nekuřáci a bývalí kuřáci. Pacientům je doporučováno přestat kouřit také vzhledem k prokázané nižší odpovědi na léčbu u kuřáků [18].
Idiopatické střevní záněty
Pacienti s gastrointestinálními potížemi a/nebo perianálními píštělemi by měli být vyšetřeni gastroenterologem k vyloučení Crohnovy choroby a ulcerózní kolitidy [1]. Test pro detekci kalprotektinu ve stolici je vysoce specifický a senzitivní k diagnostice idiopatických střevních zánětů u pacientů s HS [19].
Axiální spondyloartritida
Pacienti trpící HS mají vyšší riziko vzniku spondyloartitidy, nezávisle na věku a pohlaví a závažnosti HS. Pacienti s bolestmi v lumbální části zad by měli být vyšetřeni revmatologem [1].
Malignity
Skvamocelulární karcinom je raritní, avšak závažnou komplikací u pacientů s HS. Častěji se vyskytuje u mužů a průměrný interval mezi diagnostikou HS a rozvojem skvamocelulárního karcinomu je přibližně 24 let [20].
Lymfedém
Chronický zánět a jizvení mohou vyústit do obstrukce lymfatických cév a způsobovat lymfedém, zejména v anogenitální oblasti [21].
Psychologická zátěž
Chronicita onemocnění, zánět provázený bolestivostí a drénováním séropurulentního obsahu způsobují u pacientů pocit studu, izolace. Jejich denní aktivity, spánek i sexuální život jsou často narušeny, což může vést až k depresím a zvýšenému riziku suicidia. Proto je důležité se pacientů dotazovat i na jejich psychickou pohodu, kterou můžeme pravidelně monitorovat pomocí dotazníků DLQI, VAS, případně HiSQOL (Hidradenitis Suppurativa Quality of Life), a v indikovaných případech rizikového nemocného odeslat k psychologickému nebo psychiatrickému vyšetření [8,22].
Pacient s hidradenitis suppurativa u ambulantního dermatologa
Včasné stanovení diagnózy hraje klíčovou roli, neboť umožňuje zahájit individualizovanou léčbu [1]. Diagnózu HS stanovíme především klinicky – zhodnocením kožního povrchu pacienta, pohmatem, případně následnou sondáží tunelů. Pozornost bychom měli věnovat folikulárně vázaným zánětlivým bolestivým nodulům, abscesům, přítomnosti tunelů a jizev v predilekčních, ale také v jiných lokalizacích. Recidivy těchto lézí v posledních šesti měsících s nejméně dvěma lézemi v predilekčních lokalizacích indikují přítomnost onemocnění s přesností až 97 % [23].
Po podrobné anamnéze a stanovení diagnózy je nutné pacienta informovat nejen o nemoci, jejím průběhu, možných chorobu zhoršujících faktorech (kouření, obezita), ale i o jednotlivých možnostech léčby. V závislosti na závažnosti a lokalizaci onemocnění je rovněž žádoucí vyloučit možné komorbidity.
Podle formy a tíže onemocnění by měl ambulantní lékař neprodleně zahájit vhodnou léčbu. Před samotným zahájením antibiotické terapie lze zvážit provedení laboratorního vyšetření (krevní obraz, jaterní testy), během léčby rifampicinem se doporučují pravidelné kontroly jaterních a ledvinných parametrů a krevního obrazu [1].
V případě těžkého postižení (II.–III. stupně dle Hurleyho klasifikace, IHS4 střední až těžká forma) je nutné zahájit neprodleně systémovou antibiotickou terapii a takto předléčeného pacienta odeslat do nejbližšího centra biologické léčby. V lékařské zprávě je pak nutné kromě celkové anamnézy a dosavadní terapie uvést zvláště délku trvání antibiotické terapie včetně data jejího zahájení.
Závěr
Hidradenitis suppurativa má významný dopad na kvalitu života pacientů, přispívá k chronické bolesti, zhoršení nebo vzniku psychických komorbidit (deprese, úzkosti), ke zvýšenému riziku sebevražd, vede k poruchám spojeným s užíváním návykových látek, narušuje sociální, volnočasové aktivity a spánek postižených a zhoršuje intimní vztahy [22]. Nové guidelines proto doporučují u pacientů s HS také monitoring kvality života (DLQI) a bolesti (VAS). Včasné zahájení léčby a volba vhodných léčebných postupů jsou kruciální, neboť v době okna příležitosti výrazně snižují progresi onemocnění do ireverzibilních stadií. Aktivita onemocnění by pak měla být průběžně hodnocena, v současnosti je doporučováno použití zejména mezinárodního skórovacího systému IHS4 [1]. Onemocnění lze rozdělit na dvě formy v souvislosti s přítomností zánětu. Podle intenzity zánětlivé formy rozlišujeme pomocí klasifikace IHS4 lehkou, střední a těžkou HS a léčíme ji medikamentózně [1]. V této indikaci používáme zejména perorální tetracykliny či pětidenní intravenózní terapii klindamycinem, která se účinností vyrovná kombinované systémové léčbě klindamycinem a rifampicinem. Nejnovější léčbu představuje biologická terapie, kde jsou pro HS schváleny subkutánně podávané monoklonální protilátky adalimumab a secukinumab. Nezánětlivou formu hodnotíme pomocí Hurleyho škály stupněm I, II a III a léčíme ji převážně chirurgicky [1]. Kombinace farmakoterapeutického přístupu s chirurgickými metodami je v současnosti považována za ucelený léčebný přístup k HS [1]. Hidradenitis suppurativa je spojena s četnými komorbiditami, jako jsou např. obezita, kouření, idiopatické střevní záněty, lymfedém, malignity, kardiovaskulární onemocnění, axiální spondyloartritida aj., proto je klíčová multioborová spolupráce a také vyhledávání a identifikace rizikových faktorů.
V ambulantní dermatologii je důležité u pacientů s lehkou formou HS zahájit včas vhodnou lokální terapii a u středně závažných forem pečlivě zdokumentovanou systémovou antibiotickou léčbu, nejlépe doxycyklinem v délce 12 týdnů. Středně závažné až závažné formy HS by pak měly být léčeny v centrech biologické a cílené léčby. Terapie těchto pacientů je v ČR dokumentována pomocí registru BIOREP.
MUDr. Zuzana Cerovská
Kožní oddělení Nemocnice Znojmo
MUDr. Jana Janského 2675/11, 669 02 Znojmo 2
e-mail: zuzana.cerovska@nemzn.cz
Literatura
[1] Zouboulis CC, Bechara FG, Fritz K, et al. S2k‑Leitlinie zur Therapie der Hidradenitis suppurativa/Acne inversa (ICD‑10‑Code: L73.2). Aktuelle Dermatologie 2024; 50: 30–83.
[2] Wolk K, Join‐Lambert O, Sabat R. Aetiology and pathogenesis of hidradenitis suppurativa. Online. Brit J Dermatol 2020; 183: 999–1010.
[3] Ingram JR. Hidradenitis suppurativa: Pathogenesis, clinical features, and diagnosis. Dostupné na: https://medilib.ir/uptodate/show/5575 [last update Jun 05, 2023]
[4] Zouboulis CC, Del Marmol V, Mrowietz U, et al. Hidradenitis Suppurativa/Acne Inversa: Criteria for Diagnosis, Severity Assessment, Classification and Disease Evaluation. Dermatology 2015; 231: 184–190
[5] Von Laffert M, Stadie V, Ulrich J, et al. Morphology of Pilonidal Sinus Disease: Some Evidence of Its Being a Unilocalized Type of Hidradenitis Suppurativa. Dermatology 2012; 223: 349–355.
[6] Zouboulis CC, Tzellos T, Kyrgidis A, et al. Development and validation of the International Hidradenitis Suppurativa Severity Score System (IHS4), a novel dynamic scoring system to assess HS severity. Brit J Dermatol 2017; 177: 1401–1409.
[7] Napolitano M, Megna M, Timoshchuk E, et al. Hidradenitis suppurativa: from pathogenesis to diagnosis and treatment. Clin Cosmetic Invest Dermatol 2017; 10: 105–115.
[8] Schultheis M, Grabbe S, Staubach P, et al. Drivers of disease severity and burden of hidradenitis suppurativa: a cross‐sectional analysis on 553 German patients. Int J Dermatol 2024; 63: 188–195.
[9] Cordero‑Ramos J, Barros‑Tornay R, Toledo‑Pastrana T, et al. Effectiveness and safety of topical 15% resorcinol in the management of mild‑to‑moderate hidradenitis suppurativa: A cohort study. J Dermatol 2022; 49: 459–462.
[10] Orenstein LAV, Nguyen TV, Damiani G, et al. Medical and surgical management of hidradenitis suppurativa: a review of international treatment guidelines and implementation in general dermatology practice. Dermatology (Basel, Switzerland) 2020; 236: 393–412.
[11] Ellis LZ. Hidradenitis Suppurativa: Surgical and Other Management Techniques. Dermatol Surg 2012; 38: 517–536.
[12] Shukla R, Karagaiah P, Patil A, et al. Surgical Treatment in Hidradenitis Suppurativa. J Clin Med 2022; 11: 2311.
[13] Mendes‑Bastos P, Martorell A, Bettoli V, et al. The use of ultrasound and magnetic resonance imaging in the management of hidradenitis suppurativa: a narrative review. Brit J Dermatol 2023; 188: 591600.
[14] Poveda I, Vilarrasa E, Martorell A, et al. Serum Zinc Levels in Hidradenitis Suppurativa: A Case‑Control Study. Am J Clin Dermatol 2018; 19: 771–777.
[15] Savage KT, Singh V, Patel ZS, et al. Pain management in hidradenitis suppurativa and a proposed treatment algorithm. J Am Acad Dermatol 2021; 85: 187–199.
[16] Verde L, Cacciapuoti S, Caiazzo G, et al. Very low‑calorie ketogenic diet (VLCKD) in the management of hidradenitis suppurativa (Acne Inversa): an effective and safe tool for improvement of the clinical severity of disease. Results of a pilot study. J Transl Med 2024; 22: 149.
[17] Garg A, Papagermanos V, Midura M, Strunk A. Incidence of hidradenitis suppurativa among tobacco smokers: a population‑based retrospective analysis in the U.S.A. Brit J Dermatol 2018; 178: 709–714.
[18] Bukvić Mokos Z, Miše J, Balić A, Marinović B. Understanding the Relationship Between Smoking and Hidradenitis Suppurativa. Acta Dermatovenerol Croat 2020; 19: 9–13.
[19] Réka P, Janka EA, Soltész L, et al. Chronic Inflammatory Intestinal Disorders in Hidradenitis Suppurativa. Dermatology 2023; 239: 592–600.
[20] Dixon A, Kayarian F, Price T. Squamous Cell Carcinoma in the Setting of Hidradenitis Suppurativa: A Retrospective Review of the Literature. Wounds 2023; 35: e448–e462.
[21] Micieli R, Alavi A. Lymphedema in patients with hidradenitis suppurativa: a systematic review of published literature. Int J Dermatol 2018; 57: 1471–1480.
[22] Patel ZS, Hoffman LK, Buse DC, et al. Pain, Psychological Comorbidities, Disability, and Impaired Qualify of Life in Hidradenitis Suppurativa. Curr Pain Headache Rep 2017; 21: 49.
[23] Vinding GR, Miller IM, Zarchi K, et al. The prevalence of inverse recurrent suppuration: a population‑based study of possible hidradenitis suppurativa. Brit J Dermatol 2014; 170: 884–889.