Evoluce AI embryoscoringu – od prognózy k diagnostice a kontrole kvality
Téma AI embryoscoringu představil MVDr. Daniel Hlinka, Ph.D., (Clayo Clinic, Praha), průkopník humánní embryologie v bývalém Československu, který v roce 1993 provedl první ICSI oplodnění. V oblasti léčby neplodnosti je rovněž iniciátorem řady inovací, které se staly součástí standardních postupů na většině IVF klinik.
V medicíně je reálnou potřebou integrace dat z různých zdrojů a embryoscoring prováděný pomocí umělé inteligence (AI) je jednou z možností, jak data získávat a používat je. Systémů v této oblasti je celá řada. Jedním z nich je tzv. black box, který se u nás začal používat přibližně před 15 lety, ale byl založen pouze na výběru lepších a horších embryí. Z tohoto důvodu jsme navrhli systém (Cognitive Automation of Time‑lapse Images, CATI), který vychází z automatické detekce markerů embryonálního vývoje, tzv. klíčových ukazatelů výkonnosti (key performance indicators, KPIs). Tyto ukazatele sledují vitalitu (schopnost vývoje embrya do blastocysty) a genetickou konstituci embrya (mitotické, meiotické a dědičné chyby).
Biologické principy embryoscoringu
Embryoscoring je zdrojem základních KPIs, které tato data doplňují a vytvářejí komplexní a personalizovaný způsob léčby neplodnosti a představují možný přechod od časté empirické dojmologie k exaktní terapii. Základem je hledání určitého univerzálního principu, jímž je podle doktora Hlinky timing. Znamená to, že náš život se odehrává v cyklech, a také reprodukce je souborem cyklických dějů včetně vývoje embrya, kdy má každé buněčné dělení svůj správný čas a zároveň dokážeme zachytit diferenciaci buněk.
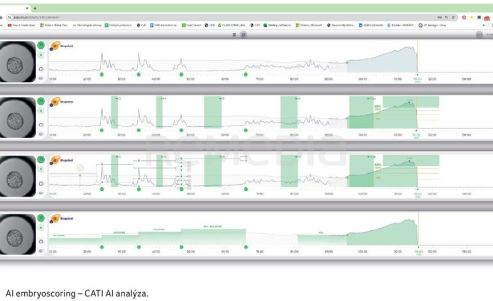 Základními markery jsou tedy časový průběh dělení dceřiných buněk, čas vzniku blastocystové dutiny, z nichž se vypočítává počet mitotických cyklů (délka mitotických cyklů, intervaly mezi děleními). Každá mitóza je specifická, sledujeme korektnost dělení a zachycujeme všechny abnormality (mitotické chyby). Timing dělení je závislý na oocytech, způsob dělení na spermiích. Základní biologické dogma zní: jedna maternální buňka se dělí na dvě dceřiné, sledujeme počet buněk v příslušné mitotické frekvenci. Zároveň zaznamenáváme dosažení úrovně expanze blastocysty (tzv. expansion rate).
Základními markery jsou tedy časový průběh dělení dceřiných buněk, čas vzniku blastocystové dutiny, z nichž se vypočítává počet mitotických cyklů (délka mitotických cyklů, intervaly mezi děleními). Každá mitóza je specifická, sledujeme korektnost dělení a zachycujeme všechny abnormality (mitotické chyby). Timing dělení je závislý na oocytech, způsob dělení na spermiích. Základní biologické dogma zní: jedna maternální buňka se dělí na dvě dceřiné, sledujeme počet buněk v příslušné mitotické frekvenci. Zároveň zaznamenáváme dosažení úrovně expanze blastocysty (tzv. expansion rate).
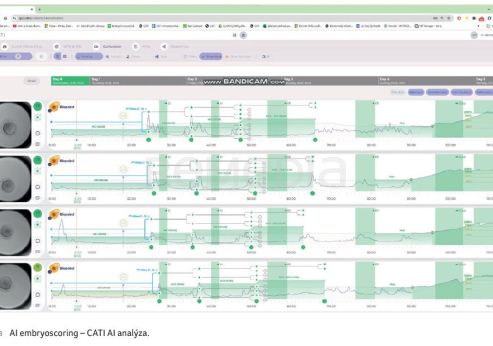 Všechna data jsou po sběru transformována do cloudu a analyzována prostřednictvím AI embryoscoringu (systém CATI). Následně získáváme data s referenčními intervaly, časy, kdy dochází k dělení, informaci o začátku expanze ad. a k dispozici je finální záznam (obr. 1A, B).
Všechna data jsou po sběru transformována do cloudu a analyzována prostřednictvím AI embryoscoringu (systém CATI). Následně získáváme data s referenčními intervaly, časy, kdy dochází k dělení, informaci o začátku expanze ad. a k dispozici je finální záznam (obr. 1A, B).
Růst folikulů a oocytární kompetence, embryonální KPIs
Růstová fáze oocytu během intrafolikulárního vývoje je základem pro embryonální vývoj. Vývojové kompetence oocytů a včasná aktivace embryonálního genomu znamenají normální vývoj embryí. Předčasné zastavení růstu a snížené vývojové kompetence oocytů jsou příčinou abnormálního vývoje embryí. Přestárlé, atretické oocyty vedou k zastavení vývoje embryí, dalším negativním faktorem je vyčerpání zásob oocytů.
„Hledáme tedy embryonální KPIs, jejichž cílem je optimalizace in vitro fertilizační (IVF) léčby,“ vysvětlil MVDr. Hlinka. Tyto KPIs mohou být prospektivní, hodnotící prognózu výsledků, a retrospektivní, jež zkoumají faktory mající vliv na to, jaké embryo získáme. Mezi prospektivní KPIs patří prognostické ukazatele, které analyzují kumulativní šance na porod zdravého dítěte a zahrnují vitalitu a genetickou konstituci embryí (klasický embryoscoring). A dále to jsou diagnostické KPIs, jež zjišťují původ embryonálních anomálií (oocyt, spermie, nebo obě gamety).
Embryo je výslednicí tří faktorů – oocytu, spermie a IVF laboratoře. Embryoscoring představuje významný systém pro kvalitu kontroly embryí. Kontrola kvality posuzuje vliv in vitro podmínek i in vitro podmínky samotné. Na základě výsledků embryonálního vývoje je možné hodnotit kvalitu všech produktů a používaných metodik.
Podle přednášejícího hrají zásadní roli diagnostické KPIs. Oocyt je odpovědný za celý embryonální vývoj z hlediska zásob, samotný oocyt je navíc uzpůsobený k tomu, aby se z něj vyvinula blastocysta. Základní funkcí spermie je aktivovat vajíčko a vytvářet dělicí aparát. Dále je důležité zkoumat procesy při výskytu abnormálního centrozomu nebo abnormálních mitóz, aneuploidie atd. Oocyty, které nemají ukončenou růstovou fázi, nebo přestárlé oocyty většinou zapříčiňují zastavení vývoje embryí.
Prostřednictvím systému CATI lze rozlišovat a zkoumat oocytární faktor a faktor spermií. Na základě procentuálního zastoupení typů embryí dokážeme zpětně dedukovat, jak proběhla stimulace oocytů a jaký je maternální zdroj. V případě posuzování spermií zjišťujeme kvalitu dělení, zaznamenáváme pravidelnost a různé odchylky. Existuje korelace mezi abnormálními spermiemi a výskytem abnormálních dělení.
Závěrem MVDr. Hlinka shrnul, že evoluce embryoscoringu je podle jeho názoru evolucí dat managementu. Navíc lze údaje získané při vývoji embrya eventuálně použít v dalších cyklech IVF.
Kompletní zápis z akce EVOLUTION by Merck 2024 najdete na https://www.remedia.cz/specialy/evolution-by-merck/