Dialogy o moderní léčbě dyslipidemie
Výzvy v léčbě a klinické zkušenosti diskutovali odborníci na nedávném setkání v pražském hotelu Stages Hotel Prague, které uspořádala společnost Novartis v odborné spolupráci s 3. interní klinikou 1. LF UK a VFN v Praze. Sympozium se zaměřilo na aktuální stav léčby dyslipidemie a zkušenosti s terapií inklisiranem.
Odborný program zahájil prof. MUDr. Michal Vrablík, Ph.D., předseda České společnosti pro aterosklerózu a garant akce. V prvním diskusním bloku se spolu s prof. MUDr. Petrem Ošťádalem, Ph.D., FESC, předsedou České kardiologické společnosti a přednostou Kardiologické kliniky FN v Motole, zaměřili na to, jak pečovat o pacienta se zvýšeným kardiovaskulárním (KV) rizikem a dyslipidemií.
Dialog 1: Aktuální situace dyslipidemie a výzvy její léčby v České republice
Celková zátěž české populace KV onemocněními je extrémní a v čase bohužel narůstá. Úmrtnost na KV onemocnění klesá, nicméně stále zaujímáme v úmrtnosti na nemoci oběhové soustavy 10. místo v Evropě. Přednášející se shodli, že před společností stojí stále hodně výzev, jak toto změnit. Mnohá úmrtí lze z hlediska příčiny smrti a věku považovat za předčasná a preventabilní. Dle metodiky EUROSTAT je předčasných zhruba 25 % úmrtí, z nichž je 40–50 % způsobeno oběhovými příčinami.
Počet léčených pacientů narůstá. Aterosklerotická KV onemocnění jsou multifaktoriální, uplatňují se zde environmentální, metabolické a behaviorální vlivy. Mezi hlavními rizikovými faktory dominují vysoký systolický krevní tlak, aterogenní dyslipidemie, vysoký index tělesné hmotnosti (BMI), vysoká glykemie nalačno, dysfunkce ledvin, stres, špatné stravovací návyky, kouření, vysoká konzumace alkoholu a nízká fyzická aktivita, znečištění ovzduší [1]. Pro celoživotní prognózu je důležitá konstelace rizikových faktorů a věk [2], a jak uvedl prof. Ošťádal, ke stanovení celkového KV rizika je třeba posuzovat všechny parametry dohromady.
Incidence KV onemocnění se zvyšuje se zvyšující se sérovou koncentrací cholesterolu s lipoproteiny s nízkou hustotou (LDL‑C) a délkou expozice. Naproti tomu se zdá, že hypolipidemická léčba prospívá pacientům bez ohledu na výši hodnot. Navíc žijeme v populaci s vysokým KV rizikem, kde je mortalita oproti jiným oblastem výrazně zvýšena, například oproti Francii je trojnásobná. Co s tím můžeme dělat?
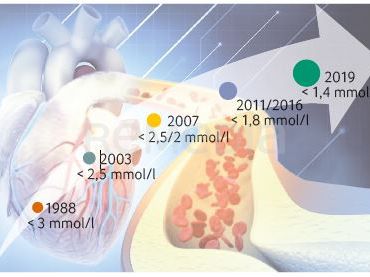 Populační KV riziko je v důsledku vysoké prevalence rizikových faktorů velmi vysoké. Intervence vysokých hladin LDL‑C patří mezi ty nejsnadněji, účinně a bezpečně ovlivnitelné rizikové faktory. Profesor Ošťádal uvedl, že již v rámci primární prevence máme evidenci, že při zvýšení hodnot jen jednoho rizikového faktoru (např. i C‑reaktivního proteinu) zlepšuje intenzivní statinová léčba prognózu pacienta, pravděpodobně i včetně snížení celkové mortality. S každým vydáním doporučených postupů se snižují cílové hodnoty LDL‑C pro rizikové pacienty (obr. 1) a stále platí, že čím níže, tím lépe. Aktuální doporučené postupy udávají pro pacienty s velmi vysokým rizikem jako cílovou hodnotu LDL‑C < 1,4 mmol/l.
Populační KV riziko je v důsledku vysoké prevalence rizikových faktorů velmi vysoké. Intervence vysokých hladin LDL‑C patří mezi ty nejsnadněji, účinně a bezpečně ovlivnitelné rizikové faktory. Profesor Ošťádal uvedl, že již v rámci primární prevence máme evidenci, že při zvýšení hodnot jen jednoho rizikového faktoru (např. i C‑reaktivního proteinu) zlepšuje intenzivní statinová léčba prognózu pacienta, pravděpodobně i včetně snížení celkové mortality. S každým vydáním doporučených postupů se snižují cílové hodnoty LDL‑C pro rizikové pacienty (obr. 1) a stále platí, že čím níže, tím lépe. Aktuální doporučené postupy udávají pro pacienty s velmi vysokým rizikem jako cílovou hodnotu LDL‑C < 1,4 mmol/l.
Přednášející se zamysleli nad tím, zda je dosažení cílových hodnot v reálném prostředí možné. Pacienti z agresivnějšího snížení hodnot LDL‑C profitují. Většina účinných léčebných modalit působí na principu zvýšení katabolismu LDL částic prostřednictvím LDL receptorů (statiny, ezetimib, inklisiran a inhibitory proprotein konvertázy subtilisin‑kexin typu 9 [PCSK9i]). Jejich kombinací je možné i u pacientů s velmi vysokým KV rizikem cílových hodnot dosáhnout. V klinické praxi se samozřejmě setkáváme s non‑adherencí pacientů, která se u dlouhodobé léčby v čase zvyšuje. Přednášející se shodli na tom, že je třeba pacientům v tématu adherence věnovat dostatek času a energie. Zároveň ale není dostatečně využit léčebný potenciál dostupné terapie. Jak ukazují výsledky observačního šetření EUROASPIRE nebo DA VINCI, rozdíly mezi klinickými doporučeními a klinickou praxí pro léčbu dyslipidemie v celé Evropě přetrvávají. Akcentována je up‑titrace dávky statiny a využití kombinační hypolipidemické terapie [3,4]. Nedávno publikovaná retrospektivní studie rovněž dokládá vysokou míru terapeutické inercie [5]. Navzdory tomu, že pacienti cílových hodnot nedosahují, není léčba intenzifikována.
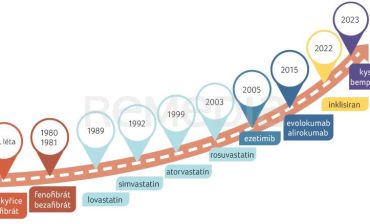 Možnosti hypolipidemické léčby se významně rozšířily (obr. 2). Profesor Vrablík zdůraznil, že inklisiran a PCSK9i představují v dosahování cílových hodnot výrazný posun, a oba přednášející shodně označili tento inovativní přístup v léčbě za historickou událost v terapii dyslipidemií. Inklisiran inhibuje jaterní syntézu PCSK9. Představuje první RNA terapii, která velmi efektivně a dlouhodobě snižuje hladiny aterogenních lipidů v pohodlném dávkovacím schématu s aplikací jednou za půl roku subkutánně. Klinický program ORION doložil snížení hodnot LDL‑C inklisiranem v kombinaci s maximální tolerovanou dávkou statinu (s ezetimibem nebo bez něj) až o 50 % [6].
Možnosti hypolipidemické léčby se významně rozšířily (obr. 2). Profesor Vrablík zdůraznil, že inklisiran a PCSK9i představují v dosahování cílových hodnot výrazný posun, a oba přednášející shodně označili tento inovativní přístup v léčbě za historickou událost v terapii dyslipidemií. Inklisiran inhibuje jaterní syntézu PCSK9. Představuje první RNA terapii, která velmi efektivně a dlouhodobě snižuje hladiny aterogenních lipidů v pohodlném dávkovacím schématu s aplikací jednou za půl roku subkutánně. Klinický program ORION doložil snížení hodnot LDL‑C inklisiranem v kombinaci s maximální tolerovanou dávkou statinu (s ezetimibem nebo bez něj) až o 50 % [6].
Na zkušenosti s léčbou inklisiranem se zaměřil druhý blok diskuse, kterého se účastnili MUDr. Libor Staněk (Ordinace pro choroby srdce s.r.o., Chomutov) a doc. MUDr. Denisa Janíčková Žďárská, Ph.D., (Interní klinika 1. LF UK, ÚVN Praha).
Dialog 2: Cílová hodnota LDL‑C? Zkušenosti z denní praxe s inklisiranem
Doktor Staněk prezentoval jako první kazuistiku případ 42leté ženy, kuřačky (10 cigaret denně po dobu 20 let) po infarktu myokardu (NSTEMI přední stěny). Jednalo se o nemoc jedné tepny, byla provedena perkutánní koronární intervence (PCI) s implantací stentu (DES), kompletní revaskularizace. Zajímavá je rodinná anamnéza: matka prodělala v 53 letech ischemickou cévní mozkovou příhodu (CMP), otec v 63 letech infarkt myokardu, strýc je po koronárním bypassu (CABG). Jedinou informací k lipidogramu, s níž byla pacientka propuštěna na spádové interní oddělení, byla hodnota celkového cholesterolu 5,8 mmol/l.
Pacientka trpí jaterní cirhózou na podkladě autoimunitní hepatitidy, jedná se u ní o překryv s primární sklerózující cholangitidou a postižením střev. Z farmakologické anamnézy (FA) při dimisi: Prednison Léčiva 5 mg tbl. nob. ½‑0‑0, Rocaltrol 0,25 µg cps. mol. 0‑0‑1, Salofalk 500 mg tbl. ent. 0‑0‑1, Vigantol gtt. 0‑20‑0 týdně, Helicid 20 mg cps. end. 1‑0‑0, Ursofalk 500 mg tbl. flm. 0‑0‑1, Anopyrin 100 mg tbl. nob. 1‑0‑0, Bisoprolol 2,5 mg tbl. ½‑0‑0, Zenon Neo 20 mg/10 mg 0‑0‑1, Imuran 50 mg tbl. flm. 1‑0‑0.
Pacientka tedy po propuštění užívala k ovlivnění dyslipidemie kombinaci 20 mg rosuvastatinu a 10 mg ezetimibu. První laboratorní vyšetření v ambulanci ukázalo: urea 3,8, kreatinin 58, kyselina močová 213, sodík 144, draslík 4,4, chloridy 102, vápník celkový 2,40, hořčík 0,85, bilirubin celkový 8,6, bilirubin přímý 5,8, ALT 0,83, AST 0,83, GGT 1,43, ALP 7,23, amyláza celková 1,51, lipáza 0,37, celkový cholesterol 5,2, HDL‑C 1,31, index chol/HDL 3,9, LDL‑C 2,91, triglyceridy 1,95, glukóza (žilní) 4,6, chylozita 1, hemolýza 0, iktericita 0, TSH 2,70.
Plánováno bylo navýšit dávku rosuvastatinu, ale tento záměr nesdílel pozitivně gastroenterolog. Doktor Staněk se společně s přítomnými zamyslel nad rizikem podávání statinů u pacientů se zánětlivým onemocněním jater ve stadiu cirhózy. Je třeba se obávat?
Rosuvastatin i atorvastatin jsou dle souhrnu údajů o přípravku (SPC) kontraindikovány u pacientů s aktivním jaterním onemocněním. U ezetimibu je doporučeno řídit se statinem podávaným v kombinaci. Pro podávání inklisiranu u pacientů s onemocněním jater není kontraindikace, což považuje přednášející za velkou výhodu přípravku.
U pacientky bylo rozhodnuto o navýšení dávky rosuvastatinu na 40 mg v kombinaci s ezetimibem. Došlo k poklesu hodnoty LDL‑C na 2,53 mmol/l, což u mladé pacientky po infarktu myokardu s pozitivní rodinnou anamnézou aterosklerotického KV onemocnění není uspokojivý výsledek.
Z tohoto důvodu byla u pacientky zahájena léčba inklisiranem, přípravkem s dobrým bezpečnostním profilem a deklarovanou vysokou účinností, který je navíc výhodný z pohledu spolupráce pacienta. K dispozici měl přednášející zatím jeden laboratorní výsledek odběru ukazující na pokles hodnoty LDL‑C o 41,5 %, který už nyní splňuje podmínku pro další podávání přípravku (viz dále). Přednášející přítomné vybídl, aby nebyli rezistentní k podávání inklisiranu. Vyzdvihl možnost jeho podávání u pacientů s jaterní, ale také renální insuficiencí, jeho vysokou účinnost a dobrou snášenlivost. Také režim aplikace jednou za půl roku je pro lékaře i pacienta velmi výhodný. Léčba inklisiranem je dle slov doktora Staňka bezproblémová.
Docentka Denisa Janíčková Žďárská, vedoucí Diabetologického centra v Ústřední vojenské nemocnici, na vystoupení navázala a zdůraznila naléhavost aktuální situace v České republice a potřebu zlepšit statistiky. V úvodu připomněla komplikovanost procesů, které provázejí zhodnocení každého pacienta, zvážení indikací u jednotlivých skupin léčiv k ovlivnění diabetu i dyslipidemie, ale vyzdvihla nutnost využít dostupné léčebné možnosti.
Docentka Janíčková Žďárská představila tři modelové situace indikace inklisiranu: v prvním případě šlo o monoterapii statinem s nedostatečnou účinností a vynechání ezetimibu z důvodu předpokládané nedostatečné účinnosti; ve druhém případě o nedostatečnou účinnost kombinační léčby maximální dávkou statinu s ezetimibem a ve třetím případě o dyslipidemii s intolerancí statinové léčby i ezetimibu. Dvě kazuistiky vybíráme v detailu blíže.
První případ prezentuje muže, r. 1959, s chronickou ICHS, po infarktu myokardu (NSTEMI v povodí RD1, PCI RMS1 + DES 12/2022), se srdečním selháním se středně redukovanou ejekční frakcí (HFmrEF), dyslipidemií, chronickou obstrukční plicní nemocí a diagnostikovaným bronchogenním karcinomem levého horního laloku v remisi. FA: Brilique 1‑0‑1, Godasal 100 mg 1‑0‑0, Torvacard 80 mg 0‑0‑1, Ezetimib 0‑0‑1, Concor 2,5 mg ½‑0‑0, Seretide Discus 50/250 µg, Ventolin dle potřeby. Z hlediska léčby dyslipidemie je tedy pacient na plné kombinační terapii statinem s ezetimibem. U tohoto pacienta je cílová hodnota LDL‑C opět < 1,4 mmol/l, nicméně aktuálně dosahuje hodnoty 2,11 mmol/l. Zahájena byla léčba inklisiranem. V čase druhé dávky byla zaznamenána hodnota LDL‑C 1,14 mmol/l, v čase třetí dávky (po půlroce) 0,78 mmol/l. Došlo tedy ke snížení o 63 %.
Druhá kazuistika představuje ženu v primární prevenci KV onemocnění, r. 1979, BMI 30. Má výraznou rodinnou anamnézu – otec i dva bratři léčeni pro hypertenzi, otec prodělal v 54 letech infarkt myokardu, na který zemřel. Jednalo se o čtvrtý infarkt (první ve 40 letech). Pacientka trpí prediabetem, zvýšená glykemie nalačno od r. 2020, má hypertenzi a dyslipidemii. FA: Triplixam 10/2,5/10 mg 1‑0‑0, Metformin XR 750 mg 0‑0‑1. Jak ozřejmila přednášející, léčba metforminem v indikaci prediabetu je u pacientů ve věku do 60 let zahajována v případě přítomnosti jednoho z rizikových faktorů, kterými jsou: pozitivní rodinná anamnéza, BMI ≥ 35, dyslipidemie, hypertenze, KV onemocnění, HbA1c ≥ 45 mmol/mol nebo gestační diabetes v anamnéze. U pacientky byla identifikována intolerance statinů (atorvastatin, lovastatin) v podobě myalgií a elevace hodnot kreatinkinázy (CK). Byl proveden test vysazení s úlevou od obtíží a normalizací hodnot CK. Při indikaci ezetimibu trpěla pacientka gastrointestinálními obtížemi s nadýmáním. LDL‑C nicméně dosahoval sérové koncentrace 6,55 mmol/l. Cílovou hodnotou u této pacientky v primární prevenci je 1,8 mmol/l. Zahájena byla terapie inklisiranem. Při aplikaci druhé dávky klesla hodnota LDL‑C na 4,36 mmol/l, při třetí o 40 % na 3,93 mmol/l.
V závěru prezentace doporučila přednášející zhodnotit u pacienta jeho cílovou hodnotu LDL‑C a možnost (reálnost) jejího dosažení. Jak je vidět na prezentovaných kazuistikách, lze při léčbě inklisiranem očekávat výrazný pokles hodnot LDL‑C (průměrně o více než 50 % po šesti měsících terapie). Léčba byla dobře snášena, bez výskytu nežádoucích účinků.
Dialog 3: Hypercholesterolemie! Kdo, kdy a kde?
Mezioborové diskuse se ve třetím bloku zúčastnili prof. MUDr. Michal Vrablík, Ph.D., prof. MUDr. Martin Prázný, CSc., Ph.D., předseda České diabetologické společnosti, doc. MUDr. Aleš Tomek, Ph.D., FESO, předseda Cerebrovaskulární sekce České neurologické společnosti, a již v předchozích prezentacích uvedení prof. MUDr. Petr Ošťádal, Ph.D., FESC, doc. MUDr. Denisa Janíčková Žďárská, Ph.D., a MUDr. Libor Staněk.
![OBR. 3 Ovlivňování rizikových faktorů v rámci péče o diabetika druhého typu; podle [8] – Škrha, et al., 2020. OBR. 3 Ovlivňování rizikových faktorů v rámci péče o diabetika druhého typu; podle [8] – Škrha, et al., 2020.](https://www.remedia.cz/photo-pg-1338---.jpg) Úvodního slova se ujal profesor Prázný, který zdůraznil spojitost mezi diabetem a KV onemocněními. Odborná literatura dokládá vysokou prevalenci KV onemocnění u diabetiků 2. typu; aterosklerotická KV onemocnění tvoří asi 29 %. Diabetici jsou ohroženi oproti běžné populaci zvýšeným KV rizikem [7]. Podílí se na něm řada proměnných rizikových faktorů a jejich ovlivnění je pro snížení rizika zásadní. Mezi ty, které může lékař účinně ovlivnit, patří hodnota HbA1c, systolického krevního tlaku a LDL‑C. Na pacienta je třeba pohlížet vždy komplexně, kompenzace pouze hyperglykemie není dostačující (obr. 3) [8]. Neméně důležitý je lipidový profil, a jak uvedl profesor Prázný, ovlivňování tradičních KV rizikových faktorů patří do náplně práce diabetologa. Dle jeho slov je dobré a žádoucí, že také diabetologové mají v rukou účinné nástroje k ovlivnění dyslipidemie, jako je inklisiran. Z vlastní zkušenosti referoval pozitivní vnímání této léčby pacienty i zájem o ni. Pro pacienty, kteří splňují indikační a úhradová kritéria, představuje jednoduchou, velmi přínosnou léčbu. Jako velmi motivační pro pacienty vnímá její vysokou účinnost.
Úvodního slova se ujal profesor Prázný, který zdůraznil spojitost mezi diabetem a KV onemocněními. Odborná literatura dokládá vysokou prevalenci KV onemocnění u diabetiků 2. typu; aterosklerotická KV onemocnění tvoří asi 29 %. Diabetici jsou ohroženi oproti běžné populaci zvýšeným KV rizikem [7]. Podílí se na něm řada proměnných rizikových faktorů a jejich ovlivnění je pro snížení rizika zásadní. Mezi ty, které může lékař účinně ovlivnit, patří hodnota HbA1c, systolického krevního tlaku a LDL‑C. Na pacienta je třeba pohlížet vždy komplexně, kompenzace pouze hyperglykemie není dostačující (obr. 3) [8]. Neméně důležitý je lipidový profil, a jak uvedl profesor Prázný, ovlivňování tradičních KV rizikových faktorů patří do náplně práce diabetologa. Dle jeho slov je dobré a žádoucí, že také diabetologové mají v rukou účinné nástroje k ovlivnění dyslipidemie, jako je inklisiran. Z vlastní zkušenosti referoval pozitivní vnímání této léčby pacienty i zájem o ni. Pro pacienty, kteří splňují indikační a úhradová kritéria, představuje jednoduchou, velmi přínosnou léčbu. Jako velmi motivační pro pacienty vnímá její vysokou účinnost.
Na hypolipidemickou léčbu v prevenci CMP se zaměřil docent Tomek z Neurologické kliniky 2. LF UK a FN v Motole. K hodnotám cholesterolu a jejich významu z hlediska KV mortality má nejblíže poměrně mladé odvětví neurologie – cévní neurologie. Dle slov přednášejícího vnímají cévní neurologové tento rizikový faktor naléhavěji než kolegové, kteří se specializují na epilepsii, Alzheimerovu chorobu či roztroušenou sklerózu.
Cévní mozková příhoda, která zaujímá celosvětově druhé místo v žebříčku mortality, představuje heterogenní skupinu onemocnění i ve vztahu k LDL‑C. Nejedná se o jedno onemocnění. Čistě aterosklerotickou příčinu CMP lze vysledovat pouze asi u 10 % mrtvic. Zhruba 10 % CMP je krvácivých, kde lze v případě intracerebrálního krvácení za majoritní příčinu považovat hypertonické krvácení. Mezi hlavní rizikové faktory ischemické CMP patří vysoký krevní tlak, vysoká glykemie nalačno a vysoká hodnota LDL‑C. Dle německých dat byla zhruba jeden rok před CMP prokázána hypertenze u 69 % pacientů, diabetes mellitus u 33 % a dyslipidemie u 31 % [9]. Zvýšené riziko je možné ovlivnit. Práce kolektivu autorů [10] dokládá, že snížení hodnoty LDL‑C o 1 mmol/l snižuje riziko CMP zhruba o 15 %.
Přítomní diskutovali také otázku „příliš“ nízké hladiny LDL‑C, na niž se zaměřily různé práce. Zajímavostí, kterou zmínil docent Tomek, je kupříkladu fakt, že pacienti v terminální fázi demence mají nižší hodnoty LDL‑C. Nicméně existují data prezentující jednoznačný přínos hypolipidemické léčby z hlediska zpomalení poklesu kognitivních funkcí ve vyšším věku. Docent Tomek zdůraznil jednoznačný benefit co nejagresivnějšího snížení hodnot LDL‑C. Jako nešťastnou vnímá doporučenou cílovou hodnotu LDL‑C u pacientů po CMP v evropských i amerických neurologických doporučeních, která je 1,8 mmol/l. Uvedl, že se za české neurology přiklání k cílové hodnotě 1,4 mmol/l.
![GRAF 1 Rostoucí riziko KV příhody s hodnotou LDL-C; podle [11] – Giugliano, et al., 2017. KV – kardiovaskulární; LDL-C – LDL cholesterol GRAF 1 Rostoucí riziko KV příhody s hodnotou LDL-C; podle [11] – Giugliano, et al., 2017. KV – kardiovaskulární; LDL-C – LDL cholesterol](https://www.remedia.cz/photo-pg-1339---.jpg) Dyslipidemii a akutnímu koronárnímu syndromu (AKS) se věnoval profesor Ošťádal. AKS je projevem koronární aterosklerózy, resp. progrese aterosklerózy koronárních tepen. Je důkazem, že LDL‑C (jakékoliv číselné hodnoty) byl příliš vysoký. Cholesterol hraje v patogenezi aterosklerózy klíčovou úlohu a platí, že čím nižších hodnot LDL‑C v sekundární prevenci v léčbě dyslipidemie u pacienta dosáhneme, tím nižší je riziko KV příhody (graf 1) [11]. Přednášející upozornil, že neexistuje žádná dolní hranice, kdy už by pacient ze snižování hodnoty LDL‑C neprofitoval nebo kde by existovalo vyšší riziko nežádoucích účinků. Pokud tedy přichází pacient s AKS s jakoukoliv hodnotou LDL‑C, je úkolem lékaře tuto hodnotu co nejvíce snížit, protože tím snížíme progresi aterosklerózy a zlepšíme prognózu pacienta.
Dyslipidemii a akutnímu koronárnímu syndromu (AKS) se věnoval profesor Ošťádal. AKS je projevem koronární aterosklerózy, resp. progrese aterosklerózy koronárních tepen. Je důkazem, že LDL‑C (jakékoliv číselné hodnoty) byl příliš vysoký. Cholesterol hraje v patogenezi aterosklerózy klíčovou úlohu a platí, že čím nižších hodnot LDL‑C v sekundární prevenci v léčbě dyslipidemie u pacienta dosáhneme, tím nižší je riziko KV příhody (graf 1) [11]. Přednášející upozornil, že neexistuje žádná dolní hranice, kdy už by pacient ze snižování hodnoty LDL‑C neprofitoval nebo kde by existovalo vyšší riziko nežádoucích účinků. Pokud tedy přichází pacient s AKS s jakoukoliv hodnotou LDL‑C, je úkolem lékaře tuto hodnotu co nejvíce snížit, protože tím snížíme progresi aterosklerózy a zlepšíme prognózu pacienta.
V loňském roce byly publikovány nové doporučené postupy Evropské kardiologické společnosti pro léčbu AKS [12], nicméně cíle hypolipidemické léčby se zde nemění; zůstává cílová hodnota LDL‑C < 1,4 mmol/l a současně dosažení redukce alespoň o 50 % oproti vstupní hodnotě. V případě opakované příhody v průběhu dvou let a při léčbě maximální tolerovanou dávkou statinu je možné zvážit cílovou hladinu < 1 mmol/l.
Jasnou evidenci a cílové hodnoty dal dále přednášející do kontextu s reálným prostředím. V závěru shrnul, že AKS vzniká v důsledku aterosklerózy a dyslipidemie. Pečlivě vedená dlouhodobá sekundární prevence může progresi aterosklerózy přinejmenším výrazně zpomalit. Významná část nemocných po AKS v ČR ale není léčena podle doporučených postupů a informovanost nemocných o sekundární prevenci po AKS zůstává hrubě nedostatečná.
Doktor Staněk z pohledu každodenní kardiologické praxe zdůraznil, že úspěch je dán poctivou prací v ambulanci. S pacientem je třeba vždy probrat aktuální hodnotu LDL‑C a tuto situaci také okomentovat a vysvětlit, proč je v léčbě postupováno daným způsobem. Doktor Staněk upozornil na přetíženost kardiologických ambulancí. Vyzdvihl spolupráci se všeobecnými praktickými lékaři v případě, že je pacient z hlediska krevního tlaku a LDL‑C dobře kompenzován a pacienti jsou následně předáváni do jejich péče. Diskutoval také otázku včasnosti dosažení kompenzace. Pacient po AKS je z hlediska recidivy nejrizikovější v prvním roce a měla by mu proto být věnována největší pozornost. Přítomní se shodli na svízelné dostupnosti a organizaci potřebné péče. Přetížené ambulance bohužel vedou k prodloužení doby, kdy se pacienti dostávají do péče.
Podmínky úhrady přípravku Leqvio v roce 2024
- Léčivý přípravek LEQVIOÒ (inklisiran) mohou předepsat lékaři se specializací: diabetologie, endokrinologie, vnitřní lékařství, kardiologie, dětská kardiologie, angiologie, neurologie, dětská neurologie nebo pracoviště J9.
Inklisiran je indikován u dospělých s primární hypercholesterolemií (heterozygotní familiární a nefamiliární) nebo smíšenou dyslipidemií:
- alespoň 3,1 mmol/l v případě heterozygotní familiární hypercholesterolemie bez manifestního kardiovaskulárního onemocnění, nebo
- alespoň 2,5 mmol/l v případě heterozygotní familiární hypercholesterolemie s manifestním kardiovaskulárním onemocněním, nebo
- alespoň 2,0 mmol/l u pacientů ve velmi vysokém kardiovaskulárním riziku s manifestním kardiovaskulárním onemocněním.
Inklisiran je schválen v kombinaci se statinem nebo statinem v kombinaci s jinými přípravky snižujícími hladiny lipidů u pacientů neschopných dosáhnout cílů pro LDL‑C při maximální tolerované dávce statinu; nebo samostatně či v kombinaci s jinými přípravky snižujícími hladiny lipidů u pacientů trpících nesnášenlivostí statinu nebo u pacientů, u nichž je statin kontraindikován.
Nevyužití ezetimibu v rámci stávající hypolipidemické terapie musí být medicínsky zdůvodněno ve zdravotnické dokumentaci pacientů. Relevantním medicínským důvodem pro nepodání ezetimibu v kombinaci se statiny (kromě jeho kontraindikace nebo nesnášenlivosti) může být u nových pacientů, kteří vyžadují vysoce intenzivní hypolipidemickou léčbu, např. počáteční koncentrace LDL‑C více než 50 % nad cílovou hodnotou pro léčbu dle jejich KV rizika. Pro skupinu pacientů, kteří již jsou na maximálně tolerované statinové léčbě, ale bez kombinace s ezetimibem, i když tento by pro ně mohl být indikován, může být relevantním medicínským důvodem pro nepodání ezetimibu fakt, že stávající dosažená koncentrace LDL‑C je stále o více než 20 % vyšší než cílová hodnota pro léčbu dle jejich KV rizika.
Statinová intolerance je definována jako intolerance alespoň dvou po sobě jdoucích statinů, která vede k jejich vysazení. Intolerance obou statinů musí pak být prokázána jako ústup klinické symptomatologie nebo normalizace hodnot CK po jeho vysazení a opětovný návrat myalgie nebo zvýšení hodnot CK po znovunasazení dalšího statinu. Za statinovou intoleranci nelze považovat zvýšení hodnot CK nepřesahující čtyřnásobek horních mezí bez klinické symptomatologie.
Efekt terapie inklisiranem je pravidelně hodnocen, prvně zaznamenán v klinické dokumentaci při druhé aplikaci (tedy přibližně 90 dní od zahájení léčby) a dále pak ve 24. týdnu (+/– 4 týdny) terapie.
Úhrada inklisiranu je ukončena při prokazatelné nespolupráci pacienta či neúčinnosti léčby spočívající v nedostatečném snížení koncentrace LDL‑C o alespoň 40 % při současném nedosažení cílové hodnoty LDL‑C nejpozději před podáním třetí dávky (pokud již nebyla prokázána ve třetím či šestém měsíci léčby).
Z prostředků veřejného zdravotního pojištění je hrazena jedna subkutánní injekce inklisiranu 284 mg jako počáteční dávka, další po třech měsících a poté každých šest měsíců [13,14].
Literatura
[1] Vaduganathan M, Mensah GA, Turco JV, et al. The Global Burden of Cardiovascular Diseases and Risk: A Compass for Future HealthFree Access. J Am Coll Cardiol 2022; 80: 2361–2371.
[2] Domanski MJ, Tian X, Wu CO, et al. Time Course of LDL Cholesterol Exposure and Cardiovascular Disease Event Risk. J Am Coll Cardiol 2020; 76: 1507–1516.
[3] Vorlíčková, Mayer O Jr, Bruthans J, et al. Změny v adherenci k doporučené cílové hodnotě LDL cholesterolu mezi lety 2006 a 2017 u českých pacientů s chronickou ischemickou chorobou srdeční. Cor Vasa 2019; 61: e20–e26.
[4] Ray KK, Molemans, B, Schoonen WM, et al. EU‑Wide Cross‑Sectional Observational Study of Lipid‑Modifying Therapy Use in Secondary and Primary Care: the DA VINCI study. Eur J Prev Cardiol 2021; 28: 1279–1289.
[5] Vrablík M, Šarkanová I, Breciková K, et al. Low LDL‑C goal attainment in patients at very high cardiovascular risk due to lacking observance of the guidelines on dyslipidaemias. Plos One 2023; 18: e0272883.
[6] Ray KK, Wright RS, Kallend D, et al. Two Phase 3 Trials of Inclisiran in Patients with Elevated LDL Cholesterol. N Engl J Med 2020; 382: 1507–1519.
[7] Rawshani A, Rawshani A, Franzén S, et al. Risk Factors, Mortality, and Cardiovascular Outcomes in Patients with Type 2 Diabetes. N Engl J Med 2018; 379: 633–644.
[8] Škrha J, Pelikánová T, Prázný M, Kvapil M. Doporučený postup péče o diabetes mellitus 2. typu. Dostupné na: https://www.diab.cz › standardy_DM_aktual_2020
[9] Stahmeyer JT, Stubenrauch S, Geyer S, et al. The Frequency and Timing of Recurrent Stroke: An Analysis of Routine Health Insurance Data. Dtsch Arztebl Int 2019; 116: 711–717.
[10] Cholesterol Treatment Trialists' (CTT) Collaboration. Efficacy and safety of more intensive lowering of LDL cholesterol: a meta‑analysis of data from 170 000 participants in 26 randomised trials. Lancet 2010; 376: P1670–1681.
[11] Giugliano RP, Pedersen TR, Park JG, et al. Clinical efficacy and safety of achieving very low LDL‑cholesterol concentrations with the PCSK9 inhibitor evolocumab: a prespecified secondary analysis of the FOURIER trial. Lancet 2017; 390: 1962–1971.
[12] 2023 ESC Guidelines for the management of acute coronary syndromes. Dostupné na: https://www.escardio.org/Guidelines/Clinical‑Practice‑Guidelines/Acute‑Coronary‑Syndromes‑ACS‑Guidelines
[13] Souhrn údajů o přípravku Leqvio 284 mg injekční roztok v předplněné injekční stříkačce. Dostupné na: https://www.sukl.cz
[14] Rozhodnutí SÚKL v rámci správního řízení sp.zn. SUKLS123881/2023, a č.j. sukl243588/2023. Dostupné na: https://verso.sukl.cz/fcgi/ verso.fpl?fname=vp_protokol&_idspis=700056353