Epoetin theta
Epoetin theta je novým preparátem z řady erytropoetinů se složením aminokyselin podobným, jako má jako přirozený endogenní erytropoetin. Byl získán rekombinantní DNA technologií vnesením genu pro erytropoetin do buněk ovaria čínského křečka. Má shodné biologické účinky jako endogenní erytropoetin a rekombinantně připravené epoetiny alfa, beta a delta. Hlavní uplatnění nachází v léčbě anémie u nemocných s chronickou renální insuficiencí, u symptomatické anémie nemyeloidních hematologických malignit a u solidních nádorů po protinádorové léčbě.
Farmakologická skupina
Epoetin theta je antianemikum, hematopoetický růstový faktor. ATC kód je B03XA01.
Chemické a fyzikální vlastnosti
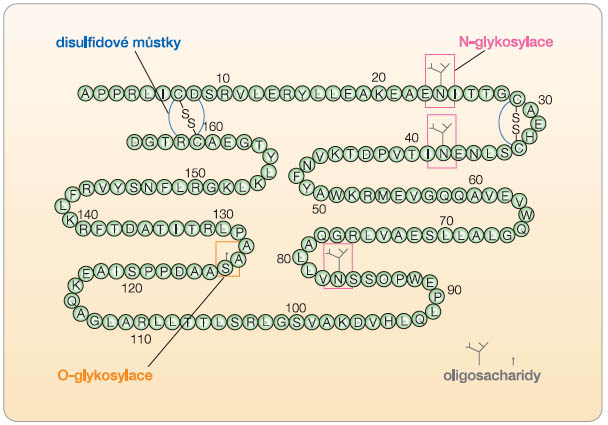 Epoetin theta (XM01) je polypeptid o 165 aminokyselinách připravený rekombinantní technologií. Od ostatních rekombinantně připravených epoetinů se liší způsobem glykosylace. Sled aminokyselin a místa glykosylace jsou znázorněna na obr. 1. Proporce sacharidů je 40 %.
Epoetin theta (XM01) je polypeptid o 165 aminokyselinách připravený rekombinantní technologií. Od ostatních rekombinantně připravených epoetinů se liší způsobem glykosylace. Sled aminokyselin a místa glykosylace jsou znázorněna na obr. 1. Proporce sacharidů je 40 %.
Mechanismus účinku, farmakodynamika
Podobně jako endogenní erytropoetin působí epoetin theta zvýšení proliferace a diferenciace erytroidní řady a zvyšuje kapacitu pro přenos kyslíku. Experimentální studie prokázaly vliv epoetinu theta na vzestup koncentrace hemoglobinu, zvýšení hodnoty hematokritu, počtu erytrocytů a retikulocytů [1]. Známky toxicity se omezovaly výhradně na důsledky erytropoetického stimulu (hypercelularita dřeně, extramedulární hematopoeza, po vyšších dávkách fibróza dřeně a kostní hyperostóza).
Farmakologické vlastnosti
 Biologická dostupnost po nitrožilním podání je 100 %, po podkožní aplikaci 31 %, nejrychleji se vstřebává při aplikaci pod kůži břicha. Biologický poločas po nitrožilní aplikaci je 4–6 hodin, po podkožní aplikaci 25–34 hodin. Maximální plazmatické koncentrace je dosaženo za 12–18 hodin (tab. 1). Vylučuje se do žluči, ale o metabolismu nejsou k dispozici žádné podrobnější údaje [1].
Biologická dostupnost po nitrožilním podání je 100 %, po podkožní aplikaci 31 %, nejrychleji se vstřebává při aplikaci pod kůži břicha. Biologický poločas po nitrožilní aplikaci je 4–6 hodin, po podkožní aplikaci 25–34 hodin. Maximální plazmatické koncentrace je dosaženo za 12–18 hodin (tab. 1). Vylučuje se do žluči, ale o metabolismu nejsou k dispozici žádné podrobnější údaje [1].
Klinické zkušenosti
Zkušenosti s použitím rekombinantně připravených epoetinů jsou velmi bohaté [2–4]. Významným terapeutickým přínosem se staly zejména v léčbě anémie provázející chronickou renální insuficienci, která ovlivňuje morbiditu a mortalitu nemocných. Patogeneze této anémie není jednotná, avšak jedním z klíčových patogenetických mechanismů je právě nedostatek endogenního erytropoetinu. Suplementace rekombinantním epoetinem tak může anémii zásadně ovlivnit a zlepšit kvalitu života nemocných [5, 6]. V pilotních klinických studiích bylo prokázáno, že epoetin theta má shodné biologické účinky s ostatními používanými epoetiny [7]. V multicentrických studiích II. a III. fáze zahrnujících více než 1000 pacientů s chronickým selháním ledvin nebyl prokázán rozdíl v ![Graf 1 Průběh koncentrace hemoglobinu po aplikaci epoetinu theta, epoetinu beta a placeba; podle [13] – Tjulandin, et al., 2010.](https://www.remedia.cz/photo-a-28455---.jpg) účinnosti epoetinu theta v porovnání s epoetinem beta, který byl ve většině studií použit jako referenční látka. Graf 1 demonstruje porovnání účinnosti epoetinu theta a epoetinu beta na koncentraci hemoglobinu v průběhu 85 dnů. Výsledky jsou porovnány s aplikací placeba [8, 13]. V rozsáhlé klinické studii u 270 hemodialyzovaných pacientů porovnávali Kohler a kol. týdenní nitrožilní aplikaci epoetinu theta a epoetinu beta a nenašli žádné rozdíly v jejich účinku a na vzestup či udržení koncentrace hemoglobinu [9]. Nebyl shledán ani rozdíl ve frekvenci nežádoucích účinků. V žádné z klinických studií s epoetinem theta nebyla zaznamenána tvorba protilátek proti erytropoetinu, které po aplikaci některých jiných epoetinů mohou způsobit vznik čisté aplazie červené řady (PRCA – pure red cell aplasia) [10]. Účinnost epoetinu theta je závislá na dávce, ale není ovlivněna způsobem aplikace.
účinnosti epoetinu theta v porovnání s epoetinem beta, který byl ve většině studií použit jako referenční látka. Graf 1 demonstruje porovnání účinnosti epoetinu theta a epoetinu beta na koncentraci hemoglobinu v průběhu 85 dnů. Výsledky jsou porovnány s aplikací placeba [8, 13]. V rozsáhlé klinické studii u 270 hemodialyzovaných pacientů porovnávali Kohler a kol. týdenní nitrožilní aplikaci epoetinu theta a epoetinu beta a nenašli žádné rozdíly v jejich účinku a na vzestup či udržení koncentrace hemoglobinu [9]. Nebyl shledán ani rozdíl ve frekvenci nežádoucích účinků. V žádné z klinických studií s epoetinem theta nebyla zaznamenána tvorba protilátek proti erytropoetinu, které po aplikaci některých jiných epoetinů mohou způsobit vznik čisté aplazie červené řady (PRCA – pure red cell aplasia) [10]. Účinnost epoetinu theta je závislá na dávce, ale není ovlivněna způsobem aplikace.
Další klinické studie zkoumaly účinnost epoetinu theta u pacientů s nádorovým onemocněním, zejména po protinádorové léčbě [11, 12]. Také u těchto nemocných je produkce endogenního erytropoetinu zpravidla snížená, i když patogeneze anémie provázející malignity je multifaktoriální. U hematologických malignit může být způsobena infiltrací dřeně nádorovými buňkami. Některé cytokiny, produkované nádorovými buňkami jako IFN-gamma, TNF a IL-1, mají vliv na snížení syntézy endogenního erytropoetinu, potlačují diferenciaci elementů červené řady z erytroidních prekurzorů a porušují metabolismus železa. Tato anémie se ještě zhoršuje po chemoterapii nebo radioterapii. Zejména platinové deriváty snižují produkci endogenního erytropoetinu poškozením renálních tubulárních buněk [13]. Anémie se vyvíjí plíživě a přispívá ke zhoršení kvality života nemocných. Ačkoliv receptory pro erytropoetin byly nalezeny na nádorových buňkách, nebylo po aplikaci epoetinu theta onkologicky nemocným prokázáno urychlení nádorového růstu a nebyla zkrácena ani doba přežívání nemocných léčených epoetinem theta.
Korekce anémie podáváním transfuzí se jeví u nefrologicky i onkologicky nemocných jako méně výhodná jak z medicínského, tak z ekonomického hlediska. Zatěžuje oběhové ústrojí a přináší riziko dalších komplikací (přenos infekce, imunizace aj.). Vzhledem k tomu, že tolerance epoetinu theta je velmi dobrá a nežádoucí účinky omezené (do 9 %), představuje jeho použití v daných indikacích terapeutický přínos.
Zařazení do současné palety léčiv
Epoetin theta rozšiřuje možnosti léčby symptomatických anémií, především u chronické renální insuficience.
Indikace
Symptomatická anémie u chronické renální insuficience u dospělých pacientů, u nemocných v pravidelném dialyzačním programu, dále symptomatická anémie u nemocných s nemyeloidními hematologickými malignitami (nehodgkinské lymfomy, chronická lymfatická leukemie, mnohočetný myelom) a anémie u nemocných se solidními nádory po protinádorové chemoterapii.
Ke zvýšení výtěžnosti erytrocytů před odběrem pro autologní transfuzi krve se epoetin theta nedoporučuje. Tuto indikaci při použití jiných epoetinů je třeba zvažovat s přihlédnutím k možnému riziku tromboembolických příhod. Proto se vyhrazuje jen u nemocných s mírnou anémií bez nedostatku železa, předpokládá-li se zvýšená spotřeba krve při chirurgickém výkonu.
Kontraindikace
Kontraindikací pro podání epoetinu theta je přecitlivělost na epoetin nebo na pomocné látky, nekorigovaná hypertenze, portální hypertenze. U pacientů s programem předoperačního autologního odběru je kontraindikací prodělaný infarkt myokardu nebo cévní příhoda mozková v anamnéze.
Nežádoucí účinky
Nejčastějším nežádoucím účinkem je hypertenze, zhoršení stávající hypertenze, flu-like syndrom, bolesti hlavy, artralgie, rash, svědění v místě aplikace a trombotické příhody. Nepříjemnou komplikací jsou zejména trombózy shuntu u pacientů v dialyzačním programu. Vytvoření protilátek proti epoetinu, které mohou způsobit čistou aplazii červené řady (PRCA), popisované po aplikaci jiných epoetinů, nebylo po podání epoetinu theta pozorováno.
Lékové interakce
Studie interakcí nebyly s epoetinem theta prováděny.
Těhotenství a kojení
Údaje o účincích epoetinu theta v graviditě nebyly publikovány. Do mateřského mléka se nevylučuje, neboť údaje o vyšetření krve novorozenců neprokazují farmakologickou aktivitu epoetinu, je-li podáván kojícím ženám
Dávkování
U nemocných s chronickým selháním ledvin, kteří ještě nejsou dialyzováni, se doporučuje podkožní aplikace v dávce 20 IU/kg 3krát týdně. Pokud se koncentrace hemoglobinu nezvýší po měsíčním podávání o 1 g/dl, zvýší se dávka epoetinu theta na 40 IU/kg aplikovaných subkutánně 3krát týdně. U dialyzovaných nemocných je vhodnější nitrožilní aplikace v dávce 40 IU/kg 3krát týdně, po 4 týdnech lze zvýšit na dávku 80 IU/kg 3krát týdně. U onkologicky nemocných je počáteční dávka 20 000 IU 1krát týdně, s postupným zvyšováním až na maximální dávku 60 000 IU/týden. Léčba epoetinem theta by měla trvat maximálně měsíc po skončené chemoterapii.
Stabilita a kompatibilita
Tekutá forma v předplněných injekčních stříkačkách je stabilní 24 měsíců při teplotě 2–8 °C. Doporučuje se chránit stříkačky před světlem. Po vyjmutí z chladničky je roztok stabilní po dobu 7 dnů při teplotě do 25 °C.
Balení
Epoetin theta je k dispozici v osmi koncentracích (1000, 2000, 3000, 4000, 5000, 10 000, 20 000 a 30 000 IU) v předplněných skleněných injekčních stříkačkách. Obsahuje tyto přísady: natriumdihydrochlorid, NaCl, polysorbát 20, trometamol, HCl k adjustaci pH a vodu pro injekce.
Seznam použité literatury
- [1] European public assessment report for authorized medicinal products for human use: Eporatio 2009, EMEA/H/C/ 001033.
- [2] Murphy F, Bewnnett L, Jenkins K. Managing anemia of chronic kidney disease. Br J Nurs 2010; 19: 1284–1286.
- [3] Del Vecchio L, Cavalli A, Tucci B, et al. Chronic kidney disease-associated anemia: New remedies. Curr Opin Invest Drugs 2010; 9: 1030–1038.
- [4] Glapsy J, Begun Y. Anemia management strategies optimizing treatment using epoetin beta. Oncology 2005; 69 Suppl 2: 8–16.
- [5] Bren A, Kandra A. Our experience with epoetins in treating renal anemia. Ther Apher Dial 2005; 3: 202–204.
- [6] Loughnan A, Ali GR, Abeygunasekara SC. Comparison of the therapeutic efficacy of epoetin beta and epoetin alfa in maintenance phase hemodialysis patients. Ren Fail 2011; 33: 373–375.
- [7] Gertz B, Kohler E, Kes P, et al. Epoetin theta efficacy and safety of iv administration in anaemic haemodialysis patients in the maintenance phase in comparison to epoetin beta. Curr Med Res Opin 2010; 10: 2393–2402.
- [8] Bias P. Eporatio (XM01): Clinical development. Presentation in Univeristy of Ulm, 2010.
- [9] Kohler GB, Kes P, Essaian A, et al. Epoetin theta: efficacy and safety of iv administration in anaemic haemodialysis patients in the maintenance phase in comparison to epoetin beta. Curr Med Res Opin 2010; 26: 2393–2402.
- [10] Casdevall N, Nataf J, Viron B, et al. Pure red-cell aplasia and antierythropoietin antibodies in patients treated with recombinant erythropoietin. N Engl J Med 2002; 346: 469–475.
- [11] Buchner A, Bias P. Epoetin theta shows efficacy and safety in a placebo controlled randomized phase III study in cancer patients receiving non-platinum chemotherapy. Onkologie 2009; 32 Suppl 4: 88.
- [12] McKinney M, Arcasoy MO. Erythropoietin for oncology supportive care. Exp Cell Res 2011; Epub ahaed of print.
- [13] Tjulandin SA, Bias P, Elsasser R, et al. Epoetin theta in anaemic cancer patients receiving platinum-based chemotherapy: A randomised controlled trial. Arch Drug Inform 2010; 3: 45–53.