Escitalopram – aktualizovaný lékový profil
Escitalopram, aktivní enantiomer racemického SSRI (selektivního inhibitoru zpětného vychytávání serotoninu) citalopramu, je vysoce selektivní inhibitor serotoninového transportéru. Vyznačuje se rychlým nástupem účinku a účinností při obecně dobré tolerabilitě. Indikován je pro léčbu střední i těžké deprese. Metaanalýzy klických studií naznačují, že escitalopram je nejméně stejně účinný jako ostatní SSRI a venlafaxin s prodlouženým uvolňováním (XR). Escitalopram může být farmakoekonomicky výhodný. Další studie by měly přispět k lepšímu poznání účinnosti ve specifických indikacích, tolerability, vlivu na kvalitu života a zejména k detailnějšímu zhodnocení ekonomického přínosu léčby escitalopramem.
Farmakologická skupina
Escitalopram je antidepresivum 3. generace, patří mezi selektivní inhibitory zpětného vychytávání serotoninu (SSRI, selective serotonin reuptake inhibitors). Inhibuje vychytávání serotoninu z interneuronálních synapsí v centrálním nervovém systému (CNS). Escitalopram je terapeuticky účinný S-enantiomer selektivního inhibitoru zpětného vychytávání serotoninu – citalopramu (racemická směs je tvořena 50 % S-citalopramu a 50 % R-citalopramu) s mírně odlišnou receptorovou charakteristikou oproti R-citalopramu (terapeuticky neúčinný, naopak účinnost S-enantiomeru snižuje). Escitalopram patří do farmakoterapeutické skupiny antidepresiv, ATC kód N06AB10.
Chemické a fyzikální vlastnosti
Escitalopram je chemicky (+)-(S)-1-[3-(dimethylamino)propyl]-1-(p-fluorofenyl)-5-ftalankarbonitril. Escitalopram je S-enantiomer citalopramu. Vyskytuje se ve formě soli s kyselinou šťavelovou – jako escitalopram oxalát (obr. 1).
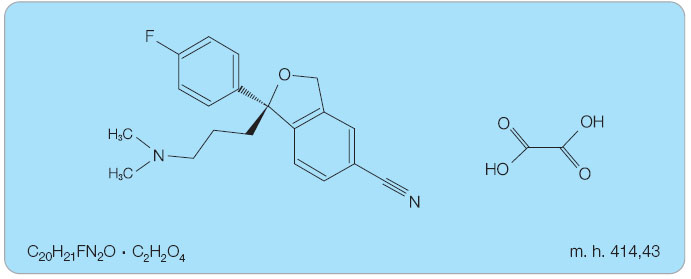
Sumární vzorec: C20H21FN2O . C2H2O4
Molekulová hmotnost: 414,43
Escitalopram oxalát je jemný bílý nebo nažloutlý prášek, snadno rozpustný v methanolu a v dimethylsulfoxidu, dobře rozpustný v izotonickém roztoku chloridu sodného, mírně rozpustný ve vodě a v ethanolu, těžce rozpustný v ethylacetátu a prakticky nerozpustný v heptanu [1].
Mechanismus účinku, farmakodynamika
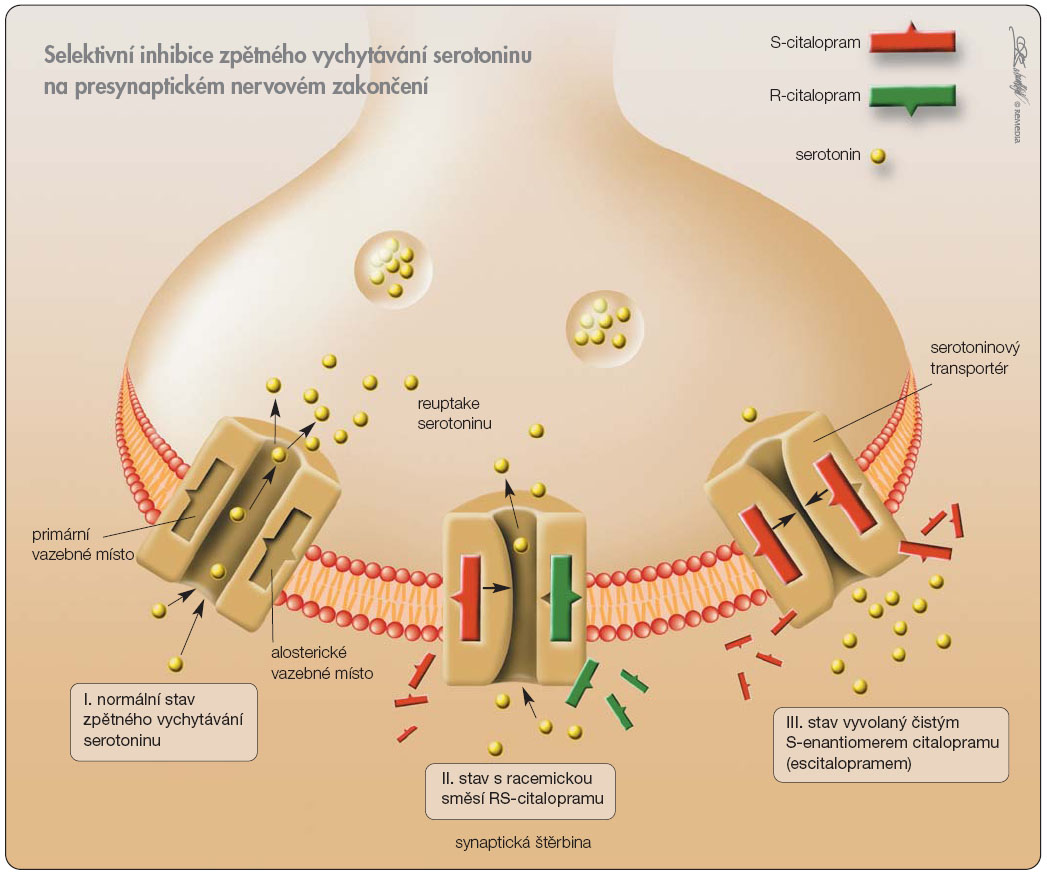 Escitalopram je v současnosti jediným SSRI, který blokuje obě vazebná místa serotoninového transportéru (5-HTT), viz obr. 2 [2]. Ten zajišťuje zpětné vstřebávání serotoninu, a tím snižuje koncentraci serotoninu v synaptické štěrbině. Má dvě vazebná místa: primární (zodpovídá za zpětné vstřebávání serotoninu) a alosterické (moduluje afinitu ligandů k primárnímu místu). Ostatní léčiva ze skupiny SSRI se vážou pouze k primárnímu vazebnému místu a výsledkem je intermitentní, nedokonalá blokáda 5-HTT.
Escitalopram je v současnosti jediným SSRI, který blokuje obě vazebná místa serotoninového transportéru (5-HTT), viz obr. 2 [2]. Ten zajišťuje zpětné vstřebávání serotoninu, a tím snižuje koncentraci serotoninu v synaptické štěrbině. Má dvě vazebná místa: primární (zodpovídá za zpětné vstřebávání serotoninu) a alosterické (moduluje afinitu ligandů k primárnímu místu). Ostatní léčiva ze skupiny SSRI se vážou pouze k primárnímu vazebnému místu a výsledkem je intermitentní, nedokonalá blokáda 5-HTT.
Escitalopram nemá žádnou nebo má jen nízkou afinitu k receptorům serotoninovým 5-HT1A, 5-HT2, dopaminovým D1, D2, adrenergním α1, α2, β, histaminovým H1, cholinergním, muskarinovým, benzodiazepinovým a opioidním. ![Graf 1 Afinita escitalopramu k lidským transportérům pro monoaminy; NA – noradrenalin; 5-HT – serotonin; DA – dopamin; podle [5] – Owens, et al., 2001.](https://www.remedia.cz/photo-a-27832---.jpg) Jedná se o vysoce selektivní SSRI (graf 1). Vykazuje tak relativně nízký počet nežádoucích účinků. Escitalopram (stejně jako jeho metabolit S-demethylcitalopram) nevykazuje významnou afinitu k žádnému z jiných druhů receptorů a/nebo vazebných míst s výjimkou nízké antagonizace receptorů sigma1+2. Escitalopram neantagonizuje serotoninové 5-HT2C receptory (R-citalopram tyto receptory antagonizuje) a histaminové H1 receptory. Ostatní SSRI nejsou těchto vlivů prosty – fluoxetin má afinitu k 5-HT2C receptorům, paroxetin k M receptorům a citalopram blokuje H1 nervová zakončení. Silnějším inhibitorem zpětného vychytávání serotoninu je paroxetin, který inhibuje také zpětné vychytávání noradrenalinu, a sertralin, který kromě zpětného vychytávání serotoninu inhibuje také vychytávání dopaminu [3–5].
Jedná se o vysoce selektivní SSRI (graf 1). Vykazuje tak relativně nízký počet nežádoucích účinků. Escitalopram (stejně jako jeho metabolit S-demethylcitalopram) nevykazuje významnou afinitu k žádnému z jiných druhů receptorů a/nebo vazebných míst s výjimkou nízké antagonizace receptorů sigma1+2. Escitalopram neantagonizuje serotoninové 5-HT2C receptory (R-citalopram tyto receptory antagonizuje) a histaminové H1 receptory. Ostatní SSRI nejsou těchto vlivů prosty – fluoxetin má afinitu k 5-HT2C receptorům, paroxetin k M receptorům a citalopram blokuje H1 nervová zakončení. Silnějším inhibitorem zpětného vychytávání serotoninu je paroxetin, který inhibuje také zpětné vychytávání noradrenalinu, a sertralin, který kromě zpětného vychytávání serotoninu inhibuje také vychytávání dopaminu [3–5].
Escitalopram u potkanů zvyšuje extracelulární koncentraci serotoninu v prefrontálním kortexu výrazně více než citalopram. R-citalopram ji nezvyšuje. Escitalopram blokuje reuptake serotoninu (IC50 2,1 nM) více než R-citalopram (IC50 280 nM) i citalopram (IC50 3,9 nM) [4, 6]. I na zdravých dobrovolnících byla prokázána pomocí SPECT (Single Photon Emission Computerized Tomography, jednofotonová emisní počítačová tomografie) selektivní inhibice reuptake serotoninu – signifikantní blokáda serotoninového transportéru při podávání běžných dávek [7].
Farmakokinetika
Farmakokinetika escitalopramu v dávce 20 mg je shodná s farmakokinetikou 40 mg racemického citalopramu. Absorpce je nezávislá na požité potravě, maximální koncentrace je dosaženo za 3–4 hodiny po požití. Escitalopram se vstřebává téměř úplně a nezávisle na příjmu potravy. Po opakovaném podání dosahuje maximální plazmatické hladiny (cmax) přibližně za 4 hodiny (tmax). Biologická dostupnost po perorálním podání je asi 80 %, tedy podobná jako u citalopramu. Escitalopram a jeho hlavní metabolity se vážou z méně než 80 % na plazmatické bílkoviny [8].
Escitalopram se metabolizuje v játrech na demethylované, didemethylované metabolity (demethyl-escitalopram a didemethyl-escitalopram), které jsou farmakologicky účinné. Nicméně účinnost je nižší (10krát méně u demethyl-escitalopramu), ale zachovávají si serotoninovou selektivitu. Koncentrace metabolitu jsou nižší (demethyl-escitalopram 2krát, didemethyl-escitalopram ještě méně) a příspěvek ke klinickému účinku mizivý. Biotransformace je zprostředkována systémem CYP2C19 (37 %), do určité míry se na tomto ději též může podílet systém CYP3A4 (35 %) a CYP2D6 (28 %). Eliminační poločas po opakovaném podání dávky je zhruba 30 hodin, perorální plazmatická clearance 0,6 l/min. Hlavní metabolity mají výrazně delší poločas vylučování. Escitalopram a hlavní metabolity se eliminují játry a ledvinami, větší část se ve formě metabolitů vyloučí močí [8].
Farmakokinetika je lineární, ustáleného stavu plazmatické hladiny je dosaženo během prvního týdne léčby. U starších pacientů je eliminace escitalopramu pomalejší, plocha pod křivkou AUC je u starších pacientů asi o 50 % vyšší než u mladších. Eliminační poločas je prodloužen (39 h), clearance snížena (0,35 l/min), proto je vhodné omezit maximální dávky na 10 mg denně, stejně jako při hepatální dysfunkci [9, 10]. Hladiny demethyl-escitalopramu jsou redukovány o cca 60 %  ketokonazolem (inhibitor CYP3A4), o cca 80 % chinidinem (inhibitor CYP2D6) a omeprazolem (inhibitor CYP2C19). Pomalí metabolizátoři CYP2C19 mají vyšší sérové koncentrace escitalopramu (nikoli však pomalí metabolizátoři CYP2D6). Demethyl-escitalopram je degradován izoenzymem 2D6 cytochromu P450 na didemethyl-escitalopram. Proces může být inhibován chinidinem (inhibitor CYP2D6). Escitalopram a dimethyl-escitalopram jsou slabými inhibitory izoenzymu 2D6, didemethyl-escitalopram je slabým inhibitorem izoenzymu 2C9 a 2C19 [9–11]. Základní farmakokinetické parametry escitalopramu jsou shrnuty v tab. 1 [8].
ketokonazolem (inhibitor CYP3A4), o cca 80 % chinidinem (inhibitor CYP2D6) a omeprazolem (inhibitor CYP2C19). Pomalí metabolizátoři CYP2C19 mají vyšší sérové koncentrace escitalopramu (nikoli však pomalí metabolizátoři CYP2D6). Demethyl-escitalopram je degradován izoenzymem 2D6 cytochromu P450 na didemethyl-escitalopram. Proces může být inhibován chinidinem (inhibitor CYP2D6). Escitalopram a dimethyl-escitalopram jsou slabými inhibitory izoenzymu 2D6, didemethyl-escitalopram je slabým inhibitorem izoenzymu 2C9 a 2C19 [9–11]. Základní farmakokinetické parametry escitalopramu jsou shrnuty v tab. 1 [8].
Klinické zkušenosti
Účinnost escitalopramu byla ověřena v řadě klinických studií. Escitalopram je účinný nejen v terapii depresivní poruchy, ale i v terapii poruchy panické, sociální, obsedantně-kompulzivní, generalizované úzkostné a premenstruální dysforické poruchy. Pro zjednodušení budeme v dalším textu vycházet zejména z metaanalýz.
Animální modely
Antidepresivní vliv escitalopramu byl v plovacím testu u myší, v testu chronického stresu, v testu asertivního chování při sociální interakci obecně shledán jako nejméně stejný, nebo přesahující ostatní SSRI. Anxiolytická účinnost escitalopramu byla úspěšně sledována v modelech černé a bílé osvětlené skříňky, ultrazvukové vokalizace na bolestivé podněty a při stimulaci dorzální periakveduktální šedi mozku [5].
Depresivní porucha
Escitalopram, SSRI, placebo
Depresivní porucha byla sledována nejdříve, proto je zde nyní k dispozici nejvíce dat. Escitalopram je účinnější než placebo. Jen málo dat hodnotí SSRI mezi sebou navzájem, natož ve srovnáních ještě navíc komparovaných placebem.
Opakovaně byly provedeny studie hodnotící účinnost escitalopramu ve srovnání s citalopramem. Jak racemický citalopram, tak i escitalopram jsou léky účinné v terapii deprese. Ve srovnání s placebem byl escitalopram (10–20 mg denně) shledán statisticky významně účinnějším již v prvním týdnu léčby. Citalopram (20–40 mg denně) byl v takovém srovnání účinný až ve čtvrtém (posouzení pomocí skóru CGI-I, Clinical Global Impression Improvement), nebo dokonce v šestém týdnu léčby (posouzení pomocí skóru MADRS, Montgomery-Asberg Depression Rating Scale). U podskupiny výrazně depresivních pacientů (MADRS > 30) byl escitalopram účinnější než placebo od prvního týdne a účinnější než citalopram (týdny 1, 6, 8) v redukci symptomatologie – hodnoceno dle OC (observed cases) i LOCF (last observation carried forward). Celkový počet respondérů byl u pacientů léčených escitalopramem 59,3 %, u nemocných léčených citalopramem 53,4 % a u pacientů, kteří dostávali placebo, 41,2 %.
Jednalo se o zhodnocení tří studií, bez odlišností mezi podávanými látkami (escitalopram, citalopram, placebo) v demografických parametrech i vstupních hodnotách MADRS. V první studii byla použita fixní dávka 10 mg nebo 20 mg escitalopramu, 40 mg citalopramu a placebo, v ostatních dvou úvodní dávka 10 mg escitalopramu, 20 mg citalopramu a placebo – dávky mohly být zvýšeny maximálně na dvojnásobek nejdříve ve 4. týdnu, pak v 6. týdnu, ve druhé studii jen ve 3. týdnu. Střední užívané dávky ve srovnání 1321 pacientů byly 13,3 Ī 3,6 mg escitalopramu a 28,9 Ī 4,6 mg citalopramu denně [12].
I další metaanalýzou zahrnující čtyři studie [13–16] v délce trvání 8–24 týdnů se vstupním skórem MADRS >/= 22 zahrnujícím 1262 pacientů (escitalopram 685, citalopram 577) byla zjištěna přinejmenším stejná nebo vyšší stejná účinnost escitalopramu vůči citalopramu. Z pacientů léčených escitalopramem odpovědělo na léčbu 55,5 %, z pacientů léčených citalopramem 50,8 %. Rozdíl v počtu respondérů byl zaznamenán jak v prvním, tak i v osmém týdnu. Změny v MADRS byly statisticky významné (1,02; Cl 95% 0,09–1,95; p = 0,03) [17].
V metaanalýze dvou 6měsíčních randomizovaných studií srovnávajících vliv SSRI na depresivní poruchu byl escitalopram oproti paroxetinu účinnější ve všech hlavních parametrech. Pokles MADRS byl o 2 body výraznější (p < 0,01), CGI tíže i zlepšení o 0,3 bodu (p < 0,01). Zároveň pacienti léčení escitalopramem po šesti měsících významně častěji dosahovali odpovědi na léčbu (83 % vs. 76,8 % při léčbě paroxetinem) i remise (76,4 % vs. 70 %, kritériem byla hodnota MADRS < 12). Nadpoloviční většina pacientů dosáhla skóre MADRS < 5. Výskyt nežádoucích účinků byl zhruba stejně častý. Výrazně méně pacientů léčených escitalopramem ve srovnání s paroxetinem (8,1 % vs. 17,6 %) ukončilo sledování předčasně, stejná situace byla v podskupině ukončení pro nežádoucí účinky (6,6 % vs. 11,7 %) [18].
I v dalších studiích byl escitalopram účinnější než srovnávaná SSRI (viz metaanalýzy níže). „Pouze“ stejné účinnosti dosáhl ve srovnání se sertralinem [19]. Escitalopram byl ještě úspěšně hodnocen ve srovnání s bupropionem a fluoxetinem. Výsledek je shrnut v odstavci o metaanalýzách.
Escitalopram a další antidepresiva (SNRI)
![Graf 2 Počet pacientů, kteří odpověděli na léčbu, a počet pacientů, u kterých bylo dosaženo remise při léčbě escitalopramem (20 mg/den) a venlafaxinem XR (225 mg/den); podle [20] – Bielski, et al., 2004.](https://www.remedia.cz/photo-a-27834---.jpg) V 8týdenní dvojitě slepé studii (wash-out perioda 1 týden) byl escitalopram (20 mg denně) ve srovnání s venlafaxinem XR (225 mg denně) shledán účinnějším v dosažení odpovědi na léčbu (>/= 50%
redukce vstupního skóru MADRS) – 58,8 %, resp. 48,0 % (graf 2). Při léčbě escitalopramem dosáhlo na konci studie kritérií remise (MADRS skór tů (n = 97), při léčbě venlafaxinem XR to bylo 36,7 % pacientů (n = 98). U obou léčiv došlo k podobnému poklesu vstupního skóru MADRS o -15,9 (z 30,7) u escitalopramu, o -13,6 (z 30,0) u venlafaxinu XR. Rozdíl však nedosáhl hladiny statistické významnosti [20].
V 8týdenní dvojitě slepé studii (wash-out perioda 1 týden) byl escitalopram (20 mg denně) ve srovnání s venlafaxinem XR (225 mg denně) shledán účinnějším v dosažení odpovědi na léčbu (>/= 50%
redukce vstupního skóru MADRS) – 58,8 %, resp. 48,0 % (graf 2). Při léčbě escitalopramem dosáhlo na konci studie kritérií remise (MADRS skór tů (n = 97), při léčbě venlafaxinem XR to bylo 36,7 % pacientů (n = 98). U obou léčiv došlo k podobnému poklesu vstupního skóru MADRS o -15,9 (z 30,7) u escitalopramu, o -13,6 (z 30,0) u venlafaxinu XR. Rozdíl však nedosáhl hladiny statistické významnosti [20].
Jiná dvojitě slepá studie s venlafaxinem XR prokázala podobnou účinnost u escitalopramu (10–20 mg denně, n = 148) jako u venlafaxinu XR (75–150 mg denně, n = 145) ve změně MADRS a HAMD-17 (Hamilton Depression Rating Scale) v 8. týdnu. Pacienti s escitalopramem dosáhli setrvalé remise (MADRS ≤ 12 až do 8. týdne) statisticky významně dříve, a to od 2. do 4. týdne (p < 0,05), tedy o 6,6 dne dříve (ANCOVA p < 0,001). Střední konečná dávka byla 12,1 mg escitalopramu denně (u 22 % pacientů byla dávka zvýšena) a 95,2 mg venlafaxinu XR denně (zvýšení dávky u 24 % pacientů) [21]. Ve 24týdenním dvojitě slepém sledování byl escitalopram (n = 141, 20 mg denně) účinnější a lépe snášený než duloxetin (n = 151, 60 mg denně), obě antidepresiva byla shledána jako účinná v léčbě deprese ve srovnání s placebem. Escitalopram byl lépe tolerován [22]. Obdobná data byla získána i z metaanalýzy studií [23].
Metaanalýzy více antidepresiv
Následně byla provedena ještě řada studií, z nichž část byla publikována ve formě posterových sdělení. Byly provedeny dvě recentní metaanalýzy použití escitalopramu ve srovnání s SSRI/SNRI (venlafaxin, duloxetin). V Kennedyho práci podporované firmou Lundbeck, která zahrnula data 4549 pacientů ze 16 randomizovaných studií, byl escitalopram významně účinnější v redukci MADRS a v odpovědi na léčbu (63,7 % vs. 58,3 %, p < 0,0001) i v počtu pacientů, kteří dosáhli remise (53,1 % vs. 49,4 %, p < 0,0059). Escitalopram byl účinnější i v jednotlivých skupinách (SSRI, SNRI), byl účinnější i vzhledem k počtu pacientů, kteří předčasně ukončili účast ve studii. V podskupině pacientů s těžkou depresí (MADRS >/= 30) byl opět escitalopram účinnější. Tento rozdíl byl zachován i při použití dalších definic „těžké deprese“. Zajímavým výsledkem bylo grafické znázornění počtu pacientů, kteří předčasně ukončili léčbu, ve srovnání se střední změnou MADRS. Tento graf může být účinnou pomůckou při rozhodování o vhodné léčebné intervenci [24].
![Graf 3 Použití 11 antidepresiv s ohledem na jejich účinnost a snášenlivost ve srovnání s fluoxetinem. Svislá osa značí pravděpodobnou snášenlivost (počty vysazení léčiva). Směrem nahoru se snášenlivost ve srovnání s fluoxetinem zvyšuje (tzn. vyšší hodnota pravděpodobnosti, 95% CI). Vodorovná osa značí pravděpodobnou účinnost (počty respondérů). Směrem doleva účinnost ve srovnání s fluoxetinem narůstá (95% CI); podle [25] – Cipriani, et al., 2009.](https://www.remedia.cz/photo-a-27835---.jpg) Ve druhé práci, která probíhala bez jakékoli podpory farmaceutické firmy, bylo hodnoceno 12 antidepresiv na základě 117 studií (25 928 pacientů). Tato rozsáhlá práce shledala escitalopram spolu se sertralinem jako nejvýhodnější antidepresiva s ohledem na poměr účinnosti a snášenlivosti ( graf 3 ). Obě metaanalýzy jsou také dobrým zdrojem jednotlivých studií [25].
Ve druhé práci, která probíhala bez jakékoli podpory farmaceutické firmy, bylo hodnoceno 12 antidepresiv na základě 117 studií (25 928 pacientů). Tato rozsáhlá práce shledala escitalopram spolu se sertralinem jako nejvýhodnější antidepresiva s ohledem na poměr účinnosti a snášenlivosti ( graf 3 ). Obě metaanalýzy jsou také dobrým zdrojem jednotlivých studií [25].
Léčba těžších depresí
V podskupině závažně nemocných (MADRS >/= 35) bylo dosaženo ještě výraznějšího rozdílu mezi escitalopramem a citalopramem (3,48; Cl 95% -0,28–7,24; p = 0,07) – již blíže hladině statické významnosti. Pacienti užívali 12,6 mg escitalopramu denně a 26,4 mg citalopramu denně. Nutno ovšem podotknout, že ve dvou studiích byla podávána fixní dávka (10 vs. 20 mg) a ve dvou studiích bylo flexibilní dávkovací schéma 10–20 mg, resp. 20–40 mg [17]. Ve všech výše zmíněných parametrech srovnání SSRI byl escitalopram také oproti paroxetinu účinnější u podskupiny pacientů s těžší depresí (MADRS >/= 30, p < 0,017) [18].
Statisticky významný rozdíl v účinnosti mezi escitalopramem a citalopramem byl dosažen i v další analýze závažně nemocných depresivních pacientů (MADRS >/= 30), skládající se ze tří studií. Respondérů v escitalopramové větvi bylo zachyceno 56 % (n = 169) vs. 41 % (n = 171) u pacientů s citalopramem (p = 0,007). Placebo bylo podáváno 166 pacientům [26].
Ve dvojitě slepé randomizované studii v léčbě ambulantních pacientů se závažnou depresí (MADRS >/= 30) byl escitalopram (n = 138) shledán účinnějším než citalopram (n = 142). Skór MADRS se snižoval více ve skupině s escitalopramem než ve skupině citalopramové (-22,4 Ī 12,9 vs. -20,3 Ī 12,7; p < 0,05). Při léčbě escitalopramem byl zaznamenán vyšší počet pacientů odpovídajících na léčbu (76,1 %) než při léčbě citalopramem (61,3 %, p < 0,01). Pacientů dosahujících kritérií remise bylo 56,1 %, resp. 43,6 %, při léčbě citalopramem (p < 0,05). Obě účinné látky byly dobře tolerovány – ve skupině s escitalopramem předčasně ukončilo studii 6 pacientů, ve skupině s citalopramem 15 pacientů (p = 0,05) [16].
Souhrnná data z patnácti srovnávacích studií prokázala, že zatímco účinek escitalopramu na vstupní tíži symptomů (MADRS, HAMD) nezávisí, u komparátorů účinnost s tíží symptomů (skupina s MADRS >/= 30) klesá, přičemž se nejedná o vliv metodiky jednotlivých studií nebo konkrétních komparátorů. Autoři měli snahu zjistit, zda lze vysledovat konkrétní prediktory lepší odpovědi na escitalopram, byly použity pouze studie s fixním dávkováním 10 mg denně. Součet položek HAMD psychomotorická retardace a beznaděj ( ≥ 2) znamenal, že pacienti s těmito symptomy při léčbě escitalopramem dosáhli významně lepších výsledků než pacienti s komparátorem. Tento nález může být významný při výběru vhodného antidepresiva [27].
Rychlost nástupu účinku
Potenciál rychlejšího nástupu účinku je sledován již několik let. Je možné jej odvodit z dvojitě slepých studií srovnávajících escitalopram s placebem. Zde byl escitalopram shledán účinnějším než placebo již v prvním týdnu (viz výše). Již animální modely chronického stresu dávají tušit možnost masivnější terapeutické odpovědi už v prvním týdnu podávání escitalopramu – na rozdíl od tricyklických antidepresiv [28]. Tuto hypotézu potvrzuje zjištěním vyšší účinnosti escitalopramu v 7. dnu léčby ve srovnání s komparátory (SSRI, venlafaxin) rovněž analýza osmi dvojitě slepých studií (n = 2290) [29].
Dlouhodobá léčba
![Graf 4 Čas do relapsu během 36 týdnů dvojitě slepé fáze studie, kdy byl pacientům podáván escitalopram, nebo placebo; podle [30] – Rapaport, et al.](https://www.remedia.cz/photo-a-27836---.jpg) Do první dvojitě slepé studie (36 týdnů) hodnotící účinnost escitalopramu byli zařazeni pacienti dosahující kritérií remise (MADRS
≤ 12) užívající escitalopram po otevřené (open-label) fázi léčby (10–20 mg escitalopramu denně) z původně 8týdenní dvojitě slepé komparované (escitalopram, citalopram, placebo) studie. Relapsů bylo zaznamenáno 26 % při léčbě escitalopramem (n = 181) a 40 % (n = 93) při použití placeba (p = 0,01). Čas do relapsu deprese byl statisticky významně delší (p = 0,013) při aktivní léčbě, viz graf 4 [30]. Obdobné výsledky byly zaznamenány v řadě dalších studií [31], místy byla prokázána superiorita escitalopramu i ve srovnání s aktivním komparátorem [32].
Do první dvojitě slepé studie (36 týdnů) hodnotící účinnost escitalopramu byli zařazeni pacienti dosahující kritérií remise (MADRS
≤ 12) užívající escitalopram po otevřené (open-label) fázi léčby (10–20 mg escitalopramu denně) z původně 8týdenní dvojitě slepé komparované (escitalopram, citalopram, placebo) studie. Relapsů bylo zaznamenáno 26 % při léčbě escitalopramem (n = 181) a 40 % (n = 93) při použití placeba (p = 0,01). Čas do relapsu deprese byl statisticky významně delší (p = 0,013) při aktivní léčbě, viz graf 4 [30]. Obdobné výsledky byly zaznamenány v řadě dalších studií [31], místy byla prokázána superiorita escitalopramu i ve srovnání s aktivním komparátorem [32].
Léčba úzkostných poruch
Pro přehlednost uvádíme jen několik vybraných studií. Escitalopram byl sledován i v dalších indikacích. V léčbě úzkostných poruch (panické poruchy, sociální fobie a generalizované úzkostné poruchy) byl účinnější než placebo, se srovnatelným výskytem nežádoucích účinků [33].
Escitalopram (n = 128) byl zhodnocen jako účinnější než placebo (n = 119) a nejméně stejně účinný jako citalopram (n = 119) v léčbě panické poruchy – v redukci panických atak a dalších symptomů panické poruchy (Panic and Agorafobia Symptoms Scale, Clinical Global Impression, Quality of Life Enjoyment and Satisfaction Questionnaire). Tolerován byl stejně dobře jako placebo [34]. V zábraně relapsů sociální fobie prokázal escitalopram vyšší účinek než placebo, s podstatným vlivem na kvalitu života [35]. Jeho přínos byl vyšší než u paroxetinu [36]. Escitalopram byl účinný v léčbě populací starších pacientů s generalizovanou úzkostnou poruchou [37].
Lze shrnout, že escitalopram má dobře prokázanou účinnost v léčbě panické poruchy a agorafobie, generalizované úzkostné poruchy, sociální fobie, obsedantně-kompulzivní poruchy. Počty studií převyšují rozsah tohoto textu, souhrnně lze odkázat na existující vodítka (guidelines) pro léčbu ze zahraničních i českých zdrojů [38].
Studie v ČR – postmarketingová sledování
V ČR se uskutečnilo více otevřených neintervenčních studií. Ve všech byl zaznamenán trend k výraznému zlepšení v populaci pacientů léčených převážně pro depresivní obtíže. Diagnostika úzkostných poruch byla řidší. V nejrozsáhlejším sledování z let 2004–2005 byla získána data od 8841 pacientů z celé ČR. Tyto údaje se staly masivním základem pro hodnocení nejen účinnosti escitalopramu a subjektivní rychlosti nástupu účinku, ale i diagnostických a léčebných zvyklostí. Nežádoucí účinky byly v první kontrole zaznamenány jen u 7,7 % léčených pacientů. Jejich frekvence rychle klesala. Po celou dobu studie byla terapeutická dávka většiny pacientů 10 mg denně bez potřeby titrace. I novější data potvrzují velmi dobrou účinnost i snášenlivost, a to bez ohledu na pohlaví, věk nebo původní tíži onemocnění. Informace lze získat v české i zahraniční literatuře [39].
Farmakoekonomika
Je snahou mnoha výrobců léků prokázat, že jejich léčivo je v cílovém efektu levnější než přípravek vyrobený konkurenční firmou (s přihlédnutím k účinnosti, rychlosti nástupu efektu…) nebo že přináší plátcům zdravotní péče úspory a je výhodné jej podávat. V oblasti farmakoekonomických studií bylo opakovaně dosaženo příznivých výsledků – escitalopram může být výhodnější než ostatní antidepresiva. Problematické je však zhodnocení v jiných státech vzhledem k odlišnému zdravotnímu systému. V ČR byla publikována jediná práce hodnotící srovnání nákladů na léčbu mezi escitalopramem a citalopramem, zároveň byla brána v potaz možnost léčby psychiatrem anebo praktickým lékařem. Při půlroční léčbě byl největší rozdíl zaznamenán mezi escitalopramem z rukou praktického lékaře vůči citalopramu od psychiatra, a to ve prospěch prvně jmenovaného způsobu indikace [40].
Zařazení do současné palety léčiv
Escitalopram je relativně novým antidepresivem na českém trhu, jde o první klinicky využitý stereoizomer mezi antidepresivy. Jeho účinnost byla ověřena v řadě poruch afektivního a úzkostného spektra, stejně tak i v zábraně relapsu depresivní poruchy. V krátkodobých studiích byl účinnější než placebo již po 1–2 týdnech podávání. V klinických studiích byl stejně účinný nebo účinnější než citalopram nebo venlafaxin.
Mezi jeho výhody patří velmi dobrá snášenlivost, téměř úplná absence klinicky významných interakcí a bezpečnost při podávání. Jako zvláště výhodný lze označit potenciál rychlejšího nástupu účinku, a to již zřejmě během prvního týdne podávání, a široké terapeutické spektrum. Escitalopram je také výrazněji více účinný u pacientů s těžší symptomatikou.
Nadějné mohou být další studie směřující k ověření escitalopramu v indikacích ostatních úzkostných poruch a k ověření profylaktické účinnosti. Další výhody mohou vyplývat z farmakoekonomických srovnání a preferencí (doporučených postupů) farmak dle efektivity – s dobře prokázaným terapeutickým efektem a vyhovující snášenlivostí.
Indikace
Léčba depresivní poruchy, panické úzkostné poruchy s agorafobií i bez agorafobie, sociální úzkostné poruchy (sociální fobie), generalizované úzkostné poruchy, obsedantně-kompulzivní poruchy.
Kontraindikace
Současné podávání IMAO (inhibitory monoaminooxidázy) nebo podávání escitalopramu v období 2 týdny po skončení léčby IMAO, přecitlivělost na složky přípravku.
Nežádoucí účinky
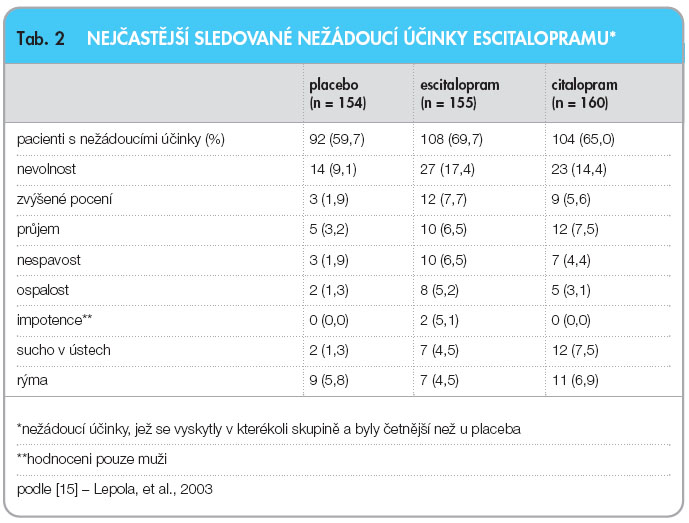 V tab. 2 jsou uvedeny nejčastější sledované nežádoucí účinky escitalopramu ve studii Lepoly [15]. Časem se výskyt některých nežádoucích účinků snižuje, zejména se tento jev týká nauzey, únavnosti, průjmu, cefalgie a insomnie.
V tab. 2 jsou uvedeny nejčastější sledované nežádoucí účinky escitalopramu ve studii Lepoly [15]. Časem se výskyt některých nežádoucích účinků snižuje, zejména se tento jev týká nauzey, únavnosti, průjmu, cefalgie a insomnie. ![Graf 5 Počet pacientů léčených escitalopramem v dávce 20 mg/den a venlafaxinem XR v dávce 225 mg/den, u kterých byly zaznamenány nežádoucí účinky nebo kteří přerušili léčbu z důvodu výskytu nežádoucích účinků; podle [20] – Bielski, et al., 2004.](https://www.remedia.cz/photo-a-27838---.jpg) Studie Bielskiho se mimo jiné zabývala bezpečností podávání escitalopramu ve srovnání s venlafaxinem XR [20]. Výsledky studie jsou shrnuty v grafu 5 .
Studie Bielskiho se mimo jiné zabývala bezpečností podávání escitalopramu ve srovnání s venlafaxinem XR [20]. Výsledky studie jsou shrnuty v grafu 5 . Lékové interakce
Není vhodná kombinace s IMAO (inhibitory monoaminooxidázy) pro riziko vzniku serotoninového syndromu, je třeba dodržet wash-out periodu po dobu dvou týdnů. U reverzibilních IMAO (RIMA, např. moklobemid) potom nejméně jeden den. Mezi ukončením podávání escitalopramu a IMAO je vhodná wash-out perioda 7 dní. Stejně tak je třeba opatrnosti u inhibitorů monoaminooxidázy B (selegilin). Rizikem je užití i jiných serotoninergních preparátů. Dále je třeba opatrnosti při současném podávání lithia, tryptofanu, preparátů z třezalky tečkované a látek snižujících křečový práh. Plazmatické hladiny escitalopramu mohou být zvýšeny při současném podání jiných psychofarmak metabolizovaných izoenzymem CYP2D6 (desipramin, nortriptylin, klomipramin, risperidon, thioridazin, haloperidol). Escitalopram může ovlivnit hladiny perorálních antikoagulancií.
Inhibitory izoenzymu 2C19 cytochromu P450 (např. omeprazol), inhibitory CYP-450 (např. cimetidin) mohou zvyšovat plazmatické koncentrace escitalopramu – při současném podávání je nezbytné snížit denní dávky escitalopramu.
Opatrnosti je třeba u epileptiků, diabetiků, u pacientů se sníženou funkcí jater a ledvin.
Těhotenství a kojení
V těhotenství a kojení by měl být escitalopram podáván jen po pečlivém zvážení přínosu a rizika. Novější antidepresiva (SSRI včetně escitalopramu a SNRI) neznamenají zřejmě vyšší rizika pro použití v těhotenství (výskyt závažných malformací), nežli je v běžné neléčené populaci [41].
Intoxikace
Byl popsán jen asymptomatický průběh s následnou plnou úpravou při dávkách 190–600 mg. Neexistuje specifické antidotum, doručuje se výplach žaludku a monitorování kardiálních a jiných vitálních funkcí. Hemodialýza je neúčinná [1].
Dávkování
Počáteční dávka 10 mg může být po týdnu dle potřeby zvýšena na 20 mg, lze samozřejmě podávat i dávku nižší. Podává se 1krát denně ráno nebo večer, po jídle nebo před jídlem. U starších nemocných a při hepatální dysfunkci by neměla být překročena dávka 10 mg denně.
Konečné dávky v randomizovaných studiích se pohybovaly (v případě flexibilního dávkování) mezi 11–15 mg (viz výše). O dávkách v běžné klinické praxi a výskytu nežádoucích účinků bránících v další léčbě dávají dobrou představu naturalistické studie. V 8týdenním sledování (n = 5453) byl escitalopram podáván v dávce 11,6 mg denně (omezeno max. 20 mg denně), 9 % pacientů ukončilo sledování pro nežádoucí účinky [42]. V jiné, menší studii (n = 797) bylo dosaženo střední dávky 12,1
Ī 4,2 mg denně [43]. V ČR byly nejčastěji podávány dávky 10 mg denně [44]. Obecně se zdá, že dávka 10 mg podávaná jednou denně vyhovuje většině pacientů z hlediska kombinace účinnosti a snášenlivosti. V případě těžké depresivní fáze (MADRS > 30) představuje účinná dávka na základě analýzy dat z více studií častěji 20 mg [45].
Balení
V ČR je dostupný jak originální přípravek s obsahem 10 mg escitalopramu v jedné tabletě, tak několik generických preparátů s obsahem 5 mg, 10 mg nebo 20 mg escitalopramu v jedné tabletě [46].
Seznam použité literatury
- [1] Lexapro prescribing information. Navštíveno 1. 3. 2010 http://www.frx.com/pi/lexapro_pi.pdf
- [2] Janů L, Racková S. Escitalopramum. Remedia 2005; 15: 477–483.
- [3] Sanchez C. The Pharmacology of Citalopram Enantiomers: The Antagonism by R-Citalopram on the Effect of S-Citalopram. Basic Clin Pharmacol Toxicol 2006; 99: 91–95.
- [4] Sanchez C, Gruca P, Papp M. R-citalopram counteracts the antidepressant-like effect of escitalopram in a rat chronic mild stress model. Behav Pharmacol 2003; 14: 465–470.
- [5] Owens MJ, Knight DL, Nemeroff CB. Second-generation SSRIs: Human monoamine transporter binding profile of escitalopram and R-fluoxetine. Biol Psychiatry 2001; 50: 345–350.
- [6] Mork A, Kreilgaard M, Sanchez C. The R-enantiomer of citalopram counteracts escitalopram-induced increase in extracellular 5-HT in the frontal cortex of freely moving rats. Neuropharmacology 2003; 45: 167–173.
- [7] Pirker W, Asenbaum S, Kasper S, et al. Beta-CIT SPECT demonstrates blockade of 5HT-uptake sites by citalopram in the human brain in vivo. J Neural Transm Gen Sect 1995; 100: 247–256.
- [8] Waugh J, Goa KL. Escitalopram: a review of its use in the management of major depressive and anxiety disorders. CNS Drugs 2003; 17: 343–362.
- [9] Drewes P, Thijssen I, Mengel H. A single-dose, crossover pharmaco-kinetic study comparing racemic citalopram (40 mg) with the S-enantiomer of citalopram (escitalopram 20 mg) in healthy male volunteers. NCDEU Annual Meeting, Phoenix, Abstracts 2001; 183.
- [10] Joffe P, Larsen FS, Pedersen V, et al. Single-dose pharmacokinetics of citalopram in patients with moderate renal insuficiency or hepatic cirrhosis compared with healthy subjects. Eur J Clin Pharmacol 1998; 54: 237–242.
- [11] Moltke von LL, Greenblatt DJ, Giancarlo GM, et al. Escitalopram (S-citalopram) and its metabolites in vitro: Cytochromes mediating biotransformation, inhibitory effects, and comparison to R-citalopram. Drug Metabol Disp 2001; 29: 1102–1109.
- [12] Gorman JM., Korotzer A, Guojin S. Efficacy of Escitalopram and Citalopram in the Treatment of Major Depressive Disorder: Pooled Analysis of Placebo-Controlled Trials. CNS Spectrums 2002; 7 (suppl.): 40–44.
- [13] Burke WJ, Gergel I, Bose A. Fixed dose trial of the single isomer SSRI escitalopram in depressed outpatients. J Clin Psychiatry 2002; 63: 331–336.
- [14] Colonna L, Reines EH, Andersen HF. Escitalopram is well tolerated and more efficacious than citalopram in long-term treatment in moderately depressed patients. Int J Psychiatr Clin Pract 2002; 6: 243–244.
- [15] Lepola UM, Loft H, Reines EH. Escitalopram (10–20 mg/day) is effective and well tolerated in a placebo-controlled study in depression in primary care. Int Clin Psychopharmacol 2003; 18: 211–217. Forest Laboratories Inc., unpublished data.
- [16] Moore N, Verdoux H, Fantino B. Prospective, multicentre, randomized, double-blind study of the efficacy of escitalopram versus citalopram in outpatient treatment of major depressive disorder. Int Clin Psychopharmacol 2005; 20: 131–137.
- [17] Auqier P, Robitail S, Llorca P, Rive B. Comparison of escitalopram and citalopram efficacy: A meta-analysis. Int J Psychiatr Clin Pract 2003; 7: 259–268.
- [18] Kasper S, et al. Superiority of escitalopram to paroxetine in the treatment of depression. Eur Neuropsychopharmacol 2009; 19: 229–237.
- [19] Ventura D, Armstrong EP, Skrepnek GH, Erder MH. Escitalopram versus sertraline in the treatment of major depressive disorder: a randomized clinical trial. Curr Med Res Opin 2007; 23: 245–250.
- [20] Bielski RJ, Ventura D, Chang CC. A double-blind comparison of escitalopram and venlafaxine extended release in the treatment of major depressive disorder. J Clin Psychiatry 2004; 65: 1190–1196.
- [21] Montgomery SA, Huusom AKT, Bithmer J. A Randomised Study Comparing Escitalopram with Venlafaxine XR in Primary Care Patients with Major Depressive Disorder. Neuropsychobiology 2004; 50: 57–64.
- [22] Wade A, Gembert K, Florea I. A comparative study of the efficacy of acute and continuation treatment with escitalopram versus duloxetine in patients with major depressive disorder. Current Medical Research and Opinion 2007; 23: 1605–1614.
- [23] Lam RW, Andersen HF, Wade AG. Escitalopram and duloxetine in the treatment of major depressive disorder: a pooled analysis of two trials. Int Clin Psychopharmacol 2008; 23: 181–187.
- [24] Kennedy SH, Andersen HF, Thase ME. Escitalopram in the treatment of major depressive disorder: A meta-analysis. Current Medical Research and Opinion 2009; 25: 161–175.
- [25] Cipriani A, Furukawa TA, Salanti G, et al. Comparative efficacy and acceptability of 12 new-generation antidepressants: a multiple-treatments meta-analysis. Lancet 2009; 373: 746–758.
- [26] Llorca PM, Azorin JM, Despiegel N, Verpillat P. Efficacy of escitalopram in patients with severe depression: a pooled analysis. Int J Clin Pract 2005; 59: 268–275.
- [27] Kilts CD, Wade AG, Andersen HF, Schlaepfer TE. Baseline severity of depression predicts antidepressant drug response relative to escitalopram. Expert Opin Pharmacother 2009; 10: 927–936.
- [28] Montgomery SA, Loft H, Sanchez C, et al. Escitalopram (S-enantiomer of citalopram): clinical efficacy and onset of action predicted from a rat model. Pharmacol Toxicol 2001; 88: 282–286.
- [29] Kasper S, Spadone C, Verpillat P, Angst J. Onset of action of escitalopram compared with other antidepressants: results of a pooled analysis. Int Clin Psychopharmacol 2006; 21: 105–110.
- [30] Rapaport MH, Bose A, Zheng H. Escitalopram Continuation Treatment Prevents Relapse of Depressive Epizode. J Clin Psychiatry 2004; 65: 44–49.
- [31] Wade A, Despiegel N, Reines H. Escitalopram in the Long-term Treatment of Major Depressive Disorder. Ann Clin Psychiatry 2006; 18: 83–89.
- [32] Boulenger JP, Huusom AKT, Weiller E, Florea I. Long-term treatment of severe major depression (MDD) with escitalopram or paroxetine. European Psychiatry 2007; 22 (Suppl. 1): S229.
- [33] Pollack MH, Bose A, Zheng H. Efficacy and tolerability of escitalopram in the treatment of anxiety disorders. Eur Neuropsychopharmacol 2002; 12 (Suppl. 3): 344.
- [34] Stahl SM, Gergel I, Li D. Escitalopram in the Treatment of Panic Disorder: A Randomized, Double-Blind, Placebo-Controlled Trial. J Clin Psychiatry 2003; 64: 1322–1327.
- [35] Servant D, Montgomery SA, Francois C. Relapse in Social Anxiety Disorder: Cost and Quality of Life. Eur Neuropsychopharmacol 2003; 13 (Suppl. 4): S370.
- [36] Lader M, Stender K, Burger V, Nil R. Fixed dose of escitalopram and paroxetine for the treatment of Social Anxiety Disorder (SAD). Neuropsychopharmacol 2003; 13 (Suppl. 4): S364.
- [37] Lenze EJ, Rollman BL, Shear MK, et al. Escitalopram for older adults with generalized anxiety disorder: a randomized controlled trial. JAMA 2009; 301: 295–303.
- [38] Bandelow B, et al. World Federation of Societies of Biological Psychiatry (WFSBP) Guidelines for the Pharmacological Treatment of Anxiety, Obsessive-Compulsive and Post-Traumatic Stress Disorders. First Revision. World J Biol Psychiatry 2008; 9: 248–312.
- [39] Anders M, Tuma I, Rösslerova H. A surveillance study of escitalopram treatment of depressed patients. Expert Opin Pharmacother 2008; 9: 1–6.
- [40] Filip V, Antoch J, Skopová J. Srovnání nákladů na léčbu velké depresivní epizody escitalopramem a citalopramem pomocí farmakoekonomického modelu. Psychiatrie pro praxi 2005; 3: 58–63.
- [41] Einarson TR, Einarson A. Newer antidepressants in pregnancy and rates of major malformations: a meta-analysis of prospective comparative studies. Pharmacoepidemiol Drug Saf 2005; 14: 823–827.
- [42] Rosenbaum JF, Hakkarainen H, Su G. Comparison of safety in placebo-controlled trials of escitalopram and citalopram. NCDEU Annual Meeting, Boca Raton, poster, 2002.
- [43] Olie JP, Tonnoir B, Menard F, Galinowski A. A prospective study of escitalopram in the treatment of major depressive episodes in the presence or absence of anxiety. Depress Anxiety 2007; 24: 318–324.
- [44] Janů L, Rösslerová H. Bezpečnost a účinnost escitalopramu v ČR 2005 (Otevřené sledování). Psychiatrie 2007; 11: Suppl. 1, p 39.
- [45] Bech P, Andersen HF, Wade A. Effective dose of escitalopram in moderate versus severe DSM-IV major depression. Pharmacopsych 2006; 39: 128–134.
- [46] AISLP verze 2010.1 – 1. 1. 2010.