Nalbufin
Opioidní analgetika jsou standardem léčby střední a silné bolesti nádorového i nenádorového původu. Léčbu však mohou komplikovat dobře známé vedlejší účinky opioidů, zahrnující nauzeu, zvracení, pruritus, obstipaci, sedaci, retenci moče nebo výskyt tolerance a závislosti. Použití smíšeného opioidního agonisty-antagonisty nalbufinu v léčbě bolesti může přispět k redukci těchto nežádoucích projevů léčby. Jako monoterapie je s úspěchem používán pro léčbu středně silné až silné pooperační bolesti. Kombinace nalbufinu s čistými opioidními agonisty přináší silný analgetický účinek s poklesem výskytu vedlejších účinků léčby.
Farmakologická skupina
Opioidní analgetika zajišťují nejefektivnější úlevu od bolesti. Jsou metodou volby v léčbě střední a silné bolesti. Mohou být aplikována všemi známými cestami, kontinuálně i v jednotlivých bolusech. Jejich působení, dávkování i nežádoucí účinky léčby jsou dobře známy. Právě vedlejší účinky opioidní léčby často limitují dosažení efektivní dávky, i když například silné opioidy nemají stanovenu maximální denní dávku. Ve snaze snížit konsumpci analgetik v léčbě bolestivých stavů jsou hledány různé postupy. Patří mezi ně kombinace opioidů s neopioidními analgetiky, používání celé řady tzv. adjuvantních analgetik (lokální anestetika, kortikoidy, antiepileptika, antidepresiva aj.) nebo využívání různých dávkovacích schémat včetně pacientem kontrolované analgezie – PCA (patient controlled analgesia).
Přesto jsou vedlejší projevy opioidní terapie limitujícím faktorem léčebného procesu. Nejčastějšími nežádoucími účinky jsou obstipace, pruritus, nauzea, zvracení, retence moči, sedace a respirační deprese nebo vývoj tolerance. Každý z těchto stavů může bránit dosažení adekvátní úlevy od bolestí v klidu nebo při pohybu. Nedostatečná analgezie u akutních bolestivých stavů je příčinou pozdní mobilizace, rehabilitace, zhoršené imunitní odpovědi, vzniku atelektáz, zvýšení incidence pooperačních komplikací apod. [1]. V léčbě chronických bolestí pak brání v pohybu, vede ke ztrátě koníčků, práce nebo sociálních vazeb.
Alternativní metodou léčby akutní bolesti je použití smíšeného agonisty-antagonisty nalbufinu. Jeho analgetický účinek je provázen nižším výskytem nežádoucích účinků opioidní léčby. Může být používán v monoterapii nebo i v kombinacích s čistými agonisty [2].
Mechanismus účinku a farmakodynamika
Nalb
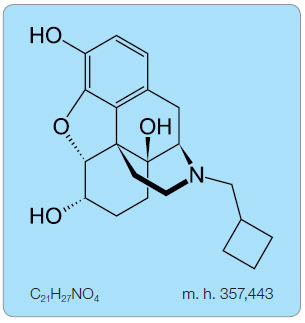 ufin hydrochlorid (obr. 1) je derivát morfinu s κ-agonistickými a μ-antagonistickými vlastnostmi (tab. 1). Na δ-opioidní receptory se váže minimálně nebo vůbec ne. Kromě hlavního agonistického účinku na κ-receptorech (mozek, Rexedova zóna I a II dorzálního míšního provazce) má nalbufin antagonistický účinek odpovídající asi čtvrtině účinku nalorfinu. Vazbou na μ-receptor nalbufin kompetitivně vytěsňuje ostatní μ-agonisty a chová se jako antagonista
ufin hydrochlorid (obr. 1) je derivát morfinu s κ-agonistickými a μ-antagonistickými vlastnostmi (tab. 1). Na δ-opioidní receptory se váže minimálně nebo vůbec ne. Kromě hlavního agonistického účinku na κ-receptorech (mozek, Rexedova zóna I a II dorzálního míšního provazce) má nalbufin antagonistický účinek odpovídající asi čtvrtině účinku nalorfinu. Vazbou na μ-receptor nalbufin kompetitivně vytěsňuje ostatní μ-agonisty a chová se jako antagonista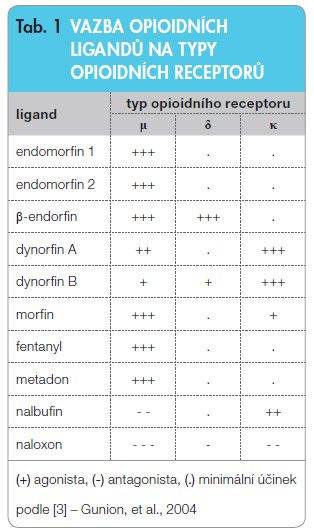 (obr. 2). Proto jej nazýváme smíšeným agonistou-antagonistou. Má jen minimální potenciál k vyvolání závislosti. Nemá téměř žádný účinek na hladké svalstvo zažívacího a močového traktu, čímž neovlivňuje negativně střevní pasáž a mikci. ATC kód je N02AF02.
(obr. 2). Proto jej nazýváme smíšeným agonistou-antagonistou. Má jen minimální potenciál k vyvolání závislosti. Nemá téměř žádný účinek na hladké svalstvo zažívacího a močového traktu, čímž neovlivňuje negativně střevní pasáž a mikci. ATC kód je N02AF02.Sumární vzorec: C21H27NO4
Molekulová hmotnost: 357,443
Farmakokinetické vlastnosti
K nástupu účinku dochází za 2–3 minuty po intravenózním podání u dětí i dospělých. Po intramuskulární nebo subkutánní injekci účinek nastupuje po 15 minutách u dospělých a po 20–30 minutách u dětí. Biologický poločas nalbufinu je 2,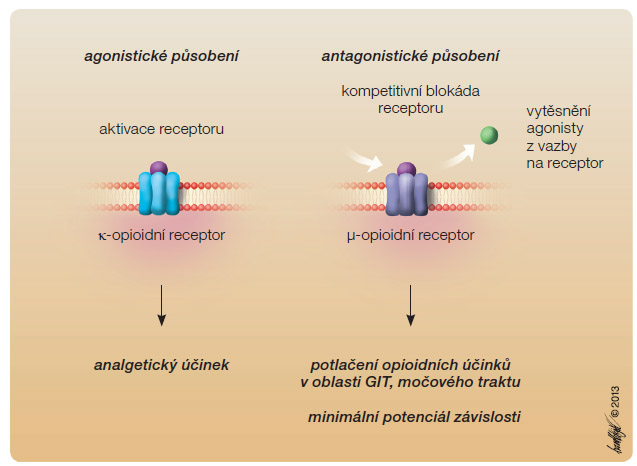 93 ± 0,795 hodiny, výrazně delší je u novorozenců (4,1 hodiny). Délka trvání účinku je 3 až 6 hodin, u dětí od 2 let věku maximálně 4 hodiny [4].Vazba na bílkoviny dosahuje asi 50 %. Nalbufin je metabolizován v játrech, avšak žádný z jeho 7 glukuronidovaných metabolitů nemá vlastní analgetickou aktivitu. Vylučovány jsou převážně do žluče a stolice, menší část pak močí [5].
93 ± 0,795 hodiny, výrazně delší je u novorozenců (4,1 hodiny). Délka trvání účinku je 3 až 6 hodin, u dětí od 2 let věku maximálně 4 hodiny [4].Vazba na bílkoviny dosahuje asi 50 %. Nalbufin je metabolizován v játrech, avšak žádný z jeho 7 glukuronidovaných metabolitů nemá vlastní analgetickou aktivitu. Vylučovány jsou převážně do žluče a stolice, menší část pak močí [5].
Klinické zkušenosti
Nalbufin nabízí svým κ-agonistickým působením efektivní potlačení středně silné akutní bolesti. V léčbě pooperační bolesti po hysterektomii [6], artroskopických výkonech nebo extrakci zubů byl jeho účinek shledán srovnatelným s působením morfinu. V léčbě pooperační bolesti je však řada stavů, kdy monoterapie nalbufinem nemůže poskytnout dostatečnou analgezii, například v léčbě bolesti po torakotomii nebo po sternotomii pro koronární bypass [7]. Limitujícím faktorem pro použití nalbufinu v těchto stavech je jeho stropový efekt – zvyšování dávky nad tuto hranici nevede v léčbě silných bolestí k dalšímu zesilování analgetického účinku [8]. Proto musí být indikace pro monoterapii nalbufinem pečlivě vybírány.
Studie Dana a kol. srovnávající efekt nalbufinu a petidinu, který byl dlouhá léta standardem v léčbě gynekologické a porodní pooperační bolesti, neprokázala významný rozdíl při podávání nalbufinu či petidinu. Nebyla shledána lepší analgetická účinnost jednoho z léčiv ani nižší výskyt vedlejších účinků léčby na matku či novorozeně [9]. Avšak další studie z Gynekologicko-porodnické kliniky FN Motol, kde byl nalbufin použit u 196 porodů, prokázala signifikantně lepší analgetickou účinnost nalbufinu proti petidinu a nevýznamně lepší průměr Apgar skóre v první minutě po porodu [10]. Proti použití petidinu však mluví jednoznačně fakt, že jeho eliminační poločas je až 32 hodin, a navíc jeho aktivní metabolit norpetidin má toxické, konvulzivní a halucinogenní účinky.
Po intravenózním podání nalbufinu dochází k poměrně rychlému transplacentárnímu přenosu, což může způsobit sedaci, bradykardii a hypotonii plodu [11]. Porodnická analgezie s použitím nalbufinu byla v jedné studii spojena s poklesem neurobehaviorálních škál u novorozence [12], naproti tomu další studie tento fakt neprokázala [13]. V pooperační analgezii u dětí byl tramadol shledán účinnějším analgetikem než nalbufin. Skupina léčená infuzí tramadolu vyžadovala signifikantně méně bolusů při vzestupu bolesti, na druhou stranu byly v této skupině častěji pozorovány nauzea a zvracení [14]. Výrazně mírnější nežádoucí účinky byly sledovány při použití PCA než při aplikaci bolusů nalbufinu [15].
Zkušenosti s používáním nalbufinu v porodnické analgezii a léčbě akutní bolesti u dětí ve Fakultní nemocnici Olomouc potvrzují velmi dobrý analgetický efekt a nízkou incidenci nežádoucích účinků. Nejčastějším vedlejším účinkem nalbufinu zůstává jeho sedativní účinek, a proto považujeme za nezbytné míru sedace monitorovat. S rostoucí zkušeností s používáním nalbufinu klesá i míra neočekávaných událostí. Nalbufin doplňuje škálu moderních postupů v porodnické analgezii, především epidurální analgezii a intravenózní infuzi remifentanilu.
Použití nalbufinu v léčbě středně silné pooperační bolesti je výhodné především pro nízký výskyt vedlejších účinků, které jsou běžné při použití čistých μ-agonistů. Jeho podání nezpůsobuje pruritus ani aktivací μ-receptorů v míše, ani uvolňováním histaminu z mastocytů. Nalbufin nestimuluje chemoreceptory v area postrema a ani při jeho použití v monoterapii nedochází k rozvoji nauzey a zvracení.
Použití nalbufinu provází mnohem nižší výskyt respirační deprese a nežádoucí sedace, což jsou nejobávanější vedlejší účinky použití μ-agonistů. Sedace a deprese dechu se může objevit již po podání malých dávek do 5 mg i.v., další zvyšování dávky ale nevede k jejich prohloubení – stropový efekt nalbufinu [8, 15]. Respirační deprese je zprostředkována vazbou opioidů na μ-receptory a antagonistické působení nalbufinu její výskyt mírní [9, 16]. Také negativní ovlivnění aktivity hladkého svalstva je při použití nalbufinu v léčbě akutní bolesti výrazně menší. Smíšený agonista-antagonista snižuje retenci moči a nutnost katetrizace močového měchýře, redukuje výskyt obstipace a minimálně ovlivňuje evakuaci žaludku a peristaltiku [17].
Indikace
Nalbufin je dostupný jako injekční roztok, který se podává při léčbě akutních středně silných a silných bolestí. Pro své vlastnosti je s výhodou používán v léčbě pooperační bolesti. Aplikovat se může intravenózně, subkutánně nebo nitrosvalovou injekcí. Orální forma nalbufinu není k dispozici. Není schváleno epidurální nebo intratekální podání, transdermální cesta podání nalbufinu je předmětem výzkumu [18].
Dávkování
Doporučená jednotlivá dávka představuje u dospělých 0,1–0,3 mg/kg, u dětí pak 0,1–0,2 mg/kg. Intravenózní jednotlivé dávky se doporučuje titrovat po 1 miligramu až do úlevy od bolesti. Často se však používá kontinuální infuze nalbufinu v dávkách 0,05–0,3 mg/kg/h [19]. V režimu PCA se podávají bolusy 1–3 mg s tzv. lock-out intervalem (doba, kdy je systém automaticky inaktivován) 6–10 minut [20]. Je-li to nezbytné, může se podání subkutánních nebo intramuskulárních dávek opakovat po 3–6 hodinách. U starších pacientů je doporučována pečlivá titrace dávky, u dětí mladších 18 měsíců nejsou až na údaje z jednotlivých případových studií dostupné relevantní údaje o léčbě.
Maximální jednotlivá dávka pro dospělé je 20 mg, pro děti 0,2 mg/kg tělesné hmotnosti. Stropového efektu analgetického účinku je dosaženo po podání 50 mg látky, pro respirační depresi nastává stropový efekt po dávce 30 mg. Antidotem nalbufinu je naloxon.Roztok pro intravenózní podání není kompatibilní pro mísení s intralipidem, nafcilinem nebo koncentrovaným ketorolakem – jsou doporučeny různé cesty podání [21]. Avšak vzhledem k faktu, že nebyly provedeny studie kompatibility, není obecně doporučeno tento léčivý přípravek mísit s jinými léčivy.
Kontraindikace
Léčba nalbufinem je kontraindikována u známé přecitlivělosti na kteroukoliv látku obsaženou v přípravku. Doporučuje se zvýšená opatrnost u pacientů s mírnou poruchou funkce ledvin a/nebo jater, u těžších poruch funkce ledvin a jater je podání nalbufinu kontraindikováno. Údaje v SPC uvádějí kontraindikaci podání nalbufinu rovněž u pacientů léčených čistými μ-agonisty [22], v praxi je však tato kombinace používána a je dobře popsána – viz závěr článku.
Při porodu by měl být nalbufin podán v případě, že očekávaný prospěch převyšuje riziko pro dítě. Matka není depresí dechu ohrožena, novorozenci by však měli být monitorováni pro možný výskyt respirační deprese, apnoe, bradykardie či arytmií [23]. Pro tyto případy by měl být dostupný naloxon jako antidotum. Nalbufin je vylučován do mateřského mléka, a proto je doporučeno přerušit kojení na 24 hodin [22].
Nežádoucí účinky
Mezi nejčastější nežádoucí účinky léčby nalbufinem patří sedace (kolem 10 % případů), ospalost, dysforie, vertigo, nauzea a zvracení nebo pocení (četnost kolem 1 %). Naopak retence moči nebo obstipace, která je velmi častá při podávání čistých opioidních agonistů, není popisována. Sedace je v léčbě akutní pooperační bolesti často žádoucím jevem a při pečlivé titraci dávky se lze nadměrného útlumu snadno vyvarovat.
Mezi vzácné nežádoucí účinky s incidencí kolem 1 ‰ patří nervozita, třes, abstinenční příznaky, zmatenost, bradykardie, tachykardie, respirační potíže, hypotenze, alergické reakce nebo kopřivka.Léčba nalbufinem je spojena s nízkým rizikem rozvoje abúzu a jeho zvyšující se dávky působí spíše dysforicky než euforicky [4]. Nízké dávky nalbufinu brání rozvoji tolerance a fyzické závislosti u pacientů léčených čistými μ-agonisty, aniž by snižovaly kvalitu analgezie. Tento jev není paradoxně způsoben μ-antagonistickým účinkem nalbufinu, ale jeho κ-agonistickým působením [24].
Nalbufin může negativně ovlivňovat pozornost a schopnost reagovat. Předávkování může vést k sedaci, spavosti, respirační depresi a bezvědomí [22].
Lékové interakce
Současné podání nalbufinu a čistých opioidních agonistů (morfin, fentanyl, sufentanil, oxykodon aj.) může způsobit kompetici na μ-opioidních receptorech a v důsledku snížení analgetického účinku (viz kontraindikace nalbufinu). Alkohol výrazně zesiluje sedativní účinky nalbufinu. Riziko respirační deprese je výrazně zesíleno při současném podání benzodiazepinů, barbiturátů, neuroleptik, sedativních antidepresiv nebo antihistaminik.
Zařazení do současné palety léčiv
Použití smíšeného agonisty-antagonisty nalbufinu v léčbě akutní bolesti přináší řadu výhod. V monoterapii účinně tlumí mírnou a středně silnou bolest. Jeho podávání je zároveň provázeno nízkou incidencí nežádoucích účinků, především sedace, respirační deprese, obstipace a retence moči. Při vědomí možných rizik je používán v léčbě akutní bolesti u dětí a v porodnictví.
V praxi může být nalbufin metodou volby pro intravenózní, subkutánní nebo intramuskulární léčbu mírné a středně silné bolesti. Je vhodné jej podat, pokud má pacient anamnesticky doložený výskyt nežádoucích účinků při použití opioidů (nauzea, zvracení, pruritus, obstipace, retence moči nebo sedace). Nalbufin je vhodný pro léčbu akutní bolesti u všech věkových skupin, ačkoli novorozenci mohou být více ohroženi výskytem respirační deprese než ostatní pacienti. Je často využíván i pro analgezii v porodnictví, lékař však musí počítat s častější kontrolou ozev plodu a monitorací dítěte po porodu.
Stropový efekt nalbufinu nepřináší s rostoucí dávkou lepší analgezii ani prohloubení možné sedace a deprese dechového centra. Při předpokladu výskytu silné akutní bolesti, kterou nemůže nalbufin v kombinaci s neopioidními analgetiky pokrýt, je vhodné zahájit léčbu bolesti čistými agonisty. Pokud změníme analgetický režim v průběhu léčby nalbufinem, může dojít k potřebě vyšších dávek μ-agonistů.
Protože stále nemáme v klinické praxi k dispozici ideální analgetikum, musíme hledat cesty, jak při stávající situaci maximálně využít analgetickou potenci dostupných látek a zároveň potlačit nežádoucí jevy spojené s jejich používáním. Nalbufin nabízí rozšíření spektra analgetických postupů a možnost, jak se přiblížit ideální léčbě akutní bolesti.
Kombinace nalbufinu s μ-agonisty
Ačkoli mezi kontraindikace podání nalbufinu dle SPC patří jeho kombinace s čistými μ-agonisty, jsou k dispozici četné důkazy o zlepšeném analgetickém efektu a/nebo potlačení nežádoucích účinků μ-agonistů. Malé dávky nalbufinu redukují výskyt svědění po podání morfinu [25].
Podobné účinky vykazuje použití nalbufinu ve snaze redukovat nauzeu a zvracení, aniž by byla ovlivněna analgezie po podání μ-agonistů [25]. Pro kombinaci čistých μ-agonistů s nalbufinem v klinické praxi hovoří i potlačení antianalgetického účinku smíšeného agonisty-antagonisty. Gear a kol. prokázali, že nízké dávky morfinu mohou
redukovat antianalgetický efekt nalbufinu u mužů [26]. Nalbufin v dostatečné dávce může blokovat analgetický efekt agonistů, a dokonce vyvolat syndrom z odnětí [27]. Pokud je však nalbufin podáván se záměrem potlačit známé vedlejší účinky čistých agonistů, je zapotřebí mnohem menších dávek, které nevyvolají kompletní blokádu
μ-receptorů.
Seznam použité literatury
- [1] Málek J, Ševčík P, et al. Léčba pooperační bolesti. Praha, Mladá fronta, 2009: 17–19.
- [2] Gutstein HB, Akil H. Opioid analgesics. In: Hardman JG, Limbird LE, editors: Goodman & Gilman‘s The pharmacological basis of therapeutics. 10th ed. New York: McGraw-Hill; 2001: 69–619.
- [3] Gunion MW, Marchionne AM, Anderson CTM. Use of the mixed agonist-antagonist nalbuphine in opioid based analgesia. Acute Pain 2004; 6: 29–39.
- [4] Jaillon P, Gardin ME, Lecocq B, et al. Pharmacokinetics of nalbuphine in infants, young healthy volunteers, and elderly patients. Clin Pharmacol Ther 1989; 46: 226–233.
- [5] Schmidt WK, Tam SW, Shotzberger GS, et al. Nalbuphine. Drug Alcohol Dep 1985; 14: 339–362.
- [6] Ho ST, Wang JJ, Hu OY, et al. Comparison of PCA nalbuphine and morphin in Chinese gynecologic patients. Acta Anaesthesiol Sin 1998; 36: 65–70.
- [7] Etches RC, Sandler AN, Lawson SL. A comparison of the analgesic and respiratory effects of epidural nalbuphine or morfine in postthoracotomy patients. Anesthesiology 1991; 75: 9–14.
- [8] Pugh GC, Drummond GB. A dose-response study with nalbuphine hydrochloride for pain in patients after upper abdominal surgery. Br J Anaesth 1987; 59: 1356–1363.
- [9] Dan U, Rabinovici Y, Barkai G, et al. Intravenous pethidine and nalbuphine during labor: a prospective double-blind comparative study. Gynecol Obstet Invest 1991; 32: 39–43.
- [10] Vavřinková B, Binder T, Horák J. Využití nalbuphinu v porodnické analgezii. Čes Gynek 2010; 75: 563–568.
- [11] Sgro C, Escousse A, Tennenbaum D, Gouyon JB. Perinatal adverse effects of nalbuphine given during labour. Lancet 1990; 336: 1070.
- [12] Wilson CM, McLean E, Moore J, Dundee JW. A double-blind comparison of intramuscular pethidine and nalbuphine in labor. Anaesthesia 1986; 41: 1207–1213.
- [13] Podlas J, Breland BB. Patient-controlled analgesia with nalbuphine during labor. Obstet Gynecol 1987; 70: 202–204.
- [14] Moyao-Garcia D, Hernández-Palacios JC, Ramírez-Mora JC, Nava-Ocampo AA. A pilot study of nalbuphine versus tramadol administered through continuous intravenous infusion for postoperative pain control in children. Acta Biomed 2009; 80: 124–130.
- [15] Romagnoli A, Keats AS. Ceiling effect for respiratory depression by nalbuphine. Clin Pharmacol Ther 1980; 27: 478–485.
- [16] Cohen SE, Ratner EF, Kreitzman TR, et al. Nalbuphine is better than naloxone for treatment of side effects after epidural morfine. Anesth Analg 1992; 75: 747–752.
- [17] Parker RK, Holtmann B, White PF. Patient-controlled epidural analgesia: interactions between nalbuphine and hydromorphone. Anesth Analg 1997; 84: 757–763.
- [18] Fang JY, Sung KC, Hu OY, et al. Transdermal delivery of nalbuphine pivalate from hydrogels by passive diffusion and iontophoresis. Arzneimittelforschung 2001; 51: 408–413.
- [19] Pugh GC, Drummond GB. A dose-response study with nalbuphine hydrochloride for pain in patients after upper abdominal surgery. Br J Anaesth 1987; 59: 1356–1363.
- [20] Krenn H, Oczenski W, Jellinek H, et al. Nalbuphine by PCA-pump for analgesia following hysterectomy: bolus application versus continuous infusion with bolus application. Eur J Pain 2001; 5: 219–226.
- [21] Shin D, Kim S, Kim CS, Kim H-S. Postoperative pain management using intravenous patient-controlled analgesia for pediatric patients. J Craniofac Surg 2001; 12: 129–133.
- [22] Souhrn údajů o přípravku Nalbuphin OrPha, dostupné na www. sukl.cz (navštíveno 20. 7. 2013).
- [23] Amin SM, Amr YM, Fathy SM, Alzeftawy AE. Maternal and neonatal effects of nalbuphine given immediately before induction of general anesthesia for elective cesarean section. Saudi J Anaesth 2011; 5: 371–375.
- [24] Lee SC, Wang JJ, Ho ST, Tao PL. Nalbuphine coadministered with morphine prevents tollerance and dependence. Anesth Analg 1997; 84: 810–815.
- [26] Gear RW, Gordon NC, Hossaini-Zadeh M, etal. A subanalgesic dose of morphine eliminates nalbuphine anti-analgesia in postoperative pain. J Pain 2008; 9: 337–341.
- [27] Jaffe RS, Moldenhauer CC, Hug CC, et al.Nalbuphine antagonism of fentanyl-induced ventilatory depression: a randomized trial.Anesthesiology 1988; 68: 254–260.