Sildenafil v léčbě erektilní dysfunkce
Sildenafil patří mezi inhibitory fosfodiesterázy typu 5 a stejně jako další dva zástupci této skupiny (vardenafil a tadalafil) se velmi úspěšně používá v léčbě erektilní dysfunkce. Vysoká účinnost, která se odráží i ve spotřebě těchto léčiv, by neměla vést k zanedbávání důkladné (diferenciální) diagnostiky onemocnění. Sildenafil má prakticky využitelný efekt (podmíněný sexuální stimulací) po 12 hodin, při podání s tučným jídlem se snižuje absorpce. Uvolňování oxidu dusnatého z neuronů v penisu vyvolá v buňkách hladkého svalstva kaskádu dějů, jejichž výsledkem je arteriální dilatace s nástupem erekce. Z vazodilatačního mechanismu působení vyplývají i nežádoucí účinky, lékové interakce a kontraindikace léčby (kardiovaskulární systém). Sildenafil je metabolizován prostřednictvím cytochromu P-450, proto je třeba pamatovat i na farmakokinetické interakce.
Farmakologická skupina
Sildenafil řadíme do skupiny léčiv používaných při poruchách erekce, ATC klasifikace je G04BE03. V dnešní době patří sildenafil k nejčastěji používaným léčivým látkám v této indikaci. Spotřeba sildenafilu byla v České republice v roce 2010 více než 780 tisíc DDD a zaujímala druhé místo mezi třemi inhibitory fosfodiesterázy typu 5 (PDE5), které jsou dostupné na tuzemském farmaceutickém trhu (sildenafil, tadalafil, vardenafil) [1].*
Mechanismus účinku, farmakodynamika
![Obr. 1 Mechanismus účinku sildenafilu; podle [2] – Kukreja, et al., 2005NO – oxid dusnatý, GC – guanylát cykláza, GTP – guanosin trifosfát, cGMP – cyklický guanosin monofosfát, PKG – proteinkináza G, PDE5 – fosfodiesteráza typu 5, GMP – guanosin monofosfát, VSM – vaskulární hladký sval (vascular smooth muscle)](https://www.remedia.cz/photo-a-28582---.jpg) Při sexuální stimulaci muže, buď psychické anebo fyzické, dochází k uvolnění oxidu dusnatého (NO) z non-adrenergních, non-cholinergních neuronů v penisu i z endoteliálních buněk. NO difunduje do cytoplazmy buněk hladkého svalstva, kde vyvolá celou kaskádu dějů, čímž dochází ke snížení intracelulární koncentrace vápenatých iontů. Tento mechanismus vede k relaxaci arterií a trabekulárního hladkého svalstva, k arteriální dilataci a venózní konstrikci, tedy k rigiditě erekce. Sildenafil selektivně a účinně inhibuje PDE5 v corpus cavernosum, jež je zodpovědná za degradaci cGMP (obr. 1). Sildenafil nemá žádný přímý relaxační účinek na izolované lidské corpus cavernosum, avšak významně zesiluje relaxační účinek NO na tuto tkáň. Při aktivaci dráhy NO/cGMP, k níž při sexuální stimulaci dochází, má inhibice PDE5 sildenafilem za následek zvýšení hladin cGMP v corpus cavernosum. Proto je k zajištění zamýšleného příznivého farmakologického účinku sildenafilu nutná sexuální stimulace [2–4].
Při sexuální stimulaci muže, buď psychické anebo fyzické, dochází k uvolnění oxidu dusnatého (NO) z non-adrenergních, non-cholinergních neuronů v penisu i z endoteliálních buněk. NO difunduje do cytoplazmy buněk hladkého svalstva, kde vyvolá celou kaskádu dějů, čímž dochází ke snížení intracelulární koncentrace vápenatých iontů. Tento mechanismus vede k relaxaci arterií a trabekulárního hladkého svalstva, k arteriální dilataci a venózní konstrikci, tedy k rigiditě erekce. Sildenafil selektivně a účinně inhibuje PDE5 v corpus cavernosum, jež je zodpovědná za degradaci cGMP (obr. 1). Sildenafil nemá žádný přímý relaxační účinek na izolované lidské corpus cavernosum, avšak významně zesiluje relaxační účinek NO na tuto tkáň. Při aktivaci dráhy NO/cGMP, k níž při sexuální stimulaci dochází, má inhibice PDE5 sildenafilem za následek zvýšení hladin cGMP v corpus cavernosum. Proto je k zajištění zamýšleného příznivého farmakologického účinku sildenafilu nutná sexuální stimulace [2–4].
Farmakokinetické vlastnosti
Základní farmakokinetické parametry sildenafilu shrnuje tab. 1.
Absorpce
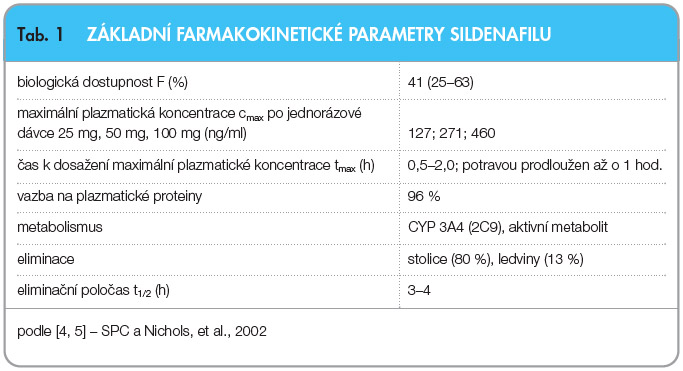 Sildenafil se po perorálním podání rychle vstřebává. Průměrná absolutní biologická dostupnost po perorálním podání je asi 40 %. Maximálních plazmatických hladin je dosaženo za 30–120 minut. Při podání s jídlem (obzvláště tučným) se snižuje rychlost absorpce, průměrně asi o 60 minut, a snižuje se i maximální plazmatická hladina (cmax) o 29 %. Systémová expozice měřená jako plocha pod křivkou plazmatických koncentrací (AUC) byla snížena při užití sildenafilu s jídlem o 11 %, což se nezdá být klinicky významné. Po perorálním podání se hodnoty AUC a cmax zvyšují víceméně úměrně s dávkou v celém rozsahu doporučených dávek (25–100 mg) [4, 5].
Sildenafil se po perorálním podání rychle vstřebává. Průměrná absolutní biologická dostupnost po perorálním podání je asi 40 %. Maximálních plazmatických hladin je dosaženo za 30–120 minut. Při podání s jídlem (obzvláště tučným) se snižuje rychlost absorpce, průměrně asi o 60 minut, a snižuje se i maximální plazmatická hladina (cmax) o 29 %. Systémová expozice měřená jako plocha pod křivkou plazmatických koncentrací (AUC) byla snížena při užití sildenafilu s jídlem o 11 %, což se nezdá být klinicky významné. Po perorálním podání se hodnoty AUC a cmax zvyšují víceméně úměrně s dávkou v celém rozsahu doporučených dávek (25–100 mg) [4, 5].
Distribuce
Průměrný distribuční objem v ustáleném stavu je u dospělých 105 l, což naznačuje distribuci do tkání. Sildenafil a jeho účinný metabolit N-desmethylsildenafil se váží z 96 % na plazmatické bílkoviny. Po perorálním podání 100 mg sildenafilu byla maximální celková plazmatická koncentrace v průměru 440 ng/ml a hladina volného sildenafilu 18 ng/ml [4, 5].
Metabolismus
Sildenafil je metabolizován převážně v játrech cytochromem P-450, zejména pak izoenzymem CYP 3A4 a minoritně též i CYP 2C9. Hlavní metabolit N-desmethylsildenafil vykazuje také selektivitu vůči PDE5 podobnou sildenafilu. In vitro byla stanovena jeho potence vůči PDE5 ve výši asi 50 % mateřské látky. Terminální poločas sildenafilu a jeho účinného metabolitu je přibližně 4 hodiny [4, 5].
Eliminace
Sildenafil se vylučuje ve formě metabolitů převážně stolicí (80 %) a v menší míře močí. Celková clearance sildenafilu je 41 l/h a může být redukována u starších pacientů anebo u pacientů s poškozením jater či ledvin [4, 5].
Klinické zkušenosti
 Sildenafil byl identifikován jako lék zlepšující erekci v rámci serendipity (schopnost nalézt neznámé, neočekávané – v tomto případě souvislosti) při výzkumu medikace určené k léčbě kardiovaskulárních (KV) onemocnění. Pacienti zařazení do studie nechtěli vracet nespotřebované tablety, neboť zaznamenali jejich příznivý efekt na erektivitu. Souvislosti s KV onemocněními a s medikací nitráty (či donory oxidu dusnatého) vyvolávaly počáteční obavy z nežádoucích účinků ve smyslu ohrožení života. Bylo tomu tak v počátcích léčby sildenafilem v USA, kde úřad FDA (Food and Drug Administration) sledoval tzv. Viagra associated deaths – úmrtí spojená s podáním sildenafilu. Pečlivé sledování a definování rizik vedlo k vytvoření pravidel medikace inhibitory PDE5 a vytvoření tzv. Princetonského konsenzu (tab. 2) [6]. Cílem byla minimalizace KV rizika při podávání inhibitorů PDE5 (PDE5i), neboť erektilní dysfunkce (ED) postihuje stejně jako onemocnění koronárních arterií nejvýznamněji skupinu mužů ve věku nad 50 let. Vytvoření přehledné pomůcky pomohlo přesněji klasifikovat stupeň KV rizika, vyhnout se nežádoucím účinkům a zbytečným obavám z předpisu sildenafilu či jiného PDE5i. Závažné vedlejší účinky se projevily řádově u stovek pacientů v poměru k miliardám předepsaných receptů.
Sildenafil byl identifikován jako lék zlepšující erekci v rámci serendipity (schopnost nalézt neznámé, neočekávané – v tomto případě souvislosti) při výzkumu medikace určené k léčbě kardiovaskulárních (KV) onemocnění. Pacienti zařazení do studie nechtěli vracet nespotřebované tablety, neboť zaznamenali jejich příznivý efekt na erektivitu. Souvislosti s KV onemocněními a s medikací nitráty (či donory oxidu dusnatého) vyvolávaly počáteční obavy z nežádoucích účinků ve smyslu ohrožení života. Bylo tomu tak v počátcích léčby sildenafilem v USA, kde úřad FDA (Food and Drug Administration) sledoval tzv. Viagra associated deaths – úmrtí spojená s podáním sildenafilu. Pečlivé sledování a definování rizik vedlo k vytvoření pravidel medikace inhibitory PDE5 a vytvoření tzv. Princetonského konsenzu (tab. 2) [6]. Cílem byla minimalizace KV rizika při podávání inhibitorů PDE5 (PDE5i), neboť erektilní dysfunkce (ED) postihuje stejně jako onemocnění koronárních arterií nejvýznamněji skupinu mužů ve věku nad 50 let. Vytvoření přehledné pomůcky pomohlo přesněji klasifikovat stupeň KV rizika, vyhnout se nežádoucím účinkům a zbytečným obavám z předpisu sildenafilu či jiného PDE5i. Závažné vedlejší účinky se projevily řádově u stovek pacientů v poměru k miliardám předepsaných receptů.
Efektivita sildenafilu je udávána v rozmezí od 43 % (např. po rozsáhlé operaci v pánvi – radikální prostatektomii) až po 84 % (psychogenní etiologie ED) [4]. Z analýz etiopatogenetického nálezu pacientů s ED vyplývá, že s výraznějším organickým nálezem klesá účinnost léčiva. Týká se to postižení vaskulogenního, kavernózogenního i hormonálního.
Zařazení do současné palety léčiv
Klinický přínos zavedení terapie ED sildenafilem spočíval zejména v podnícení zájmu o ED jako etiopatogenetickou jednotku. ED byla definována jako závažný symptom. Na přelomu tisíciletí se objevilo množství studií navazujících na možnost terapie sildenafilem.
Prevalence ED je v různých studiích uváděna v rozsahu 19–52 % mužské populace (liší se v různých věkových skupinách a podle selekce respondentů ve studiích). Incidence ED výrazně stoupá s věkem – od 40. roku života, kdy dosahuje asi 10 %, se vzestupem na 34 % po 60. roce a 50 % po 70. roce života, jak ukazuje Braunova „Cologne Male Survey“, provedená v Německu v roce 2000 [7].
Příčiny ED jsou ve většině případů vícečetné. Z medicínského hlediska jsou nejdůležitější KV rizikové faktory. Více než 92 % pacientů s ED přichází nejméně s jedním rizikovým faktorem aterosklerózy a onemocněním koronárních cév. Ve druhé polovině života je velmi častou příčinou ED kombinace vaskulogenních, hormonálních, kavernózogenních a psychogenních faktorů (v etiologii ED prokazatelně převažují organické příčiny). K tomu přistupují faktory partnerské a společenské, přičemž u každého pacienta je jejich kombinace individuální.
Včasná diagnóza metabolického onemocnění způsobujícího ED může být i velmi ekonomicky přínosná, pokud pomůže identifikovat muže s rizikem uzávěru koronárních arterií. V současné době není k dispozici validovaný marker endoteliálního poškození, nejlepší cestou je screening rizikových faktorů.
Nástup perorálních inhibitorů 5. izoenzymu fosfodiesterázy (PDE5i) výrazně změnil přístup k léčbě ED. Tyto léky jsou ve srovnání s dříve dostupnými léčivy nejsnadněji použitelnými léčivy první volby s bezprostředně dobrým efektem. Výrazný ekonomický úspěch (roční obraty v miliardách USD) povzbudil farmaceutický průmysl, který podpořil veřejnou prezentaci problému ED. Objevilo se mnoho nových publikací zabývajících se sexuálním životem a mužským sexuálním zdravím a v mnoha zemích byla sexuální problematika odtabuizována. Úspěch terapie PDE5i vedl bohužel také k tomu, že jsou tyto léky předepisovány pro téměř všechny sexuální potíže u mužů, a to s minimem diagnostiky. Ztrácí se možnost základních vyšetření a včasného záchytu onemocnění KV systému, prostaty a změn hormonálního prostředí, jejichž postižení jsou nejvýznamnější příčinou morbidity a mortality u mužů starších 50 let.
Téměř u každého muže hraje při aktuálních erektilních potížích určitou roli tzv. performance anxiety, tj. obava z nezdaru, ze selhání. Jedním z důležitých podnětů podporujících erekci je pocit nastupující erekce. Pokud se nedostavuje odpověď penisu na sexuální stimulaci, je to zneklidňující moment, který inhibuje nástup erekce a zhoršuje stav. Hovoříme o „circulus vitiosus“ (obava ze selhání – selhání – stupňovaná obava ze selhání). Lékem první volby je dnes u většiny mužů lék ze skupiny PDE5i. Bezprostřední efekt léčby často spočívá v přerušení tohoto bludného kruhu zvýšením penilní odpovědi na sexuální stimulaci. Velmi často je však tento efekt důvodem k ukončení diagnostiky příčiny ED, což může být pro pacienta nebezpečné (např. u závažných endokrinních deficiencí, aterosklerózy, hypertenze, koronárního onemocnění, karcinomu prostaty, tumoru hypofýzy, nádorových onemocnění retroperitonea, centrálního nervového systému).
V současné době jsou na trhu k dispozici tři PDE5i. Z údajů v SPC jednotlivých léků a z klinické praxe léčby ED vyplývá, že účinnost všech tří výše uvedených PDE5i je podobná, odlišují se zejména v délce účinku (s interindividuální variabilitou). Sildenafil a vardenafil mají prakticky využitelný efekt do 12 hodin (50 mg sildenafilu odpovídá 10 mg vardenafilu), tadalafil až do 48 hodin (výhodné tam, kde není možné či vhodné plánovat sexuální aktivitu). Bylo publikováno mnoho komparativních studií srovnávajících klinickou efektivitu dostupných PDE5i. Evidentní byla nejednoznačnost výsledků. Byly prezentovány také zajímavé práce popisující kombinační terapii PDE5i s androgeny.
Neúčinnost terapie PDE5i je vždy signálem k zahájení podrobné diagnostiky. Snížený efekt PDE5i byl prokázán u mužů s androgenní deficiencí. Většina mužů s krátkodobou ED a s ED mírného až středního stupně na terapii PDE5i odpovídá. Pokud je léčba neúčinná, lze ovlivnit erektivitu podáváním prostaglandinu E-1 (PGE-1) v intrakavernózních injekcích či použít podtlakový erekční přístroj. Operace cévního systému penisu mají význam v úzkých indikacích. Za poslední variantu řešení ED je v současné odborné veřejnosti považována implantace penilní protézy.
Indikace
Terapie sildenafilem (a ostatními PDE5i) je indikována u pacientů trpících ED a je symptomatologicky specifická. Léčba ED pomocí PDE5i u diabetiků musí navazovat na zvládnutí diabetu zpravidla s pomocí diabetologa [4].
Je nutné věnovat dostatek času vysvětlení, že PDE5i účinkuje jen v souvislosti s navazující sexuální stimulací tím, že zesiluje účinek nervových podnětů přicházejících z mozku do topořivé svaloviny penisu. Účinek PDE5i je možné dle „doyena“ britské andrologie prof. T. B. Hargreavea přirovnat k regulaci „volume“ na radiovém či TV přijímači: není-li dobrý signál, tak otáčení „volume doprava“ nevede ke zlepšení zvuku. Chybí-li dostatečná sexuální stimulace, je požití PDE5i bez efektu. Pacienty je nutné seznámit také s tím, že lék nemá okamžitý účinek a že může trvat 1–2 hodiny, než se dostane do cirkulace, zejména po tučném jídle.
Kontraindikace
Pacienti, u nichž není z medicínského hlediska vhodná sexuální aktivita, tj. pacienti s těžkým KV onemocněním stejně jako pacienti po právě proběhlém infarktu myokardu (IM) či cévní mozkové příhodě, by měli být z léčby ED vyloučeni. Léčba je rovněž kontraindikována u pacientů se závažnou KV příhodou v uplynulých 6 měsících [1, 4].
Všechna léčiva ze skupiny PDE5i mají vazodilatační a hypotenzní efekt, proto by neměla být podávána při výrazné arteriální či ortostatické hypotenzi, při aortální stenóze a hypertrofické obstrukční kardiomyopatii. PDE5i ovlivňují nervovou mediaci oxidu dusnatého (NO). Hlavní kontraindikací léčby PDE5i je tedy podávání donorů NO, a to i v podobě sublingválního nitroglycerinu nebo nitrospreje v podobě inhalátoru. Ty jsou předepisovány pro podporu vazodilatace při symptomech anginy pectoris. Efekty donorů NO a PDE5i jsou kumulativní a mohou vést k výraznému snížení krevního tlaku při celkové vazodilataci. Pokles perfuze koronárními arteriemi může vyústit v IM, proto je v příbalovém letáku všech PDE5i uvedena informace, že tyto léky nemohou užívat lidé s anginou pectoris a s terapií donory NO. Podobné nebezpečí jako při výše zmíněné kumulaci hypotenzního účinku může představovat kombinace PDE5i a amylnitritu („poppers“), který je užíván v některých nightclubech. Je třeba varovat také před posturální hypotenzí při současném užívání PDE5i a a-blokátorů, které jsou často podávány kvůli symptomatologii dolního močového traktu (lower urinary tract symptoms – LUTS) hlavně při hyperplazii prostaty. Starší muži s ED mají obvykle LUTS, a pokud je zachovávána dostatečná opatrnost, mohou být a-blokátory a PDE5i podávány současně [1, 4].
Oba krátkodoběji účinkující PDE5i (sildenafil i vardenafil) mají určitý inhibující efekt na izoenzym PDE6, který je důležitý při zpracovávání světelného signálu na sítnici. Mohou způsobit krátkodobé změny v percepci barevného vidění. Léčba je kontraindikována u pacientů s retinitis pigmentosa a proliferativní retinopatií [1, 4].
U pacientů s klinicky závažným onemocněním jater, ledvin a poškozením CNS je nutno velmi pečlivě a individuálně vážit indikaci k léčbě PDE5i [1, 4].
Nežádoucí účinky
Sildenafil je látka s relativně dobrou tolerancí, a to i u starších pacientů (> 75 let) i pacientů s mírně poškozenou funkcí jater a ledvin. Bezpečnostní profil byl vytvořen na základě dat z 67 dvojitě zaslepených studií kontrolovaných placebem (více než 14 000 mužů) a na základě postmarketingového sledování bezpečnosti z databází výrobců (více než 39 000 pacientů). Podávání (všech tří PDE5i) mohou doprovázet bolesti hlavy (16 % mužů), zmírňují se po 1–2 hodinách, návaly horka (10 %), dyspepsie (7 %) a kongesce nosní sliznice (4 %). K vážným nežádoucím účinkům, vyskytujícím se však vzácně, patří IM, atriální fibrilace, nearteritická přední ischemická neuropatie optického nervu (NAION), náhlá hluchota a priapismus. Postmarketingová sledování potvrdila skladbu a četnost výskytu nežádoucích účinků sildenafilu, které byly zaznamenány v kontrolovaných klinických studiích [4, 8].
Změny vidění (3 % mužů) se mohou projevovat modravými skvrnami, zvýšenou citlivostí na světlo nebo rozmazaným viděním. Pokud pacient zaznamená tyto změny, nemá řídit motorové vozidlo. Změny vidění se mohou dostavit do 2 hodin od užití sildenafilu (i vardenafilu, méně pravděpodobné jsou u tadalafilu). Trvání změn vidění je 1–2 hodiny (maximálně 8 hodin).
Ztráta zraku způsobená přední ischemickou optickou neuropatií nemusí být skutečným nežádoucím účinkem léčby PDE5i. Úřad FDA ve Spojených státech požaduje po výrobcích těchto léků, aby varování před tímto postižením zahrnovali do údajů o PDE5i. V červenci 2005 FDA podal zprávu o 43 mužích, kteří oslepli: 38 z nich užilo sildenafil, 4 tadalafil, jeden vardenafil. Je nutno dodat, že preskripce těchto léků se pohybuje v miliardových počtech receptů.
Lékové interakce
Sildenafil interaguje s dalšími léčivy dvěma různými mechanismy.
Farmakodynamické interakce
Na úrovni farmakodynamiky sildenafil potencuje efekt nitrátů i některých dalších antihypertenziv (mechanismus účinku prostřednictvím NO/cAMP). Současné užití sildenafilu s nitráty, látkami uvolňujícími NO a molsidominem je kontraindikováno pro možnost rozvoje závažné hypotenze. I když některé studie naznačují kratší dobu klinického významu interakce, neměl by být jeden lék podáván během 24 hodin po užití druhého [4].
Při společném užívání a-blokátorů (především doxazosin, terazosin) se sildenafilem může dojít u citlivých jedinců k rozvoji symptomatické posturální hypotenze, jež se může nejčastěji objevit do 4 hodin po podání sildenafilu. V hlášení těchto případů se posturální hypotenze projevovala jako závratě či mdloby, nikoli jako synkopa. Při současném užívání by měla být pacientům stabilizovaným léčbou a-blokátory (počáteční nízké dávkování) podána dávka 25 mg sildenafilu a pacient by měl být monitorován a poučen o symptomech a rizicích posturální hypotenze [4].
Opatrnosti je třeba v případě společného užívání s opiáty. Při společném užívání sildenafilu a dihydrokodeinu byly v kazuistikách zaznamenány případy vývoje priapismu [9].
Farmakokinetické interakce
Metabolismus sildenafilu probíhá zejména na CYP 3A4. Na úrovni farmakokinetiky je tedy koncentrace sildenafilu ovlivňována léčivy, která s tímto izoenzymem interferují.
Použití sildenafilu je kontraindikováno při užívání inhibitorů HIV proteáz, jež jsou silnými inhibitory CYP 3A4. Ritonavir (2krát denně 500 mg) zvýšil AUC jednorázově podaného sildenafilu (100 mg) o 1000 % a cmax o 300 %. Ne u všech inhibitorů HIV proteázy je tato interakce vyjádřena jako u ritonaviru, přesto je užití sildenafilu s inhibitory HIV proteázy kontraindikováno [4].
Dále je třeba mít na paměti, že hladiny sildenafilu mohou zvyšovat další silné inhibitory CYP 3A4, jako jsou ketokonazol, intrakonazol, klarithromycin, erythromycin a v menší míře i grapefruit, grapefruitový džus či pomelo. Společné užití sildenafilu a těchto látek je možné. Mělo by se však začít dávkami 25 mg sildenafilu a pacienta monitorovat a poučit jej, aby v případě výskytu symptomů předávkování (bolest hlavy, poruchy vidění, hypotenze, gastrointestinální obtíže, priapismus) přestal sildenafil užívat a vyhledal lékaře. Grapefruitu a pomelu by se měli pacienti vyhnout [4].
Ve farmakokinetických studiích nebyl prokázán účinek na farmakokinetiku sildenafilu, pokud byl společně podáván s inhibitory CYP 2C9 (warfarin, fenytoin) anebo s induktory cytochromu P-450 (rifampicin, barbituráty) [4].
Ovlivnění pozornosti
U mužů, kteří tyto léky užívají poprvé, je vhodné upozornění, aby po prvním užití léku neřídili motorová vozidla [4].
Dávkování
Výrobci doporučují začínat léčbu podáním střední dávky léku. Oproti tomu někteří lékaři, zabývající se prakticky sexuální medicínou, doporučují začít terapii maximální dávkou při prvním podání. Teprve dostaví-li se dobrý efekt, považují za vhodné dávku redukovat. Důvodem pro tento postup je nejvýraznější obava ze selhání právě při prvním podání léku, a pokud je styk po prvním podání úspěšný, není již vyšší dávka nutná. Pokud léčba PDE5i začíná nižší dávkou a při prvním podání dojde k selhání při styku, dojde také ke zvýšení obavy ze selhání a vyšší dávka PDE5i je méně efektivní.
Balení
Sildenafil je k dispozici v dávkování 25 mg, 50 mg a 100 mg v jedné tabletě [4].
Práce byla podpořena výzkumným projektem Univerzity Karlovy SVV 263 005.Seznam použité literatury
- [1] Mikroverze AISLP – ČR. Verze 2011.2 pro MS Windows.
- [2] Kukreja RC, Salloum F, Das A, et al. Pharmacological preconditioning with sildenafil: Basic mechanisms and clinical implications. Vascul Pharmacol 2005; 42: 219–232.
- [3] Corbin JD. Mechanisms of action of PDE5 inhibition in erectile dysfunction. Int J Impot Res 2004; 16 Suppl 1: S4–7.
- [4] Product Information: VIAGRA oral tablets, sildenafil citrate oral tablets. Pfizer Labs, New York, NY, 2008.
- [5] Nichols DJ, Muirhead GJ, Harness JA. Pharmacokinetics of sildenafil after single oral doses in healthy male subjects: absolute bioavailability, food effects and dose proportionality. Br J Clin Pharmacol 2002; 53 Suppl 1: 5S–12S.
- [6] Jackson G, Rosen RC, Kloner RA, Kostis JB. The second Princeton consensus on sexual dysfunction and cardiac risk: new guidelines for sexual medicine. J Sex Med 2006; 3: 28–36; discussion 36.
- [7] Braun M, Wassmer G, Klotz T, et al. Epidemiology of erectile dysfunction: results of the 'Cologne Male Survey'. Int J Impot Res 2000; 12: 305–311.
- [8] Giuliano F, Jackson G, Montorsi F, et al. Safety of sildenafil citrate: review of 67 double-blind placebo-controlled trials and the postmarketing safety database. Int J Clin Pract 2010; 64: 240–255.
- [9] Goldmeier D, Lamba H. Prolonged erections produced by dihydrocodeine and sildenafil. BMJ 2002; 324: 1555.