První výsledky studie PEARL – fremanezumab v reálné klinické praxi
Schválení fremanezumabu pro použití v preventivní terapii pacientů s migrénou předcházelo rozsáhlé klinické hodnocení kontrolované placebem s cílem ověřit účinnost a bezpečnost přípravku. Studie PEARL by měla nyní poskytnout důležité informace o účinnosti léčby v reálném klinickém prostředí, včetně pacientů přecházejících z léčby jinou anti‑CGRP monoklonální protilátkou a hodnocení adherence k léčbě.
Migréna představuje invalidizující onemocnění, které celosvětově sužuje více než miliardu osob [1]. Nemocným významně snižuje kvalitu života a omezuje je v práceschopnosti i ve vykonávání běžných činností. Tradiční, dosud užívaná preventivní léčba migrény byla nespecifická, pro svou nízkou účinnost a často špatnou snášenlivost neuspokojivá a spojená s nízkou adherencí pacientů k léčbě. V posledních několika letech byly pro preventivní terapii pacientů s migrénou schváleny injekčně aplikované monoklonální protilátky proti peptidu CGRP (calcitonine gene‑related peptide), které specificky ovlivňují kaskádu pochodů vedoucích k rozvoji migrény.
Fremanezumab je humanizovaná monoklonální protilátka, která se selektivně váže na ligand CGRP a blokuje jeho vazbu na receptor. Evropská léková agentura schválila fremanezumab pro prevenci migrény u dospělých pacientů s migrénou čtyři a více dní za měsíc (monthly migraine days, MMD ≥ 4) [2]. Fremanezumab se podává subkutánně, s měsíčním nebo čtvrtletním intervalem aplikace.
Prospektivní 24měsíční observační studie PEARL (Pan‑European Real Life) si dala za cíl shromáždit data o léčbě fremanezumabem v klinické praxi. Do tohoto klinického hodnocení fáze IV bylo plánováno zahrnout zhruba 1 100 pacientů s chronickou (CM) nebo epizodickou migrénou (EM) ve stovce léčebných center v 11 zemích Evropy [1].
Metodika studie
Do klinického hodnocení PEARL mohli být zařazeni dospělí pacienti ve věku 18 let a starší s diagnostikovanou CM (≥ 15 dní bolesti hlavy/měsíc po dobu > 3 měsíců, z nichž ≥ 8 splňuje kritéria pro migrénu) nebo s EM (≥ 4 dny s migrénou/měsíc), kterým byl předepsán fremanezumab k subkutánní aplikaci v dávkách 225 mg podávaných měsíčně nebo 675 mg čtvrtletně. Pacientům bylo povoleno nadále užívat akutní nebo jinou preventivní léčbu, která jim byla předepsána před zařazením do studie [1].
Primárním cílovým ukazatelem byl zvolen podíl pacientů, kteří dosáhli snížení průměrného MMD o 50 % a více během šestiměsíčního období od první dávky fremanezumabu. Jako sekundární cílové ukazatele byly určeny změna MMD od výchozí hodnoty, skóre invalidity a průměrného počtu dní za měsíc s užíváním léků na akutní bolest hlavy. Hodnoceny jsou dále adherence k léčbě fremanezumabem během 24měsíčního období sledování a rovněž důvody a výsledky ukončení a opětovného zahájení léčby. Parametry účinnosti jsou sledovány v podskupinách pacientů dle typu migrény (EM/CM) a u nemocných s obtížně léčitelnou migrénou, tj. s dokumentovaným nadužíváním léčby, u velké depresivní poruchy, generalizované úzkostné poruchy nebo s předchozí expozicí jiné monoklonální protilátce cílící na dráhu CGRP [1].
Výsledky hodnocení
Klinické hodnocení PEARL dosud probíhá, předpokládá se, že poslední pacient dokončí studii během prvního čtvrtletí roku 2024. K dispozici jsou aktuálně výsledky interim analýz.
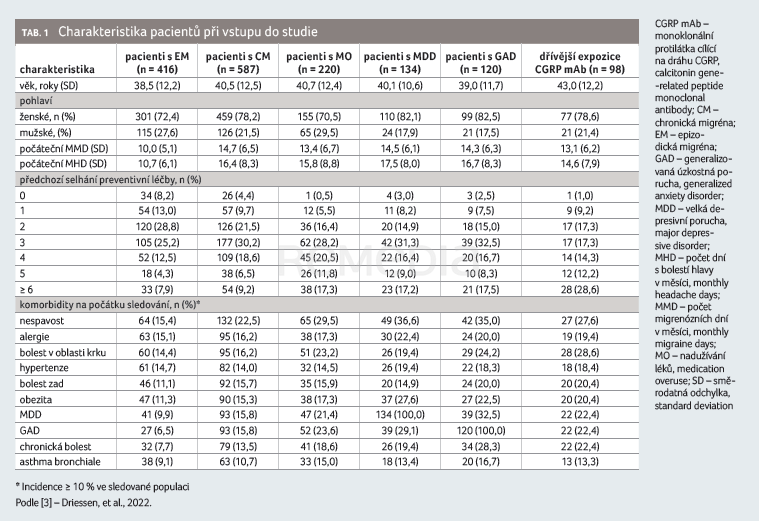
Do hodnocení bylo zahrnuto 1 003 pacientů, z nichž 416 (41,5 %) trpělo EM a 587 (58,5 %) CM. U 220 (21,9 %) nemocných bylo dokumentováno nadužívání medikace, u 134 (13,4 %) velká depresivní porucha, u 120 (12,0 %) generalizovaná úzkostná porucha a 98 (9,8 %) pacientů dříve užívalo jinou anti‑CGRP monoklonální protilátku. Fremanezumab byl aplikován v měsíčním intervalu 622 (62,0 %) pacientům a čtvrtletně 381 (38,0 %) pacientům. Charakteristiku pacientů zařazených do studie blíže popisuje tabulka 1 [3].
Adherence pacientů k léčbě fremanezumabem byla ve všech podskupinách vysoká. Více než 85 % pacientů pokračovalo v dávkovacím režimu, který započali (měsíční nebo čtvrtletní interval aplikace).
Změnu MMD přehledně uvádí graf 1. U pacientů s EM (n = 416) byl na počátku průměrný MMD 10,0, v měsíci 1 byl zaznamenán pokles MMD −3,4 (34,0 %), v měsíci 3 činil pokles −4,7 (47,0 %) a v měsíci 6 byl −7,7 (77,0 %). Podíl pacientů s ≥ 50% redukcí MMD vzrostl z 31,6 % (31/97) v měsíci 1 přes 52,1 % (49/94) v měsíci 3 až na 75,8 % (25/33) v měsíci 6 [3].
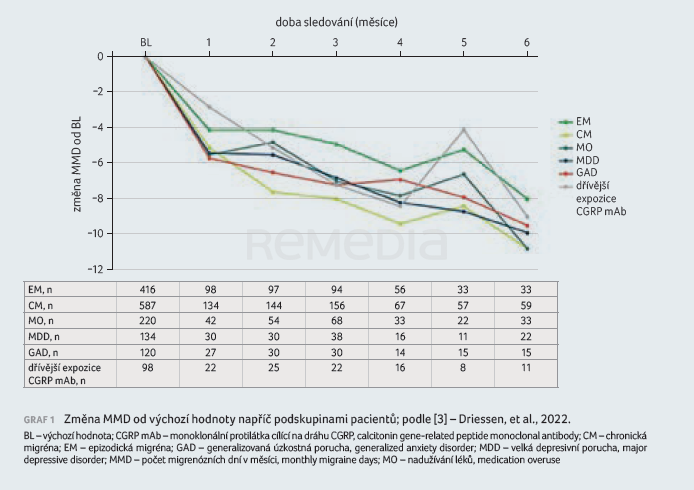
Ve skupině pacientů s CM (n = 587) byl na počátku průměrný MMD 14,7. Od počátku sledování došlo k poklesu MMD o 5,5 (38,4 %) v měsíci 1, o 7,9 (53,7 %) v měsíci 3 a o 10,1 (68,7 %) v měsíci 6. Podíl pacientů s ≥ 50% redukcí MMD vzrostl z 32,1 % (43/134) v měsíci 1 přes 58,3 % (91/156) v měsíci 3 až na 76,3 % (45/59) v měsíci 6 [3].
Ve skupině pacientů s dokumentovaným nadužíváním medikace (n = 220) byl na počátku sledování průměrný MMD 13,4. V průběhu sledování došlo ke snížení MMD o 5,5 (41,0 %) v měsíci 1, o 7,0 (52,2 %) v měsíci 3 až k poklesu o 10,9 (80,6 %) v měsíci 6. Podíl pacientů s ≥ 50% redukcí MMD vzrostl z 33,3 % (14/42) v měsíci 1 přes 48,5 % (33/68) v měsíci 3 až na 78,8 % (26/33) v měsíci 6 [3].
Ve skupině pacientů s velkou depresivní poruchou (n = 134) činil na počátku sledování průměrný MMD 14,5. V měsíci 1 došlo k redukci MMD o 5,4 (37,2 %), v měsíci 3 o 6,8 (46,9 %) a v měsíci 6 o 9,9 (68,3 %). Podíl pacientů s ≥ 50% redukcí MMD zde od měsíce 1 k měsíci 6 opět vzrůstal; z 36,7 % (11/30) přes 44,7 % (17/38) až na 81,8 % (18/22). Zmírnění závažnosti velké depresivní poruchy bylo zaznamenáno u 45,5 % (61/134) pacientů [3].
Ve skupině pacientů s generalizovanou úzkostnou poruchou (n = 120) byl na počátku sledování průměrný MMD 14,3. V měsíci 1 došlo ke snížení o 5,7 (39,9 %), v měsíci 3 o 7,2 (50,3 %) a v měsíci 6 o 9,5 (66,4 %). Podíl pacientů, u nichž došlo k ≥ 50% redukci MMD, vzrostl z 37,0 % (10/27) v měsíci 1 přes 53,3 % (16/30) v měsíci 3 až na 80,0 % (12/15) v měsíci 6. Závažnost generalizované úzkostné poruchy se zmírnila u 45,8 % (55/120) sledovaných [3].
Z pacientů s předchozí expozicí jiné monoklonální protilátce cílící na dráhu CGRP (n = 98) jich 93,9 % poskytlo důvod pro přechod na léčbu fremanezumabem. Nejčastěji se jednalo o nedostatečnou odpověď na léčbu (67,4 %) nebo nežádoucí účinky (32,6 %). V této podskupině pacientů činil průměrný MMD na počátku sledování 13,1 a došlo k jeho postupné redukci o 2,8 (21,4 %) v měsíci 1, o 7,2 (55,0 %) v měsíci 3 a o 9,0 (68,7 %) v měsíci 6. Stejně jako v ostatních podskupinách bylo i zde zaznamenáno zvýšení podílu pacientů s ≥ 50% redukcí MMD; 9,1 % (2/22) v měsíci 1, 45,5 % (10/22) v měsíci 3 a 63,6 % (7/11) v měsíci 6 [3].
Studie PEARL z reálné klinické praxe potvrdila výbornou účinnost léčby, doložila výraznější redukci MMD oproti klinickým studiím fáze III. Ve studii PEARL se změna MMD u pacientů s EM a CM pohybovala v průběhu prvních tří měsíců terapie od −4,7 až po −7,9, v klinickém hodnocení fáze II od −3,4 po −5,0 [4−6].
Shrnutí
Fremanezumab v této studii z reálného klinického prostředí demonstroval účinnost bez ohledu na typ migrény nebo přítomnost faktorů přispívajících k obtížně léčitelné migréně. Deprese a anxieta jsou běžnými komorbiditami pacientů s migrénou a jejich ovlivnění je proto velmi žádoucí. Byla pozorována setrvalá redukce MMD s konzistentními výsledky napříč podskupinami pacientů, s pokračujícím zlepšením v průběhu šesti měsíců léčby.
Druhá interim analýza
Na začátku září byly na Mezinárodním sympoziu Migraine Trust (MTIS) v Londýně představeny výsledky druhé interim analýzy studie PEARL [7], které dokládají setrvalou účinnost fremanezumabu v redukci MMD. Tato průběžná analýza studie PEARL demonstrovala, že u více než poloviny pacientů (56 %) s EM nebo CM zahrnutých do studie se během šestiměsíční léčby fremanezumabem MMD snížil o 50 % nebo více. Průměrná změna MMD byla v 6. měsíci −8, v 9. měsíci −8,5 a ve 12. měsíci −8,3.
Odraz výsledků studií v doporučených postupech
Závěry recentních klinických hodnocení (real world evidence) s anti‑CGRP monoklonálními protilátkami ukazují na výborné výsledky této terapie i mimo prostředí randomizovaných klinických studií. Nově byly také zohledněny v aktualizaci doporučených postupů Evropské federace pro bolesti hlavy (European Headache Federation, EHF) pro preventivní léčbu migrény. Profil účinnosti, bezpečnosti a snášenlivosti byl zhodnocen jako výborný, s absencí problematické adherence pacientů k léčbě. Experti v doporučení nevidí důvod pro odklad této léčby. Doporučení EHF proto nově navrhují zařazení anti‑CGRP monoklonálních protilátek již do první linie léčby oproti dřívější třetí linii a podporují také delší trvání terapie. Doposud bylo doporučeno její trvání v délce 6−12 měsíců s následnou pauzou, nově je doporučeno zvážit pauzu až po 12−18 měsících léčby s tím, že terapie by měla pokračovat tak dlouho, jak je potřeba [8,9].
Literatura
[1] Ashina M, Amin FM, Kokturk, et al. PEARL study protocol: a real‑world study of fremanezumab effectiveness in patients with chronic or episodic migraine. Pain Manag 2021; 11: 647‑654.
[2] Souhrn údajů o přípravku Ajovy. Dostupné na https://www.sukl.cz
[3] Driessen MT, Cohen JM, Thompson SF, et al. Real‑world effectiveness after initiating fremanezumab treatment in US patients with episodic and chronic migraine or difficult‑to‑treat migraine. J Headache Pain 2022; 23: 56.
[4] Silberstein SD, Dodick DW, Bigal ME, et al. Fremanezumab for the preventive treatment of chronic migraine. N Engl J Med 2017; 377: 2113–2122.
[5] Dodick DW, Silberstein SD, Bigal ME, et al. Effect of fremanezumab compared with placebo for prevention of episodic migraine: a randomized clinical trial. JAMA 2018; 319: 1999–2008.
[6] Ferrari MD, Diener HC, Ning X, et al. Fremanezumab versus placebo for migraine prevention in patients with documented failure to up to four migraine preventive medication classes (FOCUS): a randomised, double‑blind, placebo‑controlled, phase 3b trial. Lancet 2019; 394: 1030–1040.
[7] Ashina M, et al. Effectiveness of Fremanezumab for the Preventive Treatment of Migraine: Second Interim Analysis of the Observational PEARL Study. Presented at the Migraine Trust International Symposium (MTIS); 8‑11 September 2022, London. MTIS‑PO‑054.
[8] Sacco S, Amin FM, Ashina M, et al. European Headache Federation guideline on the use of monoclonal antibodies targeting the calcitonin gene related peptide pathway for migraine prevention – 2022 update. J Headache Pain 2022; 23: 67.
[9] Tisková zpráva z 8. 9. 2022. Teva announces new positive AJOVY® (fremanezumab) real world data from its migraine prevention study, PEARL and welcomes updated European Headache Federation guidelines on the use of CGRP mAbs. Dostupné na: https://www.pharmiweb.com