Acidum valproicum/natrii valproas
Kyselina valproová a její sodná sůl jsou látky se širokým antikonvulzivním spektrem účinku zahrnujícím parciální a generalizované epileptické záchvaty i některé speciální epileptické syndromy. Tato látka je též schválena k léčbě manických fází u bipolární deprese a k prevenci záchvatů migrény. Na široké terapeutické aktivitě valproatu se podílí více mechanismů, které působí na úrovni neurotransmiterů, jejich druhých poslů i transkripčních faktorů a genové exprese. Kyselina valproová/valproat sodný se rychle vstřebává, prodělává značný jaterní metabolismus, váže se poměrně ve vysokém procentu na plazmatické bílkoviny. Eliminace probíhá ledvinami, biologický poločas se pohybuje v rozmezí 8–20 hodin. Komplikací během léčby může být hepatotoxické a teratogenní působení. Kyselina valproová neindukuje aktivitu jaterních enzymů. Dávkování je přísně individuální, obvykle se pohybuje mezi 20–30 mg/kg/den.
Farmakologická skupina
Antiepileptikum se širokým spektrem účinku.
Chemické a fyzikální vlastnosti
Kyselina valproová je chemicky 2-propylpentanová kyselina (obr. 1).
Sumární vzorec:
kyselina valproová: C8H16O2
natrium valproat: C8H15NaO2
Molekulová hmotnost:
kyselina valproová: 144,21
natrium valproat: 166,20
Přibližně 0,868 mg kyseliny valproové odpovídá 1,000 mg natrium valproatu.
Kyselina valproová je bezbarvá nebo velmi slabě žlutá čirá kapalina, mírně viskózní, velmi těžce rozpustná ve vodě, mísitelná s ethanolem nebo s dichlormethanem. Rozpouští se ve zředěných roztocích alkalických hydroxidů.
Natrium valproat je bílý nebo téměř bílý krystalický hygroskopický prášek velmi snadno rozpustný ve vodě a snadno rozpustný v ethanolu.
Farmakodynamické vlastnosti
Valproat sodný i kyselina valproová v plazmě disociují, proto jsou v článku označeny souhrnně jako valproat (VPA).
Molekulární mechanismy účinku
Na široké terapeutické aktivitě valproatu se podílí více mechanismů, které působí na úrovni neurotransmiterů, jejich druhých poslů i transkripčních faktorů a genové exprese.
Neurotransmitery
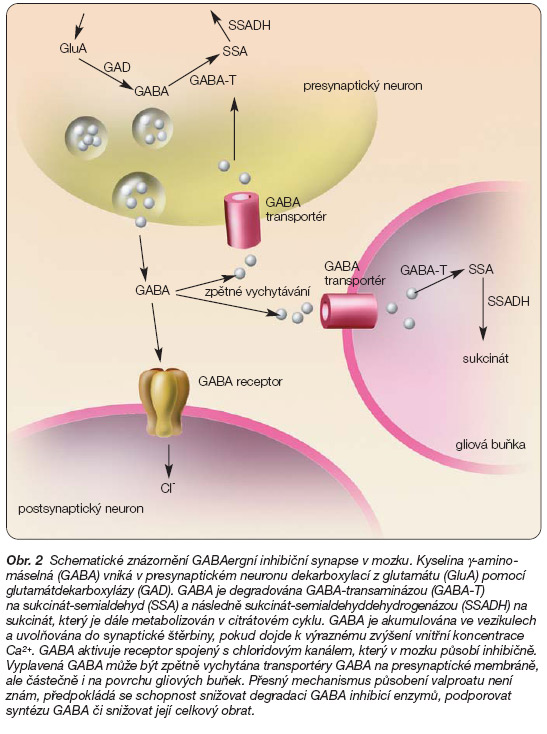
Valproat zvyšuje aktivitu hlavního inhibičního neurotransmiteru, g-aminomáselné kyseliny (GABA) – obr. 2. Tato změna přitom u zvířat časově odpovídá antikonvulzivnímu účinku.
Přesný mechanismus tohoto zvýšení i jeho fyziologický význam však zůstávají nejasné. Existují nejméně 3 hlavní mechanismy, kterými může valproat zvyšovat koncentraci GABA [1]:
1. ‑snížením degradace GABA, a to inhibicí klíčových enzymů metabolismu GABA;
2. ‑zvýšenou syntézou GABA, možné mechanismy zahrnují zvýšení aktivity syntetizujícího enzymu a zvýšení dostupnosti substrátu pro syntézu GABA, a to hlavně v substantia nigra, v oblasti s největší mírou syntézy GABA v mozku;
3. ‑celkovým snížením obratu GABA.
Valproat také snižuje glutamátergní neurotransmisi supresí N-methyl-D-aspartátové receptorem řízené excitace a zvýšením koncentrace dopaminu a serotoninu, ale vztah změn těchto neurotransmiterů k terapeutickému působení valproatu není objasněn [2].
Přenos signálu, druzí poslové
Na molekulární úrovni valproat zasahuje druhé posly, na několika místech ovlivňuje například inositolovou dráhu, protein- kinázu C (PKC), MAP kinázovou signální kaskádu, cAMP (respondse element binding protein)b a glykogen syntázkinázu 3b (GSK-3b). GSK-3b facilituje neuronální apoptózu, a proto valproat působí inhibicí GSK-3b neuroprotektivně [3, 4].
Transkripční faktory, genová exprese
Valproat ovlivňuje také transkripční faktory a expresi genů, jde například o neuroprotektivní gen bcl-2 [5] a rodinu transkripčních faktorů AP-1 (obsahuje geny pro neuropeptidy, neurotrofiny, receptory, transkripční faktory a proteiny cytoskeletu, jako je např. c-fos a c-jun).
Blokáda kanálů
Valproat způsobuje blokádu napěťově řízených kalciových a sodíkových kanálů. Tento mechanismus účinku má vztah k antiepileptické aktivitě valproatu a v případě sodíkových kanálů zřejmě také k jeho tymostabilizačnímu, analgetickému a neuroprotektivnímu působení [6]. Na sodíkových kanálech působí také lamotrigin, ale odlišným způsobem, a to spolu s dalšími rozdíly v jejich mechanismech účinku může vysvětlovat rozdíly v terapeutickém profilu těchto léků.
Antiepileptický účinek
Antiepileptický účinek valproatu je založen na zvýšení aktivity celého GABAergního systému. Tímto způsobem dochází ke snížení excitability neuronů a snížení rizika vzniku epileptického záchvatu. Efekt je navíc zesílen snížením neuronálních hladin glutamátu up-regulací gliových glutamát-aspartátových transportérů [7].
Antiepileptické vlastnosti jsou dále potencovány působením na iontové proudy a kanály. Valproat přímo působí na sodíkové neuronální kanály a zpomaluje jejich reaktivaci. Pohyb vápníkových iontů je zřejmě ovlivňován sekundárně inhibicí N-methyl-D-aspartátových receptorů [8].
Shank a kol. prokázali, že na antiepileptickém účinku valproatu se podílí i nor-adrenalin [9]. Svoji hypotézu ověřili při akutním i chronickém podání valproatu u záchvatů vyvolaných fluorothylem na myších s deficitem dopamin b-hydroxylázy.
Hodnota plazmatické koncentrace valproatu, která je u epilepsií považována za terapeutickou, se pohybuje v rozmezí 60–100 mg/ml [10].
Antimigrenózní účinek
Působení kyseliny valproové na sodíkové a neuronální vápníkové kanály může mít vliv na cerebrální aktivaci, která se objevuje v časných fázích migrény. Na zvířecích modelech migrény byla prokázána schopnost valproatu ovlivňovat přes GABAA-receptory procesy neurogenního zánětu a snižovat extravazaci plazmatických proteinů a c-fos imunoreaktivitu v trigeminálním nucleus caudalis. Tento mechanismus může být důležitý pro zabránění vzniku záchvatu migrény. Působením na mozkové cévy blokuje rozvoj neurologicky podmíněného sterilního zánětu, který následuje po vazodilataci zprostředkované serotoninem. Inhibiční efekt valproatu na senzitizaci u perzistující migrenózní bolesti je důležitý v prevenci krátko- i dlouhodobých vlivů migrény na nucleus caudalis.
Efektivní terapeutické dávky valproatu v indikaci u migrény se pohybují mezi 400–1000 mg/den a plazmatické hladiny v rozmezí 50–100 mg/ml [11].
Antipsychotický a náladu stabilizující účinek
Zesílení GABAergní aktivity a vliv valproatu na iontové kanály [8] nemá pouze antiepileptický, ale i náladu stabilizující efekt. GABA může regulovat aktivitu mezolimbické dopaminergní dráhy, což se může projevit jako antipsychotický účinek. Snížená hladina GABA je pozorována například u schizofrenních pacientů [12]. Zvýšené uvolňování dopaminu v prefrontální kortikální oblasti po podání valproatu bylo prokázáno v pokusu na potkanech [13].
Na stabilizaci nálady působí zřejmě vliv valproatu na kortikotropin uvolňující faktor (CRF) [14].
Antineoplastický účinek
Antiproliferativní účinek valproatu byl zjištěn náhodně při studiu teratogenních účinků valproatu na modelu neoplasticky transformovaných neuroektodermálních buňek, když bylo zjištěno zpomalení růstu buněk v kultuře [10]. Kyselina valproová působí též jako inhibitor histon-de-acetylázy [15]. Obecně lze říct, že acetylace histonů vede ke zvýšení transkripce genů a deacetylace má účinek opačný.
Neuroprotektivní vlastnosti
Kromě výše popsaných biologických efektů lze po podání valproatu pozorovat i neuroprotektivní účinek. Projevuje se například zvýšením hladiny glutamát vázajícího proteinu po náhlém uvolnění glutamátu u epilepsií. Tímto způsobem může valproat snižovat excitotoxické neuronální poškození u epilepsií, při poraněních hlavy a u hypoxicko-ischemické encefalopatie [16]. Snížení metabolismu glukózy a průtoku krve v mozku [10] může mít také neuroprotektivní efekt u ischemických stavů. Ve studii na myších kortikálních neuronech bylo v kultuře pozorováno po přidání valproatu v koncentraci 0,5 mmol/l prodloužení délky života buněk. Dále byl zjištěn i protektivní efekt proti stářím vyvolané spontánní buněčné smrti. Výše uvedené efekty zřejmě souvisejí s blokem histon-deacetylázy a markantním zvýšením v acetylaci histonu H3 [17].
Léčba kyselinou valproovou je však zřejmě provázena oxidačním stresem. Jak bylo dokázáno na potkanech, valproat v dávce 500 mg/kg zvyšoval plazmatické hladiny 15-F2t-izoprostanu, který slouží jako marker lipidové peroxidace. Podle Tonga je lipoperoxidace spojena s glukuronidizací valproatu při jeho biotransformaci a lze jí zabránit borneolem jako inhibitorem glukuronidizace [18].
Farmakokinetické vlastnosti
Valproat se dobře vstřebává po perorální aplikaci, eliminační poločas je krátký, okolo 15 hodin, proto musí být podáván ve 2–3 denních dávkách. Celková denní dávka valproatu se pohybuje mezi 750–1250 mg [19]. Terapeutické plazmatické hladiny jsou v rozmezí 50–100 mg/ml. Dosažení ustálených plazmatických koncentrací valproatu nastává v průběhu 3–5 dní od zahájení léčby [20].
Absorpce
Biologická dostupnost valproatu po perorálním podání se pohybuje mezi 90–100 % (tab. 1) [20]. Rychlost absorpce závisí na použité lékové formě a přítomnosti potravy. Specifická léková forma může upravovat rychlost absorpce iontů valproatu a tyto rozdíly nemohou podstatně ovlivnit rozsah absorpce. Porovnání různých forem pro perorální podání ukázalo prodloužení časového intervalu od podání po dosažení cmax. Při podání valproatu ve formě sirupu dochází k úplné absorpci v rozmezí 15–60 minut, ve formě kapslí v rozmezí 1–3 hodin a ve formě enterosol- ventních kapslí v rozmezí 3–5 hodin [21].
Perorální podání valproatu současně s potravou může způsobit prodloužení dosažení tmax bez vlivu na úplnost absorpce. Vrchol plazmatické koncentrace po požití tablety valproatu s jídlem se pohybuje v rozmezí 3–7,5 hodin [21].
Distribuce
Valproat má vysokou afinitu k plazmatickým bílkovinám, především k albuminu. Navázaná frakce při terapeutických koncentracích představuje přibližně 90 %. Při nízkých dávkách se valproat váže na plazmatické proteiny lineárně, při zvýšení plazmatických koncentrací se podíl vázáné látky snižuje.
Vysoká afinita valproatu k plazmatickým bílkovinám a kompetice o vazebná místa může být podstatou závažných lékových interakcí. Úprava dávkování je potřebná u pacientů se sníženou hladinou plazmatických proteinů (vyšší věk, chronické onemocnění jater, renální insuficience) [22].
Distribuční objem se pohybuje v rozmezí 0,13–0,15 l/kg. Valproat se koncentruje v místech, kde je zvýšený obrat GABA, zejména v séru, játrech, plicích, slezině a kosterním svalstvu [21].
Valproat prostupuje přes hematoencefalickou bariéru. Koncentrace v cerebrospinálním likvoru dosahují 10 % z celkové plazmatické koncentrace.
Metabolismus
Valproat je intenzivně metabolizován játry a patří mezi léčiva s výrazným first pass efektem. Množství netransformovaného léčiva v moči představuje 3 % podané dávky.
Nejčastější metabolickou cestou (50 %) je konjugace s kyselinou glukuronovou, reakce je zprostředkovaná enzymem UDP-glukuronyltransferázou (UDPGT). Přibližně 40 % léčiva je transformováno v mitochondriích b-oxidací za vzniku 2-en metabolitu valproatu. Další méně významné metabolické cesty představuje b-oxidace a oxidace systémem cytochromu P-450. Některé z takto vzniklých metabolitů jsou hepatotoxické, ale jejich plazmatické hladiny jsou velmi nízké [7, 20].
V lidské krvi a moči bylo identifikováno více než 10 metabolitů valproatu, z nichž pouze 2-en byl detekován v mozku v koncentraci 1,3krát vyšší, než byla koncentrace valproatu. Jako jediný z metabolitů přispívá 2-en valproat k antikonvulzivnímu účinku.
Eliminace
Eliminace metabolitů valproatu probíhá exkrecí do moče (70–80 %) a do stolice. Procentuální zastoupení metabolitů v moči je: glukuronid 20 %, 3-oxovalproat 3–60 %, netransformované léčivo 1–3 %. Přibližně 7 % z podané dávky prodělává enterohepatální cyklus.
Biologický poločas valproatu je 8–20 hodin. Horní hranici se blíží starší pacienti, pacienti s cirhózou jater a novorozenci. Rozdíl mezi biologickým poločasem valproatu u chronického a akutního podání nebyl pozorován. Při kombinaci valproatu s jinými antikonvulzivy se může biologický poločas snižovat na 8–9 hodin [21].
Celková systémová clearance valproatu je 0,11 ml/min/kg. U pacientů s onemocněním jater je clearance redukována a je potřeba upravit dávkování.
Klinické zkušenosti
Epilepsie
Parciální záchvaty (simplexní i sekundárně generalizované) a primárně generalizované tonicko-klonické záchvaty
Množství klinických studií porovnávalo monoterapii valproatem s ostatními antiepileptiky.
Turnbull a kol. v roce 1985 jako první porovnávali účinnost phenytoinu a valproatu jako iniciální terapie u 140 pacientů po prvním epileptickém záchvatu. Mezi oběma léky nebyly nalezeny významné rozdíly [24]. Účinnost monoterapie valproatem zkoumala též studie sponzorovaná UK Medical Research Council na počátku 90. let. V této studii bylo 243 pacientů randomizováno do skupin léčených valproatem, carbamazepinem, phenytoinem nebo phenobarbitalem a léčeno po dobu 3 let. Mezi látkami nebyly prokázány rozdíly v účinnosti, avšak bezpečnostní profil byl nejlepší u phenytoinu a valproatu [25]. Systematické review 5 klinických studií s 669 pacienty potvrdilo předchozí výsledky klinických studií a nenašlo rozdíly v terapeutické účinnosti phenytoinu a valproatu [26].
Další studie srovnávaly účinnost valproatu a carbamazepinu. Ve studii EPITEG bylo hodnoceno 300 dospělých pacientů s nově diagnostikovanou epilepsií. Po třech letech studie byly valproat a carbamazepin stejně účinné, nezávisle na tom, zda šlo o parciální záchvaty nebo primárně generalizované tonicko-klonické záchvaty. Vyšší počet nežádoucích účinků (hlavně kožní vyrážky) byl pozorován ve skupině léčené carbamazepinem [27]. Do designem stejné studie u dětí bylo zahrnuto 260 dětí, rozdíl v léčbě carbamazepinem a valproatem nebyl statisticky signifikantní. Třetí velkou studií zkoumající rozdíly v léčbě mezi valproatem a carbamazepinem byla studie vedená Mattsonem a kol. [28]. Oproti předchozí studii EPITEG bylo do studie zařazeno 480 pacientů (97 % mužů) začínajících s léčbou i již suboptimálně léčených. Dávky valproatu po 24 měsících byly dvojnásobné (2099 mg/den) oproti studii EPITEG (924 mg/den). Valproat byl v této studii stejně účinný jako carbamazepin v kontrole generalizovaných tonicko-klonických záchvatů, carbamazepin lépe kontroloval parciální záchvaty. Závěry studie (lepší kontrola carbamazepinem) byly některými autory zpochybněny kvůli vysokému procentu pacientů, kteří předčasně ukončili studii, vysokým (až téměř toxickým) plazmatickým hladinám valproatu a kvůli arbitrárně vytvořeným skupinám pacientů. Autoři systematického review srovnávající data 1265 pacientů též nenalezli rozdíl v účinnosti valproatu a carbamazepinu v monoterapii epilepsie [29].
Informace o účinnosti valproatu ve srovnání s novými antiepileptiky nejsou stále dostatečné. Ve studii Whelesse a kol. byl u 119 dětí ve věku 6–16 let s nově diagnostikovanou epilepsií srovnáván topiramat, carbamazepin a valproat. Nebyly pozorovány rozdíly mezi léčivy v žádném ze sledovaných parametrů (čas do prvního záchvatu, čas ukončení terapie, procento dětí bez záchvatu v posledních 6 měsících před ukončením studie) [30].
Jiné generalizované záchvaty
Carbamazepin, phenytoin, vigabatrin a tiagabin by měly být používány u generalizovaných forem epilepsie s opatrností, protože tyto látky mají potenciál přivodit či zesílit myoklonické záškuby a záchvaty absencí. Valproat je naopak ve většině případů lékem volby. Např. studie s ethosuximidem ukázaly podobný a vysoký účinek na juvenilní absence – snižovaly jejich počet o 80 % [31]. U systematického review srovnávajícího účinnost valproatu, ethosuximidu a lamotriginu u záchvatů absencí nebyla provedena metaanalýza z důvodu malého a nestejnorodého počtu studií, avšak autoři uvádějí, že v těchto studiích nebyl mezi těmito léky zaznamenán rozdíl [32]. Valproat byl účinný v léčbě status epilepticus, údaje z randomizovaných klinických studií jsou však minimální [33].
Bipolární afektivní porucha
Manická fáze
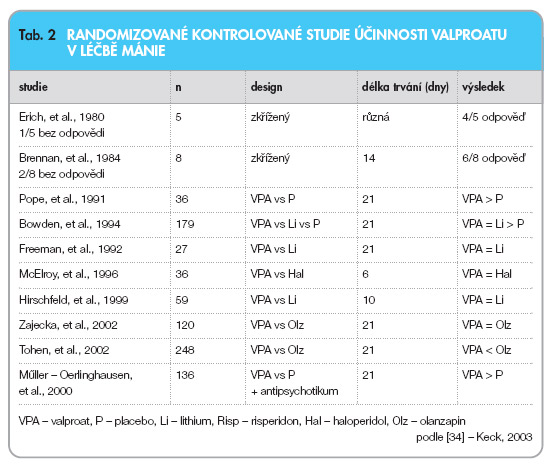
Valproat byl v léčbě mánie studován v několika randomizovaných kontrolovaných studiích (viz tab. 2) [34]. Valproat byl lepší než placebo v monoterapii i v kombinaci s typickým antipsychotikem a srovnatelný v účinnosti s lithiem, haloperidolem a olanzapinem. V dalším klinickém srovnání s olanzapinem však pacienti léčení olanzapinem dosáhli signifikantně většího snížení celkového skóre v Young Mania Rating Scale (YRMS) a častějších odpovědí ve srovnání s pacienty léčenými valproatem.
Charakteristiky spojené s responzivitou na valproat
Relativně lepší odpověď na valproat je podle sekundárních analýz studie Bowdena a kol. [35] ve srovnání s jinými stabilizátory nálady spojena s určitými klinickými charakteristikami pacientů. Mezi tyto charakteristiky patří:
1. smíšená mánie
2. ‑non-responzivita na lithium
3. ‑vysoký počet afektivních fází (více než 10 epizod) nebo více než 2 depresivní epizody
4. ‑neurologické abnormality a mentální retardace.
I podle výsledků dalších studií na valproat dobře odpovídá mánie s iritabilitou a hyperaktivitou. Iritabilita také nejvíce odlišuje pacienty s dobrou odpovědí na valproat v rámci jiných diagnóz, než je bipolární afektivní porucha (poruchy osobnosti a schizofrenie).
Výsledky otevřených studií ukazují, že na valproat lépe odpovídají pacienti s atypickými mániemi, např. spojenými s neurologickými obtížemi a abúzem psychoaktivních látek. Obdobné randomizované dvojitě slepé studie nebyly provedeny.
Augmentace a kombinovaná léčba
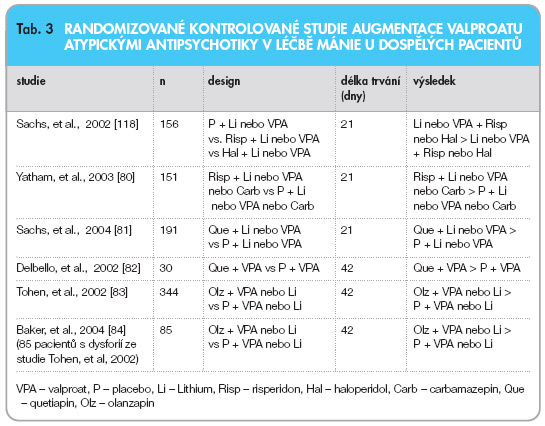
Kazuistiky, série kazuistických případů a výsledky randomizovaných, kontrolovaných studií ukazují, že antimanický účinek valproatu může být augmentován lithiem, carbamazepinem a atypickými antipsychotiky – clozapinem, risperidonem, olanzapinem a quetiapinem [34]. Klinické studie z poslední doby ukazují, že augmentace stabilizátorů nálady atypickými antipsychotiky, jako je risperidon, olanzapin a quetiapin, je účinnějším postupem než monoterapie (viz tab. 3). Podle studie Sachse a kol. [36], která porovnávala účinnost léčby mánie risperidonem nebo haloperidolem v kombinaci s lithiem nebo valproatem, profitovala z kombinované léčby podskupina pacientů, kteří předtím neodpověděli na valproat nebo lithium. Skupina pacientů s kombinovanou léčbou zahájenou najednou z ní neměla prospěch. Podle této studie je kombinovaná terapie vhodná pro pacienty, u kterých nedošlo k odpovědi po relativně krátké době adekvátní léčby prvním lékem.
Studie zaměřené na účinek valproatu po přidání k atypickému antipsychotiku nebyly publikovány.
Depresivní fáze
Výsledky většiny studií ukazují, že valproat je méně účinný v léčbě akutních depresivních epizod než v léčbě manických a smíšených epizod [34, 37].
Udržovací a profylaktická léčba
Udržovací léčba valproatem byla studována v jedné placebem kontrolované dvojitě slepé studii, v jedné randomizované otevřené srovnávací studii s lithiem a ve dvou naturalistických srovnáních s lithiem.
V placebem kontrolované studii nebyl nalezen signifikantní rozdíl v době do relapsu jakékoli epizody bipolární poruchy mezi 372 pacienty léčenými divalproexem, lithiem a placebem, i když lepšího trendu bylo dosaženo v léčbě divalproexem ve srovnání s lithiem [38]. Předčasné přerušení léčby z důvodu intolerance nebo vedlejších účinků bylo nižší u pacientů léčených valproatem proti pacientům léčeným lithiem (22 % vs 35 %, p < 0,03). Vyšší účinnost valproatu oproti placebu byla nalezena u podsouboru 149 pacientů, kteří byli léčeni VPA z důvodu manické epizody v průběhu otevřené fáze studie.
V 18měsíční otevřené randomizované studii byl zjištěn o 20 % nižší počet relapsů epizod bipolární poruchy u pacientů léčených valproatem proti pacientům léčeným lithiem [39].
Dlouhodobá naturalistická studie 38 pacientů s bipolární poruchou léčených lithiem nebo valproatem ukázala stejnou účinnost a toleranci valproatu jako lithia [40]. Pacienti, kteří neodpovídali na léčbu lithiem, odpověděli dobře na terapii valproatem (50 %), a naopak nemocní, kteří se bez úspěchu léčili valproatem, odpověděli dobře na terapii lithiem (44 %).
V druhé naturalistické studii bylo 201 pacientů s bipolární poruchou typu I v manické nebo smíšené fázi randomizováno k valproatu nebo lithiu a sledováno 1 rok [41]. Pacienti léčení valproatem ukončovali studii méně často kvůli nedostatečnému účinku nebo pro nežádoucí účinky (12 %) oproti pacientům léčeným lithiem (23 %). Pacienti, kteří pokračovali v léčbě stabilizátory nálady, měli po 3 měsících lepší zdravotní stav a podstatně nižší finanční náklady na léčbu.
Účinek valproatu v dlouhodobé léčbě bipolární afektivní poruchy tedy není klinickými studiemi jednoznačně potvrzen.
Rychlé střídání epizod
Léčba pacientů s rychlým střídáním epizod (cyklováním) je obtížná, tito pacienti méně odpovídají na farmakologickou léčbu než pacienti s bipolární poruchou bez rychlého cyklování epizod.
Valproat je ve stabilizaci nálady účinnější u těch pacientů, u kterých byla léčba zahájena v manické nebo smíšené fázi.
Otevřená studie 55 pacientů s rychlým cyklováním [42] popisuje značnou účinnost valproatu v monoterapii u 89 % pacientů, kteří léčbu započali v manické fázi, a to v akutní léčbě i profylaxi. Pacienti s rychlým cyklováním, kteří léčbu začali v depresivní fázi, měli míru akutní odpovědi 57 % a míru profylaktické odpovědi 65 %.
Během otevřené stabilizační fáze studie pacientů s rychlým cyklováním bylo při porovnávání léčby lithiem nebo valproatem potvrzeno, že stabilizace nálady oběma léky byla úspěšná především u pacientů, kteří měli na začátku studie manickou nebo smíšenou epizodu (24 % nemocných), na rozdíl od pacientů s přítomnou refrakterní depresí na začátku studie (76 % nemocných) [43].
Nedávná 20měsíční dvojitě slepá studie udržovací léčby porovnávala tymostabilizační účinnost VPA a lithia při léčbě rychlého cyklování u 254 pacientů, kteří v akutní mánii nebo hypomanii dobře odpověděli na kombinovanou léčbu valproatem a lithiem. Vyšší účinnost valproatu oproti lithiu se nepodařilo prokázat [44]. Problémem při léčbě rychlého cyklování se ve shodě s výše uvedenou studií ukázala vysoce rekurentní refrakterní deprese.
Kombinovaná udržovací léčba
Pilotní studie porovnávala účinnost kombinace lithia a valproatu oproti monoterapii lithiem u 12 pacientů s bipolární afektivní poruchou typu I [45]. Ve skupině léčené kombinací lithia a valproatu (n = 5) nedošlo během jednoročního prospektivního sledování k žádnému relapsu oproti 71 % relapsů ve skupině léčené kombinací lithia a placeba (n = 7; p = 0,014). Vedlejší nežádoucí účinky se vyskytovaly dvakrát častěji při kombinované léčbě, která byla také spojena s vyšší mírou odstoupení ze studie.
Druhá, větší studie zjistila, že podávání olanzapinu s valproatem nebo olanzapinu s lithiem po dobu 18 měsíců 99 pacientům, kteří v akutní fázi dobře odpověděli na kombinaci olanzapinu se stabilizátorem nálady a pak byli znovu randomizováni, je účinnější než podávání placeba s valproatem nebo s lithiem [46].
Hraniční porucha osobnosti
Malé kontrolované studie usuzují na schopnost valproatu snižovat u pacientů s hraniční poruchou osobnosti impulzivitu, agitaci, agresivitu, úzkost, vztek a iritabilitu i depresivní náladu.
Studie v délce trvání 6 měsíců sledovala 30 žen s hraniční poruchou osobnosti a komorbidní bipolární afektivní poruchou typu II [47]. Valproat ve srovnání s placebem výrazně snižoval iritabilitu, vztek/hostilitu a impulzivní agresivitu, a byl dobře tolerován.
Další dvojitě slepá randomizovaná placebem kontrolovaná studie s 12 pacienty byla zaměřena pouze na hraniční poruchu osobnosti [48]. Valproat byl lepší než placebo ve snížení impulzivní agresivity. Přítomnost afektivních symptomů na počátku studie neovlivnila odpověď na léčbu, což svědčí o přímém antiagresivním účinku valproatu, nikoli o vlivu zprostředkovaném zlepšením afektivní nestability.
Schizofrenie
Symptomy schizofrenie
Kazuistická sdělení popisují klinické zlepšení u pacientů s rezistentní schizofrenií po nasazení monoterapie valproatem i po přidání valproatu k typickému nebo atypickému neuroleptiku. Oproti tomu jsou popisovány případy, kdy léčba valproatem, ať v monoterapii nebo v kombinaci s neuroleptiky, ke zlepšení zdravotního stavu pacientů s chronickou schizofrenií nevedla.
První velká randomizovaná multicentrická studie zahrnovala 249 pacientů s diagnózou schizofrenie podle DSM IV [49]. Pacienti s rezistentní schizofrenií nebyli do studie zařazeni. Po vymývací periodě 1–5 dnů byl ve studii porovnáván po období 28 dnů účinek olanzapinu a valproatu, olanzapinu a placeba, risperidonu a valproatu a risperidonu a placeba. Skupina kombinované léčby dosáhla oproti skupině s monoterapií signifikantního zlepšení ve škále Positive and Negative Syndrome Scale (PANSS) (ANOVA, p = 0,020), s nejvýraznějším vlivem na pozitivní symptomy schizofrenie. Analýza respondérů ukázala, že 50 % pacientů ze skupiny s kombinovanou léčbou dosáhlo 20% snížení v celkovém PANSS ke dni 7, zatímco skupina s antipsychotickou monoterapií dosáhla tohoto snížení po 14 dnech léčby. Léčba kombinací valproatu a atypického antipsychotika byla tolerována stejně dobře jako monoterapie a ve skupině s kombinovanou léčbou bylo méně případů odstoupení ze studie.
Tato velká studie poskytuje zatím nejpřesvědčivější důkazy o účinnosti přídatné léčby valproatem u schizofrenie, její výsledky však vzhledem k výběru účastníků studie nelze generalizovat na pacienty s rezistentní formou nemoci.
Metaanalýza Basana a kol. [50] zkoumala výsledky všech randomizovaných kontrolovaných studií, které srovnávaly valproat s antipsychotikem nebo s placebem (nebo s pacienty bez intervence) v léčbě schizofrenie a schizofrenii podobných psychóz a byly dostupné k červenci 2002. Vstupní kritéria splnilo 5 studií, do nichž bylo zahrnuto celkem 379 pacientů. Výsledky neukázaly signifikantní účinek použití valproatu po přidání k antipsychotické medikaci na celkový stav nebo na obecný duševní stav pacienta. Jedna studie (viz výše) ukázala rychlejší nástup účinku ve skupině s kombinovanou terapií.
Agresivita
Kazuistiky a retrospektivní studie také referují o snížení agresivity schizofrenních pacientů při medikaci valproatem. Prospektivní jednoletá otevřená studie s valproatem přidaným k olanzapinu u 10 pacientů s paranoidní schizofrenií nalezla statisticky signifikantní snížení hostility [51]. Sekundární post-hoc analýza studie Ca-seye [49] ukázala, že kombinovaná léčba s valproatem měla signifikantně větší účinek na snížení hostility již ve dnech 3 a 7 než antipsychotická monoterapie (p < 0,05) podle měření na položce hostility na škále PANSS. Vliv na hostilitu je zřejmě statisticky nezávislý na antipsychotickém účinku na jiných položkách PANSS, které odpovídají bludnému myšlení, formální poruše myšlení nebo halucinacím.
Léčba závislostí a abstinenčního syndromu
Abstinenční syndrom
Stávající literatura pojednávající o použití valproatu u alkoholového abstinenčního syndromu pokrývá šíři od kazuistik po dvojitě slepé studie [52]. Léčba abstinenčního syndromu antikonvulzivem ve srovnání s benzodiazepiny má několik výhod. Jednou z nejzávažnějších komplikací alkoholového abstinenčního syndromu jsou epileptické záchvaty, kterým by použití valproatu mělo pomoci předejít. Antikonvulziva také blokují neuronální senzitizaci neboli „kindling", který hraje roli v neurobiologii závislosti a odvykacích stavů a je zřejmě výsledkem opakovaných detoxifikací. Antikonvulziva přitom oproti benzodiazepinům nevyvolávají závislost a k interakcím s alkoholem dochází s menší pravděpodobností.
V několika otevřených studiích, v jedné randomizované studii (n = 48) i v jedné dvojitě slepé studii (n = 138) byl při léčbě valproatem zjištěn rychlejší ústup abstinenčních příznaků a snížení výskytu epileptických záchvatů buď před započetím léčby valproatem a po jejím zahájení, nebo v porovnání s jinou medikací (carbamazepinem) nebo placebem (např. u 545 pacientů došlo po nasazení valproatu ke snížení výskytu epileptických záchvatů z 2,5 % na 0,18 %).
Přehledová práce týkající se celkem 1500 pacientů celkově shrnuje, že při léčbě valproatem ve srovnání s použitím jiné medikace dochází k rychlejšímu zmírnění abstinenčního syndromu a k rychlejšímu ústupu některých vybraných symptomů, jako je třes a zmatenost, a to bez zvýšení hladiny jaterních enzymů nebo snížení počtu krevních destiček.
V nedávno uskutečněné randomizované studii kontrolované placebem dostávalo 36 pacientů valproat, nebo placebo [53]. Při závažných abstinenčních příznacích byla povolena medikace oxazepamem. Pacienti léčení valproatem potřebovali signifikantně méně oxazepamu a při škálování závažnosti abstinenčních příznaků dosáhli nižších skóre.
Nekontrolované studie ukazovaly možnou účinnost valproatu v léčbě benzodiazepinového odvykacího syndromu, dvojitě slepá studie se 78 pacienty, ve které byl srovnáván účinek valproatu, trazodonu a placeba, ale neprokázala vliv valproatu na snížení intenzity odvykacího syndromu [54].
Prevence relapsu
Valproat byl studován při použití v prevenci relapsu u závislosti na alkoholu a na kokainu. V nedávné dvojitě slepé placebem kontrolované studii valproatu v prevenci relapsu u alkoholové závislosti začalo znovu užívat alkohol menší procento pacientů léčených valproatem [55]. U pacientů léčených valproatem došlo také k poklesu iritability. Podobně i v další studii, do níž byli zahrnuti pacienti léčení valproatem při alkoholovém odvykacím syndromu a poté ponechaní na této medikaci, zcela abstinovalo větší procento pacientů oproti pacientům léčeným benzodiazepiny [56].
U léčby kokainové závislosti studie referují o signifikantním snížení cravingu (bažení), pozitivním screeningu moči při léčbě valproatem a nižším procentu relapsů u závislých na kokainu [57, 58].
V případě použití valproatu při léčbě závislostí se jedná o menší a předběžné práce, které však ukazují možnou roli valproatu při udržování abstinence u závislých na alkoholu a jiných návykových látkách.
Komorbidita
Valproat je účinným lékem při léčbě bipolární poruchy. Zneužívání návykových látek a závislost na nich je častou komorbiditou pacientů s diagnózou bipolární afektivní poruchy (prevalence abúzu 21–58 %), k abúzu návykových látek dochází u jedinců s touto nemocí 6–8krát častěji než v obecné populaci. Menší otevřené studie užití valproatu u pacientů s bipolární afektivní poruchou a abúzem alkoholu ukázaly dobrý účinek valproatu při kontrole abstinenčních a afektivních příznaků a ve snížení užívání alkoholu. Dvojitě slepá studie zkoumala účinek valproatu na snížení užívání alkoholu a na stabilizaci afektivních symptomů u 52 alkoholiků [59]. Pacienti byli randomizováni k léčbě valproatem a k obvyklé terapii, nebo k užívání placeba a k obvyklé terapii, která představovala podávání lithia a psychosociální léčbu. Po 24 týdnech léčby došlo v obou skupinách ke zlepšení afektivních symptomů, ale pacienti léčení valproatem měli ve srovnání s placebem menší podíl dnů těžkého pití (abúzu alkoholu). Další studie zjistila lepší compliance a tolerabilitu u léčby valproatem oproti léčbě lithiem u 44 pacientů s komorbidní bipolární poruchou a abúzem návykových látek [60].
Demence
Agitace a agresivita
Použití valproatu ke kontrole agitovanosti u pacientů s demencí popisuje více než 18 kazuistických sdělení nebo sérií kazuistik. V těchto kazuistikách je široké rozpětí použité denní dávky VPA (240–4000 mg/ den) a odpovídajících plazmatických hladin valproatu (14–107/mg/ml). Přibližně u dvou třetin pacientů došlo ke klinickému zlepšení v agitaci.
Jsou dostupné 3 placebem kontrolované studie:
První randomizovaná placebem kontrolovaná studie čítala 56 pacientů s diagnózou Alzheimerovy, vaskulární nebo smíšené demence [61]. Stupeň agitace byl hodnocen podle Brief Psychiatric Rating Scale (BPRS) na položkách tenze, hostility, nespolupráce a vzrušení. 68 % pacientů na VPA dosáhlo zlepšení ve srovnání s 52 % ve skupině placeba (p = 0,07). Průměrná denní dávka VPA při ukončení studie byla 826 mg/den.
Účinnost valproatu v léčbě sekundární mánie u obyvatel domovů důchodců s demencí byla zkoumána v multicentrické randomizované dvojitě slepé placebem kontrolované studii u 173 pacientů [62]. Vstupním kritériem byla klinická diagnóza Alzheimerovy a/nebo vaskulární demence a přítomnost sekundární mánie. Nejčastější dávka valproatu při ukončení studie byla 1000 mg/den. Signifikantně více pacientů léčených valproatem oproti placebu ukončilo studii předčasně (54 % vs 29 %, p = 0,001), a to hlavně kvůli somnolenci. Mezi skupinami nebyl zjištěn rozdíl v kontrole sekundárních manických symptomů.
Dvojitě slepá placebem kontrolovaná randomizovaná studie 42 pacientů s demencí a agresivním chováním nezjistila rozdíl v hodnocení agresivního chování mezi skupinami léčenými valproatem a placebem [63], valproat však dosáhl signifikantního účinku na neklidné, melancholické a úzkostné chování.
Otevřená randomizovaná studie účinku valproatu u 39 agresivních pacientů s demencí, která navazovala na randomizovanou kontrolovanou studii, ukázala zmírnění agresivity po 12 týdnech léčby. Sedm pacientů během studie zemřelo [64].
Tyto studie ukazují možný antiagitační účinek valproatu u části pacientů s demencí a agresivitou.
Migréna
Terapeutická účinnost valproatu byla hodnocena v randomizovaných klinických studiích. První dvojitě slepou randomizovanou překříženou studií s 29 pacienty byla studie Heringa a kol. Pacientům byl podáván valproat 400 mg 2krát denně, či placebo po dobu 8 týdnů a po překřížení dalších 8 týdnů. Výsledkem studie bylo 47% snížení frekvence záchvatů (8,8 během léčby valproatem, 15,6 placebem), 42% snížení intenzity bolesti subjektivně označené pacienty na škále bolesti. Zkrátila se i délka záchvatů [86].
V roce 1994 Jensen a kol. popsali zkušenosti s 43 pacienty s migrénou bez aury zařazenými do slepé placebem kontrolované překřížené studie. Studii dokončilo 34 pacientů. Počet dní s migrénou byl 3,5/4 týdny ve skupině léčené valproatem v počáteční dávce 1000 mg/den vs 6,1 při užívání placeba. Intenzita bolesti a délka záchvatu nebyly léčbou valproatem ovlivněny [87].
Další studie Mathewa a kol. srovnávala účinnost divalproexu oproti placebu u 107 pacientů po dobu 12 týdnů. Dávka divalproexu byla titrována podle plazmatických hladin a pohybovala se mezi 250–1000 mg/ den. Do studie byli zařazeni pacienti s migrénou bez aury i s aurou. Cílem studie bylo sledovat změny ve frekvenci záchvatů. Během léčebné fáze byla průměrná frekvence 3,5 záchvatů během 4 týdnů ve skupině divalproexu a 5,7 v placebové skupině. Opět nebyla pozorována změna v trvání a intenzitě záchvatů [88].
Účinnost antiepileptik v prevenci migrény byla předmětem systematického review. Do metaanalýzy bylo zahrnuto celkem 2024 pacientů. Léčba antiepileptiky vedla k průměrnému snížení o 1,4 záchvatů za 4 týdny. Aby bylo dosaženo 50% snížení frekvence záchvatů, bylo třeba léčit 3,1 pacientů valproatem (95% CI: 1,9–8,9) a 4,8 pacientů komplexem kyseliny a soli valproatu – divalproexem – (95% CI: 3,5–7,4) [90].
Neuropatická bolest
Antiepileptika jsou užívána v léčbě neuropatických bolestí. Účinnost valproatu v terapii diabetické neuropatie měla za cíl analyzovat randomizovaná dvojitě slepá studie Kochara a kol., v níž bylo 43 pacientů rozděleno do skupin léčených valproatem 1200 mg/den a užívajících placebo. Po třech měsících léčby bylo pozorováno pomocí McGill Pain Questionnaire snížení bolesti, avšak elektrofyziologické ukazatele zůstaly nezměněny [91].
V randomizované dvojitě slepé překřížené studii trvající celkem 8 týdnů nevedla léčba kyselinou valproovou u 31 pacientů s bolestivými polyneuropatiemi k úlevě od bolesti [92].
Autoři systematického review zabývajícího se účinkem antikonvulziv na neuropatickou bolest došli k závěru, že dobře prokázaný efekt u diabetické neuropatie a postherpetické neuralgie je u carbamazepinu a gabapentinu. Důkazy o účinnosti valproatu jsou zatím nedostatečné [93].
Zařazení do palety léčiv
Epilepsie
Distribuovány jsou tři typy preparátů, kdy je účinnou látkou kyselina valproová či valproat sodný a nebo kombinace soli a kyseliny. Valproat má v současné epileptologii jednoznačně vedoucí postavení. Valproat a carbamazepin jako léky tzv. druhé generace vytlačily z preskripce pro první volbu generaci první (barbituráty, hydantoináty a sukcinimidy) a patří mezi nejčastěji podávaná antiepileptika (dále AE). Nová antiepileptika 3. generace se zatím jako léky první volby uplatňují v omezené míře. V naší anketní studii srovnávající užívání antiepileptik u školních dětí v ČR jsme zjistili, že v roce 1995 bylo valproatem léčeno 39 % z 1189 dětí užívajících antiepileptika a v roce 2004 to bylo 63 % z 612 dětí. Sledovali jsme též přesun spotřeby od neretardované formy léčiva k modernějším preparátům s pomalu se uvolňující účinnou složkou.
Výše zmíněné rozsáhlé využití valproatu v léčbě epilepsie je dáno několika faktory.
Za prvé – z hlediska účinnosti má valproat velmi široké spektrum indikací a je efektivní nejen u primárně generalizovaných epileptických záchvatů, ale až na výjimky i u ostatních forem záchvatů.
Za druhé – valproat na rozdíl od řady ostatních AE nevyvolává žádné typy epileptických záchvatů a lze jej použít i u syndromů, u kterých jsou přítomny různé typy záchvatů současně. Jedinou zmínkou o možnosti zhoršení epileptického syndromu valproatem je práce Sarisjulise a Dulaca [94], kteří nedoporučují VPA u ESES a LKS. Opačného mínění je však Tassinari [95], který naopak u ESES kombinaci VPA s BZD doporučuje.
A konečně za třetí – až na výjimky je valproat dobře snášen, nemá nežádoucí kognitivně behaviorální účinky, a naopak může zlepšit celkovou pohodu (viz kapitoly o využití VPA v psychiatrii).
Na druhé straně jsou v posledních letech zdůrazňována určitá negativa relativizující výše zmíněnou chválu valproatu. Týká se to především mladých žen, a to zejména pro vysoké riziko výskytu vrozených vývojových vad u plodů žen užívajících v těhotenství valproat. Diskutovány jsou i hormonální poruchy u dospívajících, zvláště tzv. syndrom polycystických ovarií. Naopak dříve zdůrazňovaná rizika steatální hepatózy a jiných závažných komplikací u kojenců a malých dětí se ukázala jako méně častá a tedy i méně významná.
Dalším diskutovaným faktorem je interakce valproatu s ostatními antiepileptiky, jejichž metabolismus zpomaluje, a případné zvýšení hladiny může být spojeno s nežádoucími účinky, a to zejména v případě kombinace valproatu s lamotriginem [96].
Indikace valproatu k dlouhodobé léčbě epilepsie lze rozdělit na jeho podávání u jednotlivých forem záchvatů a indikace v dětském věku u věkově vázaných epileptických syndromů. Velmi specifickou indikací je podávání valproatu intravenózně při léčbě nakupených epileptických záchvatů a status epilepticus.
Valproat v léčbě epileptických záchvatů
Hlavní indikací nasazení jsou všechny formy primárně generalizovaných záchvatů, kde je valproat jednoznačně lékem první volby. V tom smyslu se shoduje většina doporučených postupů, a to jak česká [97], tak jiná národní (NICE-UK), evropská (EUREPA) i mezinárodní (ILAE) doporučení. Je indikován i u parciálních záchvatů, zejména idiopatických s jednoduchou symptomatologií, kde prokázal obdobnou účinnost jako carbamazepin, nicméně u komplexních parciálních záchvatů je dle VA-II (Veteran Administration Study II) carbamazepin efektivnější [98].
Valproat v léčbě věkově vázaných syndromů
V dětském věku byl popsán výskyt zhruba třiceti specifických epileptických syndromů s vazbou na určité věkové období, charakteristickou sémiologií, patognomickým nálezem EEG a v některých případech dobře predikovatelnou prognózou. Až na několik výjimek je u většiny z těchto syndromů valproat indikován jako první volba [99–101, 96, 102].
Valproat není indikován u novorozeneckých epileptických syndromů, kde vzhledem k známému paradoxnímu účinku GABAergních preparátů na nezralý mozek dáváme spíše přednost barbiturátům a hydantoinátům. Rovněž u Ohtaharova syndromu provázeného burst suppression EEG vzorci nebyla prokázána účinnost valproatu. Naopak u Westova syndromu je valproat jako lék druhé volby indikován v případě neúspěchu či nemožnosti podávání ACTH a vigabatrinu.
Lékem první volby je VPA u Dooseho myoklonicko-astatické epilepsie (MAE), se sporným efektem je podáván u syndromu Dravetové (severe myoclonic epilepsy of infancy).
U Lennoxova-Gastautova syndromu je sice valproat lékem první volby, ale obvykle nedokáže pokrýt celé spektrum záchvatů v monoterapii.
VPA je lékem první volby u všech forem idiopatických generalizovaných syndromů, a to jak u dětských či juvenilních absencí, tak i u juvenilní myoklonické epilepsie (JME) a u generalizovaných záchvatů po probuzení (GMA – Grand mal awakening).
Lékem druhé a dle některých doporučení i první volby je valproat u nejčastější věkově vázané benigní epilepsie s rolandickými hroty (BERS) a u BEOS [99].
Valproat v léčbě status epilepticus
Valproat patří k několika málo antiepileptikům, která jsou dostupná nejen pro perorální, ale i pro intravenózní podávání. Nabízí se tak možnost překlenout kritická peroperační nebo jiná období nemožnosti perorálního příjmu léčiva i využití pro intenzivní terapii.
U pokračujícího status epilepticus je valproat po benzodiazepinech a hydantoinátech indikován obvykle jako třetí lék, a to zejména u myoklonických a nonkonvulzivních statů [103].
Léčba bývá zahajována iniciálním bolusem cca 15 mg valproatu na kilogram hmotnosti pacienta (obykle 400–800 mg) a pokračuje kontinuální infuzí s dávkou 1–2 mg na kilogram a hodinu. Doba i.v. aplikace se řídí klinickým efektem a EEG odezvou. Při nasazení i.v. aplikace valproatu musíme zvážit rizika intoxikace u pacientů léčených lamotriginem.
Psychiatrické poruchy
Valproat je antiepileptikum se širokým záběrem klinického účinku u psychiatrických poruch, jehož podkladem je komplexní ovlivnění funkce nervových buněk. Hlavním léčebným využitím valproatu v psychiatrii je terapie bipolární afektivní poruchy, a to jednak léčba manické fáze a dále udržovací léčba a tymoprofylaxe.
V léčbě manické epizody je prvním krokem nejčastěji podání valproatu s antipsychotikem nebo lithia s antipsychotikem. Antimanické působení valproatu bylo ověřeno v řadě klinických studií, ve kterých byl valproat lepší než placebo a v naprosté většině srovnatelný v účinnosti s lithiem a haloperidolem. Valproat má také obdobnou účinnost jako olanzapin, ale odlišnou tolerabilitu. Lepší odpověď na valproat v manické fázi je nacházena u pacientů se smíšenou anebo atypickou mánií, nonresponzivitou na lithium a vyšším počtem afektivních fází v anamnéze a u pacientů s neurologickými abnormalitami. Antimanický účinek valproatu může být augmentován lithiem, carbamazepinem a atypickými antipsychotiky. Kombinovaná terapie je vhodná hlavně pro ty pacienty, u kterých nedošlo k odpovědi po adekvátní léčbě prvním lékem.
Valproat patří v běžné praxi mezi nejčastěji používané léky v udržovací léčbě a v tymoprofylaxi v České republice i ve světě, ve Spojených státech je divalproex (komplex soli a kyseliny valproové) vůbec nejčastější medikací v dlouhodobé léčbě bipolární poruchy. V udržovací fázi léčby bipolární poruchy charakterizované převahou hypomanických a manických epizod nad depresivními jsou léky první volby lithium a valproat. Účinek valproatu byl jasně potvrzen v nedávné studii bipolárních pacientů s komorbidním užíváním alkoholu, jiným studiím se však jeho účinnost v dlouhodobé profylaxi jednoznačně prokázat nepodařilo. Dosavadní studie ukazují, že valproat je při dlouhodobém podávání poněkud lépe tolerován než lithium, ovšem na rozdíl od lithia u něj nebylo prokázáno antisuicidiální působení.
Klinické zkušenosti dobrého výsledku profylaktické léčby kombinací valproatu s dalším stabilizátorem nálady potvrzují i randomizované kontrolované studie léčby kombinací valproatu s lithiem nebo s olanzapinem. Augmentace VPA atypickými antipsychotiky v dlouhodobé udržovací terapii zřejmě lépe kontroluje depresivní fázi bipolární poruchy než monoterapie valproatem. Při léčbě kombinací stabilizátorů nálady však častěji dochází k rozvoji vedlejších nežádoucích účinků.
Valproat je také používán v léčbě pacientů s hraniční poruchou osobnosti ke snížení impulzivity, agitace a agresivity. Oprávněnost tohoto užití valproatu u této poruchy osobnosti potvrzuje několik dvojitě slepých studií menšího rozsahu.
Použití valproatu v léčbě dalších poruch není časté. V léčbě alkoholové závislosti může být valproat použit v terapii odvykacího syndromu. Dobře prokázáno je zmírnění abstinenčních příznaků a hlavně prevence vzniku epileptických záchvatů při medikaci valproatem, a to bez výrazného narušení jaterních funkcí a poklesu počtu trombocytů. S dobrým efektem je možné použít valproat v léčbě bipolární poruchy komorbidní s abúzem psychoaktivních látek nebo se závislostí na těchto látkách. Předběžné studie ukazují také možný příznivý vliv valproatu na prevenci relapsu při závislosti na alkoholu a zřejmě i na kokainu (u pacientů bez komorbidní bipolární poruchy).
U pacientů se schizofrenií může podání valproatu snižovat agresivitu a hostilitu, v ojedinělých případech také zlepšit celkový stav pacienta s chronickou nebo rezistentní formou nemoci. Také u části pacientů s demencí je možné využít antiagitační a antiagresivní účinek valproatu, za pečlivého sledování hladin léku a jeho nežádoucích účinků. Antiagresivní působení valproatu bylo nalezeno také u dalších diagnostických kategorií, například u explozivních a labilních dětí a adolescentů, u mužů s impulzivní agresivitou a v léčbě poruch chování/disociální poruchy osobnosti.
Léčba bolesti
Valproat v klinických studiích prokázal vysokou účinnost v prevenci migrény. V doporučených postupech Společnosti pro diagnostiku a léčbu bolestí hlavy je valproat spolu s b-blokátory bez vnitřní aktivity, tricyklickými antidepresivy a pizotifenem první volbou profylaktické léčby migrény [115].
V léčbě neuropatické bolesti nejsou dosud s valproatem dostatečné klinické zkušenosti. Přednost v této indikaci dostávají jiná antiepileptika (např. carbamazepin, gabapentin, pregabalin, lamotrigin).
Indikace
Valproat je v současnosti hlavním lékem v léčbě velké většiny epileptických záchvatů a syndromů, kromě dobrých klinických zkušeností svědčí pro jeho podávání i farmakoekonomické aspekty. S úspěchem může být použit u generalizovaných záchvatů a parciálních záchvatů se sekundární generalizací (absence, myoklonické záchvaty, tonicko-klonické záchvaty, atonické záchvaty, smíšené záchvaty); u parciálních záchvatů (jednoduchých i komplexních) a též u specifických syndromů (Westův, Lennoxův-Gastautův). Jinou indikací valproatu je prevence manických fází u bipolárních depresivních poruch. Valproat může být indikován též k profylaxi záchvatů migrény.
Kontraindikace
Valproat by neměl být používán u pacientů s vážným poškozením jater, přecitlivělostí na účinnou látku nebo porfyrií. Velké opatrnosti je třeba v těhotenství, kdy léčba valproatem (podobně jako ostatními antiepileptiky) zvyšuje riziko malformace plodu.
Nežádoucí účinky
Incidence nežádoucích účinků je kvantifikována následovně:
časté nežádoucí účinky > 10 % pacientů, méně časté nežádoucí účinky 1–10 % pacientů, vzácné nežádoucí účinky 0,1–1 % pacientů, velmi vzácné nežádoucí účinky < 0,1 % pacientů.
Nežádoucí účinky postihují 10–20 % pacientů, obvykle jsou přechodného charakteru a většina z nich ustoupí spontánně nebo po přechodném snížení dávek [116].
Nejzávažnějším nežádoucím účinkem je hepatotoxicita. K jejím projevům dochází obvykle v prvních 6 měsících terapie valproatem. Po přerušení terapie je obvykle reverzibilní, může však vést k fatálnímu vyústění. Riziko hepatotoxicity je zvýšené u dětí do 2 let věku, především v případě organického poškození mozku, v případě mentální retardace nebo při vrozeném metabolickém onemocnění. Dalším velmi vzácným, ale závažným nežádoucím účinkem je pankreatitida, která též může vést k fatálnímu vyústění.
Kyselina valproová je teratogen. Její podávání v období těhotenství může vést ke vzniku spina bifida (1–2% riziko), fetálnímu valproatovému syndromu s charakteristickým výrazem v obličeji a k dalším malformacím.
a) ‑časté nežádoucí účinky
Nechutenství, nauzea, zvracení, křečovité bolesti břicha, průjem, celková slabost, bolesti hlavy, závratě, třes rukou, útlum krvetvorby (trombocytopenie, vzácně leukopenie až arganulocytóza, pancytopenie).
b) méně časté nežádoucí účinky
Pyróza, zácpa, zvýšení chuti k jídlu, hepatotoxicita (zvýšení hodnot jaterních transamináz, vzácně hyperbilirubinémie, hyperamonémie, cholestatický ikterus, velmi vzácně hepatitida, hyperamonemická encefalopatie, jaterní nekróza, selhání funkce jater), emoční labilita, úzkost, noční můry, poruchy rovnováhy, poruchy koordinace, diplopie, zastřené vidění či jiné poruchy vidění, nystagmus, hypertenze, tachykardie, palpitace, parestezie, bolesti svalů nebo kloubů, křeče dolních končetin, alergické kožní reakce, svědění.
c) vzácné nežádoucí účinky
Deprese, bradykineze, abulie, lymfacytóza, hypofibrinogenémie až velmi vzácně afibrinogenémie, krvácení (epistaxe, hematomy, petechie, děložní krvácení, velmi vzácně závažné krvácivé příhody), fotosenzitivita, alopecie, po nitrožilní aplikaci možnost anafylaktického šoku.
d) velmi vzácné nežádoucí účinky
Pankreatitida (včetně hemoragické pankreatitidy), akutní ataka porfyrie, syndrom nepřiměřené sekrece antidiuretického hormonu, hyponatrémie, Stevensův-Johnsonův syndrom, erythema multiforme, toxická epidermální nekrolýza.
Interakce
Kyselina valproová prakticky neovlivňuje aktivitu jednotlivých izoenzymů cytochromu P-450 (pravděpodobně jen velmi slabě inhibuje CYP3A4) a ani není jejich významnějším substrátem [117]. Biotransformace kyseliny valproové probíhá převážně konjugací (30–50 % podané dávky), dále mitochondriální b-oxidací (40 % podané dávky) a v malé míře též mikrozomální oxidací (15–20 % podané dávky). Kyselina valproová je inhibitorem uridin-5-difosfát-glukuronosyltransferázy (UGT). S léčivy, která se biotransformují konjugací za vzniku glukuronidů (l
Seznam použité literatury
- [1] Nemeroff CB, Owens MJ. Pharmacology of Valproate. Psychopharmacol Bull 2003; 37 (Suppl 2): 17–24.
- [2] Biggs CS, Pearce BR, Fowler LJ, et al. Regional effects of sodium valproate on extracellular concentrations of 5-hydroxytryptamine, dopamine, and their metabolites in the rat brain: an in vivo microdialysis study. J Neurochem 1992; 59: 1702–1708.
- [3] Manji HK, Moore GJ, Rajkowska G, et al. Neuroplasticity and cellular resilience in mood disorders. Mol Psychiatry 2000; 5: 578–593.
- [4] Jope RS, Bijur GN. Mood stabilizers, glycogen synthase kinase-3beta and cell survival. Mol Psych 2002; 7: 35–45.
- [5] Chen G, Zeng WZ, Yuan PX, et al. The mood-stabilizing agents lithium and valproate robustly increase the levels of the neuroprotective protein bcl-2 in the CNS. J. Neurochem 1999; 72: 879–882.
- [6] Farber NB, Juang XP, Heinkel C, Nemmers B. Antiepileptic drugs and agents that inhibit voltage-gated sodium channels prevent NMDA antagonist neurotoxicity. Mol Psychiatry 2002; 7: 726–733.
- [7] Willmore LJ. Divalproex and Epilpsy. Psycho-pharmacology Bulletin 2003; 37; 43–53.
- [8] Owens MJ, Nemeroff CB. Pharmacology of Valproate. Psychopharmacology Bulletin 2003; 37; 17–24.
- [9] Schank RJ, Liles LC, Weinschenker D. Reduced anticonvulsiant efficacy of valproic acid in dopamine -hydroxylase knockout mice. Epilepsy Research 2005; 65; 23–31.
- [10] Henry TR. The History of Valproate in Clinical Nueroscience. Psychopharmacology Bulletin 2003; 37; 5–16.
- [11] Freitag FG. Divalproex in the Treatment of Migraine. Psychopharmacology Bulletin 2003; 37; 98–115.
- [12] Citrome BL. Schizophrenia and Valproate. Psychopharmacology Bulletin 2003; 37; 74–88.
- [13] Ichikawa J, Chung YC, Dai J, Meltzer HY. Valproic acid potentiantes both typical and atypical antipsychotic-induced prefrontal cortical dopamine release. Brain Research 2005; 1052; 56–62.
- [14] Tringali G, Aubry JM, Moscianese K, Zamori C, Vairano M, Preziosi P, Navarra P, Pozzoli G. Valproic acid inhibits corticotropin-releasing factor synthesis and release from the rat hypothalamus in vitro: evidence for the involvement of GABAergic neurotransmission. Journal of Psychiatry and Neuroscience 2004; 29; 459–466.
- [15] Yildirim E, Zhang Z, Uz T, et al. Valproate administration to mice increases histone acetylation and 5-lipoxygenase content in the hippocampus. Neuroscience Letters 2003; 345; 141–143.
- [16] Smith MC. The Efficacy of Divalproex for Partial Epilepsie. Psychopharmacology Bulletin 2003; 37; 54–66.
- [17] Jeong MR, Hashimoto R, Sentorov VV, et al. Valproic acid, a mood stabilizer and anticonvulsant, protects rat cerebral cortical neurons from spontaneous cell death: a role of histone deacetylase inhibition. FEBS Letters 2003; 542; 74–78.
- [18] Tong V, Teng XW, Karagiozov S, et al. Valproic acid glucuronidation is associated with increases in 15-F2t-isoprostane in rats. Free Radical Biology and Medicine 2005; 38; 1471–1483.
- [19] Lülmann H, Mohr K, Wehling M. Farmakologie a toxikologie. Praha, Grada Publishing, 2004.
- [20] DeVane L. Pharmacokineticss, Drug Interactions, and Tolerability of Valproate. Psychopharmacology Bulletin 2003; 37; 25–42.
- [21] http://www.inchem.org/documents/pims/pharm/ pim551.htm 26.1.2006
- [22] Davis R, Peters DH, Mc Tavish D. Valproic acid. A reappraisal of its pharmacological properties and clinical efficacy in epilepsy. Drugs 1994; 47; 332–372.
- [23] Levy RH, Mattson RH, Meldrum BS. Antiepileptic drugs. Raven Press 1995, New York.
- [24] Turnbull DM, Howel D, Rawlins MD et al. Which drug for the adult epileptic patient: phenytoin or valproate? BMJ 1985; 290: 815–819.
- [25] Heller AJ, Chesterman P, Elwes RDC, et al. Phenobarbitone, phenytoin, carbamazepine, or sodium valproate for newly diagnosed adult epilepsy: a randomised comparative monotherapy trial. J Neurol Neurosurg Psychiatry 1995; 58: 44–50.
- [26] Smith TC, Marson AG, Williamson PR. Phenytoin versus valproate monotherapy for partial onset seizures and generalised onset tonic-klonic seizures. The Cochrane Database of Systematic Reviews 1. 2006.
- [27] Richens A, Davidson DL, Cartlidge NE, et al. A multicentre comparative trial of sodium valproate and carbamazepine in adult onset epilepsy. Adult EPITEG Collaborative Group. J Neurol Neurosurg Psychiatry 1994; 57: 682–687.
- [28] Mattson RH, Cramer JA, Collins JF. Related Articles, Links. A comparison of valproate with carbamazepine for the treatment of complex partial seizures and secondarily generalized tonic-clonic seizures in adults. The Department of Veterans Affairs Epilepsy Cooperative Study No. 264 Group. N Engl J Med 1992; 327: 765–771.
- [29] Marson AG, Williamson PR, Hutton JL, et al. Carbamazepine versus valproate monotherapy for epilepsy. The Cochrane Database of Systematic Reviews 1. 2006.
- [30] Wheless JW, Neto W, Wang S. EPMN-105 Study Group. Topiramate, carbamazepine, and valproate monotherapy: double-blind comparison in children with newly diagnosed epilepsy. J Child Neurol 2004; 19: 135–141.
- [31] Callaghan N, O´Hare J, O´Driscoll D, et al. Comparative study of ethosuximide and sodium valproate in the treatment of typical absence seizures (petit mal). Dev Med Child Neurol 1982; 24: 830–836.
- [32] Posner EB, Mohamed K, Marson AG. Ethosuximide, sodium valproate or lamotrigine for absence seizures in children and adolescents. The Chochrane Database of Systemic Reviews 1. 2006.
- [33] Jha S, Jose M, Patel R. Intravenous sodium valproate in status epilepticus. Neurol India 2003; 51: 421–422.
- [34] Keck PE Jr, McElroy SL. Divalproex in the treatment of bipolar disorder. Psychopharmacol Bull 2003; 37 (Suppl 2): 67–73.
- [35] Bowden CL. Valproate. Bipolar Disord 2003; 5: 189–202.
- [36] Sachs GS, Grossman F, Ghaemi SN, et al. Combination of a mood stabilizer with risperidone or haloperidol for treatment of acute mania: a double-blind, placebo-controlled comparison of efficacy and safety. Am J Psychiatry 2002; 159: 1146–1154.
- [37] Davis LL, Bartolucci A, Petty F. Divalproex in the treatment of bipolar depression: a placebo-controlled study. J Affect Disord. 2005; 85: 259–266.
- [38] Bowden CL, Calabrese JR, McElroy SL, et al. A randomized, placebo-controlled 12-month trial of divalproex and lithium in treatment of outpatients with bipolar I disorder. Divalproex Maintenance Study Group. Arch Gen Psychiatry 2000; 57: 481–489.
- [39] Lambert PA, Venaud G. Comparative study of valpromide versus lithium as prophylactic treatment in affective disorders. Nervure 1992; 5: 57–65.
- [40] Ghaemi SN, Goodwin FK. Long-term naturalistic treatment of depressive symptoms in bipolar illness with divalproex vs. lithium in the setting of minimal antidepressant use. J Affect Disord 2001; 65: 281–287.
- [41] Revicki DA, Hirschfeld RM, Ahearn EP, et al. Effectiveness and medical costs of divalproex versus lithium in the treatment of bipolar disorder: results of a naturalistic clinical trial. J Affect Disord 2005; 86: 183–193.
- [42] Calabrese JR, Delucchi GA. Spectrum of efficacy of valproate in 55 patients with rapid-cyclingbipolar disorder. Am J Psychiatry 1990; 147: 431–434.
- [43] Calabrese JR, Shelton MD, Bowden CL, et al. Bipolar rapid cycling: focus on depression as its hallmark. J Clin Psychiatry 2001; 62 (Suppl. 14): 34–41.
- [44] Calabrese JR, Shelton MD, Rapport DJ, et al. A 20-month, double-blind, maintenance trial of lithium versus divalproex in rapid-cycling bipolar disorder. Am J Psychiatry 2005; 162: 2152–2161.
- [45] Solomon DA, Ryan CE, Keitner GI, et al. A pilot study of lithium carbonate plus divalproex sodium for the continuation and maintenance treatment of patients with bipolar I disorder. J Clin Psychiatry 1997; 58: 95–99.
- [46] Tohen M, Chengappa KNR, Suppes T, et al. Relapse prevention in bipolar I disorder: 18- month comparison of olanzapine plus mood stabiliser v. mood stabiliser alone. Br J Psychiatry 2004; 184: 337–345.
- [47] Frankenburg FR, Zanarini MC. Divalproex sodium treatment of women with borderline personality disorder and bipolar II disorder: a double-blind placebo-controlled pilot study. J Clin Psychiatry 2002; 63: 442–446.
- [48] Hollander E, Swann CA, Coccaro EF, et al. Impact of Trait Impulsivity and State Aggression on Divalproex Versus Placebo Response in Borderline Personality Disorder. Am J Psychiatry 2005; 162: 621–624.
- [49] Casey DE, Daniel DG, Wassef AA, et al. Effect of divalproex combined with olanzapine or risperidone in patients with an acute exacerbation of schizophrenia. Neuropsychopharmacol 2003; 28:182–192.
- [50] Basan A, Leucht S. Valproate for schizophrenia. Cochrane Database Syst Rev 2004; CD004028.
- [51] Littrell KH, Petty RG, Hilligoss NM, et al. Valproate for hostility in schizophrenia patients. J Clin Psychiatry 2004; 65: 134.
- [52] Myrick H, Brady KT. The Use of Divalproex in the Treatment of Addictive Disorders. Psychopharmacol Bull 2003; 37 (Suppl. 2): 89–97.
- [53] Reoux JP, Saxon AJ, Malte CA, et al. Divalproex in alcohol withdrawal: a randomized double-blind placebo-controlled clinical trial. Alcohol Clin Exp Res 2001; 25: 1324–1329.
- [54] Rickels K, Schweizer E, Garcia Espana F, et al. Trazodone and valproate in patients discontinuing long-term benzodiazepine therapy: effects on withdrawal symptoms and taper outcome. Psychopharmacology (Berl) 1999; 141: 1–5.
- [55] Brady KT, Myrick H, Henderson S. Divalproex in the prevention of relapse to alcohol use. Drug Alcohol Depend 2002; 67: 323–330.
- [56] Longo LP, Campbell C, Hubatch S. Divalproex sodium for alcohol withdrawal and relapse prevention. J Addict Dis 2002; 21: 55–64.
- [57] Myrick H, Henderson S, Brady KT, et al. Dival-proex loading in the treatment of cocaine dependence. J Psychoactive Drugs 2001; 33: 283–287.
- [58] Halikas JA, Center BA, Pearson VL, et al. A pilot, open clinical study of depakote in the treatment of cocaine abuse. Hum Psychopharmacol 2001; 3: 257–264.
- [59] Salloum I, Cornelius JR, Daley DC, et al. Efficacy of valproate maintenance in bipolar alco holics: preliminary findings. Proc Am Acad Addict Psychiatry 2002; 63.
- [60] Weiss RD,Greenfield SF,Najavits LM, et al. Medication compliance among patients with bipolar disorder and substance use disorder. J Clin Psychiatry 1998; 59:172–174.
- [61] Porsteinsson AP, Tariot PN, Erb R, et al. Placebo-controlled study of divalproex sodium for agitation in dementia. Am J Geriatr Psychiatry 2001; 9: 58–66.
- [62] Tariot PN, Schneider L, Mintzer J, et al. Safety and tolerability of divalproex sodium for the treatment of signs and symptoms of mania in elderly patients with dementia: results of a double-blind, placebocontrolled trial. Curr Ther Res 2000; 62: 51–67.
- [63] Sival RC, Haffmans PMJ, Jansen PAF, et al. Sodium valproate in the treatment of aggressive behavior in patients with dementia – a randomized placebo-controlled clinical trial. Int J Geriatr Psychiatry 2002; 17: 579–585.
- [64] Sival RC, Duivenvoorden HJ, Jansen PA, et al. Sodium valproate in aggressive behaviour in dementia: a twelve-week open label follow-up study. Int J Geriatr Psychiatry 2004; 19: 305–312.
- [65] Citrome L. Schizophrenia and Valproate. Psychopharmacol Bull 2003; 37 (Suppl. 2).
- [66] Barzman DH, McConville BJ, Masterson B, et al. Impulsive aggression with irritability and responsive to divalproex: a pediatric bipolar spectrum disorder phenotype? J Affect Disord 2005; 88: 279–285.
- [67] Stanford MS, Helfritz LE, Conklin SM, et al. A comparison of anticonvulsants in the treatment of impulsive aggression. Exp Clin Psychopharmacol 2005; 13: 72–77.
- [68] Steiner H, Petersen ML, Saxena K, et al. Dival-proex sodium for the treatment of conduct disorder: a randomized controlled clinical trial. J Clin Psychiatry 2003; 64: 1183–1191.
- [69] Debattista C, Solomon A, Arnow B, et al. The efficacy of divalproex sodium in the treatment of agitation associated with major depression. J Clin Psychopharmacol 2005; 25: 476–479.
- [70] Emrich HM, von Zerssen D, Kissling W, et al. Effect of sodium valproate on mania: the GABA hypothesis of affective disorders. Arch Psychiatr Nervenkr 1980; 229:1–16.
- [71] Brennan M, Sandyk R, Borsook D. Use of sodium valproate in the management of affective disorders. Basic and clinical aspects. In: Emrich HM, et al., eds. Anticonvulsants in Affective Disorders. Amsterdam, The Netherlands: Elsevier Science Publishers1984; 56–65.
- [72] Pope HG, Jr, McElroy SL, Keck PE, Jr, Hudson JI. Valproate in the treatment of acute mania: a placebo-controlled trial. Arch Gen Psychiat. 1991; 48: 62–68.
- [73] Bowden CL, Brugger AM, Swann AC, et al. Efficacy of divalproex sodium versus lithium and placebo in the treatment of acute mania. JAMA 1994; 271: 918–924.
- [74] Freeman TW, Clothier JL, Pazzaglia P, et al. A double-blind comparison of valproate and lithium in the treatment of acute mania. Am J Psychiatry 1992; 149: 108–111.
- [75] McElroy SL, Keck PE, Jr, Stanton SP, et al. A randomized comparison of divalproex oral loading versus haloperidol in the initial treatment of acute psychotic mania. J Clin Psychiatry 1996; 57: 142–146.
- [76] Hirschfeld RMA, Allen MH, McEvoy JP, et al. Safety and tolerability of oral loading divalproex sodium in acutely manic bipolar patients. J Clin Psychiatry 1999; 60: 815–818.
- [77] Zajecka JM,Weisler R, Sachs G, et al. A comparison of the efficacy, safety, and tolerability of divalproex in the treatment of bipolar disorder. J Clin Psychiatry 2002; 63: 1148–1155.
- [78] Tohen M, Baker RW, Altshuler LL, et al. Olanzapine versus divalproex in the treatment of acute mania. Am J Psychiatry 2002; 159: 1011–1017.
- [79] Muller-Oerlinghausen B, Retzow A, Henn F, et al. Valproate as an adjunct to neuroleptic medication for the treatment of acute episodes of mania: a prospective, randomized, double-blind, placebo-controlled, multicenter study. J Clin Psychopharmacol 2000; 20: 195–203.
- [80] Yatham LN, Binder C, Riccardelli R, Leblanc J, Connolly M, Kusumakar V; RIS-CAN 25 Study Group. Risperidone in acute and continuation treatment of mania. Int Clin Psychopharmacol 2003 Jul; 18: 227–235.
- [81] Sachs G, Chengappa KN, Suppes T, Mullen JA, Brecher M, Devine NA, Sweitzer DE. Quetiapine with lithium or divalproex for the treatment of bipolar mania: a randomized, double-blind, placebo-controlled study. Bipolar Disord 2004; 6: 213–223.
- [82] Delbello MP, Schwiers ML, Rosenberg HL, Strakowski SM. A double-blind, randomized, placebo-controlled study of quetiapine as adjunctive treatment for adolescent mania. J Am Acad Child Adolesc Psychiatry 2002; 41: 1216–1223.
- [83] Tohen M, Chengappa KN, Suppes T, et al. Efficacy of olanzapine in combination with valproate or lithium in the treatment of mania in patients partially nonresponsive to valproate or lithium monotherapy. Arch Gen Psychiatry 2002; 59: 62–69.
- [84] Baker RW, Brown E, Akiskal HS, et al. Efficacy of olanzapine combined with valproate or lithium in the treatment of dysphoric mania. Br J Psychiatry 2004; 185: 472–478.
- [85] Hosak L, Libiger J. Antiepileptic drugs in schizophrenia: a review. Eur Psychiatry 2002; 17: 371–378.
- [86] Hering R, Kuritzky A. Sodium valproate in the prophylactic treatment of migraine: a double-blind study versus placebo. Cephalalgia. 1992; 12: 81–84.
- [87] Jensen R, Brinck T, Olesen J. Sodium valproate has a prophylactic effect in migraine without aura: a triple-blind, placebo-controlled cross-over study. Neurology 1994; 44: 647–651.
- [88] Mathew NT, Saper JR, Silberstein SD, et al. Migraine prophylaxis with divalproex. Arch Neurol 1995; 52: 281–286.
- [89] Klapper J. Divalproex sodium in migraine prophylaxis: a dose-controlled study. Cephalalgia. 1997; 17: 103–108.
- [90] Chronicle E, Mulleners W. Anticonvulsant drugs for migraine prophylaxis. The Cochrane Database of Systematic Reviews 1. 2006.
- [91] Kochar DK, Rawat N, Agrawal RP, et al. Sodium valproate for painful diabetic neuropathy: a randomized double-blind placebo-controlled study. QJM 2004; 97: 33–38.
- [92] Otto M, Bach FW, Jensen TS, et al. Valproic acid has no effect on pain in polyneuropathy: a randomized, controlled trial. Neurology 2004; 62: 285–288.
- [93] Wiffen P, Collins S, McQuay H et al. Anticonvulsant drugs for acute and chronic pain. The Cochrane Database of Systematic Reviews 1. 2006.
- [94] Sarisjulis N, Dulac O. Valproate in the treatment of epilepsies in children in Loescher W., ed.: Valproate, in Milestones in drug therapy, Birkhauser, 1999.
- [95] Tassinari CA. Encephalopathy with electrical status epilepticus during slow slep. Clin Neuro- physiol 2000; S94–S102, L.
- [96] Komárek V. Nežádoucí účinky a interakce nových antiepileptik. Farmakologie pro praxi 2005; 4 (chybí str.).
- [97] Zárubová J, et al. Žena a epilepsie. EPISTOP 2004.
- [98] http://www.ilae-epilepsy.org
- [99] Panayiotopoulos CP. The Epilepsie. Bladon Medical Publishing, 2005.
- [100] Bourgeois B. Chronic Management of Seizures in the Syndromes of Idiopathic Generalized Epilepsy. Epilepsia 2003; 27–32.
- [101] Komárek V, et al. Soubor minimálních diagnostických a terapeutických standardů u pacientů s epilepsií I-VII, MEDIFORUM/EPISTOP 2002.
- [102] Šlapal R, Kunčíková M. Věkově vázané epileptické syndromy. Dopor. postup 101/055 2001.
- [103] Uberall M, Trollmann R. Intravenous valproate in pediatric epilepsy patients with refractory status epilepticus. Neurology 2000; 54: 2188–2189.
- [104] de Silva M, MacArdle B, McGowan M, et al. Randomised comparative monotherapy trial of phenobarbitone, phenytoin, carbamazepine, or sodium valproate for newly diagnosed childhood epilepsy. Lancet 1996; 16: 709–713.
- [105] Keller J, Chesterman P, Elwes RD, et al. Phenobarbitone, phenytoin, carbamazepine, or sodium valproate for newly diagnosed adult epilepsy: a randomised comparative monotherapy trial. J Neurol, Neurosurgery, and Psychiatry 1995; 58: 44–50.
- [106] Komárek V, Štěrbová K. Epileptické záchvaty a syndromy dětí. Postgraduální medicína 2005; 7: 10–14.
- [107] Komárek V, Urban P, Bočan P, Rektor I. Epilepsie, kapitola V; in: Jedlička P, Keller O, et al. Speciální neurologie Praha, Galén, 2005.
- [108] Nadkarni S, Lajoie J, Devinski O. Current treatments of epilepsy. Neurology 2005 (Suppl. 3): S2–S11.
- [109] Pinder RM, Brogden RN, Speight TM, et al. Sodium valproate: a review of its pharmacological properties and therapeutic efficacy in epilepsy. Drugs 1977; 13: 81–123.
- [110] Prevey ML, Delaney RC, Cramer JA, Cattanach J. Effect of valproate on cognitive functioning. Comparison with carbamazepine. The Department of Veterans Affairs Epilepsy Cooperative Study 264 Group. Archives of Neurology Vol. 53 No. 10.
- [111] Wheless WJ. Treatment Choices of Antiepileptic Drugs in Children, AAN, 2002.
- [112] http://www.epilepsy-academy.org
- [113] http://www.eguidelines.co.uk
- [114] http://www.postgradmed.com
- [115] Společnost pro diagnostiku a léčbu bolestí hlavy. http://www.czech-hs.cz/detail_odbornik.php ?id=1031
- [116] valproic acid – Drug Evaluations, Drugdex, Micromedex, 1.2006
- [117] Suchopár J. Compendium lékových interakcí. Praha, InfoPHARM, 2005.
- [118] Sachs GS, Grossman F, Ghaemi SN, et al. Combination of a mood stabilizer with risperidone or haloperidol for treatment of acute mania: a double-blind, placebo-controlled comparison of efficacy and safety. Am J Psychiatry 2002; 159: 1146–1154.