Porovnání účinnosti profylaktik migrény v systematickém přehledu a síťové metaanalýze
Ačkoliv jsou k dispozici výsledky několika studií, které podporují efektivitu různých profylaktik migrény oproti placebu, existují zatím jen omezené důkazy pro srovnání bezpečnosti a účinnosti těchto léků. Autoři Lampl a kol. provedli systematický přehled a síťovou metaanalýzu pro snazší vzájemné porovnání přípravků pro profylaxi migrény [1].
Úvod
Migréna představuje pro jedince výrazně zatěžující a vyčerpávající onemocnění [2–4], které je rovněž spojeno s nezanedbatelnými finančními náklady [5]. K profylaxi migrény se běžně používá několik tříd léků včetně antidepresiv, antikonvulziv, antihypertenziv, gepantů a monoklonálních protilátek proti CGRP (calcitonin gene‑related peptide). Předchozí studie a systematické přehledy doložily účinnost těchto léků. Novější léky jako anti‑CGRP monoklonální protilátky a gepanty jsou i přes průkaz své účinnosti a snášenlivosti většinou dostupné za mnohem vyšší cenu oproti ostatním přípravkům, což omezuje přístup k jejich použití [6]. Řada studií zkoumala efektivitu a bezpečnost profylaktik migrény, zatím jsou však k dispozici jen omezené důkazy pro vzájemné porovnání jejich účinnosti [7–11]. Doposud byla ve studii srovnávána pouze anti‑CGRP monoklonální protilátka s topiramátem [12].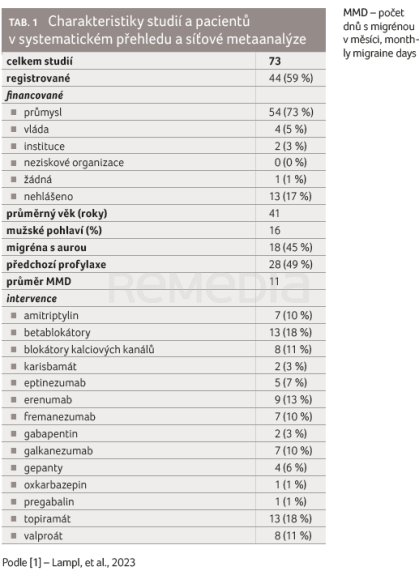
Metody a charakteristika
Autoři studie vyhledávali v databázích MEDLINE, EMBASE, CENTRAL a clinictrials.gov do srpna 2022 randomizované studie s medikací pro profylaxi migrény u dospělých jedinců. Třídění referencí, extrahování dat a posouzení rizika zkreslení (bias) probíhalo nezávisle a duplicitně. Autoři provedli síťovou metaanalýzu a ohodnotili jistotu důkazů jako vysokou, střední, nízkou nebo velmi nízkou podle systému GRADE.
Charakteristiky studií a pacientů shrnuje tabulka 1.
Výsledky metaanalýzy
Pokles počtu dní s migrénou v měsíci o 50 % a více
Celkem 57 studií, které zahrnuly 26 378 pacientů a uváděly 50% a vyšší snížení počtu dní s migrénou v měsíci (monthly migraine days, MMD), mohlo být začleněno do síťové metaanalýzy (obr. 1). Tabulka 2 a graf 1 představují výsledky síťové metaanalýzy pro porovnání s placebem. Metaanalýza prokázala, že fremanezumab, eptinezumab, erenumab, galkanezumab, gepanty a topiramát zvyšují podíl pacientů, kteří zaznamenali 50% a vyšší pokles MMD ve srovnání s placebem. Pravděpodobnost tohoto poklesu (důkaz střední jistoty) byla přiřazena k betablokátorům, valproátu a amitriptylinu; karisbamát a oxkarbazepin se pravděpodobně neliší od placeba. Důkaz nízké jistoty byl zaznamenán u gabapentinu a velmi nízké jistoty u blokátorů kalciových kanálů.
Fremanezumab se jevil jako nejpřínosnější (důkaz vysoké jistoty) ve zvyšování podílu pacientů, kteří zaznamenali 50% a vyšší redukci MMD ve srovnání s gepanty, topiramátem a karisbamátem. Fremanezumab vykazuje střední jistotu důkazů ve srovnání s amitriptylinem, betablokátory, blokátory kalciových kanálů, oxkarbazepinem, galkanezumabem, eptinezumabem, erenumabem a valproátem a nízkou jistotu důkazů ve srovnání s gabapentinem.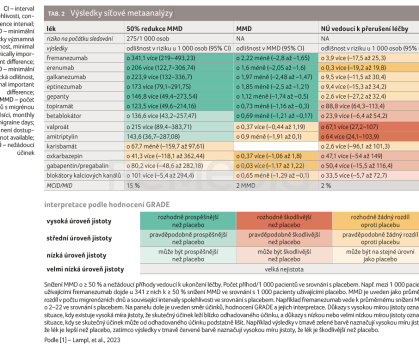
Počet dní s migrénou/bolestí hlavy za měsíc
Pro sledování počtu dní s migrénou nebo bolestí hlavy za měsíc bylo hlášeno celkem 62 studií zahrnujících 29 156 pacientů. Vysoce jistý důkaz ve srovnání s placebem byl zaznamenán u fremanezumabu, erenumabu, galkanezumabu, eptinezumabu, gepantů, topiramátu a betablokátorů; oxkarbazepin a gabapentin se neliší od placeba. Také valproát, amitriptylin a blokátory kalciových kanálů se pravděpodobně neliší od placeba (střední jistota důkazů).
Nežádoucí účinky vedoucí k přerušení léčby
Celkem v 66 studiích s 29 327 pacienty byly hlášeny nežádoucí účinky vedoucí k přerušení léčby. Autoři zaznamenali vysoce jistý důkaz, že valproát a amitriptylin mají za následek více nežádoucích účinků vedoucích k přerušení léčby ve srovnání s placebem a že erenumab se neliší od placeba. Léčba topiramátem, betablokátory, oxkarbazepinem a gabapentinem pravděpodobně vede k většímu počtu nežádoucích účinků (důkaz střední jistoty); fremanezumab, galkanezumab, eptinezumab, gepanty a karisbamát se pravděpodobně neliší od placeba. Blokátory kalciových kanálů mohou zvýšit výskyt nežádoucích účinků ve srovnání s placebem (nízká jistota důkazů).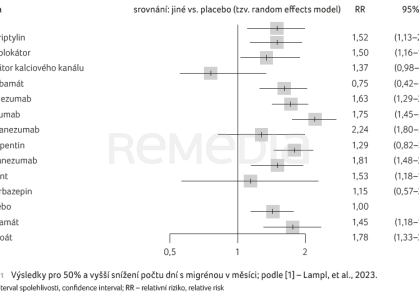
Shrnutí
Autoři metaanalýzy identifikovali 74 vhodných studií s 32 990 pacienty. Práce potvrdila vysoce jistý důkaz, že anti‑CGRP monoklonální protilátky, gepanty a topiramát zvyšují podíl pacientů s 50% nebo vyšší redukcí MMD ve srovnání s placebem. Betablokátory, valproát a amitriptylin tento podíl zvyšují v rámci důkazu střední jistoty; gabapentin se neliší od placeba (nízká jistota). V porovnání s placebem léčba valproátem a amitriptylinem vede k nežádoucím účinkům, které jsou příčinou přerušení terapie (vysoká jistota); topiramát, betablokátory a gabapentin způsobují nárůst výskytu nežádoucích účinků vedoucích k přerušení léčby (střední jistota). Metaanalýza přinesla střední až vysoce jistý důkaz, že anti‑CGRP monoklonální protilátky a gepanty nezvyšují výskyt nežádoucích účinků. Monoklonální protilátky proti CGRP mají tedy dle výsledků této práce nejlepší profil bezpečnosti a účinnosti ze všech léků na profylaxi migrény, hned za nimi následují gepanty.
Literatura
[1] Lampl C, MaassenVanDenBrink A, Deligianni CI, et al. The comparative effectiveness of migraine preventive drugs: a systematic review and network meta‑analysis. J Headache Pain 2023; 24: 56.
[2] Blumenfeld AM, Varon SF, Wilcox TK, et al. Disability, HRQoL and resource use among chronic and episodic migraineurs: results from the International Burden of Migraine Study (IBMS). Cephalalgia 2011; 31: 301–315.
[3] Steiner TJ, Stovner LJ, Katsarava Z, et al. The impact of headache in Europe: principal results of the Eurolight project. J Headache Pain 2014; 5: 31.
[4] Lampl C, Thomas H, Stovner LJ, et al. Interictal burden attributable to episodic headache: findings from the Eurolight project. J Headache Pain 2016; 7: 9.
[5] Linde M, Gustavsson A, Stovner LJ, et al. The cost of headache disorders in Europe: the Eurolight project. Eur J Neurol 2012; 19: 703–711.
[6] Siddiqui M, Shah PV, Balani P, et al. Comparing the Efficacy, Safety, and Superiority of Calcitonin Gene‑Related Peptide Monoclonal Antibodies and Botox in Preventing and Treating Migraines. Cureus 2021; 13: e13002.
[7] Mulleners WM, McCrory DC, Linde M. Antiepileptics in migraine prophylaxis: an updated Cochrane review. Cephalalgia 2015; 35: 51–62.
[8] Jackson JL, Shimeall W, Sessums L, et al. Tricyclic antidepressants and headaches: systematic review and meta‑analysis. BMJ 2010; 341: c5222.
[9] Jackson JL, Kuriyama A, Kuwatsuka Y, et al. Beta‑blockers for the prevention of headache in adults, a systematic review and meta‑analysis. PLoS ONE 2019; 14: e0212785.
[10] Stubberud A, Flaaen NM, McCrory DC, et al. Flunarizine as prophylaxis for episodic migraine: a systematic review with meta‑analysis. Pain 2019; 160: 762–772.
[11] Sacco S, Amin FM, Ashina M, et al. European Headache Federation guideline on the use of monoclonal antibodies targeting the calcitonin gene related peptide pathway for migraine prevention – 2022 update. J Headache Pain 2022; 23: 67.
[12] Reuter U, Ehrlich M, Gendolla A, et al. Erenumab versus topiramate for the prevention of migraine – a randomised, double‑blind, active‑controlled phase 4 trial. Cephalalgia 2022; 42: 108–118.