Studie ONTARGET/TRANSCEND
Léčba inhibitory ACE vede ke snížení morbidity i mortality u celé řady onemocnění. Jednou z nevýhod inhibitorů ACE je však častý výskyt vedlejších účinků, které mohou u některých pacientů limitovat jejich použití nebo snižovat adherenci k léčbě. Zvláště experimentální data ukazují, že při léčbě inhibitory ACE nedochází k plnému potlačení systému renin-angiotenzin-aldosteron. V posledních letech přibývá dokladů pro příznivé působení antagonistů angiotenzinu II v podobných indikacích, v jakých se dříve osvědčily inhibitory ACE. Výhodou antagonistů angiotenzinu II je navíc jejich vynikající tolerabilita. Při současné léčbě inhibitory ACE i antagonisty angiotenzinu II lze předpokládat úplnější potlačení osy renin-angiotenzin-aldosteron. Antagonisté angiotenzinu II se samozřejmě nabízejí jako léky první volby u pacientů, kteří netolerují inhibitory ACE.
Ve studii HOPE, do které byli zařazeni pacienti s výrazným rizikem kardiovaskulárních komplikací (věk nad 55 let, prokázané kardiovaskulární onemocnění či diabetes mellitus a přítomnost dalších rizikových faktorů, jako hypertenze, dyslipidémie, kuřáctví či mikroalbuminurie), se prokázalo statisticky významné 22% relativní snížení rizika primárního endpointu (infarkt myokardu, cévní mozková příhoda nebo kardiovaskulární smrt) při léčbě 10 mg ramiprilu denně ve srovnání s placebem. Zatím není jasné, jaká je u podobných vysoce rizikových pacientů role antagonistů angiotenzinu II, případně kombi- nace obou lékových skupin.
Hlavním cílem studie ONTARGET (Ongoing Telmisartan Alone and in Combination with Ramipril Global Endpoint Trial) je tedy zjistit u vysoce rizikových pacientů, zda kombinace 10 mg inhibitoru ACE ramiprilu a 80 mg antagonisty angiotenzinu II telmisartanu je účinnější v prevenci orgánových komplikací než léčba samotným ramiprilem v dávce 10 mg 1x denně. Dalším cílem je prokázat, že léčba samotným telmisartanem v dávce 80 mg 1x denně je minimálně stejně účinná jako léčba 10 mg ramiprilu 1x denně.
Cílem studie TRANSCEND (Telmi-sartan Randomized AssessmeNt Study in aCE iNtolerant subjects with cardiovascular Disease) je dokázat, že u pa-cientů, kteří netolerují z různých důvodů inhibitory ACE, je léčba samotným telmi-sartanem v dávce 80 mg denně účinnější než placebo. Primární endpoint obou studií je tvořen kombinací výskytu kardiovas-kulární mortality, infarktů myokardu, cévních mozkových příhod a hospitalizací pro srdeční selhání. Dalšími sledovanými ukazateli v obou studiích je např. výskyt nově diagnostikovaného srdečního selhání, revaskularizační výkony, nově diagnostikovaný diabetes mellitus, rozvoj demence či zhoršení kognitivních funkcí, vznik fibrilace síní a řada dalších. Je analyzována také řada velmi zajímavých epidemiologických a demografických dat.
V rámci programu ONTARGET/TRANSCEND je prováděno 7 podstudií (např. studie erektilní dysfunkce, ambulantního monitorování krevního tlaku, detekce poruch glukózové tolerance či analýza elastických vlastností tepen).
Zařazovací kritéria pro studii ONTARGET jsou podobná jako ve studii HOPE: pacienti starší než 55 let, kteří mají buď ischemickou chorobu srdeční, nebo ischemickou chorobu dolních končetin, nebo stav po cévní mozkové příhodě, případně TIA, nebo vysoce rizikový diabetes mellitus s prokázanými orgánovými komplikacemi.
Pro zařazení do studie TRANSCEND je navíc nutná přítomnost intolerance inhibitorů ACE.
Studie ONTARGET měla v úvodu titrační fázi k posouzení tolerability a compliance k terapii při zvyšujících se dávkách ramiprilu a telmisartanu. Pouze 1,7 % pacientů nemohlo být zařazeno pro výskyt hypotenze během titrační fáze. Po ran-domizaci pak pacienti byli sledováni po 6 týdnech a dále v intervalu 6 měsíců. Pa-cienti byli zařazováni v 730 centrech ve 40 zemích včetně České republiky. Nábor pacientů do studie ONTARGET byl ukončen v červenci 2003. Zařazování do studie TRANSCEND probíhalo pomaleji a bylo ukončeno v květnu 2004. Do konce května 2004 bylo zařazeno 25 620 pacientů do studie ONTARGET a 5 926 pacientů do studie TRANSCEND, což činí z tohoto programu jednu z největších sekundárně preventivních studií vůbec. Jedná se zároveň vlastně o první rozsáhlou klinickou studii s antagonisty angiotenzinu II u vysoce rizikové, dobře léčené populace bez přítomnosti srdečního selhání a s normálními hodnotami krevního tlaku. Česká republika přispěla k počtu pacientů významným dílem: v 10 centrech bylo zařazeno do obou studií dohromady přes 600 pacientů.
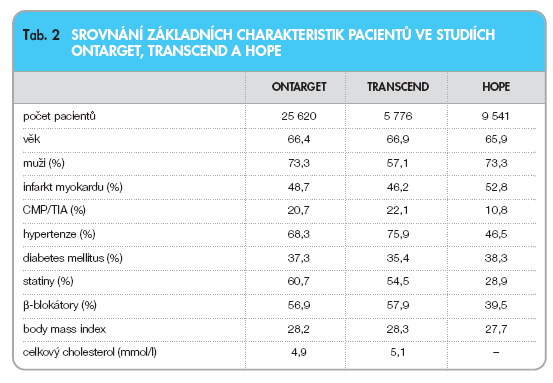
Ve srovnání se studií HOPE jsou pacienti při zařazení do programu ONTARGET/ TRANSCEND lehce starší, mají vyšší výskyt cerebrovaskulárních onemocnění v anamnéze, častěji jsou léčeni b-blokátory a hypolipidemiky. Ve studii TRANSCEND je vyšší podíl žen. Průměrné hodnoty krevního tlaku při randomizaci byly ve studii ONTARGET 134/77 mmHg a ve studii TRANSCEND 135/78 mmHg.
Minimální doba sledování pacientů ve studiích ONTARGET/TRANSCEND je 3,5 roku, takže ukončení studie a zveřejnění výsledků se dá předpokládat v průběhu roku 2007.
Seznam použité literatury
- [1] The HOPE Study Investigators. Effects of an angio-tensin-converting-enzyme inhibitor, ramipril, on CV events in high-risk patients. N Engl J Med 2000; 342: 145–153.
- [2] The ONTARGET/TRANSCEND Investigators. Ratio-nale, design, and baseline characteristics of 2 large, simple, randomized trials evaluating telmisartan, ramipril, and their combination in high-risk patients: The Ongoing Telmisartan Alone and in Combination with Ramipril Global Endpoint Trial/Telmisartan Randomized Assessment Study in ACE Intolerant Subjects with Cardiovascular Disease (ONTARGET/TRANSCEND) trials. Am Heart J 2004; 148: 52–61