Studie REACT jako důkaz dlouhodobé účinnosti alergenové imunoterapie u pacientů s respirační alergií
Souhrn:
Krčmová I. Studie REACT jako důkaz dlouhodobé účinnosti alergenové imunoterapie u pacientů s respirační alergií. Remedia 2022; 32: 380–386.
Alergenová imunoterapie (AIT) je jedinou kauzální léčbou respiračních alergií. Dlouhodobá efektivita AIT v reálné klinické praxi je však nadále otázkou diskusí. Proto jsou cenné studie typu RWE (real‑word evidence), které užívají data z reálného života a přinášejí důkazy nad rámec výsledků z randomizovaných kontrolovaných studií. REACT je retrospektivní kohortová studie využívající data z období let 2007–2017. Indikací pro zařazení do sledování byla diagnóza alergické rýmy (AR) s astmatem nebo bez něj a s léčbou či bez léčby AIT. Pro zajištění srovnatelných skupin byl soubor pacientů léčených AIT srovnán s kontrolní skupinou v poměru 1 : 1 s odpovídajícími charakteristikami. Výsledky byly analyzovány jak uvnitř skupin (před AIT vs. po AIT), tak mezi skupinami (AIT vs. kontrola) během devíti let sledování. Data 46 024 subjektů léčených AIT byla porovnána s kontrolními subjekty a 14 614 z nich bylo zahrnuto do astmatické kohorty. Při srovnání s rokem před indexem AIT bylo zjištěno konzistentní snížení předepsané farmakoterapie pro AR a astma ve srovnání s kontrolními subjekty. Navíc skupina s AIT měla významně vyšší pravděpodobnost ukončení léčby astmatu (p < 0,0001). Kromě redukce léčby astmatu ve skupině s AIT bylo prokázáno významnější snížení počtu těžkých exacerbací astmatu (p < 0,05). Zajímavým nálezem byla redukce počtu respiračních infekcí ve prospěch kohorty s AIT – snížení výskytu pneumonie se spotřebou antibiotik, četností a délkou hospitalizací. Studie REACT rozšiřuje stávající důkazy randomizovaných kontrolovaných klinických hodnocení s AIT, neboť potvrzuje dlouhodobé přetrvávání účinnosti AIT v reálné klinické praxi a její imunomodulační efekt v dlouhém časovém horizontu
Summary:
Krcmova I. REACT study as evidence of long‑term efficacy of allergen immunotherapy in patients with respiratory allergy. Remedia 2022; 32: 380–386.
Allergen immunotherapy (AIT) is the only causal treatment of respiratory allergies. However, the long‑term efficacy of AIT in real‑world clinical practice is still being discussed. Therefore, type RWE (real‑world evidence) studies that use data from real life and bring evidence beyond the framework of randomized controlled trials are valuable. The REACT study is a retrospective cohort evaluation using data from 2007 to 2017. The indication for eligibility was a diagnosis of allergic rhinitis (AR) with or without asthma and AIT. Ensuring the groups are comparable, a group of patients treated with AIT was compared with a control group in a 1 : 1 ratio with corresponding characteristics. The results were analyzed both within the groups (before AIT vs after AIT) and between groups (AIT vs control) in a 9‑year‑long observational period. The data of 46,024 subjects treated with AIT were compared with control subjects, and 14,614 were included in the asthma cohort. According to the results, compared with a year before administering AIT, a consistent decrease in prescribed pharmacotherapy for AR and asthma was found compared to control subjects. Moreover, the AIT group had a significantly higher probability of asthma treatment termination (p < 0.0001). Alongside the reduction of asthma treatment, a significant decrease in the number of severe asthma exacerbations was proved in the AIT group (p < 0.05). The interesting finding was a reduction in the number of respiratory infections in the AIT cohort – a decrease in the occurrence of pneumonia with antibiotic treatment, frequency and the length of hospitalizations. The REACT study adds to the current evidence from randomized controlled trials with AIT because it confirms the long‑term efficacy of AIT in real‑world clinical practice and its immunomodulatory effect in the long term.
Key words: allergen immunotherapy, REACT study, real‑world evidence, respiratory allergy.
Úvod
Výsledky z klinických randomizovaných kontrolovaných studií nelze plně zobecnit na širokou populaci pro přísná kritéria vstupu do těchto studií. Proto jsou následná sledování velkých souborů pacientů v rutinní klinické praxi velmi potřebná.
V odborné literatuře se
setkáváme s termíny „real world data“ (RWD)
a „real world evidence“ (RWE), které se od sebe
liší v pojetí problému. Data z reálné praxe (RWD)
jsou údaje týkající se zdravotního stavu pacientů a/nebo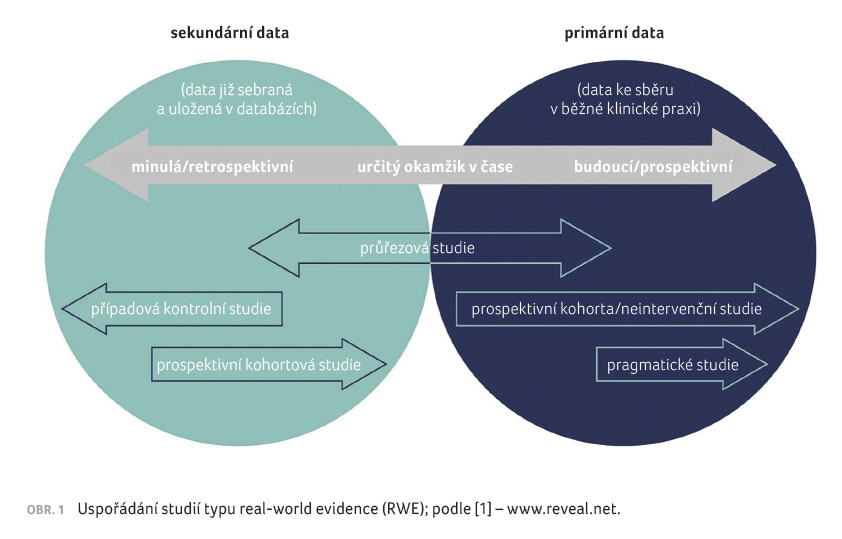 poskytování zdravotní péče, jež jsou rutinně shromažďovány
z různých zdrojů jako údaje zdravotních pojišťoven,
registry lékové či registry dle diagnóz, data generovaná
pacientem (selfmonitoring), třeba i za pomoci
telemedicíny.
poskytování zdravotní péče, jež jsou rutinně shromažďovány
z různých zdrojů jako údaje zdravotních pojišťoven,
registry lékové či registry dle diagnóz, data generovaná
pacientem (selfmonitoring), třeba i za pomoci
telemedicíny.
Pojem RWE značí skutečné důkazy z klinické praxe generované z cílených prospektivních/retrospektivních studií z reálných dat a jejich analýz. Studie RWE doplňují klinické kontrolované studie tím, že zobecňují tyto poznatky na běžnou populaci. Kromě toho může studie typu RWE poskytovat informace o dalších oblastech, jako jsou přirozený průběh choroby, důkazy účinnosti a bezpečnosti konkrétního léčivého přípravku. Důkazy získané z RWE studií hrají v současnosti významnější roli při rozhodování o zdravotní péči, přispívají ke sledování postmarketingové bezpečnosti a jsou důležité pro přijímání regulačních rozhodnutí. Vědci používají výsledky RWE studií k podpoře návrhů kontrolovaných klinických a observačních studií k vytvoření inovativních léčebných přístupů (obr. 1) [1].
Data a důkazy z reálné klinické praxe jsou tedy cenné pro získané výsledky mimo kontext randomizovaných kontrolovaných studií. Tato kritéria splňuje studie REACT, která se zabývala retrospektivním sledováním dlouhodobé účinnosti alergenové imunoterapie (AIT) u pacientů s alergickou rýmou (AR) a s astmatem či bez astmatu [2].
Alergenová imunoterapie je dosud jedinou kauzální léčbou respiračních alergií. Zvýšené tolerance vůči kauzálnímu alergenu je dosaženo opakovaným podáváním terapeutického alergenu, což má za následek modulaci imunologické odpovědi. Alergenovou imunoterapii lze podávat sublinguálně (SLIT) ve formě tablet nebo kapek (alergen v roztoku) nebo subkutánně (SCIT) po dobu minimálně tří let [3].
Jedná se o časově náročný víceletý imunomodulační proces, a právě proto jsou důkazy o dlouhodobé účinnosti AIT potřebné jak z hlediska medicínského, tak z pohledu regulačních autorit. V čase účinné farmakoterapie (ačkoliv s krátkodobým efektem) je třeba přinášet důkazy o nezastupitelném přínosu dlouhodobé imunomodulace. Randomizované kontrolované studie pro SLIT a SCIT (s obsahem alergenů pylu trav) potvrdily, že AIT může modifikovat alergické onemocnění až dva roky po ukončení léčby u pacientů s AR [4,5]. Přestože je AIT označována jako jediná kauzální léčba, víceleté údaje jsou omezené.
Respirační alergie jsou heterogenní skupinou onemocnění, která se projevují AR, alergickým bronchiálním astmatem a dalšími přidruženými chorobami, jako jsou časté respirační infekce charakteru rinosinusitid, záněty středouší apod. Je uváděno dle různých zdrojů, že 10–40 % pacientů s AR má alergické astma a naprostá převaha astmatiků má příznaky AR (60–80 %) [6,7]. Alergická rýma je dobře známým rizikovým faktorem pro obtížnou kontrolu nad astmatem. Je obecně známo, že u astmatiků s těžkou AR je 4–5krát vyšší pravděpodobnost nedostatečné kontroly astmatu [8,9].
V randomizovaných klinických studiích poskytla léčba SLIT tabletami (SQ HDM – standardizovaný extrakt z roztočů domácího prachu) u alergických astmatiků redukci dávky inhalačních kortikosteroidů (IKS) a bylo prokázáno 34% snížení relativního rizika výskytu středně těžkých až těžkých exacerbací astmatu [10,11].
Přesto je AIT stále podrobována odborné diskusi ohledně účinnosti v reálné klinické praxi, zejména pokud jde o výsledky související s astmatem. Jsou potřeba další robustní důkazy z reálného světa (RWE), aby podpořily doplňující důkazy pro stávající randomizované kontrolované studie.
Studie REACT
Metodika
REACT (Real world Effectiveness in Allergy immunotherapy) je retrospektivní observační kohortová studie [2], která využívá anonymizovaná data z období let 2007–2017 získaná z německé databáze zdravotních pojišťoven pokrývající přibližně 90 % německé populace [12].
Podmínkou pro zařazení do studie bylo potvrzení diagnózy AR s astmatem nebo bez astmatu a stav s AIT či bez AIT. Pacienti byli zahrnuti do souboru, pokud měli předpis pro léčbu AIT mezi daty 1. 1. 2008 až 31. 12. 2016, aby byla umožněna dostupnost dat před podáváním AIT a po AIT nejméně jeden rok. Studie byla provedena v souladu s evropskými a německými předpisy o ochraně dat a byla předregistrována na webu clinictrials.gov (NCT04125888). Základní populaci studie tvořili jedinci s AR s astmatem nebo bez astmatu a souběžně léčení AIT (skupina s AIT) a kontrolní skupina s obdobnými parametry bez léčby AIT. Potvrzená diagnóza AR musela být uvedena pro obě skupiny. Kritéria způsobilosti pro skupinu s AIT představovaly dva po sobě jdoucí recepty stejné AIT během období identifikace osob. Vylučovacím kritériem pro obě skupiny byla preskripce AIT během období před započetím sledování. Soubor studie se skládal ze tří kohort (hlavní kohorta, kohorta s již existujícím astmatem a kohorta bez astmatu), z nichž každá zahrnovala subjekty léčené AIT a jejich odpovídající kontrolní subjekty s obdobnými charaktekteristikami (věk, pohlaví, AR, astma) [2].
Výběru souboru a kohort byla
věnována mimořádná pozornost. Od roku 2007 do roku
2017 mělo alespoň jeden předpis AIT celkem 115 098 alergiků
z 5 983 511 osob v databázi. Z tohoto počtu bylo
47 440 alergiků s preskripcí AIT způsobilých pro studii
a bylo zahrnuto spolu s 1 003 332 kontrolních subjektů
s diagnózou AR a bez AIT 12 měsíců před datem indexu.
Bylo důležité, aby byly dobře vyváženy obě kohorty splňující
předem specifikovaná kritéria standardizovaných průměrných
rozdílů < 10 % pro všechny proměnné. Konečná
kohorta s AIT tedy zahrnovala 46 024 pacientů odpovídajících
v poměru 1 : 1 kontrolním subjektům, což vedlo k hlavní
kohortě 92 048 osob. Léčení jedinci byli porovnáváni
s neléčenými jedinci s obdobnými demografickými
a zdravotními údaji [2]. Všechny modifikace proběhly před
uzamčením kohorty a analýzou výsledků (obr. 2)
[2,13].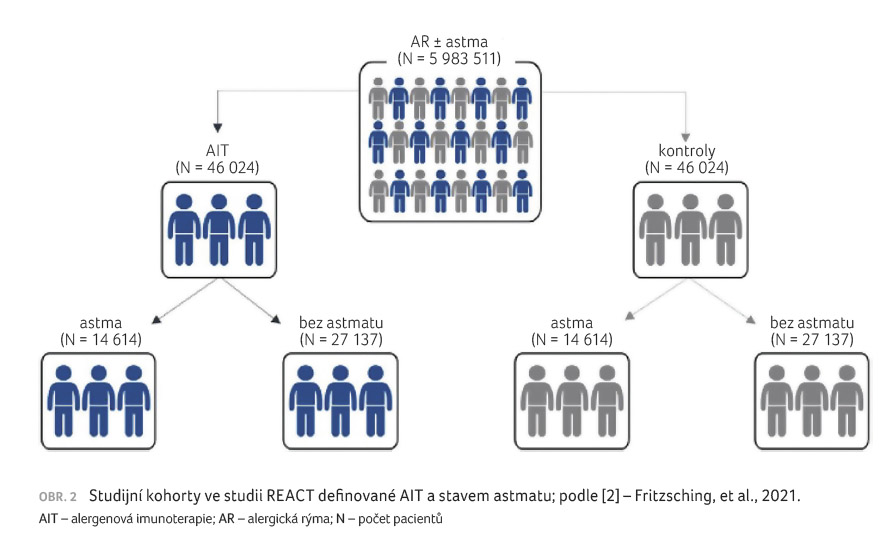
V hlavní kohortě měli pacienti ve skupině s AIT průměrný věk 29,5 (16,3) roku, 53 % tvořili muži. Subjekty léčené AIT byly vystaveny léčbě AIT v průměru 549 (284) dnů.
Z hlavní kohorty bylo 29 228 subjektů zahrnuto do kohorty s již existujícím astmatem a 54 274 do kohorty bez astmatu. Jedinci s preexistujícím astmatem byli převážně na 1.–3. kroku léčby astmatu. Navíc 16 % osob mělo alespoň jednu těžkou exacerbaci astmatu.
V kohortě s AIT byly dle způsobu aplikace alergenu uvedeny tyto počty: N = 36 927 pro SCIT; N = 4 816 pro SLIT (kapky) a N = 3 754 pro SLIT (tablety). Podskupiny dle druhu léčebného alergenu zahrnovaly následující počty: 11 713 osob aplikovalo alergen pylu trav, 7 774 osob alergen roztočů domácího prachu a 11 897 osob alergen pylu stromů, celkem 9 726 pacientů aplikovalo alergeny s jiným obsahem. Index AIT (předpis) mohl být určen pouze ve skupině s AIT, proto bylo kontrolním subjektům přiřazeno stejné datum indexu jako subjektům ve skupině s AIT [2].
Primárním cílovým ukazatelem studie REACT byla preskripce pro diagnózu AR v každém roce. Sekundárními cílovými ukazateli byly preskripce pro diagnózu astmatu, těžké exacerbace astmatu a změna kroků v léčbě astmatu dle tíže. V kohortě bez astmatu byl jako údaj hodnocen nový nástup astmatu. K posouzení změn v léčbě astmatu byly použity diagnostické kódy pro astma a použití kontrolních léků napodobujících kroky GINA (Globální iniciativa pro astma). Spotřeba úlevových krátkodobě působících beta2 agonistů (short acting beta2 agonist, SABA) byla uvedena samostatně. Významné výsledky průzkumu zahrnovaly využití zdrojů zdravotní péče, náklady na nemocenskou dovolenou a frekvenci infekcí dýchacích cest. Byly zahrnuty analýzy podskupin napříč různými populacemi a léčebnými modalitami. V hlavní analýze postačoval jeden předpis během jednoho roku, aby byl kvalifikován léčebný krok v rámci stejné lékové skupiny [2].
Statistická metodika je uvedena v Dodatkovém protokolu Plán statistické analýzy.
Výsledky
V hlavní kohortě bylo jak
ve skupině AIT, tak v kontrolní skupině zaznamenáno
snížení preskripce pro AR na subjekt během celého sledování
ve srovnání s rokem před indexem. Kohorta s AIT
však byla spojena s výraznější redukcí sledované
preskripce v průběhu devíti let ve srovnání
s kontrolní skupinou (graf 1) [2,13]. Celkové snížení
bylo konzistentní napříč třídami léků, ale bylo výraznější
u antihistaminik ve srovnání s intranazálními
kortikosteroidy. Kohorta s AIT v období 1.–4. roku
absolvovala více návštěv ambulantní péče (včetně návštěv
specialistů) ve srovnání s kontrolní kohortou, což je
pochopitelné vzhledem k probíhající AIT (graf 1)
[2,13].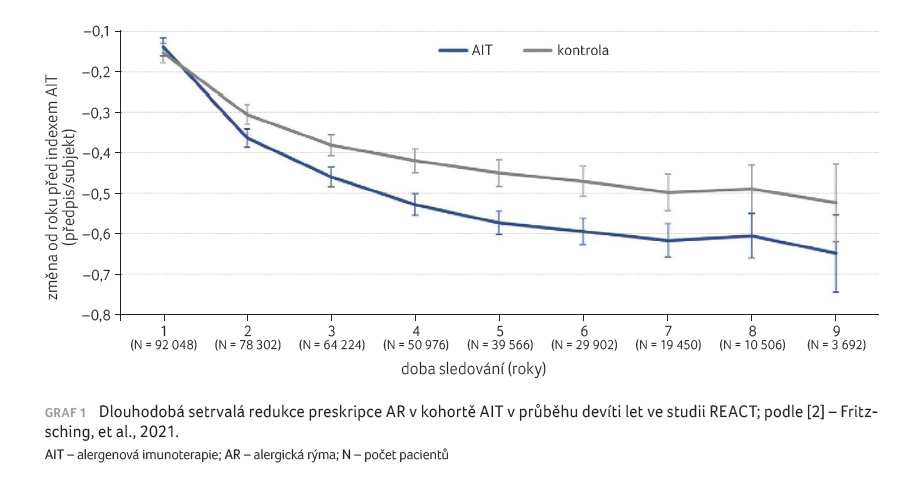
V astmatické kohortě bylo prokázáno ve skupině s AIT vyšší snížení preskripce antiastmatických léků ve srovnání s kontrolní skupinou po dobu devíti let sledování. Rozdíly mezi skupinami v preskripci léků byly způsobeny redukcí předepisování úlevových léků (SABA) a kombinace IKS/dlouhodobě působících beta2 agonistů (long acting beta2 agonist, LABA). Významnější redukce preskripce antiastmatik u subjektů léčených AIT měla za následek významně vyšší pravděpodobnost ukončení léčby astmatu ve všech letech sledování. Analýzy citlivosti pro kroky léčby astmatu byly méně robustní, nicméně pravděpodobnost ukončení léčby zůstala významná ve prospěch AIT zejména ve 4.–6. roce (graf 2) [2,13].
V astmatické skupině s AIT
nehrozilo žádné zvýšené riziko zintenzivnění léčby astmatu,
protože pravděpodobnosti byly obdobné mezi AIT a kontrolní
skupinou v průběhu let sledování. Čas do prvního
zintenzivnění léčby ukázal významně nižší riziko pro
skupinu AIT (p < 0,0001). Subjekty léčené AIT
měly souběžně nižší pravděpodobnost výskytu těžké
exacerbace astmatu. Tato zjištění byla podpořena dobou do první
a dobou do jakékoliv exacerbace astmatu v kohortě
s již existujícím astmatem (graf 3) [2,13]. V kohortě
s AIT bez astmatu byl počet předepsaných antiastmatik
v průběhu času nízký, preskripce antiastmatik v kontrolní
skupině měla tendenci se zvyšovat.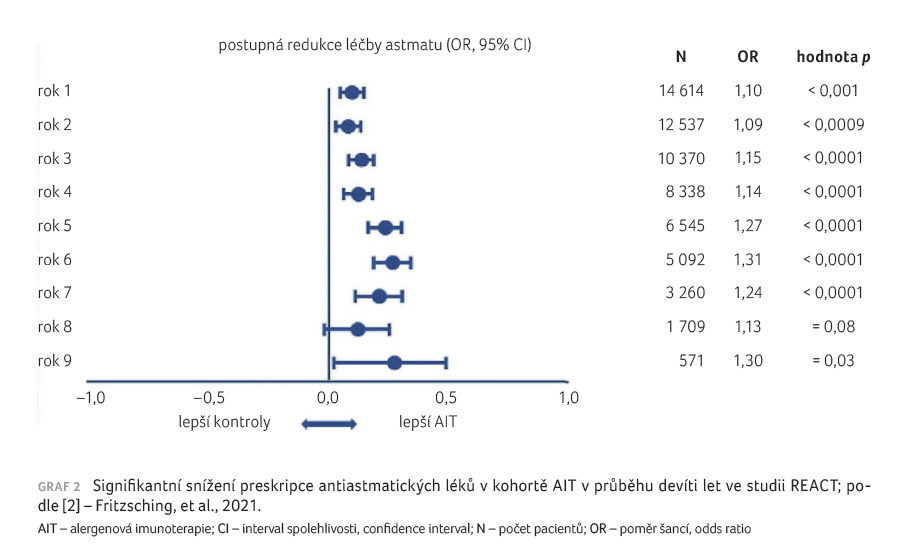
V kohortě s AIT ve srovnání
s kontrolní skupinou byl doložen nižší výskyt infekce
dýchacích cest s užíváním antibiotik, nižším počtem
návštěv a pobytů v nemocnici, nákladů
na hospitalizaci. Podobně jako u návštěv ambulantní
péče byly nárůsty celkových nákladů na zdravotní péči
vyšší po třech letech sledování ve skupině s AIT,
zatímco po pěti a devíti letech celkové náklady
na zdravotní péči vzrostly více v kontrolní skupině.
Diagnostické kódy pro klíčové komorbidity související
s astmatem, jako jsou bronchitida a chronický kašel, byly
také nižší ve skupině s AIT (graf 4A, B) [2].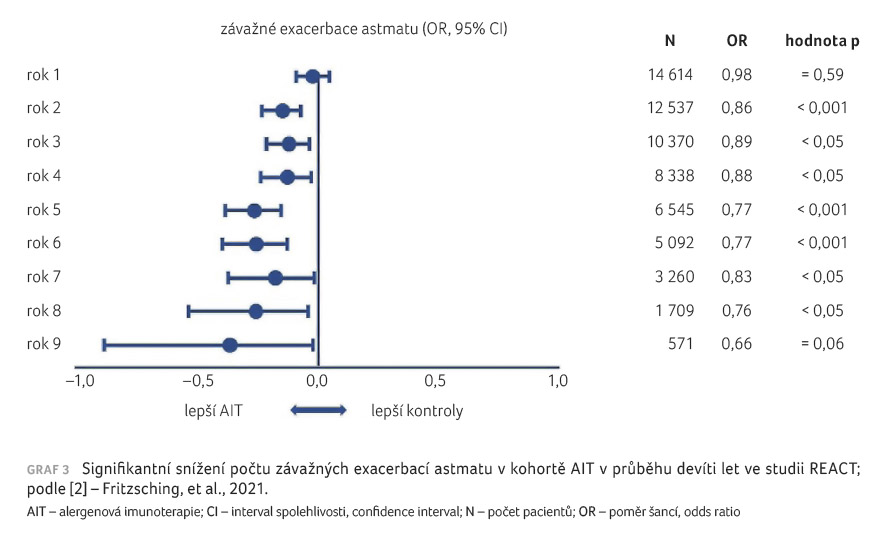
Celkový počet případů anafylaxe byl nízký. Mezi alergiky léčenými AIT bylo zaznamenáno celkem 33 případů: 30 z 36 927 alergiků léčených SCIT, 2 ze 4 816 subjektů léčených SLIT kapkami a 1 z 3 754 pacientů léčených SLIT tabletami.
Diskuse
REACT je dosud největší
a nejkomplexnější studií účinnosti AIT v reálné
praxi, která prokazuje trvalé a dlouhodobé snižování
užívání léků na AR i astma, zlepšenou kontrolu
astmatu, prevenci exacerbací astmatu a infekcí dýchacích
cest [2]. Chorobu modifikující účinky AIT byly již dříve
potvrzeny trvalým zmírněním symptomů a redukcí užívání
symptomatických léků dva roky po tříleté léčbě SLIT
tabletami SQ (extrakt pylu bojínku) v randomizované studii
kontrolované placebem [4]. Ve studii REACT byla účinnost AIT
potvrzena dalším snížením medikace AR ve skupině s AIT
během devíti let sledování, což prokázalo dlouhodobé a trvalé
účinky podstatně přesahující období sledování
z randomizovaných studií [2]. Alergenová imunoterapie je
považována za kauzální terapii, proto mají dlouhodobá
sledování zásadní význam.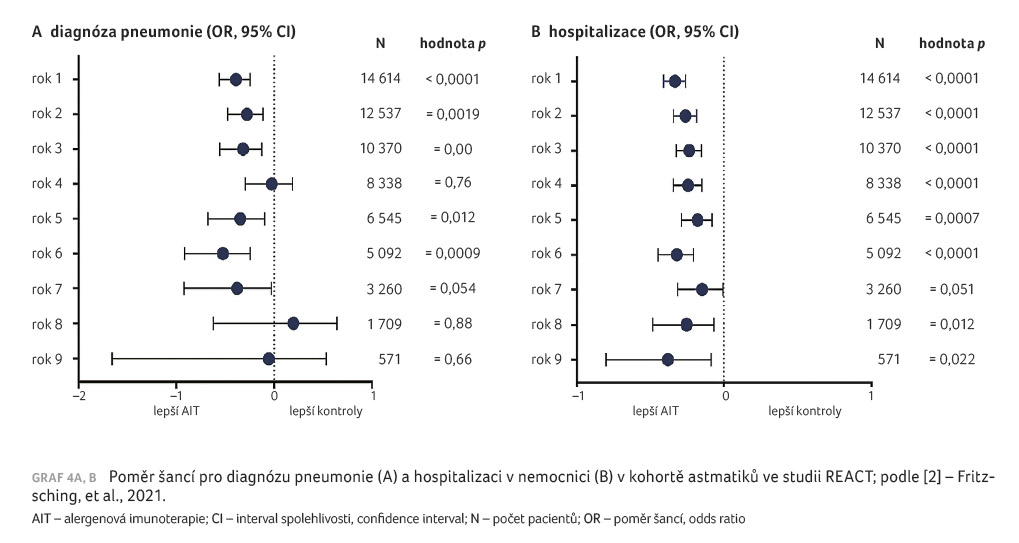
Dosud dvě velké randomizované kontrolované studie s tabletami s obsahem alergenu roztočů domácího prachu (SLIT tablety 12SQ HDM) potvrdily účinnost AIT v léčbě alergického astmatu. Bylo dokladováno významné snížení denní dávky IKS ve srovnání s placebem a významné snížení rizika středně těžké až těžké exacerbace astmatu [10,11]. V současné studii bylo u pacientů léčených AIT s AR a s astmatem zaznamenáno významné snížení jak kontrolní, tak úlevové medikace, což souvisí se zlepšenou kontrolou astmatu. Současně byla doložena vyšší pravděpodobnost ukončení léčby astmatu v kohortě s AIT v průběhu devíti let observace [2]. Vzhledem k příznivým výsledkům lze usuzovat, že AIT účinně zabraňuje progresi astmatu. Zajímavé je, že příznivé účinky AIT z hlediska astmatu byly zjištěny u populace s méně závažným astmatem (pouze 4 % astmatiků byla ve 4. léčebném kroku). To podporuje hypotézu, že AIT může být schopna zabránit progresi z mírného na těžší astma a měla by být zvážena dříve při léčbě alergických pacientů s astmatem [14].
U alergiků léčených AIT byla menší pravděpodobnost výskytu infekcí dýchacích cest vyžadujících antibiotika. Infekce dýchacích cest a alergie jsou známými rizikovými faktory pro exacerbace astmatu. Tato zjištění jsou dále podpořena důkazy i z dalších studií [15]. Klinické přínosy AIT pozorované u AR a astmatu byly podpořeny snížením počtu a délky hospitalizací a souvisejících nákladů. Byla zaznamenána nízká frekvence případů anafylaxe.
Několik studií typu RWE také posuzovalo nástup astmatu s protichůdnými výsledky [16–18]. Vzhledem k různým použitým metodologiím a definicím a kvůli riziku zkreslení v těchto studiích je těžké dělat obecné závěry. Alergici s AIT byli v některých studiích léčeni především SCIT, která se podává ambulantně, a proto měly skupiny s AIT více odborných návštěv, zejména během tříletého období léčby AIT. Protože nový nástup astmatu vyžadoval ve studiích potvrzenou diagnózu astmatu, vyšší frekvence návštěv specialistů mohla vést k tomu, že ve skupině s AIT byla kódována vyšší frekvence astmatu, přestože preskripce pro astma zůstala ve skupině s AIT ve srovnání s kontrolní skupinou nižší.
REACT byla registrovanou studií a všechny výsledky a statistické analýzy byly předem specifikovány v protokolu. Mezi silné stránky studie patří shoda kohorty s AIT a kontrolního souboru zdokumentovaná a uzamčená před analýzou výsledků, dále předem definované kroky validace výsledků, robustnost kohort a výsledků (i mezi podskupinami) a dlouhodobé sledování [2].
Studie REACT může z hlediska metodiky mít i svá určitá omezení:
- Při hodnocení účinnosti AIT pomocí vyplněných receptů chybějí informace o kontrole symptomů subjektů.
- Mnoho léků na AR je k dispozici také jako volně prodejné léky, a proto nejsou zachyceny v databázi.
- Preskripce nemusí nutně znamenat užívání léků.
Další omezení sledování ve studii REACT může představovat fakt, že zvýšený počet návštěv u specialistů může znevýhodnit skupinu s AIT. Vyšší počet návštěv ve skupině s AIT může vést k vyššímu podílu jedinců s preskripcí ve srovnání s kontrolní skupinou. Přestože alergici léčení AIT měli vyšší pravděpodobnost získání preskripce než kontrolní kohorta, vykázali významnější redukci předpisu pro AR na jedince.
Závěr
Přestože AIT je v současnosti jedinou kauzální léčbou inhalačních alergií, víceleté údaje o její účinnosti jsou omezené. Studie REACT díky přísné metodologii, velkému vzorku a dlouhodobému sledování podpořila existující důkazy a přidala nové informace o účincích AIT nad rámec omezeného časového sledování z randomizovaných kontrolních studií.
Ve srovnání s rokem před započetím sledování byla kohorta AIT konzistentně spojena s výraznější redukcí preskripce pro diagnózu AR a astmatu ve srovnání s kontrolními subjekty bez AIT, včetně antiastmatické léčby (jak kontrolní, tak úlevové). Skupina s AIT měla významně vyšší pravděpodobnost ukončení léčby pro diagnózu astmatu (p < 0,0001). Kromě snížení léčby astmatu ve skupině s AIT byla prokázána významnější redukce těžkých exacerbací astmatu (p < 0,05), stejně tak respiračních infekcí a snížení spotřeby antibiotik [2]. Důkazy zjištěné ve studii REACT zdůraznily AIT jako bezpečnou a účinnou kauzální léčbu pacientů s respiračními alergiemi.
Seznam použité literatury
- [1] https://www.reveal.net
- [2] Fritzsching B, Contoli M, Porsbjerg C, et al. Long‑term real‑world effectiveness of allergy immunotherapy in patients with allergic rhinitis and asthma: Results from the REACT study, a retrospective cohort study. Lancet Reg Health Eur 2021; 13: 100275.
- [3] Roberts G, Pfaar O, Akdis CA, et al. EAACI Guidelines on Allergen Immunotherapy: allergic rhinoconjunctivitis. Allergy 2018; 73: 765–798.
- [4] Durham SR, Emminger W, Kapp A, et al. SQ‑standardized sublingual grass immunotherapy: confirmation of disease modification 2 years after 3 years of treatment in a randomized trial. J Allergy Clin Immunol 2012; 129: 717–725.e5.
- [5] Durham SR, Walker SM, Varga EM, et al. Long‑term clinical efficacy of grass‑pollen immunotherapy. N Engl J Med 1999; 341: 468–475.
- [6] Bousquet J, Hellings PW, Agache I, et al. Allergic Rhinitis and its Impact on Asthma (ARIA) Phase 4 (2018): change management in allergic rhinitis and asthma multimorbidity using mobile technology. J Allergy Clin Immunol 2019; 143: 864–879.
- [7] GINA. Global Strategy for Asthma Management and Prevention 2021; https://ginasthma.org/
- [8] Bousquet J, Van Cauwenberge P, Khaltaev N. Allergic rhinitis and its impact on asthma. J Allergy Clin Immunol 2001; 108(5 Suppl): S147–334.
- [9] Braido F, Baiardini I, Brandi S, et al. Allergic rhinitis and asthma ad hoc survey: clinical and psychological perspectives. Clin Exp Allergy 2007; 37: 788–793.
- [10] Mosbech H, Deckelmann R, de Blay F, et al. Standardized quality (SQ) house dust mite sublingual immunotherapy tablet (ALK) reduces inhaled corticosteroid use while maintaining asthma control: a randomized, double‑blind, placebo‑controlled trial. J Allergy Clin Immunol 2014; 134: 568–575.e7.
- [11] Virchow JC, Backer V, Kuna P, et al. Efficacy of a House Dust Mite Sublingual Allergen Immunotherapy Tablet in Adults With Allergic Asthma: a Randomized Clinical Trial. JAMA 2016; 315: 1715–1725.
- [12] Busse R, Blumel M, Knieps F, Barnighausen T. Statutory health insurance in Germany: a health system shaped by 135 years of solidarity, self‑governance, and competition. Lancet 2017; 390: 882–897.
- [13] Fritzsching B. The REACT study: Long‑term effectiveness of AIT in the real world. Presented at eSOSA (Symposium on Specific Allergy) 2021 July 4.
- [14] Schmitt J, Wustenberg E, Kuster D, et al. The moderating role of allergen immunotherapy in asthma progression: results of a population‑based cohort study. Allergy 2020; 75: 596–602.
- [15] Woehlk C, von Bulow A, Kriegbaum M, et al. Allergic asthma is associated with increased risk of infections requiring antibiotics. Ann Allergy Asthma Immunol 2018; 120: 169–176.e1.
- [16] Zielen S, Devillier P, Heinrich J, et al. Sublingual immunotherapy provides long‑term relief in allergic rhinitis and reduces the risk of asthma: a retrospective, real‑world database analysis. Allergy 2018; 73: 165–177.
- [17] Schmitt J, Schwarz K, Stadler E, Wustenberg EG. Allergy immunotherapy for allergic rhinitis effectively prevents asthma: results from a large retrospective cohort study. J Allergy Clin Immunol 2015; 136: 1511–1516.
- [18] Wahn U, Bachert C, Heinrich J, et al. Real‑world benefits of allergen immunotherapy for birch pollen‑associated allergic rhinitis and asthma. Allergy 2019; 74: 594–604.