Těžké formy psoriázy léčené ustekinumabem
Psoriáza je jednou z nejčastějších dermatologických chorob, postihuje 2–3 % středoevropské populace. Možnosti léčby jsou lokální nebo celkové, často ve vzájemné kombinaci. Klasická systémová terapie zahrnuje fototerapii (UVB záření, PUVA – psoralen a UVA záření), methotrexát, cyklosporin a acitretin. Nejnovější skupinu systémových léčiv tvoří tzv. biologika. Zde uvádíme dva případy těžké formy psoriázy, které byly úspěšně léčeny biologickou léčbou po předchozím selhání klasické systémové terapie.
Úvod
Psoriáza je jednou z nejčastějších dermatologických chorob. Jedná se o chronické zánětlivé onemocnění postihující 2–3 % středoevropské populace. I když přesná etiologie není dosud známa, předpokládá se genetický podklad onemocnění, kdy u predisponovaných jedinců dojde ke spuštění patogenetických pochodů, ve kterých mají zásadní roli T lymfocyty [1]. Choroba neohrožuje život pacienta přímo, avšak má nesporný vliv na fyzické, sociální a psychické aspekty života [2]. Dle současného hodnocení jsou pacienti se středně těžkou až těžkou psoriázou řazeni na druhé místo v žebříčku negativního dopadu chorob na kvalitu života – hned za depresí – a jejich postižení je srovnatelné s jinými závažnými onemocněními (revmatoidní artritida, malignity, choroby srdce) [3].
V současné době již víme, že lupénka není omezena pouze na kožní povrch, ale je rovněž spojena s řadou komorbidit, jakými jsou psoriatická artritida (přibližně 25 %), Crohnova choroba, ulcerózní kolitida, Bechtěrevova choroba a zejména nemoci tzv. metabolického syndromu, jako je např. diabetes mellitus 2. typu, arteriální hypertenze nebo dyslipidemie, což může snížit délku života psoriatika o 3,5 roku až deset let ve srovnání se zdravou populací [4].
Vzhledem ke chronickému průběhu onemocnění je naším hlavním cílem dlouhodobá kontrola choroby, v ideálním případě dosažení úplného vymizení psoriatických ložisek. Možnosti léčby jsou lokální nebo celkové, často ve vzájemné kombinaci. Klasická systémová terapie zahrnuje fototerapii (UVB záření; PUVA, tj. psoralen a UVA záření), podávání methotrexátu, cyklosporinu a acitretinu [5].
Nejnovější skupinu systémových léčiv tvoří tzv. biologika. Tyto látky cíleně interferují na molekulární úrovni s patogenetickými pochody vzniku psoriázy. Biologická terapie je určena pouze pro středně závažné až závažné ložiskové formy psoriázy s postižením více než 10 % povrchu těla, u kterých nebyla jiná celková terapie dostatečně účinná, případně je tato terapie kontraindikována nebo ji pacient netoleruje [6]. Dostupnou biologickou léčbu psoriázy lze rozdělit podle mechanismu působení do dvou skupin: léky blokující nádor nekrotizující faktor alfa (TNFα) – adalimumab, etanercept, infliximab – a léky blokující interleukin 12 a 23 (IL-12/23) – ustekinumab [7].
Ustekinumab
Ustekinumab představuje první biologikum v nové třídě biologických léků, které cíleně inhibují účinek IL-12 a IL-23. Stejně jako ostatní biologika je i ustekinumab indikován k léčbě středně závažné až závažné ložiskové formy psoriázy u dospělých pacientů, u kterých nebyla jiná systémová terapie – konkrétně retinoidy, cyklosporin, methotrexát nebo fototerapie – dostatečně účinná, případně je tato terapie kontraindikována nebo ji pacient netoleruje.
Heterodimerické cytokiny IL-12 a IL-23, které mají identickou podjednotku p40, patří mezi klíčové regulátory v patogenezi psoriázy. Ustekinumab je plně humanizovaná monoklonální protilátka IgG1κ, která se váže specificky a s vysokou afinitou na tuto společnou podjednotku p40 a inhibuje tak aktivitu obou interleukinů tím, že jim zabraňuje navázat se na receptor (protein IL-12Rβ1) exprimovaný na povrchu imunitních buněk. IL-12 a IL-23
jsou vylučovány buňkami aktivovanými antigeny, jako jsou makrofágy a dendritické buňky, a podílejí se na imunitní odpovědi tím, že přispívají k aktivaci „přirozených zabíječů“ (NK buněk, z angl. natural killer) a k diferenciaci a aktivaci CD4+ T buněk. Ustekinumab zabraňuje IL-12 a IL-23, aby se podílely na aktivaci imunitních buněk, čímž přerušuje signály a kaskády cytokinů, které jsou relevantní pro patogenezi psoriázy, v časnější fázi než přípravky
anti-TNFα.
Podávání ustekinumabu je subkutánní, aplikuje se nejprve po čtyřech týdnech od prvního podání a dále jednou za 12 týdnů, což je velmi výhodné zejména pro pacienty, kteří dojíždějí do centra biologické léčby z větší vzdálenosti. Pokud pacient váží do 100 kg, aplikuje se jedna injekce 45 mg, u pacientů s tělesnou hmotností nad 100 kg jsou potřeba dvě injekce. Dle dosavadních klinických zkušeností je dávka 45 mg účinná i u pacientů vážících více než 100 kg, ale zpravidla měsíc až dva týdny před aplikací další dávky dochází k postupnému zhoršení projevů psoriázy, proto se doporučuje dodržovat výše uvedené dávkování.
Odpověď PASI-75 (75% zlepšení indexu plochy postižení a závažnosti psoriázy, Psoriasis Area and Severity Index, oproti výchozímu stavu) nastala při dávce 45 mg ustekinumabu již po 12 týdnech (po dvou injekcích). Maximální hodnota PASI skóre může být 72, minimální je 0 (kompletní remise). Plný účinek léčby (PASI-75 bylo dosaženo u 70–79 % pacientů) byl v obou studiích fáze III pozorován v 28. týdnu. Údaje z klinických studií vypovídají také o účinku na psoriatické nehty. V první „head to head“ klinické studii s biologiky byl ustekinumab účinnější než etanercept. Při přerušení a opětovném zahájení léčby nedochází ke ztrátě účinnosti a při opakovaném podávání ustekinumabu je léčba účinná stejně jako na začátku. Tvorba protilátek se objevila u 5 % pacientů [8].
Kazuistika 1
Jedná se o 40letého pacienta trpícího lupénkou od 13 let, který se dále léčil s arteriální hypertenzí, hyperlipidemií, hyperurikemií a diabetem 2. typu. Pacient byl silně obézní – hmotnost 132 kg při výšce 182 cm (body mass index, BMI, 39,9 – ted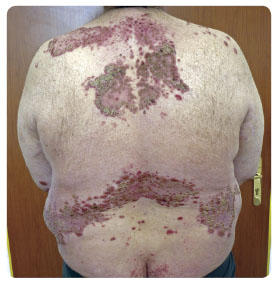 y na hranici monstrózní obezity). V předchozí systémové terapii byly použity retinoidy a fototerapie – obojí bez efektu – a cyklosporin A, který musel být pro zhoršení renálních funkcí vysazen. Při vstupním vyšetření byly pacientovi vypočítány následující hodnoty: BSA = 30 % (BSA – Body Surface Area, index hodnocení rozsahu postižené plochy kůže), PASI = 38 (obr. 1). Screeningová vyšetření na tuberkulózu, hepatitidy a HIV byla negativní.
y na hranici monstrózní obezity). V předchozí systémové terapii byly použity retinoidy a fototerapie – obojí bez efektu – a cyklosporin A, který musel být pro zhoršení renálních funkcí vysazen. Při vstupním vyšetření byly pacientovi vypočítány následující hodnoty: BSA = 30 % (BSA – Body Surface Area, index hodnocení rozsahu postižené plochy kůže), PASI = 38 (obr. 1). Screeningová vyšetření na tuberkulózu, hepatitidy a HIV byla negativní.
Vzhledem k hmotnosti pacienta byla zahájena terapie ustekinumabem v dávce 90 mg s.c. Již při první kontrole po jednom měsíci, kdy se pacient dostavil k aplikaci druhé dávky přípravku, bylo vidět značné zlepšení, PASI se zlepšilo o 75 %. P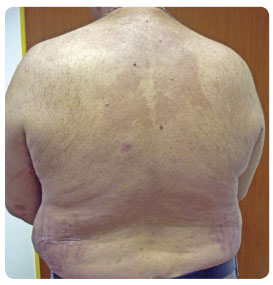 ři následující návštěvě po 16 týdnech pacient dosáhl téměř PASI-100
ři následující návštěvě po 16 týdnech pacient dosáhl téměř PASI-100
(kompletní vymizení ložisek lupénky – obr. 2). V současné době, po více než třech letech, je pacient léčen stále stejným biologickým přípravkem a i přes přidružené komorbidity, které mohou zhoršovat účinnost terapie (zejména jeho obezita), je skóre PASI stabilně udržováno na 90% zlepšení oproti stavu na počátku terapie. Laboratorní hodnoty zůstávají bez patologického nálezu, renální funkce se zlepšily po vysazení cyklosporinu a přechodu na biologickou terapii. Pacient je se svým stavem velmi spokojen.
Kazuistika 2
Jedná se o 26letou pacientku, která trpí od 12 let lupénkou a naši kliniku navštívila při akutní exacerbaci tohoto onemocnění. V posledních čtyřech týdnech byla pacientka téměř v erytrodermickém stavu. Ložiska se nacházela na cca 95 % povrchu těla, stěžovala si na silné svědění a pálení kůže. Při fyzikálním vyšetření byly zjištěny otoky bilaterálně na obou dolních končetinách, které doprovázely výše uvedenou erytrodermii. Interní příčina otok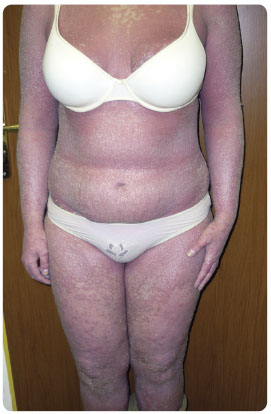 ů byla vyloučena. Pacientka se kromě psoriázy s ničím dlouhodobě neléčila. V minulosti, kdy její projevy nebyly takového rozsahu, docházela na fototerapii s dobrým efektem, ale zpravidla měsíc po jejím ukončení nastávala recidiva projevů. V její rodině trpí lupénkou i její bratr.
ů byla vyloučena. Pacientka se kromě psoriázy s ničím dlouhodobě neléčila. V minulosti, kdy její projevy nebyly takového rozsahu, docházela na fototerapii s dobrým efektem, ale zpravidla měsíc po jejím ukončení nastávala recidiva projevů. V její rodině trpí lupénkou i její bratr.
Zahájili jsme léčbu cyklosporinem v dávce 300 mg denně, ale ani po 12 týdnech podávání cyklosporinu nebylo pozorováno výraznější zlepšení, navíc se objevily i kolísavé hodnoty krevního tlak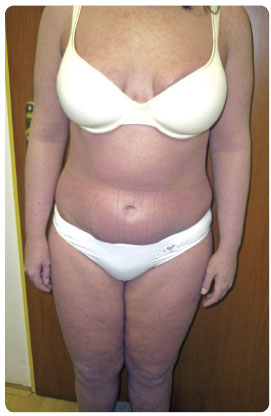 u, a proto jsme se rozhodli přejít na biologickou léčbu. Screening na tuberkulózu, hepatitidy a HIV byl negativní. Pacientce byly vypočítány následující hodnoty: BSA = 93 % a PASI = 42 (obr. 3). Zahájili jsme terapii ustekinumabem v dávce 45 mg (hmotnost 89 kg). Již po čtyřech týdnech bylo pozorováno dramatické zlepšení stavu, vznik nových ložisek byl zastaven a stávající začala rychle blednout a ustupovat. Po 16 týdnech bylo dosaženo PASI-90, jež přetrvává dodnes (déle než dva roky trvající terapie ustekinumabem – obr. 4). Její stav je stabilní, nemocná dochází na pravidelné aplikace ustekinumabu jednou za 12 týdnů, laboratorní hodnoty jsou v normě.
u, a proto jsme se rozhodli přejít na biologickou léčbu. Screening na tuberkulózu, hepatitidy a HIV byl negativní. Pacientce byly vypočítány následující hodnoty: BSA = 93 % a PASI = 42 (obr. 3). Zahájili jsme terapii ustekinumabem v dávce 45 mg (hmotnost 89 kg). Již po čtyřech týdnech bylo pozorováno dramatické zlepšení stavu, vznik nových ložisek byl zastaven a stávající začala rychle blednout a ustupovat. Po 16 týdnech bylo dosaženo PASI-90, jež přetrvává dodnes (déle než dva roky trvající terapie ustekinumabem – obr. 4). Její stav je stabilní, nemocná dochází na pravidelné aplikace ustekinumabu jednou za 12 týdnů, laboratorní hodnoty jsou v normě.
Diskuse
V obou prezentovaných případech vedlo podání biologické terapie ke zlepšení stavu pacientů, které úspěšně přetrvává několik let (u prvního případu déle než tři roky a u druhého přes dva roky). Jak již bylo zmíněno výše, psoriáza je spojena s řadou komorbidit. Přidružená onemocnění jsou vždy potenciálním rizikem snížení účinnosti biologické terapie. Jedním z takových onemocnění je i obezita. Proto u pacientů s obezitou vždy vyvstává otázka, nakolik bude jejich léčba úspěšná, zejména u pacientů s hmotností převyšující 100 kg, jejichž prevalence dosahuje mezi všemi nemocnými s psoriázou 25–30 % [9]. Kromě infliximabu a ustekinumabu mají všechny ostatní biologické přípravky fixně stanovenou dávku, která nezohledňuje hmotnost pacientů. I proto jsme se rozhodli v našem konkrétním případě zvolit jako léčivo ustekinumab. U pacientů s hmotností vyšší než 100 kg je schéma aplikace totožné, ale podává se 90 mg, tj. dvojnásobné množství léčiva. Přiložená fotodokumentace ukazuje, že efekt léčby byl velmi uspokojivý i přes těžkou obezitu našeho pacienta (132 kg).
Prevalence erytrodermické formy psoriázy se odhaduje na 1–2,25 % u psoriatických pacientů [10, 11]. Pokud jejich stav progreduje do tohoto stadia, jsou ohroženi řadou závažných komplikací, a jejich léčba proto musí být rychlá a razantní. Přestože je obecně účinnost léčby biologiky velmi vysoká, u pacientů v erytrodermii tomu tak nemusí být. Z recentních studií vyplývá, že ustekinumab je velmi dobrým kandidátem pro zvládnutí této závažné formy psoriázy, protože si zachovává účinnost léčby i u pacientů, u nichž selhaly jiné biologické přípravky [10]. Jak dokládají obě kazuistiky, efekt terapie ustekinumabem byl okamžitý a velice úspěšný.
Důležité je rovněž zmínit, že oba pacienti, jejichž kazuistiky prezentujeme, setrvávají na léčbě ustekinumabem již několik let, léčbu tolerují velice dobře a laboratorní parametry zůstávají v normě. Bezpečnost-
ní profil ustekinumabu se jeví příznivě i při dlouhodobějším podávání. V literatuře jsou dostupná data vypovídající o pětiletém kontinuálním podávání [12].
Závěr
Výhodou biologické terapie je nejen její vysoká účinnost, ale i možnost dlouhodobého podávání, což je podmínka úspěšné léčby psoriázy. Vždy je zapotřebí vybrat správného kandidáta, provést před zahájením léčby screening a následně pacienta pravidelně a pečlivě sledovat. Věříme, že při dodržení všech daných kritérií jsou biologika pro pacienty velkým přínosem. Výzkum v oblasti psoriázy se stále intenzivněji rozvíjí, proto v následujících letech očekáváme příchod dalších moderních léčiv, která budou přínosná nejen pro pacienta, ale i pro celý obor dermatovenerologie.
Seznam použité literatury
- [1] Nestle FO, Kaplan DH, Barker J. Psoriasis. N Engl J Med 2009; 361: 496–509.
- [2] Gkalpakiotis S, Arenberger P, Adenubiová E. Psychosociální aspekty života pacientů s psoriázou v České republice. Čes-slov Derm 2013; 4: 189–196.
- [3] Schmitt JM, Ford DE. Role of depression in quality of life for patients with psoriasis. Dermatology 2007; 215: 17–27.
- [4] Christophers E. Comorbidities in psoriasis. J Eur Acad Dermatol Venerol 2006; 20: 52–55.
- [5] Cetkovská P, Kojanová M. Česká doporučení k biologické léčbě závažné chronické ložiskové psoriázy. Čes-slov Derm 2012; 87: 1–30.
- [6] Menter A, Griffiths CE. Current and future management of psoriasis. Lancet 2007; 370: 272–284.
- [7] van de Kerkhof PC. Novel biologic therapies in development targeting IL-12/IL-23. J Eur Acad Dermatol 2010; 24: 5–9.
- [8] Puig L. Obesity and psoriasis: body weight and body mass index influence the response to biological treatment. J Eur Acad Dermatol Venereol 2011; 25: 1007–1011.
- [9] Wang TS, Tsai TF. Clinical experience of ustekinumab in the treatment of erythrodermic psoriasis: a case series. J Dermatol 2011; 38: 1096–1099.
- [10] Castiñeiras I, Fernández-Diaz L, Juárez Y, Lueiro M. Sustained efficacy of ustekinumab in refractory erythrodermic psoriasis after failure of antitumor necrosis factor therapies. J Dermatol 2012; 39: 730–731.
- [11] Saraceno R, Talamonti M, Galluzzo M, et al. Ustekinumab treatment of erythrodermic psoriasis occurring after physical stress: a report of two cases. Case Rep Dermatol 2013; 5: 254–259.
- [12] Kumar N, Narang K, Cressey BD, Gottlieb AB. Long-term safety of ustekinumab for psoriasis. Expert Opin Drug Saf 2013; 12: 757–765.