Nahradí ARNI inhibitory angiotenzin konvertujícího enzymu?
Key words: ACE inhibitors, sacubitril valsartan, PARADIGM‑HF, heart failure.
Úvod
Základním kamenem léčby chronického srdečního selhání se sníženou ejekční frakcí levé komory (heart failure with reduced ejection fraction, HFrEF) byly od roku 1987 inhibitory angiotenzin konvertujícího enzymu (ACE). V dlouhodobém sledování ve studii SOLVD prokázal enalapril snížení rizika úmrtí o 16 %. Další studie u pacientů se srdečním selháním prokázaly účinek na snížení mortality při léčbě betablokátory a blokátory aldosteronu, které se tak staly dalšími lékovými skupinami přinášejícími tvrdá data. U nemocných, kteří netolerují inhibitory ACE z důvodu suchého dráždivého kašle, jsou doporučovány blokátory receptorů AT1 pro angiotenzin II (ARB, sartany), u nichž se většinou udává, že jsou mírně méně účinné než vlastní inhibitory ACE. Inhibitory ACE a sartany byly v randomizovaných studiích porovnávány u srdečního selhání – studie Val HeFT ‒ a u ischemické choroby srdeční – studie VALIANT a ONTARGET. V klinickém zkoušení fáze III–IV se nacházel přímý blokátor reninu – aliskiren, který blokuje renin na úrovni konverze angiotenzinogenu na angiotenzin I. V rozsáhlém programu ASPIRE HIGHER byl tento přípravek zkoušen ve stejných indikacích, v jakých jsou podávány inhibitory ACE či ARB, nakonec však byl výzkum aliskirenu ukončen kvůli zvýšenému výskytu nežádoucích účinků [1]. První klinická studie PARAMOUNT s molekulou LCZ696 (sakubitril valsartan) v léčbě srdečního selhání se zachovalou ejekční frakcí levé komory (heart failure with preserved ejection fraction, HFpEF) prokázala významné snížení koncentrace N terminálního fragmentu natriuretického peptidu typu B (NT proBNP) [2‒4]. V roce 2014 byly uvedeny výsledky studie PARADIGM HF se sakubitril valsartanem a po jejich prezentaci na Evropském kardiologickém kongresu vyslovil prof. Milton Packer historickou větu: „Užívání inhibitorů ACE po více než 25 let s efektem na snížení kardiovaskulární mortality o 18 % jim dalo mandát být na prvním místě v léčbě chronického srdečního selhání. LCZ696 měl účinek na kardiovaskulární mortalitu o 20 % lepší oproti inhibitorům ACE, není tedy čas uvažovat o jejich náhradě tímto lékem?“
Inhibitory ACE versus sartany
Srovnáme li inhibitory ACE a ARB, pak není pochyb o tom, že hlavní předností ARB proti inhibitorům ACE je jejich výborná tolerance. Neobjevuje se kašel, výrazně nižší je i výskyt angioedému. Z těchto důvodů byla u sartanů pozorována větší adherence k léčbě. Výskyt ostatních nežádoucích účinků se neliší, srovnatelné je riziko hyperkalemie (nutno počítat se zvýšením v průměru o 0,5 mmol/l).
K tradičním indikacím obou skupin patří hypertenze. Na základě prací sledujících antihypertenzní účinek farmakoekvivalentních dávek ARB a inhibitorů ACE bylo konstatováno, že díky zvýšení nabídky natriureticky a vazodilatačně působícího bradykininu jsou inhibitory ACE v případě snížení krevního tlaku i úpravy endoteliální dysfunkce mírně účinnější.
Podobně jsou inhibitory ACE výhodnější i u srdečního selhání. Proto guidelines Evropské kardiologické společnosti (ESC) doporučují ARB pouze při intoleranci inhibitorů ACE v případě výskytu suchého dráždivého kašle. Kombinace obou skupin není vhodná. Tato doporučení jsou podpořena především přímým srovnáním ve studii VALIANT (valsartan a kaptopril) [5] a v programu CHARM (kandesartan samostatně nebo v kombinaci s inhibitory ACE) [6].
V řadě klíčových indikací je doložen výraznější efekt inhibitorů ACE než ARB. Při srovnání jednotlivých inhibitorů ACE jsou ale taktéž rozdíly ve snížení mortality a morbidity v řadě indikací. Při nepřímém srovnání je velmi pravděpodobný výraznější efekt perindoprilu a ramiprilu.
Dosud chybí prospektivní přímá (head to head) studie, která by porovnávala jednotlivé inhibitory ACE v indikaci sekundární prevence či srdeční selhání. Nicméně na rozdíl od léčby hypertenze máme v oblasti sekundární prevence velmi cennou retrospektivní analýzu dopadu léčby různými inhibitory založenou na analýze dat zdravotní pojišťovny z Kanady, tedy dat nezávislých. Cílem této retrospektivní kohortové studie s názvem ONTARIO I bylo porovnat mortalitu starších pacientů (≥ 65 let), kteří byli hospitalizováni pro akutní infarkt myokardu a kteří byli dále v rámci sekundární prevence dlouhodobě léčeni inhibitory ACE [7]. Celkem bylo sledováno téměř 8 000 nemocných léčených déle než rok. Mortalita pacientů léčených kaptoprilem, enalaprilem, fosinoprilem nebo quinaprilem byla statisticky významně vyšší než mortalita pacientů léčených ramiprilem nebo perindoprilem. Je však třeba vzít v úvahu, že pacienti užívající perindopril byli léčeni po kratší dobu a měli účinnější terapii doprovodných onemocnění, a že se tedy nejedná o přímé srovnání, ale pouze o registr, kdy perindopril a ramipril patřily v té době k nově registrovaným „moderním“ inhibitorům ACE.
Podobně máme i registr ONTARIO II u srdečního selhání [8]. Také v tomto případě, při srovnávání neadjustovaných hodnot, bylo relativní riziko úmrtí pro kaptopril i enalapril zvýšeno. I tato studie má však podobné limitace jako studie ONTARIO I.
Poznatky o významu natriuretických peptidů (NP) ve fyziologii a patofyziologii chronického srdečního selhání byly předpodkladem pro výzkum jejich léčebného použití. Krátkodobé infuze farmakologických dávek atriálních natriuretických peptidů (ANP) a mozkových natriuretických peptidů (BNP) vedly u pacientů s chronickým srdečním selháním k příznivým hemodynamickým účinkům [9,10]. Došlo k poklesu tlaku v pravé síni, tlaku v zaklínění a ke vzestupu srdečního výdeje. Dále byl zaznamenán pokles koncentrací aldosteronu a plazmatické reninové aktivity a vzestup diurézy a natriurézy. Podobného účinku bylo dosaženo pomocí rekombinantně připraveného BNP nesiritidu [11]. Bohužel však podobná látka ularitid ve studii TRUE AHF nepotvrdila příznivý efekt na snížení morbidity a mortality [12].
Nový lék ze třídy ARNI
Toto vše bylo výzvou k použití inhibitorů degradace NP v prevenci progrese srdeční dysfunkce do stadia srdečního selhání [13]. Dosud bylo připraveno několik inhibitorů neutrální endopeptidázy, které zvyšují plazmatické koncentrace NP a vedou ke zvýšení natriurézy. Zkušenosti byly s inhibitorem vazopeptidázy omapatrilátem, který měl některé výhody v terapii nemocných s chronickým srdečním selháním ve srovnání s inhibitorem ACE lisinoprilem [14]. První velká, dvojitě zaslepená randomizovaná studie srovnávající omapatrilát a enalapril u nemocných s hypertenzí – OCTAVE ‒ sice prokázala účinnější hypotenzní vliv omapatrilátu, avšak s vyšším výskytem angioedému [15].
Potvrzení nebo vyvrácení teorie o přednosti inhibitorů vazopeptidázy před inhibitory ACE v léčbě chronického srdečního selhání měla přinést studie OVERTURE, která srovnávala účinek omapatrilátu a enalaprilu u pacientů s tímto onemocněním. Omapatrilát nebyl účinnější ve snížení rizika definovaného primárního výsledku ‒ kombinovaného cílového ukazatele rizika úmrtí a hospitalizace pro chronické srdeční selhání vyžadující intravenózní terapii [16].
Novým lékem, který byl podáván u pacientů se srdečním selháním a ukázal pozitivní výsledky v ovlivnění mortality, je LCZ696. Jedná se o látku, která se skládá ze sakubitrilu (AHU377), což je inhibitor neprilysinu, a z blokátoru receptorů AT1 pro angiotenzin II valsartanu. Pro novou třídu duálních inhibitorů se užívá termín ARNI (Angiotensin Receptor – Neprilysin Inhibitor). Neprilysin je neutrální endopeptidáza degradující několik vazoaktivních peptidů, zejména NP, bradykinin a adrenomedulin. Inhibicí neprilysinu se tak zvyšuje počet vazodilatačních látek, které jsou kontraregulační oproti negativním vazokonstrikčním látkám. Kombinovaný účinek blokády degradace NP a současně inhibice renin angiotenzinového systému by mohl přinést další prospěch pro pacienty se srdečním selháním. Předchozí studie, které sledovaly efekt užívání inhibitoru neprilysinu s inhibitorem ACE, vykazovaly vyšší výskyt angioedému (např. studie OVERTURE). Kombinace inhibitoru neprilysinu s ARB má teoretický předpoklad, že výskyt angioedému nebude vyšší.
Studie PARADIGM HF a její nedostatky
Studie PARADIGM HF (Prospective
comparison of ARNI with ACE I to Determine Impact on Global
Mortality and morbidity in Heart Failure) sledovala podávání
sakubitril valsartanu oproti enalaprilu [17‒20]. Zahrnula
pacienty se srdečním selháním třídy
NYHA (New York Heart Association) II‒IV, s ejekční
frakcí levé komory nižší než 40 % (později sníženo
na 35 %), kteří měli koncentraci BNP převyšující
150 pg/ml nebo NT proBNP vyšší než 600 pg/ml. Pokud byli
nemocní hospitalizováni v posledních 12
měsících, byla požadována hodnota BNP vyšší než
100 pg/ml a NT proBNP převyšující
400 pg/ml. Studie probíhala v letech 2009–2012 ve 47
zemích, v 1 043 centrech a u 10 521 pacientů.
Celkově bylo zařazeno 4 187 osob k léčbě
sakubitril valsartanem a 4 212
osob k léčbě
enalaprilem. Celkem 2 079 osob nesplnilo
kritéria pro zařazení, 43 nemocných
bylo randomizováno nesprávně. Základní charakteristiku pacientů
ukazuje tabulka 1.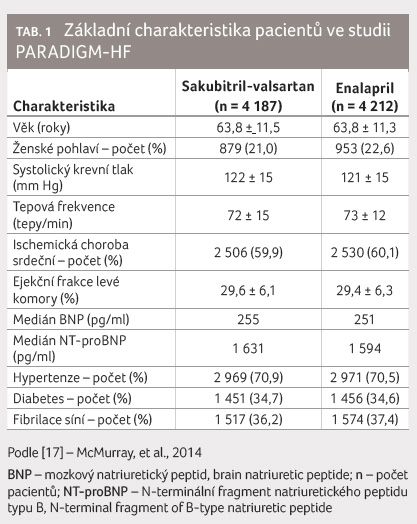
Před vlastní randomizací do dvojitě zaslepené studie byli nejprve pacienti převedeni z léčby stávajícím inhibitorem ACE nebo ARB na podávání enalaprilu v dávce 2× 10 mg po dobu dvou týdnů. Dále následovala fáze s užíváním sakubitril valsartanu po dobu dalších 4‒6 týdnů. Teprve po této vstupní fázi byli pacienti randomizováni do vlastní dvojitě zaslepené, randomizované studie, která srovnávala užití sakubitril valsartanu v dávce 2× 200 mg oproti enalaprilu v dávce 2× 10 mg. Průměrný věk nemocných činil 63,8 ± 11,5 roku, resp. 11,3 roku, počet žen byl 879 (21,0 %), resp. 952 (22,6 %), krevní tlak 121‒122/72‒77 mm Hg, tepová frekvence 72‒73 tepů/min, hypertoniků bylo 71 %, diabetiků 36 % a pacientů s fibrilací síní 37 %. Už ze vstupní charakteristiky je patrné, že nebyli zahrnuti typičtí pacienti se srdečním selháním, protože průměrný věk těchto nemocných činí 70‒75 let, podíl žen je asi 50 % a výskyt diabetes mellitus a/nebo fibrilace síní kolem 40 %, jak ukazují epidemiologické průzkumy ze začátku tohoto století [21].
 Doporučené postupy ESC uvádějí, že
chronické srdeční selhání se v evropských zemích
vyskytuje u 0,4–2 % populace s výrazným nárůstem
ve vyšších věkových skupinách (0,2 % < 50
let, 2–5 % 50–80 let, > 10 % nad 80 let), se
stoupajícím věkem roste i procento pacientů ženského
pohlaví [22‒24]. Jde tedy o onemocnění především vyššího
věku. Studie PARADIGM HF však
zahrnula především mladší muže a nezahrnula
starší ženy.
Doporučené postupy ESC uvádějí, že
chronické srdeční selhání se v evropských zemích
vyskytuje u 0,4–2 % populace s výrazným nárůstem
ve vyšších věkových skupinách (0,2 % < 50
let, 2–5 % 50–80 let, > 10 % nad 80 let), se
stoupajícím věkem roste i procento pacientů ženského
pohlaví [22‒24]. Jde tedy o onemocnění především vyššího
věku. Studie PARADIGM HF však
zahrnula především mladší muže a nezahrnula
starší ženy.
Léčba studijním lékem byla
přerušena u 746 (17,8 %) nemocných a u 833
(19,8 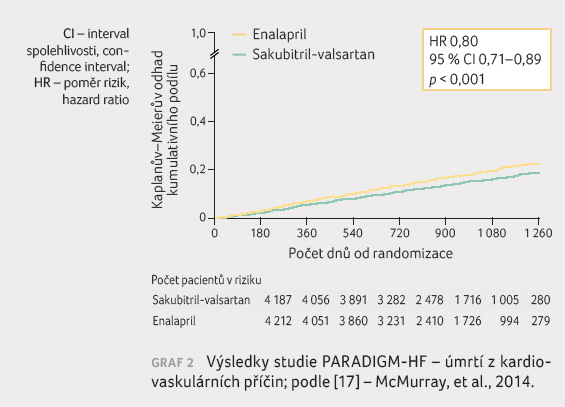 %) nemocných léčených enalaprilem. Celkem 11 nemocných
léčených sakubitril valsartanem a devět nemocných
léčených enalaprilem bylo ztraceno. Průměrná doba sledování
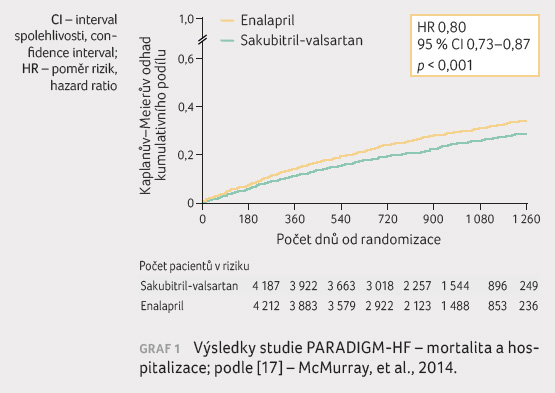
činila 27 měsíců. Hlavní výsledky
studie ukazují grafy 1‒3 a tabulka 2. Primární cílové ukazatele vyzněly vysoce
statisticky významně ve prospěch sakubitril valsartanu,
a to jak pro složený cílový ukazatel kardiovaskulární
úmrtí a první hospitalizace pro srdeční selhání
(p < 0,001),
tak pro oba jednotlivé parametry, tedy pro kardiovaskulární
mortalitu (p < 0,001)
a pro první hospitalizaci pro srdeční selhání (p < 0,001).
Statisticky významně byla nižší rovněž celková mortalita
(p < 0,001).
Naopak pokles renálních funkcí a nový výskyt
%) nemocných léčených enalaprilem. Celkem 11 nemocných
léčených sakubitril valsartanem a devět nemocných
léčených enalaprilem bylo ztraceno. Průměrná doba sledování
činila 27 měsíců. Hlavní výsledky
studie ukazují grafy 1‒3 a tabulka 2. Primární cílové ukazatele vyzněly vysoce
statisticky významně ve prospěch sakubitril valsartanu,
a to jak pro složený cílový ukazatel kardiovaskulární
úmrtí a první hospitalizace pro srdeční selhání
(p < 0,001),
tak pro oba jednotlivé parametry, tedy pro kardiovaskulární
mortalitu (p < 0,001)
a pro první hospitalizaci pro srdeční selhání (p < 0,001).
Statisticky významně byla nižší rovněž celková mortalita
(p < 0,001).
Naopak pokles renálních funkcí a nový výskyt 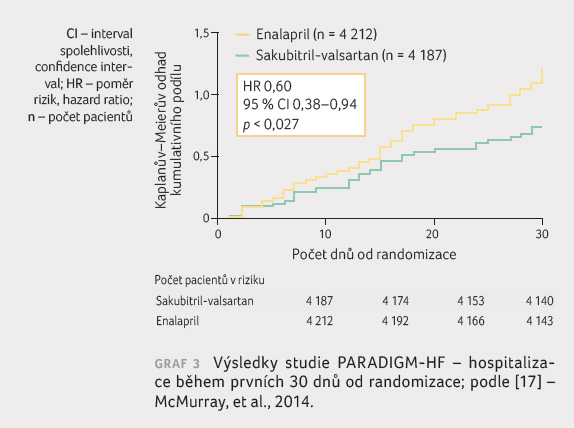 fibrilace síní
byl v obou skupinách podobný.
fibrilace síní
byl v obou skupinách podobný.
V rámci podskupinových
analýz nebyl zjištěn zásadní rozdíl pro
kardiovaskulární úmrtí podle věku, pohlaví nebo rasy.
Nenastal ani rozdíl podle klasifikace NYHA či podle renálních
funkcí. Mírně větší efekt byl pozorován
u nediabetiků než u diabetiků (p = 0,05).
Rozdíl byl podobný u nemocných s fibrilací
síní i bez ní a nebyl zaznamenán rozdíl
podle ejekční frakce levé komory.
Čtyři nemocní (dva v každé skupině) nezahájili léčbu vůbec. Během vstupní periody se u 12 % pacientů objevily nežádoucí účinky. Po randomizaci se u nemocných léčených sakubitril valsartanem častěji vyskytla hypotenze než u nemocných léčených enalaprilem, tento fakt však byl jen vzácně příčinou ukončení terapie. Nežádoucí účinky byly důvodem přerušení léčby u 10,7 % nemocných léčených sakubitril valsartanem a u 12,3 % nemocných léčených enalaprilem (p = 0,03). Nebyl zaznamenán rozdíl v tepové frekvenci mezi oběma skupinami. Angioedém se vyskytl u 19 pacientů léčených sakubitril valsartanem a u 10 pacientů léčených enalaprilem (p = 0,13). Ani jeden angioedém nebyl důvodem pro intubaci.
Ve studii PARADIGM HF prokázal sakubitril valsartan větší efektivitu v parametrech celkové mortality, kardiovaskulární mortality i hospitalizací pro srdeční selhání oproti enalaprilu jako zavedenému inhibitoru ACE. Po dlouhé době je to studie s pozitivními výsledky u pacientů se srdečním selháním. Na rozdíl od omapatrilátu nedošlo v tomto případě k výraznějšímu výskytu nežádoucích účinků. Jednalo se zejména o objevení se závažného angioedému, který v případě omapatrilátu rovněž přispěl k tomu, že tato látka nebyla dále používána. U sakubitril valsartanu byl výskyt angioedému ve srovnání s enalaprilem statisticky nevýznamný, léčba tímto přípravkem byla taktéž spojena se statisticky významně nižším výskytem dráždivého kašle než léčba enalaprilem. Tento výsledek je bezpochyby dán tím, že na rozdíl od omapatrilátu je molekula LCZ696 tvořena inhibitorem neprilysinu a ARB valsartanem. V současnosti jsou základními kameny léčby chronického srdečního selhání inhibitory ACE, při jejich intoleranci se indikují ARB, betablokátory a antagonisté aldosteronu. Je otázkou, jaké místo si LCZ696 najde v terapii srdečního selhání ‒ zda se stane nástupcem inhibitorů ACE a blokátoru receptorů AT1 pro angiotenzin II.
Již výše jsme upozornili, že studie PARADIGM HF zahrnula především mladší nemocné mužského pohlaví, nezaměřila se tedy na celé spektrum pacientů se srdečním selháním. Dalším nedostatkem je, že nemocní museli být předléčeni po dobu dvou týdnů dávkou 2× 10 mg enalaprilu a následně 2‒4 týdny sakubitril valsartanem a museli tuto terapii tolerovat. Již toto předléčení eliminuje nemocné netolerující inhibitor ACE z důvodu výskytu suchého kašle (takových pacientů je asi 10 %) a současně nemocné netolerující inhibitor ACE či sakubitril valsartan z důvodu hypotenze, kteří budou tvořit nezanedbatelné procento pacientů. Celkově bylo vyřazeno 2 079 nemocných, což je 19,8 % screenovaných, a dalších 19,8 %, resp. 17,8 % osob léčbu přerušilo. Poslední nutné upozornění v rámci uspořádání studie se týká hodnot BNP, resp. NT proBNP, které musely být 150 pg/ml, resp. 600 pg/ml nebo 100 pg/ml, resp. 400 pg/ml při hospitalizaci. Na základě rozložení hodnot NT proBNP v našem souboru FAR NHL (FARmakologie a NeuroHumoráLní aktivace) u 1 050 nemocných se domníváme, že kritérium koncentrace NT proBNP 600 pg/ml by nesplnilo více než 50 % (v našem souboru 52,7 %) nemocných. Dále je třeba zopakovat, že jako srovnávací lék byl zvolen dnes již téměř nepoužívaný a pravděpodobně méně účinný inhibitor ACE enalapril. Hlavní nedostatky studie PARADIGM HF tedy spočívají v zahrnuté studijní populaci, jež nepředstavuje obecnou populaci osob se srdečním selháním:
a) pacienti byli o 10 let mladší než běžná populace nemocných se srdečním selháním;
b) ženy tvořily pouze 20 % z celkového počtu sledovaných pacientů;
c) výskyt komorbidit byl nízký;
d) hodnoty NT proBNP jako kritérium pro zařazení do studie byly příliš vysoké;
e) pacienti museli tolerovat dávku minimálně 2× 10 mg enalaprilu;
f) enalapril patří k méně účinným inhibitorům ACE.
Závěr
Pokusili jsme se analyzovat, pro jaké množství nemocných byl sakubitril valsartan vhodný v českém registru chronického srdečního selhání známém jako FAR NHL, v němž byli studijně sledováni nemocní v letech 2015‒2016 na třech pracovištích v České republice ‒ na Interní kardiologické klinice FN Brno, na Interní kardioangiologické klinice FN u sv. Anny v Brně a na Kardiologickém oddělení Nemocnice Na Homolce [25]. Do registru bylo zařazeno 1 050 nemocných, kteří jsou dlouhodobě sledováni. Podle vstupních parametrů byli rozděleni na nemocné s ejekční frakcí levé komory vyšší než 35 % (27 % osob) a na nemocné s hodnotou glomerulární filtrace nedosahující 30 ml/min/1,73 m2 (3 % osob). Pro další analýzu (splňující kritéria studie PARADIGM HF) pak byli zvoleni nemocní bez hospitalizace a s hodnotou NT proBNP převyšující 600 pg/ml (36,7 %) nebo s hospitalizací a s hodnotou NT proBNP vyšší než 400 pg/ml (2,1 %). Z uvedených skupin byli vybráni pacienti tolerující alespoň střední nebo vyšší dávky inhibitorů ACE nebo sartanů, jichž bylo 171 (15,5 % osob). V našem souboru bychom tedy náhradu inhibitoru ACE za ARNI mohli v souladu se současnými doporučenými postupy a v souladu s výsledky studie PARADIGM HF doporučit asi 15 % nemocných s chronickým srdečním selháním. Zbylých 85 % indikační kritéria nesplňovalo!
Pokud bychom se tedy pokusili odpovědět na otázku položenou v úvodu článku, zda není čas uvažovat o náhradě inhibitorů ACE novým lékem ze třídy ARNI, je nutné na základě našich poznatků uvést, že jistě existuje nezanedbatelné množství pacientů s chronickým srdečním selháním a se sníženou ejekční frakcí levé komory, kteří si zaslouží záměnu inhibitoru ACE za sakubitril valsartan. Při odhadu 200 000 nemocných trpících chronickým srdečním selháním v České republice by to zřejmě bylo přibližně 30 000 osob (15 % z celkového počtu těchto pacientů).
Práce byla podpořena projektem (Ministerstva zdravotnictví ČR) koncepčního rozvoje výzkumné organizace 65269705 (FN Brno).
Seznam použité literatury
- [1] Špinar J, Vítovec J. Blokáda systému renin‑angiotenzin v léčbě kardiovaskulárních onemocnění. Intervenční a akutní kardiologie 2010; 9: 252‒257.
- [2] Málek F. Duální inhibice angiotenzinu a neprilysinu – revoluční princip léčby chronického srdečního selhání se sníženou ejekční frakcí levé komory. Kardiol Rev Int Med 2016; 18: 295‒298.
- [3] Ruilope LM, Dukat A, Bohm M, et al. Blood‑pressure reduction with LCZ696, a novel dual‑acting inhibitor of the angiotensin II receptor and neprilysin: a randomised, double‑blind, placebo‑controlled, active comparator study. Lancet 2010; 375: 1255‒1266.
- [4] Solomon SD, Zile M, Pieske B, et al. The angiotensin receptor neprilysin inhibitor LCZ696 in heart failure with preserved ejection fraction: a phase 2 double‑blind randomised controlled trial. Lancet 2012; 380: 1387‒1395.
- [5] Vítovec J, Špinar J. VALIANT ‒ Valsartan, captopril nebo obojí u infarktu myokardu komplikovaného srdečním selháním a/nebo dysfunkcí levé komory ‒ samostatně ano, společně ne. Klin Farmakol Farm 2004; 18: 53‒54.
- [6] Pfeffer MA, Swedberger K, Granger CB, et al. Effects of candesartan on mortality and morbidity in patients with chronic heart failure: the CHARM – Overall programme. Lancet 2003; 362: 759‒766.
- [7] Pilote L, Abrahamowicz M, Eisenberg M, et al. Effect of different angiotensin‑converting‑enzyme inhibitors on mortality among elderly patients with congestive heart failure. CMAJ 2008; 178: 1303–1311.
- [8] Pilote L, Abrahamowicz M, Rodrigues E, et al. Mortality Rates in Elderly Patients Who Take Different Angiotenzin‑Converting Enzyme Inhibitors after Acute Myocardial Infarction: A Class Effect? Ann Intern Med 2004; 141: 102–112.
- [9] Marcus LS, Hart D, Packer M, et al. Hemodynamic and renal excretory effects of human brain natriuretic peptide infusion in patients with congestive heart failure. Circulation 1996; 94: 3184–3189.
- [10] Yoshimura M, Yasue H, Morita E, et al. Hemodynamic, renal and hormonal responses to brain natriuretic peptide infusion in patients with congestive heart failure. Circulation 1991; 84: 1581–1588.
- [11] Colucci WS, Elkayam U, Horton DP, et al. Intravenous nesiritide, a natriuretic peptide, in the treatment of decompensated congestive heart failure. N Engl J Med 2000; 343: 264–253.
- [12] Ludka O. Ularitid v léčbě akutně dekompenzovaného srdečního selhání ‒ výsledky studie TRUE‑AHF. Kardiol Rev Int Med 2017; 19: 172‒176.
- [13] Margulies KB, Barclay PL, Burnett JC jr. The role of neutral endopeptidase in dogs with evolving congestive heart failure. Circulation 1995; 91: 2036–2042.
- [14] Rouleau JL, Pfeffer MA, Stewart DJ, et al. Comparison of vasopeptidase inhibitor, omapatrilat, and lisinopril on exercise tolerance and morbidity in patients with heart failure: IMPRESS randomised trial. Lancet 2000; 356: 615–620.
- [15] Kostis JB, Packer M, Black HR, et al. Omapatrilat and enalapril in patients with hypertension: the Omapatrilat Cardiovascular Treatment vs. Enalapril (OCTAVE) trial. Am J Hypertens 2004; 17: 103‒111.
- [16] Packer M, Califf RM, Konstam MA, et al. OVERTURE Study Group. Comparison of omapatrilat and enalapril in patients with chronic heart failure. Circulation 2002; 106: 920–926.
- [17] McMurray JJV, Packer M, Desai AS, et al. Angiotensin‑Neprilysin Inhibition versus Enalapril in Heart Failure. N Engl J Med 2014; 371: 993‒1004.
- [18] Špinar J, Špinarová L, Vítovec J. Studie PARADIGM‑HF možná změní léčbu srdečního selhání. Hypertenze a kardiovaskulární prevence 2014; 2: 25‒26.
- [19] Špinarová L, Špinar J, Vítovec J. Co nám přináší studie PARADIGM‑HF. Kardiol Rev Int Med 2014; 16: 395‒397.
- [20] Špinarová L, Špinar J. Co zaznělo na kongresu AHA 2016 v New Orleansu. Kardiol Rev Int Med 2016; 18: 295‒298.
- [21] Widimský J, Lánská V, Magulová D, Sachová M. Průzkum stavu aktuální praxe diagnostiky a léčby srdečního selhání v ordinacích všeobecných lékařů v České a Slovenské republice v roce 1999. 2. část programu IMPROVEMENT of HF. Cor Vasa 2001; 43: 345‒352.
- [22] 2016 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. The Task Force for the diagnosis and treatment of acute and chronic heart failure of the European Society of Cardiology (ESC). Eur Heart J 2016; 37: 2129–2200.
- [23] Špinar J, Hradec J, Špinarová L, Vítovec J. Summary of the 2016 ESC Guidelines on the diagnosis and treatment of acute and chronic heart failure. Prepared by the Czech Society of Cardiology. Cor Vasa 2016; 58: e530–e568.
- [24] Strömberg A, Mårtensson J. Gender differences in patients with heart failure. Eur J Cardiovasc Nurs 2003; 2: 7–18.
- [25] Špinar J, Špinarová L, Pařenica J. FAR NHL – FARmacology and NeuroHumoraL activation in chronic heart failure ‒ the role of disease severity, neurohumoral activation and comorbidities for one year prognosis. Eur J Heart Failure 2018; 20: [v tisku].