Atomoxetin
Hyperkinetické poruchy jsou diagnostickou kategorií F90 dle MKN (ADHD dle DSM-IV), která se objevuje ve všech věkových skupinách – od dětství do dospělosti. Neurovývojové opoždění a časté minimální organické poškození s kumulací zevních stresů vede k maladaptivnímu chování s vysokou psychiatrickou komorbiditou. Děti s ADHD mají odchylnou maturaci CNS a odlišný vývoj neurotransmiterových systémů. Úspěšná je terapie stimulancii a od roku 2002 atomoxetinem. Atomoxetin je centrální sympatomimetikum působící inhibici zpětného vychytávání noradrenalinu. Přímým i nepřímým účinkem tak dochází ke zvýšení obratu noradrenalinu a dopaminu v prefrontální kůře, bez negativných vlivů na striatum a nucleus accumbens. Atomoxetin nezhoršuje tiky, úzkost a není provázen rizikem vzniku závislosti. Terapeutický účinek po titraci přetrvává při dávkování jednou denně ráno po celých 24 hodin i s pozitivním efektem na večerní usínání. Atomoxetin jako lék první volby by měl být podán u hyperkinetické poruchy aktivity a pozornosti (F90.0) tam, kde léčba psychostimulující látkou je nevhodná z aspektu psychiatrického i z aspektu environmentálního.
Úvod
Hyperkinetické poruchy jsou typickou neurovývojovou poruchou projevující se od nejútlejšího dětství do dospělosti. Dle MKN-10 jsou rozděleny do dvou jednotek: porucha aktivity a pozornosti (odpovídající ADHD) a hyperkinetická porucha chová-ní. V DSM-IV je používán název ADHD (Attention Deficit Hyperactivity Disorder) a třídění do 3 skupin (porucha pozornosti, porucha pozornosti s impulzivitou a hyperaktivitou a kombinovaný typ). Porucha chování je v americké klasifikaci pojímána jako komorbidní. Hyperkinetické poruchy jsou modelovou poruchou pro interakci mezi faktory genetickými, neurobiologickými a zevními epigenetickými [1]. Odchylná maturace CNS je prokazatelná zobrazovacími metodami. Tangovány jsou prefrontální korové oblasti, bazální ganglia a mozeček. Zde hraje důležitou úlohu dopamin. Dopamin zprostředkovává komunikaci mezi neurony a je tzv. přenašečem hluku. Jeho koncentrace v prefrontálním kortexu ovlivňuje kognitivní funkce, pozornost a impulzivitu.
Mnoho příznaků se zmírňuje v době, kdy se začíná objevovat inhibice excitačních systémů. Tato inhibice probíhá paralelně s poklesem aktivity dopaminu v mozku. ADHD má výraznou genetickou komponentu, pravděpodobně jde o polygenetickou poruchu vytvářenou mutací více genů. Riziko vzniku ADHD poruchy u jednovaječných dvojčat je 11–18krát vyšší než u dvojvaječných. Genetické studie předpokládají, že jedinci s ADHD mohou mít změny v genech kódujících dopaminový receptor D4 nebo dopaminový přenašeč. ADHD je také rizikovou diagnózou pro vznik dalších psychiatrických a psychosomatických poruch (např. porucha opozičního vzdoru, poruchy chování, depresivní a anxiózní poruchy, specifické poruchy školních dovedností, zneužívání návykových látek atd.). Více než samotnou hyperkinetickou poruchou je nepříznivá prognóza dána vysokou psychiatrickou komorbiditou [1].
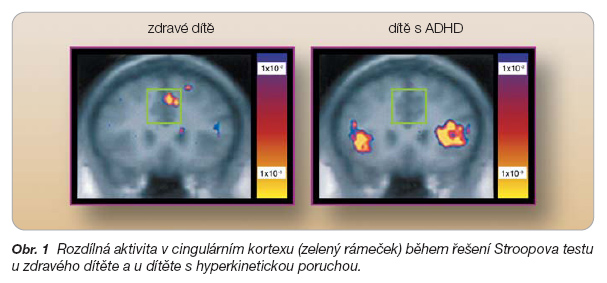
Dle Biedermana [2] je celosvětová prevalence ADHD udávána v rozmezí 3–9 %. Porucha narušuje školní výkonnost dětí s normálním intelektovým potenciálem, takže jejich špatné výsledky jsou v rozporu s jejich dobrým intelektem. Porucha emocí, hyperaktivita a impulzivita se ztrátou vnitřní kontroly vede k výrazné sociální maladaptaci. Neurovývojové opoždění u ADHD se projevuje odchylnou maturací CNS a odlišným vývojem neurotransmiterových systémů. Největší dysregulace je v systému noradrenergním a dopaminerg-ním [2]. Děti s hyperkinetickými poruchami vykazují proti zdravým kontrolám odchylnou aktivitu a inhibici mozkových struktur na zevní podněty z okolí. Tyto odlišnosti jsou objektivizovány zobrazovacími metodami, např. rozdílná aktivace mozkových struktur při řešení Stroopova testu u dětí s ADHD a u zdravých kontrol je znázorněna na obr. 1.
U ADHD je zobrazovacími metodami zjišťován signifikantně menší (-3,5 %) objem mozku a mozečku, zmenšený objem bazálních ganglií a zmenšené corpus callosum [3].
Dopaminová a noradrenalinová hypotéza o dysregulaci noradrenergního a dopaminergního systému u ADHD odpovídá nacházeným změnám transmise dopaminu a noradrenalinu v prefrontální kůře, v bazálních gangliích a v oblasti vermis cerebelli.
Tyto nálezy jsou důležité pro farmakologickou intervenci. Psychofarmaka přinášejí výrazné ovlivnění nežádoucích projevů (hlavně zlepšení kontroly chování) a tedy i příznivější sociální odezvu.
Do roku 2002 byly léky první volby psychostimulancia. V naší republice je doposud jediným dostupným psychostimulanciem methylfenidát. Dlouho očekávaný atomoxetin, psychofarmakon, které má v USA schválenou indikaci pro léčbu ADHD jak u dětí (od 6 let) a adolescentů, tak u dospělých již několik let, je nyní i na našem trhu.
Farmakologické vlastnosti
Mechanismus účinku
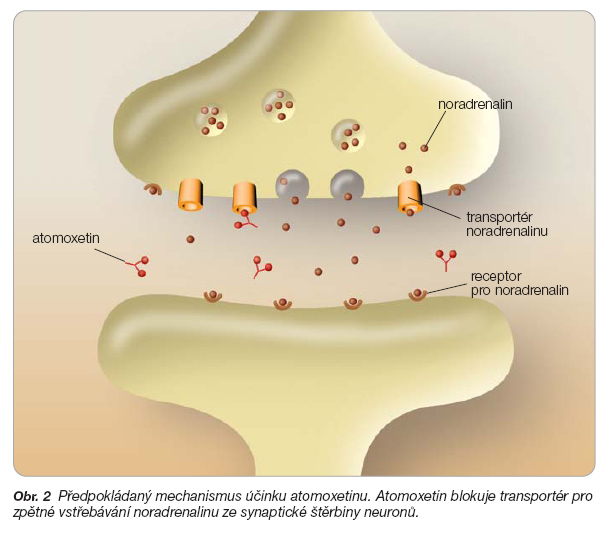
Atomoxetin je centrální sympatomimetikum působící s vysokou afinitou a selektivitou inhibici zpětného vychytávání noradrenalinu blokádou presynap-tického noradrenalinového transportéru, obr. 2. Blokuje nebo zpomaluje reabsorpci noradrenalinu v mozku.
Noradrenalinový transportér je nespecifický, to znamená, že je schopen vracet zpět do presynaptického noradrenergního neuronu jak noradrenalin, tak dopamin. Dojde-li k zamezení zpětného vychytávání noradrenalinu v prefrontální kůře, zvýší se množství dostupného dopaminu. Tak oba transmiterové systémy pracují v prefrontální kůře v součinnosti a tímto způsobem noradrenergní systém nepřímo moduluje systém dopaminergní.
Atomoxetin byl původně vyvíjen jako antidepresivum. V subkortikálních oblastech mozku potkanů (nucleus accumbens a striatum) je po podání atomoxetinu selektivně blokováno zpětné vychytávání noradrenalinu, extracelulární hladiny dopaminu nejsou ovlivněny. Zvýšené hladiny noradrenalinu pak mohou hrát roli nejen v účinku atomoxetinu při terapii poruchy pozornosti s hyperaktivitou, ale také ve zmírnění doprovodných symptomů deprese a úzkosti. Na rozdíl od psychostimulancií ovlivňujících hladinu dopaminu, atomoxetin neovlivňuje hladiny dopaminu ve striatu ani v nucleus accumbens. Proto 406 pravděpodobně není léčba atomoxetinem provázena vznikem tiků nebo zhoršením komorbidní tikové poruchy a rizikem vzniku závislosti [2, 4].
Farmakokinetické vlastnosti
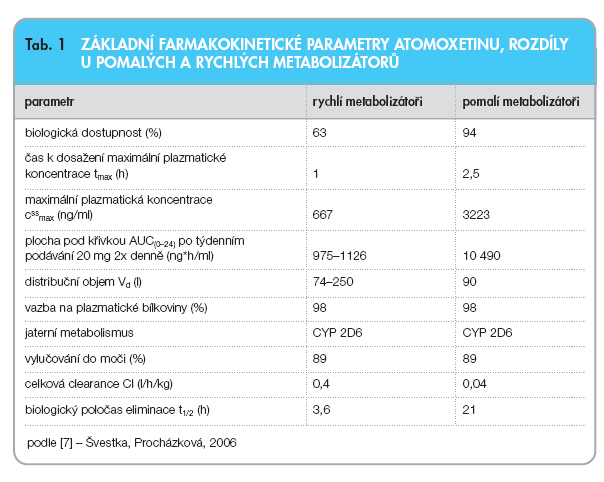
Farmakokinetika atomoxetinu nebyla signifikantně ovlivněna věkem, kouřením, pohlavím ani rasou. Po perorálním podání se atomoxetin dobře a rychle vstřebává a tento proces je minimálně ovlivněn potravou (tab. 1).
Stolicí se vylučuje 17 % a močí více než 8 % podané látky. Poločas rozpadu se pohybuje kolem 5 hodin [5]. Průměrný eliminační poločas atomoxetinu po perorálním podání je u rychlých metabolizátorů 3,6 hodiny a u pomalých metabolizátorů 21 hodin [6]. Atomoxetin je metabolizován v játrech převážně oxidativní enzymatickou cestou přes cytochrom P-450 2D6 (CYP2D6). Atomoxetin může být pacientům podáván bez genotypizace, protože nedochází k signifikantní změně klinického obrazu ani ke změně tolerability. Pomalí metabolizátoři (asi 9 % populace) mají ve větším procentu lehce zvýšený pulz a vyšší hmotnostní úbytek [7]. U rychlých i pomalých metabolizátorů je farmakokinetika atomoxetinu lineární. Je-li atomoxetin kombinován s látkami, které inhibují CYP2D6, jako jsou např. antidepresiva SSRI (fluoxetin, paroxetin), je jeho vylučování pomalejší a odpovídá vylučování u pomalých metabolizátorů. Specifická pozornost musí být věnována lidem s jaterní insuficiencí. Pacienti, kteří trpí onemocněním jater, mají signifikantně sníženou clearance atomoxetinu. Výrobce proto doporučuje redukovat počáteční dávku na 25–50 % normální dávky. Žádné úpravy dávkování nejsou nutné u pacientů s onemocněním ledvin [2]. V řadě zemí byl atomoxetin přiřazen k antidepresivům, to znamená nutnost povinného uvádění tzv. black box warning, což znamená, že podobně jako při léčbě antidepresivy má být při léčbě dětí a mladistvých atomoxetinem kladen zvláštní důraz na zjišťování suicidiálních představ, myšlenek a tendencí [8].
Klinické zkušenosti
Atomoxetin patří do skupiny centrálně působících sympatomimetik a je jediným nestimulanciem určeným k léčbě hyperkinetických poruch. Jako lék první volby má být podán tam, kde je diagnostikována specifická komorbidita nebo kde není dostatečné psychosociální zázemí pro podávání psychostimulancií dětem [9].
K léčbě ADHD dle klinických vodítek (guidelines of treatment) jsou jako léky první volby určena stimulancia nebo atomoxetin [8]. Doporučené postupy byly zpracovány jak v ČR a v zemích EU, tak v USA a záštitu nad nimi převzaly odborné společnosti (např. ČLS JEP, AACAP, ESCAP) [10]. Atomoxetin je jediná léčivá látka svého druhu, od stimulancií se liší svým kontinuálním 24hodinovým ovlivněním příznaků ADHD včetně poruch usínání a účinkem na zlepšení kognitivních i psychosociál-ních funkcí. Lze jej podávat jednou denně a postupnou titrací se dosahuje plného účinku za 4–6 týdnů. Atomoxetin zlepšuje pozornost, náladu a sociabilitu, snižuje impulzivitu a agresivitu. Byl testován ve studiích kontrolovaných placebem, v randomizovaných, dvojitě slepých i otevřených studiích s dospělými jedinci i s dětmi a adolescenty.
Od roku 2002 je podáván v indikaci porucha aktivity a pozornosti u dětí (od 6 let), adolescentů a dospělých. V letech 2002–2005 byly atomoxetinem léčeny více než 4 miliony pacientů a u dětí a adolescentů bylo provedeno 22 různě koncipovaných studií, v nichž byl jasně prokázán terapeutický efekt jak atomoxetinu (ATX), tak methylfenidátu (MPH) [11–13]. Atomoxetin, na rozdíl od stimulancií, nemá efekt jedné dávky ani nepůsobí euforii, nemá návykový potenciál a nezhoršuje tiky ani úzkost.
Stručné zhodnocení
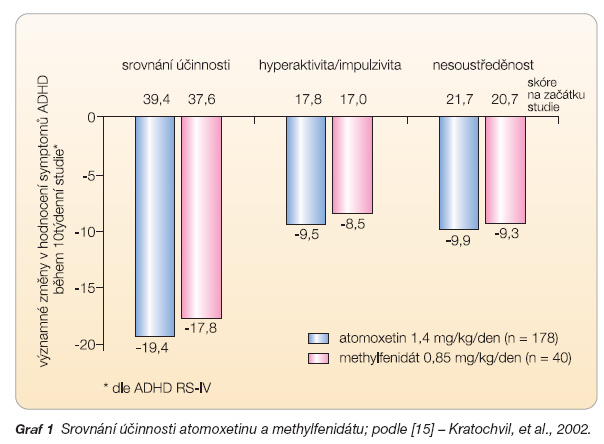
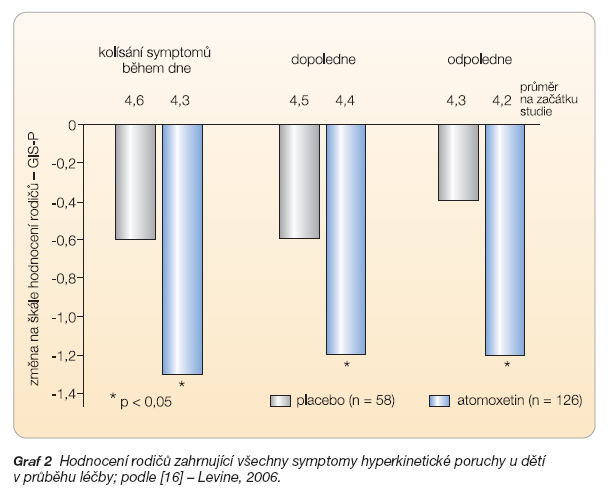
Léčba atomoxetinem pomáhá zlepšovat sociální adaptaci a komunikaci tím, že pozitivně ovlivňuje příznaky, jako jsou hyper-aktivita, impulzivita, nesoustředěnost. To vede k většímu přijetí léčeného dítěte ze strany rodičů, učitelů, ale i vrstevníků [14]. Tím se zvyšuje i sebevědomí a sebehodnocení pacienta – jeho sociální kompetence – a zároveň se předchází negativním sociálním důsledkům při perzistenci do dospělosti [9]. Atomoxetin nevykazuje „off-on efekt", pro kontinuální 24hodinové působení je nazýván „termostatem". Zlepšuje začátek spánku, nevyvolává insomnii, neovlivňuje pocit hladu, nesnižuje hmotnost, není návykový. Atomoxetin signifikantně zmírňuje symptomy u „čisté" ADHD a rovněž u ADHD s komorbidními poruchami. U obou skupin není rozdíl v účinné terapeutické odpovědi např. při ovlivnění ADHD a ADHD s poruchou opozičního vzdoru. Ve srovnávacích studiích byla zaznamenána lepší terapeutická odpověď na léčbu atomoxetinem u pacientů, kteří neprodělali předchozí léčbu stimulancii, proto je výhodné, aby byl atomoxetin lékem první volby [2]. Léčba atomoxetinem má několik výhod z hlediska akceptace. Ocení ji lékaři, protože nepodléhá speciálnímu režimu, tj. opatřením, která jsou nutná pro vysoce návykové látky (např. „recepty s modrým pruhem", trezory, zvláštní evidence atd.). Léčbu atomoxetinem lépe přijímají i rodiče, kteří se vždy zaleknou možnosti podávání pychostimulancií svým dětem. Bojí se, že mnohaměsíčním užíváním se z dítěte stane toxikoman, že bude hubené a malé. Toto vše odpadá při terapii atomoxetinem, která vykazuje stejnou účinnost jako léčba psychostimulancii (graf 1)
a signifikantně vyšší účinnosti než podávání placeba (graf 2) [15, 16].
Dávkování
Atomoxetin je podáván v účinné dávce 1,2 mg/kg/den. Dávka atomoxetinu se stanoví dle hmotnosti:
– ‑pro děti a adolescenty < 70 kg je obvyk-lá dávka prvních 7 dní 0,5 mg/kg/den; pak nastává pomalá vzestupná titrace na dávku 1,2 mg/kg/den, která je zároveň dávkou udržovací. Při nízkém efektu může být dávka zvýšena na 1,5 mg/kg/den. Maximální bezpečná denní dávka je 1,8 mg/kg/den. Při vyšším dávkování může být atomoxetin podáván 2krát denně.
– ‑u adolescentů a dospělých > 70 kg je počáteční dávka 40 mg/den, minimální doba podávání 7 dní, pak nastává období titrace – vzestupná titrace na udržovací dávku 80 mg/den.
V prvních 4–6 týdnech je dosaženo plného účinku. Zlepšení může být patrné již během titrace. Významné ovlivnění symptomů nastává v 75 %.
Nežádoucí účinky
Nežádoucí vedlejší reakce u dětí a adolescentů, které se objevují asi u 5 % lé-čených pacientů, jsou dle Thomasona a Michelsona následující: bolesti břicha, nechutenství, zvracení, somnolence, dráždivost. U dospělých léčených atomoxetinem se vyskytlo více nežádoucích příznaků než u dětí, hlavně v oblasti gastrointestinálního nebo urogenitálního traktu [17]. Potenciálním rizikem při podávání atomoxetinu jsou epileptické záchvaty. Atomoxetin by měl být podáván se zvýšenou opatrností u pacientů se záchvaty v anamnéze.
Atomoxetin nemá zásadní vliv na:
– ‑hmotnost – přechodný váhový úbytek se normalizuje do 18 měsíců,
– ‑výšku – atomoxetin má minimální efekt na růst a po počátečním odklonu růstové křivky nastává rychlá stabilizace.
Zároveň zatím nebylo zjištěno, že by atomoxetin měl škodlivý účinek nebo že by negativně ovlivňoval sexuální zrání dětí.
Studie hodnotící účinky na schopnost řídit a obsluhovat stroje nebyly provedeny. Je vhodné pacientům doporučit, aby při řízení vozidel nebo při obsluze nebezpečných strojů byli opatrní, než si budou spolehlivě jistí, že jejich výkon není ovlivněn atomoxetinem.
S předávkováním atomoxetinem v klinických studiích jsou jen omezené zkušenosti a nebyly pozorovány žádné smrtelné případy. Po zavedení přípravku na trh se vyskytla hlášení o předávkování atomoxetinem. Nejčastěji popisovanými projevy doprovázejícími akutní a chronické předávkování byly somnolence, agitovanost, hyperaktivita, abnormální chování a gastrointestinální symptomy. Všichni pacienti se z těchto příhod uzdravili.
Interakce
Atomoxetin se nedoporučuje podávat s inhibitory monoaminooxidázy (IMAO). Kombinace s hypnotiky také není doporučována.
Atomoxetin podávaný s léky, které mohou prodlužovat QT interval, může potencovat tento účinek. Jedná se např. o antipsychotika, antiarytmika IA a III, moxi-floxacin, erythromycin, methadon, meflochin, tricyklická antidepresiva, lithium, cisaprid [2].
Závěr
Atomoxetin ve formě tvrdých tobolek je v ČR schválen pro léčbu hyperkinetické poruchy od 1. 4. 2007. Indikován je „k léčbě hyperkinetické poruchy (Attention-Deficit/Hyperactivity Disorder, ADHD) u dětí ve věku 6 let a starších a u dospívajících jako součást komplexního léčebného programu. Léčba musí být zahájena odborníkem na léčbu ADHD. Diagnóza má být stanovena dle kritérií DSM-IV nebo vodítek v MKN-10". U mladších dětí a u dospělých je jeho použití mimo indikační vymezení.
Při podání atomoxetinu pacientovi s komorbidními poruchami je nutné se rozhodnout, zda léčit napřed komorbidní poruchu a k léčbě ADHD se vrátit později, nebo léčit ADHD, a teprve když je tato cesta neúspěšná, léčit komorbiditu.
Atomoxetin jako lék první volby by měl být podán u hyperkinetické poruchy aktivity a pozornosti tam, kde je léčba stimulancii nevhodná jak z aspektu psychiatrického, tak environmentálního.
Seznam použité literatury
- [1] Malá E. Hyperkinetické poruchy. Postgraduální medicína 2005; 1: 1–8.
- [2] Biederman J, Farone SV. Attention-deficit hyper-activity disorder. Lancet 2005; 366: 237–248.
- [3] Castellanos FX, Giedd JN, Marsh NL, et al. Quantitative brain magnetic resonance in attention-deficity hyperactivity disorder. Arch Gen Psychiatry 1996; 53: 607–617.
- [4] Bradley JDD, Golden CJ. Biological contributions to the presentation and understanding of attention-deficit/hyperactivity disorder. A review. Clinical Psychology Review 2001; 21: 907–929.
- [5] Ring BJ, Gillespie JS, Eckstein JA, Wrighton SA. Identification of the human cytochromes P450 responsible for atomoxetine metabolism. Drug Metab Dispos 2002; 30: 319–323.
- [6] Witcher JW, Long A, Smith B, et al. Atomoxetine pharmacokinetics in children and adolescents with attention deficit hyperactivity disorder. J Child Adolesc Psychopharmacol 2003; 13: 53–63.
- [7] Švestka J, Procházková M. Atomoxetin – selektivní inhibitor zpětného vychytávání noradrenalinu v léčbě poruchy pozornosti s hyperaktivitou. Farmakoterapie 2006; 537–541.
- [8] Drtílková I, Hrdlička M, Paclt I. Klinická vodítka léčby hyperkinetické poruchy u dětí. Guideline České psychiatriké společnosti. Dostupné z http://www.ceskapsychiatrie.cz/download/ hyperkineticka_porucha_deti.pdf (navštíveno 25. 6. 2007).
- [9] Kessler RC, Adler LA, Barkley R, et al. Patterns and predictors of attention-deficit/hyperactivity disorder persistence into adulthood. Results from the National Comorbidity Survey Replication. Biological Psychiatry 2005; 57: 1442–1445.
- [10] Banaschewski T, Coghill D, Santosh P, et al. Long-acting medications for the hyperkinetic disorders. A systematic review and European treatment guidelines. Eur Child Adolesc Psychiatry 2006; 15: 476–495.
- [11] Michelson D. Results from a double-blind study of atomoxetine, OROS methylphenidate, and placebo. Scientific Proceedings of the 51st Annual Meeting of the American Academy of Child and Adolescent Psychiatry (AACAP), Washington D. C. (USA), 19–24 Oct 2004: 49.
- [12] Popper CW. Pharmacologic alternatives to psychostimulants for the treatment of attention-deficit/hyperactivity disorder. Child and Adolescent Psychiatric Clinics of North America 2000; 9: 605–645.
- [13] Thomason C, Michelson D. Atomoxetine: treatment of attention deficit hyperactivity disorder: beyond stimulants. Drugs of Today 2004; 40: 465–473.
- [14] Becker K, Buitelaar JK, Danckaerts M, et al. Does atomoxetine treatment improve psychosocial and family functioning in children and adolescents with ADHD? Acta Psych Scand 2004; 110: 48.
- [15] Kratochvil CJ, Heiligenstein JH, Dittmann R, et al. Atomoxetine and methylphenidate treatment in children with ADHD: a prospective, randomized, open-label trial. J Am Acad Child Adolesc Psychiatry 2002;41: 776–784.
- [16] Levine LR. Neuroscience meeting, Barcelona, 2006.
- [17] Wernicke JF, Adler L, Spencer T, et al. Changes in symptoms and adverse events after discon-tinuation of atomoxetine in children and adults with attention deficit/hyperactivity disorder: a prospective, placebo-controlled assessment. Journal of Clinical Psychopharmacology 2004; 24: 1–6.