Dabrafenib v léčbě metastazujícího melanomu
Metastazující melanom patří mezi nádory s vysokou mortalitou i vysokou rezistencí ke klasickým léčebným postupům, jako je chemoterapie či aktinoterapie. Významného pokroku bylo dosaženo až cílenou imunoterapií zaměřenou na důležité kontrolní body imunitních reakcí a rozvojem molekulární biologie s objevem somatické mutace genu BRAF jako jedné z řídících onkogenních mutací u melanomu. Mutace BRAF je popisována přibližně u 50 % kožních melanomů a jednoznačně převažující variantou je mutace BRAF V600E. Selektivní inhibice této mutace se projevuje prodloužením přežití bez progrese i celkového přežívání nemocných. Dabrafenib je reverzibilní ATP kompetitivní inhibitor mutace BRAF, který selektivně inhibuje zejména kinázu BRAF V600E. Prokazuje velmi dobrou účinnost v prodloužení PFS (progression free survival, medián přežití bez známek progrese) i OS (overall survival, celkové přežití) u pacientů s metastazujícím melanomem. Nežádoucí účinky se popisují přibližně u 50–60 % nemocných, jsou převážně stupně 1 a 2 a zcela výjimečně bývají důvodem ukončení léčby. Dabrafenib byl v květnu 2013 schválen pro léčbu neresekovatelného metastazujícího melanomu u pacientů s pozitivní mutací BRAF V600.
Úvod
Pokročilý melanom je nádor s vysokou mortalitou způsobenou zejména rezistencí ke klasickým léčebným postupům. Až do roku 2010 neexistovala žádná léčba, která by dokázala statisticky významně prodloužit celkové přežívání pacientů s metastazujícím melanomem. Medián přežití se pohyboval na úrovni 6–9 měsíců; 3 roky přežívalo při aplikaci chemoterapie, aktinoterapie či jiných kombinovaných léčebných postupů pouze 10–15 % nemocných [1]. Rozvoj specifické imunoterapie cíleně zaměřené na kontrolní body imunitních reakcí znamenal zásadní pokrok v terapii metastazujícího melanomu. Prvním lékem, který podstatně zlepšil šance těchto pacientů, byl ipilimumab. Výsledky registrační studie MDX10-020 publikované v roce 2010 prokázaly, že ipilimumab dokáže statisticky významně prodloužit celkové přežití (overall survival – OS) těchto nemocných a že dosažené léčebné odpovědi přetrvávají mnoho měsíců i let [2]. Současně probíhající rozvoj molekulární biologie umožnil rozpoznání řady onkogenů, které jsou spojeny s proliferací a invazivitou nádorových buněk. Objev somatické mutace genu BRAF, jedné z převažujících řídících onkogenních mutací u kožních melanomů, znamenal nalezení nového významného terapeutického cíle a podnítil vývoj léků zaměřených na inhibici této aktivační mutace.
Mutace BRAF u melanomu
Signální dráha RAS/RAF/MEK/ERK (označována též jako MAPK) bývá aktivována u řady maligních nádorů včetně melanomu. Signální dráha MAPK je hlavní intracelulární dráha, která je odpovědná za buněčnou proliferaci, expresi genů, diferenciaci buněk, jejich mitotickou aktivitu, schopnost buněk přežít i za apoptózu. Aktivační mutace v signální dráze MAPK způsobují trvalou onkogenní proliferaci nádorových buněk i potlačení apoptózy. V roce 2002 popsal Davies, že téměř u 50 % kožních melanomů je možné nalézt mutaci BRAF V600E [3]. Tato mutace, způsobená záměnou valinu za kyselinu glutamovou, představuje 80–90 % všech prokazovaných mutací u melanomu. Výrazně méně často, v necelých 20 %, jsou nalézány další mutace – V600K, způsobená substitucí valinu lysinem, a velmi vzácně i další mutace – V600R nebo V600D. Zastoupení jednotlivých typů mutací BRAF se liší v různých zeměpisných oblastech, druhá nejčastější mutace – V600K – se vyskytuje na severu Evropy pouze u 10 % pacientů, zatímco v Austrálii, Texasu nebo na Floridě bývá prokazována u 20–30 % nádorů. Za jednu z příčin rozdílného výskytu mutace BRAF V600K je považována rozdílná intenzita ultrafialového záření [4]. Byl prokázán onkogenní vliv mutace BRAF u melanomu, ale její přesný význam při rozvoji nádoru není zcela znám. Mutace BRAF je velmi častá u melanocytárních névů a předpokládá se, že stojí na počátku neoplastické transformace melanocytů, avšak není sama o sobě schopna vést až k maligní transformaci. Tu nejspíše podmiňuje kooperace mutace s dalšími genetickými změnami, jako je alterace p53, či s dalšími dosud nepoznanými onkogenními mutacemi. Není přesně znám ani vliv mutace BRAF na progresi melanomu a vznik metastáz. Některé práce uvádějí, že přítomnost mutace BRAF označuje nádory s agresivnějším průběhem, ale jednoznačné spojení tohoto typu mutace s kratším obdobím do progrese (PFS – medián přežití bez známek progrese) nebo s kratším OS nebylo potvrzeno [5]. Aktivační mutace genu BRAF je popisována u 33–47 % primárních melanomů a u 41–55 % metastatických nádorů. V případě primárních melanomů je mutace BRAF popisována zejména u mladších jedinců s melanomy na na kůži poškozené sluncem minimálně a u lidí s vyšším počtem melanocytárních névů. Častěji je prokazována také u silněji pigmentovaných epiteloidních melanomů s prominentním intraepidermálním šířením melanocytů [4]. Relativně častá detekce mutace BRAF u melanomu vedla k vývoji léků, jejichž úkolem je inhibice proteinu BRAF a zablokování jeho onkogenní aktivity. Studie in vitro i první preklinické studie ukázaly, že inhibice mutovaného genu BRAF má u melanomů s mutací BRAF jednoznačný antiproliferační účinek, který není patrný u melanomů s divokým typem BRAF.
Inhibitory BRAF u melanomu
V léčbě pacientů s metastazujícím melanomem s prokázanou pozitivní mutací BRAF se zpočátku zkoušely takzvané neselektivní inhibitory BRAF, jejichž hlavním představitelem je sorafenib. Inhibuje mutovaný i divoký typ proteinu BRAF, protein CRAF a kinázy, jako je VEGFR (vascular endothelial growth factor receptor, receptor pro vaskulární endoteliální růstový faktor) 2, 3, PDGF (platelet-derived growth factor, destičkový růstový faktor), c-kit (receptorová tyrosinkináza), a řadu dalších. V žádné studii však neprokázal v léčbě metastazujícího melanomu dostatečnou účinnost, nedokázal prodloužit PFS ani OS [5].
Významně vyšší účinnost prokázaly až selektivní inhibitory BRAF zaměřené cíleně na mutovanou variantu proteinu BRAF, zejmén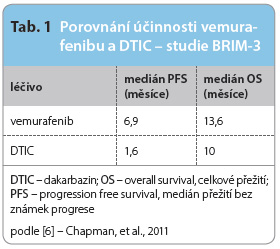 a na mutaci V600E.Prvním selektivním inhibitorem BRAF využívaným v klinické praxi byl vemurafenib, který prokazoval vysokou účinnost v léčbě metastazujícího BRAF V600E pozitivního melanomu již ve studiích fáze I a II. Zásadní byly výsledky studie BRIM-3, které byly publikovány v roce 2011 a aktualizovány v roce 2012 [6, 7]. Vemurafenib v porovnání s léčbou DTIC (dakarbazin) dosáhl vyšší četnosti léčebných odpovědí a významně prodloužil PFS i OS, viz tab. 1. Na základě výsledků studie BRIM-3 byl vemurafenib schválen v roce 2012 FDA (Food and Drug Administration) a EMA (European Medicines Agency) pro léčbu neresekovatelného metastazujícího melanomu s pozitivní mutací BRAF V600.
a na mutaci V600E.Prvním selektivním inhibitorem BRAF využívaným v klinické praxi byl vemurafenib, který prokazoval vysokou účinnost v léčbě metastazujícího BRAF V600E pozitivního melanomu již ve studiích fáze I a II. Zásadní byly výsledky studie BRIM-3, které byly publikovány v roce 2011 a aktualizovány v roce 2012 [6, 7]. Vemurafenib v porovnání s léčbou DTIC (dakarbazin) dosáhl vyšší četnosti léčebných odpovědí a významně prodloužil PFS i OS, viz tab. 1. Na základě výsledků studie BRIM-3 byl vemurafenib schválen v roce 2012 FDA (Food and Drug Administration) a EMA (European Medicines Agency) pro léčbu neresekovatelného metastazujícího melanomu s pozitivní mutací BRAF V600.
Dabrafenib v léčbě metastazujícího melanomu
Dabrafenib je reverzibilní ATP (adenosin-triphosphate) kompetitivní inhibitor mutace BRAF, který selektivně inhibuje zejména kinázu BRAF V600E, viz obr. 1, ale v preklinických studiích prokazoval inhibiční účinek i na buněčných liniích s mutací V600K. První klinické studie s využitím dabrafenibu v léčbě metastazujícího melanomu i dalších solidních nádorů byly zahá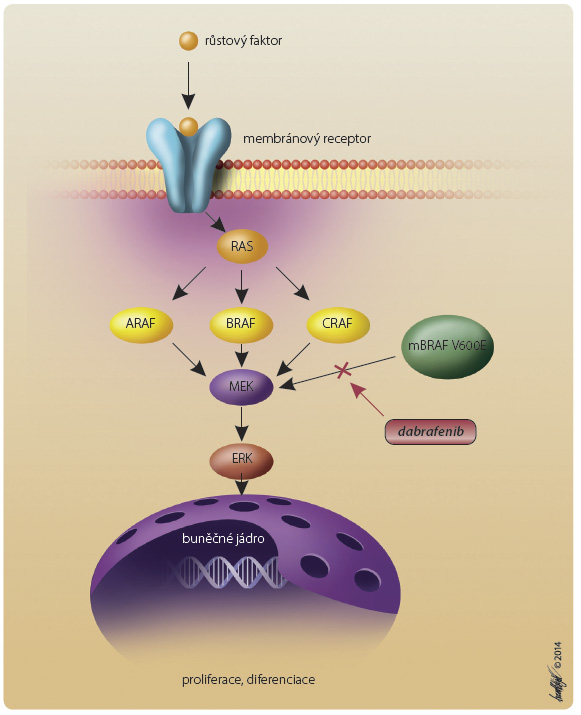 jeny v roce 2009 a první výsledky studií fáze I/II byly publikovány v roce 2010 [8]. Již v průběhu těchto studií byla prokázána účinnost a dobrá snášenlivost dabrafenibu. Současně byla jako dostatečně efektivní a dobře tolerovatelná určena denní dávka 150 mg per os (p.o.) 2krát denně
jeny v roce 2009 a první výsledky studií fáze I/II byly publikovány v roce 2010 [8]. Již v průběhu těchto studií byla prokázána účinnost a dobrá snášenlivost dabrafenibu. Současně byla jako dostatečně efektivní a dobře tolerovatelná určena denní dávka 150 mg per os (p.o.) 2krát denně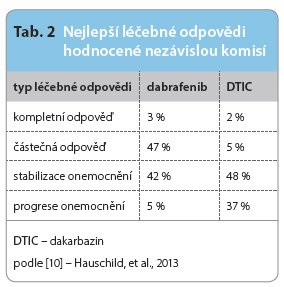 . V roce 2012 a 2013 byly zveřejněny výsledky studie BREAK-3, která porovnávala účinnost dabrafenibu v dávce 150 mg p.o. 2krát denně proti DTIC v dávce 1000 mg/m2 podávané jednou za tři týdny v první linii léčby pacientů s metastazujícím melanomem. U nemocných léčených dabrafenibem dosahoval medián PFS 5,1 měsíce, zatímco u nemocných léčených DTIC dosáhla doba do progrese pouze 2,7 měsíce. Kompletní remise byly popsány u 3 % pacientů a částečné odpovědi až u 47 % nemocných užívajících dabrafenib. Ve skupině nemocných, kteří dostávali DTIC, dosáhlo PR (partial response – částečná odpověď) pouze 5 % pacientů, viz tab. 2. Většina nemocných léčených dabrafenibem odpověděla na léčbu alespoň částečným zmenšením metastáz, což je dobře zřetelné na vodopádovém grafu 1. Výsledky této studie tak prokázaly statisticky významné zlepšení přežití bez progrese a byly konzistentní s výsledky studie BRIM-3 s dalším selektivním inhibitorem BRAF vemurafenibem [9]. Aktualizovaná data studie BREAK-3, přednesená na ASCO (American Society of Clinical Oncology) v roce 2013, potvrdila významné prodloužení PFS, ale prodloužení OS nedosáhlo statistické významnosti. Jedním z důvodů byla pravděpodobně možnost převedení nemocných, u kterých selhala léčba
. V roce 2012 a 2013 byly zveřejněny výsledky studie BREAK-3, která porovnávala účinnost dabrafenibu v dávce 150 mg p.o. 2krát denně proti DTIC v dávce 1000 mg/m2 podávané jednou za tři týdny v první linii léčby pacientů s metastazujícím melanomem. U nemocných léčených dabrafenibem dosahoval medián PFS 5,1 měsíce, zatímco u nemocných léčených DTIC dosáhla doba do progrese pouze 2,7 měsíce. Kompletní remise byly popsány u 3 % pacientů a částečné odpovědi až u 47 % nemocných užívajících dabrafenib. Ve skupině nemocných, kteří dostávali DTIC, dosáhlo PR (partial response – částečná odpověď) pouze 5 % pacientů, viz tab. 2. Většina nemocných léčených dabrafenibem odpověděla na léčbu alespoň částečným zmenšením metastáz, což je dobře zřetelné na vodopádovém grafu 1. Výsledky této studie tak prokázaly statisticky významné zlepšení přežití bez progrese a byly konzistentní s výsledky studie BRIM-3 s dalším selektivním inhibitorem BRAF vemurafenibem [9]. Aktualizovaná data studie BREAK-3, přednesená na ASCO (American Society of Clinical Oncology) v roce 2013, potvrdila významné prodloužení PFS, ale prodloužení OS nedosáhlo statistické významnosti. Jedním z důvodů byla pravděpodobně možnost převedení nemocných, u kterých selhala léčba ![Graf 1 Maximální dosažená změna velikosti nádorové masy od zahájení léčby dabrafenibem; podle [9] – Hauschild, et al., 2012. Každý pacient je označen sloupečkem a jednotlivé barvy označují stadium onemocnění.](https://www.remedia.cz/photo-a-29775---.jpg) DTIC, na léčbu dabrafenibem [10]. Velmi zajímavá jsou publikovaná data ze studie BREAK-MB, hodnotící účinnost dabrafenibu u nemocných s mozkovými metastázami. Obecně platí, že metastázy melanomu v CNS znamenají výrazně horší prognózu a rychlý průběh onemocnění. Medián OS se u těchto pacientů pohybuje mezi 17–22 týdny. Většinu těchto nemocných není možné zařadit do klinických studií, protože mozkové metastázy bývají jedním ze základních vylučujících kritérií. Účinnost léků se tak převážně hodnotí pouze retrospektivně z dat získaných od pacientů s dodatečně prokázanými asymptomatickými mozkovým
DTIC, na léčbu dabrafenibem [10]. Velmi zajímavá jsou publikovaná data ze studie BREAK-MB, hodnotící účinnost dabrafenibu u nemocných s mozkovými metastázami. Obecně platí, že metastázy melanomu v CNS znamenají výrazně horší prognózu a rychlý průběh onemocnění. Medián OS se u těchto pacientů pohybuje mezi 17–22 týdny. Většinu těchto nemocných není možné zařadit do klinických studií, protože mozkové metastázy bývají jedním ze základních vylučujících kritérií. Účinnost léků se tak převážně hodnotí pouze retrospektivně z dat získaných od pacientů s dodatečně prokázanými asymptomatickými mozkovým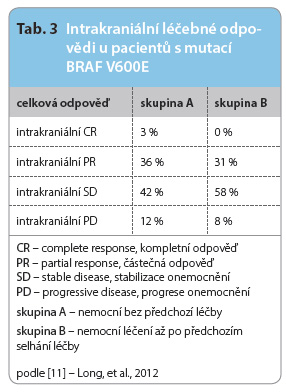 i metastázami. Do studie BREAK-MB byli zařazováni nemocní s minimálně jednou asymptomatickou metastázou v CNS o velikosti 5–40 mm. Nemocní v celkově dobrém klinickém stavu ECOG 0–1 byli rozděleni do dvou skupin podle toho, zda ještě nepodstoupili léčbu mozkových metastáz, nebo u nich již došlo k progresi po předchozí léčbě. V jednotlivých ramenech byli pacienti stratifikováni podle typu V600E nebo V600K mutace BRAF. Primárním cílem studie bylo hodnocení kvality a četnosti léčebných odpovědí u nemocných s mutací BRAF V600E. Pacienti dostávali dabrafenib v dávce 150 mg 2krát denně do progrese nebo toxicity. Pozorované léčebné odpovědi v závislosti na typu mutace jsou uvedeny v tab. 3 a 4. Z výsledků studie je zřejmé, že dabrafenib prokazuje účinnost i v léčbě mozkových metastáz u pacientů s mutací BRAF V600E [11].
i metastázami. Do studie BREAK-MB byli zařazováni nemocní s minimálně jednou asymptomatickou metastázou v CNS o velikosti 5–40 mm. Nemocní v celkově dobrém klinickém stavu ECOG 0–1 byli rozděleni do dvou skupin podle toho, zda ještě nepodstoupili léčbu mozkových metastáz, nebo u nich již došlo k progresi po předchozí léčbě. V jednotlivých ramenech byli pacienti stratifikováni podle typu V600E nebo V600K mutace BRAF. Primárním cílem studie bylo hodnocení kvality a četnosti léčebných odpovědí u nemocných s mutací BRAF V600E. Pacienti dostávali dabrafenib v dávce 150 mg 2krát denně do progrese nebo toxicity. Pozorované léčebné odpovědi v závislosti na typu mutace jsou uvedeny v tab. 3 a 4. Z výsledků studie je zřejmé, že dabrafenib prokazuje účinnost i v léčbě mozkových metastáz u pacientů s mutací BRAF V600E [11].
V roce 2013 byl na základě výsledků studie BREAK-3 dabrafenib schválen FDA a EMA pro léčbu neresekovatelného metastazujícího melanomu s pozitivní mutací BRAF V600.
Nežádoucí účinky léčby dabrafenibem
Dabrafenib je dobře tolerován. Nežádoucí účinky (NÚ) jsou uváděny přibližně u 50–60 % nemocných, bývají převážně stupně 1 a 2 a zcela výjimečně jsou důvodem k ukončení léčby. Nejčastějším NÚ je kožní toxi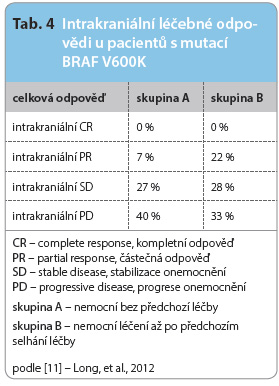 cita. Popisuje se u 30–40 % nemocných a projevuje se vznikem kožního exantému nebo tvorbou hyperkeratotických ložisek. Vzácněji je popisována palmoplantární erytrodysestezie. Fotosenzitivita není příliš častá, uvádí se asi u 2 % léčených pacientů. Stejně jako u vemurafenibu může při léčbě dabrafenibem docházet ke vzniku keratoakantomů a skvamózních karcinomů, které se vyskytují asi u 10 % nemocných, většinou v prvních měsících léčby. Nejsou důvodem ukončení léčby ani snížení dávky [9]. Sporadicky jsou uváděny i další nádorové duplicity, jako je bazaliom nebo nový primární melanom. Mezi NÚ specifické pro dabrafenib patří pyrexie, jejíž etiologie nebyla zatím dostatečně objasněna. Objevuje se většinou v prvních týdnech léčby a u nekomplikovaných případů postačuje pro její zvládnutí podání paracetamolu nebo nesteroidních antiflogistik. V závažnějších případech je nutné dočasné přerušení léčby a po kompenzaci pacienta je možné nové zahájení léčby s nižším dávkováním. Ve studii BREAK-3 byla pyrexie popsána u 16 % nemocných, ale pouze u 1 % nemocných byla provázena závažnými komplikacemi, jako je dehydratace, hypotenze či renální selhání. Přibližně u pětiny nemocných bývá léčba provázena bolestmi kloubů, hlavy nebo zvýšenou únavou. Při léčbě dabrafenibem je nezbytné pravidelné sledování kardiotoxicity pomocí EKG a echokardiografie, za kontraindikaci léčby je považováno skóre NYHA (New York Heart Association) > 2 a interval QTc > 500 ms. Mezi velmi vzácné NÚ patří dále oční či renální toxicita. Pozornost je nutné věnovat také současně podávané medikaci, zejména lékům prodlužujícím interval QT. Dabrafenib, stejně jako ostatní inhibitory BRAF, je substrátem řady enzymů včetně CYP2C8 a CYP3A4. Současné podávání jejich induktorů (například rifampicinu, fenytoinu, fenobarbitalu, třezalky tečkované) nebo inhibitorů (například ketokonazolu, klarithromycinu, ritonaviru) tak může ovlivňovat hladinu dabrafenibu a jeho účinnost či toxicitu [12].
cita. Popisuje se u 30–40 % nemocných a projevuje se vznikem kožního exantému nebo tvorbou hyperkeratotických ložisek. Vzácněji je popisována palmoplantární erytrodysestezie. Fotosenzitivita není příliš častá, uvádí se asi u 2 % léčených pacientů. Stejně jako u vemurafenibu může při léčbě dabrafenibem docházet ke vzniku keratoakantomů a skvamózních karcinomů, které se vyskytují asi u 10 % nemocných, většinou v prvních měsících léčby. Nejsou důvodem ukončení léčby ani snížení dávky [9]. Sporadicky jsou uváděny i další nádorové duplicity, jako je bazaliom nebo nový primární melanom. Mezi NÚ specifické pro dabrafenib patří pyrexie, jejíž etiologie nebyla zatím dostatečně objasněna. Objevuje se většinou v prvních týdnech léčby a u nekomplikovaných případů postačuje pro její zvládnutí podání paracetamolu nebo nesteroidních antiflogistik. V závažnějších případech je nutné dočasné přerušení léčby a po kompenzaci pacienta je možné nové zahájení léčby s nižším dávkováním. Ve studii BREAK-3 byla pyrexie popsána u 16 % nemocných, ale pouze u 1 % nemocných byla provázena závažnými komplikacemi, jako je dehydratace, hypotenze či renální selhání. Přibližně u pětiny nemocných bývá léčba provázena bolestmi kloubů, hlavy nebo zvýšenou únavou. Při léčbě dabrafenibem je nezbytné pravidelné sledování kardiotoxicity pomocí EKG a echokardiografie, za kontraindikaci léčby je považováno skóre NYHA (New York Heart Association) > 2 a interval QTc > 500 ms. Mezi velmi vzácné NÚ patří dále oční či renální toxicita. Pozornost je nutné věnovat také současně podávané medikaci, zejména lékům prodlužujícím interval QT. Dabrafenib, stejně jako ostatní inhibitory BRAF, je substrátem řady enzymů včetně CYP2C8 a CYP3A4. Současné podávání jejich induktorů (například rifampicinu, fenytoinu, fenobarbitalu, třezalky tečkované) nebo inhibitorů (například ketokonazolu, klarithromycinu, ritonaviru) tak může ovlivňovat hladinu dabrafenibu a jeho účinnost či toxicitu [12].
Závěr
Mutace BRAF V600 je popisována přibližně u poloviny nemocných s metastazujícím melanomem. Inhibice této mutace vede k rychlému nástupu léčebného účinku, který se pohybuje na úrovni maximálně několika málo týdnů. Pacienti pozorují brzy po zahájení léčby inhibitory BRAF klinicky zřetelné zmenšování nádorových ložisek i subjektivní úlevu od potíží způsobených metastázami. Velmi příznivý je vysoký počet léčebných odpovědí, který je popisován napříč studie-
mi. U většiny nemocných léčených inhibitory BRAF dochází k alespoň částečnému zmenšení nádorové masy a objektivní léčebné odpovědi (CR + PR) se objevují minimálně u poloviny nemocných. Dabrafenib patří mezi tak zvané selektivní inhibitory BRAF, léky schopné zablokovat aktivační mutaci BRAF V600E a tím potlačit nádorovou proliferaci. V klinických studiích prokázal dabrafenib, že je účinný v léčbě metastazujícího melanomu s pozitivní mutací BRAF V600, zejména s variantami V600E a V600K [13]. Vyvolává dostatečně vysoké procento léčebných odpovědí a prokazuje aktivitu i u mozkových metastáz. Díky výsledkům klinických studií, zejména studie BREAK-3, byl dabrafenib schválen FDA a EMA pro léčbu metastazujícího melanomu s pozitivní mutací BRAF V600. Dabrafenib je možné používat v monoterapii, ale očekávají se také výsledky studií kombinované léčby s inhibitory MEK, které by mohly ještě zvýšit jeho účinnost a oddálit vznik případné rezistence.
Seznam použité literatury
- [1] Korn EL, Lin PY, Lee SJ, et al. Meta-analysis of phase II coop. group trials in metastatic stage IV melanoma to determine PFS and OS benchmarks for future phase II trials. JCO 2008; 26: 527–534.
- [2] Hodi FS, O’Day SJ, McDermott DF, et al. Improved Survival with Ipilimumab in Patients with Metastatic Melanoma. N Engl J Med 2010; 363: 711–723. doi:10.1056/NEJMoa1003466.
- [3] Davies H, Bignell GR, Cox C, et al. Mutations of the BRAF gene in human cancer. Nature 2002; 417: 949–954.
- [4] Long GV, Menzies AM, Nagrial AM, et al. Prognostic and Clinicopathologic Associations of Oncogenic BRAF in Metastatic Melanoma. J Clin Oncol 2011; 29: 1239–1246.
- [5] Menzies MA, Long GV, Murali R. Dabrafenib and its potential for the treatment of metastatic melanoma. Drug Des Devel Ther 2012; 6: 391–405.
- [6] Chapman PB, Hauschild A, Robert,C, et al. BRIM-3 study group. Improved survival with vemurafenib in melanoma with BRAF V600E mutation. N Engl J Med 2011; 364: 2507–2516.
- [7] Chapman PB, Hauschild A, Robert C, et al. Updated overall survival (OS) results for BRIM-3, a phase III randomized, open-label, multicenter trial comparing BRAF inhibitor vemurafenib (vem) with dacarbazine (DTIC) in previously untreated patients with BRAFV600E-mutated melanoma [abstract]. J Clin Oncol 2012; 30 (15 Suppl): Abstract 8502.
- [8] Kefford R, Arkenau H, Brown MP, et al. PhaseI/II study of GSK22118436, a selective inhibitor of oncogenic mutant BRAF kinase in patients with metastatic melanoma and other solid tumors. (abstract). J Clin Oncol 2010; 28 (15 Suppl): S611. Abstract 8503.
- [9] Hauschild A, Grob JJ, Demidov LV, et al. Dabrafenib in BRAF mutated metastatic melanoma: a multicentre, open-label, phase 3 randomized controlled trial. Lancet 2012; 380: 358–365.
- [10] Hauschild A, Grob JJ, Demidov LV, et al. An update on BREAK-3 a phase III randomized trial: dabrafenib versus DTIC in patients with BRAF V600E positive mutation metastatic melanoma. ASCO, 2013. Abstract 19013.
- [11] Long GV, Trefzer U, Davies MA, et al. Dabrafenib in patients with Val600Glu or Val600Lys BRAF-mutant melanoma metastatic to the brain (BREAK-MB):a multicentre, open-label, phase 2 trial. Lancet 2012, Published online October 8, 2012 http://dx.doi.org/10.1016/S1470-2045(12)70431-X
- [12] Tafinlar: Souhrn údajů o přípravku. dostupné na http://www.ema.europa.eu/docs/cs_CZ/document_library/EPAR_-_Product_Information/human/002604/WC500149671.pdf
- [13] Kainthla R, Kim KB, Falchook GS. Dabrafenib for treatment of BRAF-mutant melanoma. Pharmacogeno-mics Pers Med 2013; 7: 21–29.