Dronedaron ve světle nových klinických studií
Dronedaron je nové perorální antiarytmikum III. třídy dle klasifikace Vaughana-Williamse. Jedná se o benzofuranový derivát, který má obdobné elektrofyziologické účinky jako amiodaron, nevykazuje však plicní toxicitu a neovlivňuje funkci štítné žlázy. Má příznivý efekt v prevenci paroxysmů fibrilace síní, snižuje frekvenci komor při fibrilaci síní. Není vhodný u nemocných s pokročilým srdečním selháním. Jako první antiarytmikum v léčbě fibrilace síní ovlivnil kardiovaskulární mortalitu.
Úvod
Fibrilace síní představuje nejčastější setrvalou arytmii v dospělé populaci. Její výskyt roste s věkem a prevalence stoupá až k 10 % u osob starších 80 let. Symptomy nemocných mohou být způsobeny urychlenou komorovou odpovědí, ztrátou síňového příspěvku a vnímáním nepravidelné srdeční akce. Vedle zhoršené kvality života je důležité, že fibrilace síní vede i ke zvýšené morbiditě a mortalitě. U nemocných s paroxysmální, perzistující či permanentní fibrilací síní lze zvolit dva léčebné farmakologické přístupy: buď usilovat o obnovu a udržení sinusového rytmu, nebo ponechat fibrilaci síní a kontrolovat přiměřenou frekvenci komor. U výrazně symptomatických nemocných je udržení sinusového rytmu důležité. Kontrolu rytmu bychom měli preferovat v počátečních fázích léčby a samozřejmě u mladších pacientů [1–4].
Přes veškeré pokroky v nefarmakologické léčbě poruch rytmu zůstává u velké většiny nemocných s fibrilací síní farmakologická léčba základní léčebnou metodou. Při strategii kontroly srdečního rytmu jsou používána antiarytmika a další léčiva k obnově a udržení sinusového rytmu (především konvenční antiarytmika třídy III a I – dle původní klasifikace). Hlavní nevýhodou dosavadních antiarytmik je jejich omezená účinnost v udržení sinusového rytmu a současně závažné nežádoucí účinky. Nejúčinnějším antiarytmikem v udržení sinusového rytmu se dle výsledků studie CTAF [5] jeví amiodaron (69 % vs. 39 % pro propafenon nebo sotalol), při léčbě tímto antiarytmikem je však výskyt klinicky závažnějších nežádoucích účinků uváděn až ve 35 %. Je tedy mimořádná snaha o vývoj účinné a současně bezpečné antiarytmické medikamentózní léčby.
Dronedaron
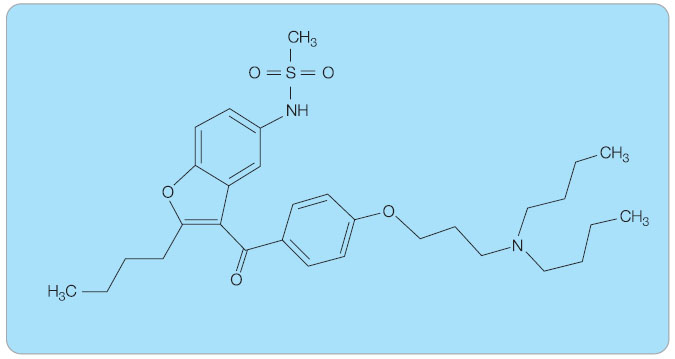 Dronedaron (SR33589B) představuje nové perorální antiarytmikum řazené do III. třídy dle Vaughana-Williamse [6]. Dronedaron, chemicky N-[2-butyl-3-[p-[3-(dibutylamino)propoxy]benzoyl]-5-benzofuranyl]methansulfonamid, je benzofuranový derivát (obr. 1), který na rozdíl od amiodaronu postrádá molekulu jodu a navíc má methansulfonamidovou skupinu. Právě chybění jodu vysvětluje fakt, že dronedaron nemá závažné nežádoucí účinky na plicní funkce a na funkci štítné žlázy. Naopak přítomnost methansulfonamidové skupiny vysvětluje nižší lipofilii, kratší poločas vylučování a menší akumulaci ve tkáních ve srovnání s amiodaronem. Stejně jako amiodaron vykazuje efekt všech čtyř tříd podle Vaughanovy-Williamsovy klasifikace. Blokuje sodíkový kanál, má antiadrenergní vlastnosti, prodlužuje délku akčního potenciálu a má negativně chronotropní efekt na buňky v sinoatriálním a atrioventrikulárním uzlu. Působí i jako antagonista kalcia.
Dronedaron (SR33589B) představuje nové perorální antiarytmikum řazené do III. třídy dle Vaughana-Williamse [6]. Dronedaron, chemicky N-[2-butyl-3-[p-[3-(dibutylamino)propoxy]benzoyl]-5-benzofuranyl]methansulfonamid, je benzofuranový derivát (obr. 1), který na rozdíl od amiodaronu postrádá molekulu jodu a navíc má methansulfonamidovou skupinu. Právě chybění jodu vysvětluje fakt, že dronedaron nemá závažné nežádoucí účinky na plicní funkce a na funkci štítné žlázy. Naopak přítomnost methansulfonamidové skupiny vysvětluje nižší lipofilii, kratší poločas vylučování a menší akumulaci ve tkáních ve srovnání s amiodaronem. Stejně jako amiodaron vykazuje efekt všech čtyř tříd podle Vaughanovy-Williamsovy klasifikace. Blokuje sodíkový kanál, má antiadrenergní vlastnosti, prodlužuje délku akčního potenciálu a má negativně chronotropní efekt na buňky v sinoatriálním a atrioventrikulárním uzlu. Působí i jako antagonista kalcia.
Farmakokinetické vlastnosti
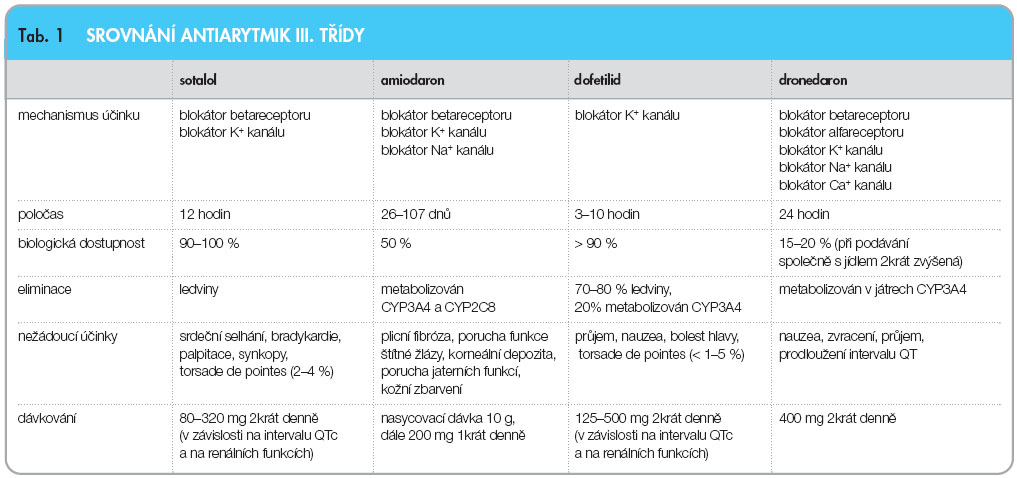 V tab. 1 jsou srovnány některé vlastnosti antiarytmik řazených do III. třídy dle Vaughana-Williamse. Poločas vylučování dronedaronu je 24 hodin, vylučuje se stolicí, bez prokazatelných metabolických produktů v moči. Biologická dostupnost je vzhledem k first-pass efektu 15–20 %, ale pokud je lék podáván spolu s potravou, zvyšuje se jeho biologická dostupnost minimálně dvojnásobně. Při obvyklém dávkování 2krát 400 mg denně je dosaženo vyrovnané hladiny dronedaronu (steady state) za 5–7 dní. Přípravek je metabolizován v játrech, a to cytochromoxidázovým systémem CYP3A4, podobně jako amiodaron a dofetilid, což je třeba respektovat například při léčbě warfarinem, INR zvyšuje lehce, 1,07krát.
V tab. 1 jsou srovnány některé vlastnosti antiarytmik řazených do III. třídy dle Vaughana-Williamse. Poločas vylučování dronedaronu je 24 hodin, vylučuje se stolicí, bez prokazatelných metabolických produktů v moči. Biologická dostupnost je vzhledem k first-pass efektu 15–20 %, ale pokud je lék podáván spolu s potravou, zvyšuje se jeho biologická dostupnost minimálně dvojnásobně. Při obvyklém dávkování 2krát 400 mg denně je dosaženo vyrovnané hladiny dronedaronu (steady state) za 5–7 dní. Přípravek je metabolizován v játrech, a to cytochromoxidázovým systémem CYP3A4, podobně jako amiodaron a dofetilid, což je třeba respektovat například při léčbě warfarinem, INR zvyšuje lehce, 1,07krát.
Nežádoucí účinky dronedaronu
Dronedaron prodlužuje interval QTc, nicméně v žádné z dosud provedených klinických studií nebyl prokázán jeho proarytmogenní efekt. Dronedaron snižuje srdeční frekvenci, může vést k symptomatické bradykardii. Nejčastějším nežádoucím účinkem jsou gastrointestinální obtíže – průjem a nauzea, dále vyrážka. Je popisováno zvýšení hladiny sérového kreatininu o 18 %, nebyl však prokázán vliv na glomerulární filtraci [7]. Důležité je, že nebyly v souvislosti s léčbou dronedaronem popsány obávané nežádoucí účinky vyskytující se při léčbě amiodaronem, to jest nebylo přítomno žádné plicní postižení ani porucha funkce štítné žlázy.
Klinické studie s dronedaronem
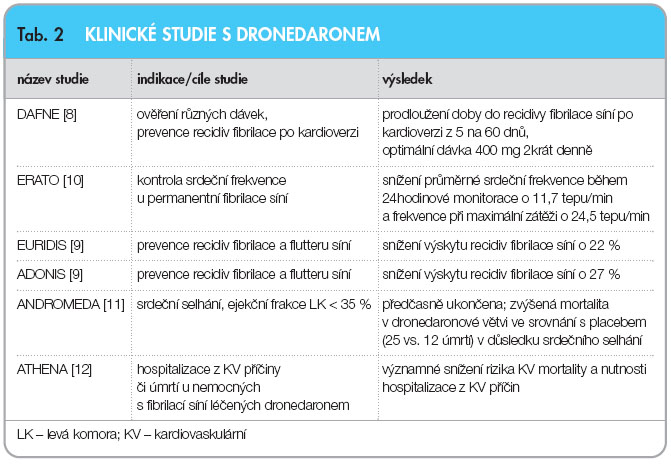 Tab. 2 uvádí přehled nejdůležitějších klinických studií, které byly dokončeny a publikovány od roku 2006. Studie DAFNE (Dronedaron Atrial FibrillatioN study after Electrical cardioversion) [8] ověřovala účinnost různých dávek dronedaronu na dobu do recidivy fibrilace síní po elektrické kardioverzi. Byla ověřena účinnost dronedaronu ve srovnání s placebem, prodloužena doba do první recidivy z 5 na 60 dnů a zjištěna optimální účinnost dávky 400 mg dvakrát denně. Dávky 600 mg a 800 mg dvakrát denně nevedly k lepšímu antiarytmickému efektu.
Tab. 2 uvádí přehled nejdůležitějších klinických studií, které byly dokončeny a publikovány od roku 2006. Studie DAFNE (Dronedaron Atrial FibrillatioN study after Electrical cardioversion) [8] ověřovala účinnost různých dávek dronedaronu na dobu do recidivy fibrilace síní po elektrické kardioverzi. Byla ověřena účinnost dronedaronu ve srovnání s placebem, prodloužena doba do první recidivy z 5 na 60 dnů a zjištěna optimální účinnost dávky 400 mg dvakrát denně. Dávky 600 mg a 800 mg dvakrát denně nevedly k lepšímu antiarytmickému efektu.
V následujících dvou analogických studiích [9] byl ověřován efekt a bezpečnost dronedaronu u nemocných s paroxysmální fibrilací síní. Jednalo se o evropskou studii EURIDIS (EURopean trial In atrial fibrillation or flutter patients receiving Dronedaron for the maintenance of Sinus rhythm) a americko-australskou studii ADONIS (American-Australian trial with Dronedaron In atrial fibrillation or flutter patients for the maintenance of Sinus rhythm). V obou studiích bylo při dávce 400 mg 2krát denně pozorováno snížení počtu recidiv fibrilace síní o 22 %, resp. o 27 %. Dále byl prokázán příznivý dopad na průměrnou srdeční frekvenci při recidivě arytmie. Studie ERATO (Efficacy and safety of dronedaron for The cOntrol of ventricular rate) [10] potvrdila schopnost dronedaronu snížit průměrnou srdeční frekvenci komor při fibrilaci síní během 24hodinové monitorace o 11,7 tepu/min a při maximální zátěži o 24,5 tepu/min.
Studie ANDROMEDA (ANtiarrhythmic trial with Dronedaron in Moderate to severe congestive heart failure Evaluation morbidity DecreAse) [11] byla předčasně ukončena. Byla zahájena 12. 6. 2002 a ukončena 16. 1. 2003, průměrná doba sledování činila 2 měsíce. Cílem studie bylo ověřit vliv dronedaronu na úmrtí a hospitalizace na srdeční selhání u nemocných se srdeční insuficiencí a dysfunkcí levé komory srdeční (EF < 35 %). Fibrilace síní byla přítomna v anamnéze u necelých 40 % nemocných a v době randomizace u 25 % pacientů. V léčené skupině byla ve srovnání s placebem vyšší mortalita (25 vs. 12 úmrtí) především v důsledku progrese srdečního selhání, zemřelo 10 nemocných v dronedaronové větvi a pouze 2 nemocní v placebové větvi. Post hoc analýza ukázala korelaci mezi vyšší incidencí mortality a ukončením léčby inhibitory ACE či sartany v dronedaronové větvi. Důvodem ukončení léčby inhibitory ACE či sartany mohlo být i zvýšení koncentrace sérové hladiny kreatininu, které bylo popisováno v dronedaronové větvi. Nelze však vyloučit ani možný negativně inotropní efekt dronedaronu u nemocných s těžkou systolickou dysfunkcí. Zajímavé je, že nebyl zaznamenán žádný proarytmogenní efekt dronedaronu ani u této vysoce rizikové skupiny. Z výsledků studie vyplývá, že dronedaron by neměl být podáván u nemocných s manifestním srdečním selháním a omezenou funkcí levé komory srdeční.
S mimořádným zájmem byly očekávány výsledky studie ATHENA (A Trial with dronedaron to prevent Hospitalization or death in patiENts with Atrial fibrillation) [12]. Tato multicentrická studie randomizovala 4628 nemocných s fibrilací síní a dalším kardiovaskulárním rizikem (alespoň jeden z následujících rizikových faktorů: věk nad 70 let, hypertenze, diabetes mellitus, anamnéza cévní mozkové příhody, tranzitorní ischemické ataky, dilatace levé síně, ejekční frakce levé komory < 40 %). Do studie byli zařazeni nemocní s paroxysmální či perzistentní fibrilací síní, průměrná doba sledování činila 21 měsíců. Léčbu dronedaronem předčasně ![Graf 1 Výsledky studie ATHENA. Vliv podávání dronedaronu na (A) počet hospitalizací z kardiovaskulární příčiny či úmrtí, (B) celkovou mortalitu, (C) kardiovaskulární mortalitu, (D) hospitalizace pro kardiovaskulární onemocnění; podle [12] – Hohnloser, et al., 2009.](https://www.remedia.cz/photo-a-27706---.jpg) ukončilo 696 nemocných (30,2 %), nicméně v placebové větvi byla léčba předčasně ukončena u 716 nemocných (30,8 %). Primárním sledovaným cílem byla hospitalizace z kardiovaskulární příčiny či úmrtí. Sekundárním sledovaným cílem byla celková mortalita, kardiovaskulární mortalita a hospitalizace. Výsledky byly publikovány v letošním roce a jsou uvedeny v grafu 1. Dronedaron ve srovnání s placebem významně snížil riziko kardiovaskulární mortality a nutnosti hospitalizace z kardiovaskulárních příčin. Post hoc analýza prokázala navíc snížení rizika cévní mozkové příhody o 34 % u nemocných randomizovaných k léčbě dronedaronem [13], tento zajímavý efekt není dosud jednoznačně vysvětlen a vyžaduje další studie.
ukončilo 696 nemocných (30,2 %), nicméně v placebové větvi byla léčba předčasně ukončena u 716 nemocných (30,8 %). Primárním sledovaným cílem byla hospitalizace z kardiovaskulární příčiny či úmrtí. Sekundárním sledovaným cílem byla celková mortalita, kardiovaskulární mortalita a hospitalizace. Výsledky byly publikovány v letošním roce a jsou uvedeny v grafu 1. Dronedaron ve srovnání s placebem významně snížil riziko kardiovaskulární mortality a nutnosti hospitalizace z kardiovaskulárních příčin. Post hoc analýza prokázala navíc snížení rizika cévní mozkové příhody o 34 % u nemocných randomizovaných k léčbě dronedaronem [13], tento zajímavý efekt není dosud jednoznačně vysvětlen a vyžaduje další studie.
Vzhledem k tomu, že amiodaron je v současné době nejúčinnějším antiarytmikem v prevenci recidiv fibrilace síní, nabízí se otázka srovnání účinnosti amiodaronu a dronedaronu. Recentně byla publikována metaanalýza [14] porovnávající tato dvě antiarytmika ve srovnání s placebem. Práce prokazuje, že amiodaron je účinnější v prevenci recidiv fibrilace síní než dronedaron, nicméně dronedaron je lépe tolerován; léčba je provázena menším výskytem nežádoucích účinků a není nutné ji tak často z důvodu nežádoucích účinků přerušovat. Výsledky této metaanalýzy odpovídají i závěrům studie DIONYSOS (Efficacy and Safety of Dronedarone Versus Amiodarone for the Maintenance of Sinus Rhythm in Patients with Atrial Fibrillation), která dosud nebyla publikována v odborném písemnictví, ale data jsou k dispozici na webových stránkách společnosti sanofi-aventis. Studie porovnávala účinnost a bezpečnost amiodaronu a dronedaronu u 504 nemocných s perzistentní fibrilací síní. Fibrilace síní po elektrické kardioverzi se vyskytla u 36,5 % nemocných léčených dronedaronem a u 24,3 % nemocných léčených amiodaronem. Pro nežádoucí účinky však bylo třeba přerušit léčbu u 34 nemocných léčených amiodaronem, zatímco u nemocných léčených dronedaronem tomu bylo v 26 případech. Současně byl potvrzen i vyšší výskyt poruchy funkce štítné žlázy a neurologických nežádoucích účinků u nemocných léčených amiodaronem.
V současné době probíhají další studie s dronedaronem u nemocných s implantovaným kardioverterem/defibrilátorem, v pilotních studiích dronedaron snižoval nutnost aplikace léčby pro komorové tachyarytmie.
Závěr
Seznam použité literatury
- [1] Čihák R, Heinc P. Doporučení pro léčbu pacientů s fibrilací síní. Cor Vasa 2004; 46: K 67–77.
- [2] Fuster V, Ryden LE, Cannom DS, et al. ACC/AHA/ESC 2006 guidelines for the management of patients with atrial fibrillation. Europace 2006; 8: 651–745.
- [3] Wyse DG, Waldo AL, DiMarco JP, et al. Atrial Fibrillation Follow-up Investigation of Rhythm Management (AFFIRM) Investigators. A comparison of rate control and rhythm control in patients with atrial fibrillation. N Engl J Med 2002; 347: 1825–1833.
- [4] Wijffels MC, Crijns HJ. Recent advances in drug therapy for atrial fibrillation. J Cardiovasc Electrophysiol 2003; 14: S40–47.
- [5] Roy D, Talajic M, Dorian P, et al., for the Canadian Trial of Atrial Fibrillation Investigators. Amiodaron to prevent recurrence of atrial fibrillation. N Engl J Med 2000; 342: 913–920.
- [6] Čihák R. Dronedaron. Remedia 2006; 4: 443–446.
- [7] Tschuppert Y, Buclin T, Rothuizen LE, et al. Effect of dronedaron on renal function in healthy subjects. Br J Clin Pharmacol 2007; 64: 785–791.
- [8] Toubol P, Brugada J, Capucci A, et al. Dronedaron for prevention of atrial fibrillation: a dose ranging Study. Eur Heart J 2003; 24: 1481–1487.
- [9] Singh BN, Connolly SJ, Crijns HJ, et al. Dronedaron for maintenance of sinus rhythm in atrial fibrillation or flutter. N Engl J Med 2007; 357: 987–999.
- [10] Davy JM, Herold M, Hoglund C, et al. Dronedaron for the control of ventricular rate in permanent atrial fibrillation: The Efficacy and safety of dronedaron for the control of ventricular rate during atrial fibrillation (ERATO study). Am Heart J 2008; 156: 527–529.
- [11] Kober L, Torp-Pedersen C, McMurray JV, et al. Increased mortality after dronedaron therapy for severe heart failure. N Engl J Med 2008; 358: 2678–2687.
- [12] Hohnloser SH, Crijns HJ, van Eickels M, et al., for the ATHENA Investigators. Effect of dronedaron on cardiovascular events in atrial fibrillation. N Engl J Med 2009; 360: 668–678.
- [13] Connolly SJ, Crijns HJ, Torp-Pedersen C, et al. Analysis of stroke in ATHENA: A placebo controlled, double- blind, parallel-arm trial to assess the efficacy of dronedarone 400mg bid for the prevention of cardiovascular hospitalization or death from any cause in patients with atrial fibrillation/atrial flutter. Circulation 2009; 120: 1174–1180.
- [14] Piccini JP, Hasselblad V, Peterson ED, et al. Comparative efficacy of dronedarone and amiodarone for the maintenance of sinus rhythm in patients with atrial fibrillation. J Am Coll Cardiol 2009; 54: 1089–1095.