Itoprid
Prokinetikum, periferní antagonista dopaminových receptorů a inhibitor acetylcholinesterázy s predilekčním účinkem na horní část trávicí trubice, především žaludek. Jeho užití v klinické medicíně je omezeno jen na několik asijských zemí, v západní Evropě a v USA není používán. V České republice je registrován od roku 2000. Podrobné randomizované placebem kontrolované studie chybí. Hlavními indikacemi jsou funkční žaludeční dyspepsie typu chabého žaludku a diabetická viscerální gastropatie. Jako doplňkovou terapii je možné itoprid využít u nekomplikované refluxní choroby jícnu a postgastrektomického syndromu. Pro jeho menší antiemetogenní vliv jej lze užít jako součást komplexní terapie některých organických onemocnění horní části trávicí trubice. Obvyklá denní dávka je 150 mg rozdělená do tří dílčích dávek a podávaných půl hodiny před větším jídlem. Nedostaví-li se efekt, je možné dávky léku zdvojnásobit. Itoprid je velmi dobře snášen a má minimum nežádoucích účinků.
Úvod
Prokinetika jsou skupinou látek, které svým působením stimulují a normalizují motilitu trávicího ústrojí. Rychlejším vyprazdňováním žaludku zabraňují retenci a refluxu žaludeční kyseliny a jídla. Po celé délce trávicího traktu působil cisaprid, který stimuloval uvolňování acetylcholinu v myenterickém plexu. Byl však pro své nežádoucí (kardiotoxické) účinky stažen z trhu. Další prokinetika – metoclopramid a domperidon – jsou antagonisty dopaminu a nemají účinek na motilitu tlustého střeva. Nová látka itoprid se vyznačuje duálním působením – působí proto po celé délce trávicího traktu.
Mechanismus účinku
Itoprid zvyšuje koncentraci acetylcholinu v postgangliovém zakončení neuronů ve stěně trávicího ústrojí. Zvýšenou dostupnost acetylcholinu na neuromuskulární synapsi itoprid zajišťuje dvojím způsobem:
1. ‑Inhibicí dopaminových D2-receptorů, které mají inhibiční účinek na nervosvalovou dráždivost v trávicí trubici. Tyto receptory jsou lokalizovány pouze na horní části trávicí trubice na jícnu a žaludku, nikoliv na tenkém a tlustém střevě. To vysvětluje rozsah prokinetického účinku itopridu.
2. ‑Inhibicí aktivity acetylcholinesterázy se významně snižuje rychlost odbourávání acetylcholinu. Vysoká hladina acetylcholinu na neuromuskulárních synapsích je odpovědná za zvýšení peristaltiky jícnu, stimulaci žaludeční motility, urychlení vyprazdňování žaludku a zlepšení gastroduodenální koordinace.
Při studiu gastrointestinální motility byl zjištěn nejvýraznější účinek itopridu na zvýšení motility žaludečního antra [1].
Farmakokinetické vlastnosti
Itoprid je po perorálním podání rychle a téměř kompletně absorbován. Relativní biologická dostupnost je vzhledem k „first pass efektu" asi 60 %. Důležité je, že jídlem není významně ovlivněna. Maximální plazmatické koncentrace bývá dosaženo za 30 minut po podání 50mg tablety itopridu. Z 96 % se váže na plazmatické bílkoviny. Metabolizuje se v játrech cestou flavinmonooxygenázy a hlavním metabolitem je N-oxid-itoprid [12]. Vylučuje se ze 75 % močí. Poločas vylučování je 6 hodin. Farmakokinetika je v rozsahu terapeutické dávky lineární [1].
Klinické zkušenosti
Itoprid byl vyvinut v laboratoři Hokuriku Seiyaku Co., Ltd. v Japonsku v roce 1987 a označen jako prokinetikum (gastrokinetikum) s antiemetickým účinkem. V letech 1989–1992 proběhly klinické fáze výzkumu. V Japonsku bylo schváleno klinické používání v roce 1995, v Koreji v roce 1998 a v České republice v roce 2000.
V běžně dostupné zahraniční (evropské a severoamerické) literatuře nejsou s tímto prokinetikem žádné větší zkušenosti. Zajímavé je, že na velkých světových gastroenterologických konferencích (USA-DDW nebo Evropa-UEGW) nebyla ve farmakologických přehledech o ovlivnění motility trávicí trubice věnována itopridu žádná pozornost. V našem písemnictví existují pouze dvě práce [2, 4]. Vlivem itopridu u pacientů s funkční dyspepsií horního typu se zabývala první z nich. Jednalo se o nerandomizovanou a nekontrolovanou zkoušku. Do sledování bylo zahrnuto 91 osob v průměrném věku 39 let. Po 56 dnech léčby itopridem bylo zaznamenáno významné zlepšení klinického stavu u 88 % pacientů s bolestmi hlavy, u 88 % nemocných s břišním dyskomfortem, u 83 % pacientů s pocity plnosti v nadbřišku; 83 % léčených vykazovalo ústup nauzey a (nebo) zvracení, 85,0 % nemocných uvedlo zlepšení pocitu předčasné sytosti. Při podávání léku nedošlo u skupiny pacientů k signifikantnímu prodloužení intervalu QTc na EKG. Žádná ze sledovaných laboratorních hodnot se statisticky významně neodchýlila od normy. Z vedlejších účinků se vyskytla po 28 dnech u jednoho pacienta bolest hlavy a tento byl ze studie vyřazen [2]. Gurlich se spolupracovníky zkoumal vliv aplikace itopridu na zkrácení postoperační atonie trávicí trubice u nemocných, kteří se podrobili laparoskopické bandáži žaludku nebo laparoskopické cholecystektomii. Vedle klinických parametrů užil k monitorování motility žaludku také perkutánní elektrogastrografii. Autoři prokázali, že aplikace itopridu před operací vede k významnému zkrácení pooperační atonie horní části trávicí trubice. Lék byl velmi dobře snášen a neobjevily se žádné vedlejší účinky [4]. Rane hodnotil efektivitu a bezpečnost 2týdenní léčby itopridem u nemocných s funkční dyspepsií horního typu. Na souboru 60 nemocných byla porovnávána účinnost itopridu (50 mg 3x denně) a mosapridu (5 mg 3x denně). Ve skupině nemocných léčených itopridem byl zaznamenán signifikantně vyšší účinek na potlačení dyspeptických obtíží v porovnání s kontrolním prokinetikem [5].
V roce 1999 byla provedena srovnávací studie se zdravou populací, která prokázala signifikantně vyšší výskyt trávicích obtíží v horní části GIT u diabetiků. Prevalence zažívacích obtíží se zdá být u těchto pacientů extrémně častá a dosahuje hodnoty 45–76 %. Symptomy jsou způsobeny poruchami motility v důsledku diabetické autonomní (viscerální) neuropatie, a navíc mohou být také ovlivňovány kolísající hladinou glykémie [6]. Klíčovými orgány postiženými u pacientů s diabetes mellitus jsou jícen a žaludek. Klinické projevy zahrnují pocit plnosti v epigastriu, pocit předčasné sytosti, nauzeu, nadýmání a zvracení. Jde o poruchy motility jícnu a především abnormální vyprazdňování žaludku. Při patologickém vyprazdňování žaludku jde o poruchu gastroduodenálního tlakového gradientu, na kterém se podílejí největší měrou prolongované kontrakce svaloviny pylorického kanálu. Laboratorně jsou u těchto nemocných prokazovány vysoké plazmatické hladiny motilinu, které se po zavedení terapie prokinetiky normalizují. Protože hlavním místem příznivého účinku itopridu je právě žaludeční antrum a pylorus, jehož motilita bývá při diabetické viscerální neuropatii nejvíce postižena, je aplikace léčiva v této indikaci velmi perspektivní. V tomto ohledu však bude nutno vyčkat výsledků dalších kontrolovaných studií. Raritní koincidence diabetes mellitus s achalázií byla popsána u 54leté pacientky. Tato pacientka podstoupila laparoskopickou myotomii, jejíž rozsah byl předoperačně ověřen jícnovou manometrií. Zhruba měsíc po výkonu přetrvávaly dysfagické obtíže, zvláště po požití tuhé stravy a některých druhů ovoce. Balonová kalibrace kardie nepřinesla vysvětlení těchto obtíží a ke zlepšení vedlo podání itopridu (3x denně 50 mg) [7].
Účinek itopridu byl podle japonských údajů ověřen u horní funkční dyspepsie u velké skupiny 5 447 pacientů s dobrým efektem u 5 183 (95,1 %) z nich. Také u postgastrektomického syndromu byl prokazatelně příznivý vliv léčiva potvrzen u 32 (88,9 %) z 36členné léčené skupiny. Podobně příznivé výsledky po podání itopridu byly v Japonsku uveřejněny při léčbě refluxní choroby jícnu. Ze 36 pacientů léčených pro reflux byl příznivý vliv (zlepšení symptomového skóre) zjištěn u 32 (88,9 %) z nich [3]. Pozitivní efekt u pacientů s refluxní chorobou jícnu ověřila také studie provedená v Jižní Koreji. Tato studie zkoumala účinnost 150 mg a 300 mg itopridu podaného ve třech denních dávkách, přičemž jako účinnější byla prokázána dávka vyšší [9].
Účinnost a tolerabilitu itropridu u pacientů s horní funkční dyspepsií ověřila i studie provedená v Indii. Ta kromě zmírnění klinických obtíží u většiny pacientů (27 pacientů – 90 %) prokázala i vynikající tolerabilitu u 28 pacientů (93 %) a dobrou tolerabilitu u 2 pacientů (7 %). U žádného z pacientů nedošlo k prodloužení QT intervalu na EKG a rovněž se u žádného pacienta neobjevily abnormální hodnoty biochemických vyšetření (jaterní testy, urea, kreatinin). Nebyly zaznamenány žádné změny v krevním obraze v jediném z případů [8].
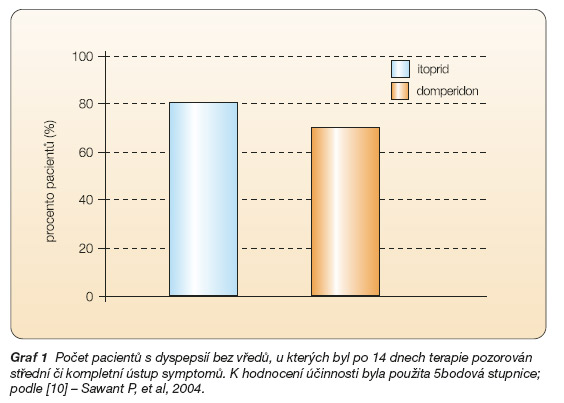
Další studie se zabývaly porovnáním účinků a bezpečnosti itopridu a domperidonu [10] a itopridu s mosapridem [11] u pacientů s funkční dyspepsií. Ve srovnání s domperidonem vykazoval itoprid shodnou účinnost (81 % vs 70 %) (p > 0,05) (graf 1).
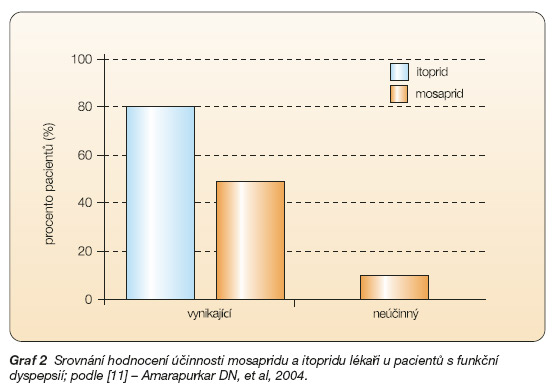
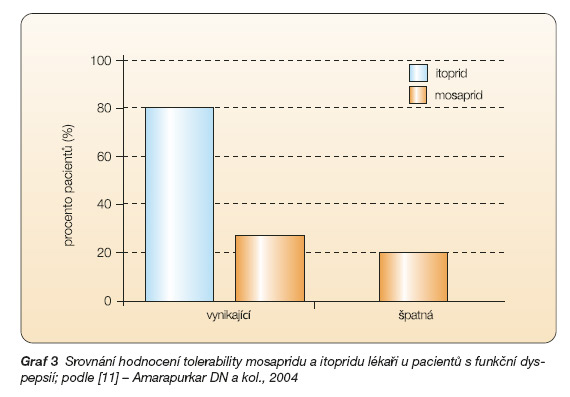
Obě látky byly dobře snášeny a ani u jedné z nich se neobjevilo prodloužení QT intervalu na EKG a nebyly zaznamenány abnormality v hodnotách biochemických vyšetření [10]. Srovnání s mosapridem dopadlo výrazně lépe pro itoprid, a to jak v dosažení ústupu klinických symptomů, tak i v hodnocení snášenlivosti a výskytu nežádoucích účinků [11] (graf 2, 3).
Indikace
– ‑funkční žaludeční dyspepsie (chabý žaludek)
– ‑diabetická gastroparéza
– ‑stavy po resekcích žaludku s druhotnou dysmotilitou žludku
– ‑doplňková terapie refluxní choroby jícnu
– ‑doplňková terapie organických onemocnění GIT.
Vedlejší účinky
Vedlejší účinky této látky byly zjišťovány v Japonsku u skupiny 572 pacientů. Byly zjištěny pouze u 2,45 % pacientů. Z gastrointestinálních příznaků se vyskytl nejčastěji průjem (0,7 %), bolesti břicha (0,35 %), zácpa (0,17 %), pyróza (0,17 %) a žízeň (0,17 %). Z ostatních příznaků se objevila bolest hlavy (0,35 %), výjimečně podrážděnost, poruchy spánku, závrať a škytavka. Jiné závažné příznaky nebyly zjištěny. Zcela výjimečně může dojít ke zvýšení hladiny prolaktinu s nepříjemnými až bolestivými pocity v prsech, nebo dokonce galaktoreou nebo gynekomastií; léčbu je nutno okamžitě ukončit. Vzácně se může vyskytnout např. vyrážka, zarudnutí a pocit svědění kůže [3].
Kontraindikace
Známá přecitlivělost na itoprid nebo jinou složku přípravku, krvácení z trávicího traktu, neprůchodnost trávicí trubice, podezření na perforaci. Nepodává se těhotným a kojícím ženám.
Interakce
Nebyla zjištěna interakce při současném podání itopridu s warfarinem, diazepamem, diclofenacem, ticlopidinem a nifedipinem.
Metabolismus itopridu probíhá přes flavinmonooxygenázový systém, a nezasahuje tedy cytochrom P-450(CYP) 3A4. Zatímco tedy inhibitory cytochromu P-4503A4 jako ketoconazol, cimetidin, erythromycin, clarithromycin ovlivňují metabolismus cisapridu a mosapridu, farmakokinetika itopridu není těmito léky alterována a itoprid sám pravděpodobně neovlivňuje farmakokinetiku konkomitantně užívaných medikamentů [12].
Anticholinergní látky snižují účinek itopridu. Látky jako např. cimetidin, ranitidin, tepronon a cetrexat neovlivňují prokinetickou aktivitu itopridu.
Dávkování
Doporučené dávkování je 1 tableta půl hodiny před jídlem, obvykle třikrát denně. Nedostaví-li se žádoucí efekt léčby, je možné dávku zvýšit, resp. zdvojnásobit na 6 tbl. denně.
Itopridi hydrochloridum 50 mg v 1 potahované tabletě, balení obsahuje 40 a 100 tablet, výrobce Abbott.
Seznam použité literatury
- [1] Abbott data on file.
- [2] Lukáš K, Bureš J, Dítě P, et al. Klinický účinek itopridu (Ganaton®) u pacientů s horní funkční dyspepsií. Čes Slov Gastroent Hepatol 2002; 56: 146–152.
- [3] Inoue K, Sanada Y, Fujimura J, Mihara O. Clinical effect of itopride hydrochloride on digestive symptoms of chronic gastritis with reflux esophagitis. Clin Med 1999; 15: 1804–1809.
- [4] Gurlich R, Fraško P. The onset of physiological stomach´s activity in the postoperative period. A comparative study with a prokinetic preparation, Ganaton. Rozhl Chir 2004; 83: 527–530.
- [5] Rane P. Randomised, double-blind, comparative study to evaluate the efficacy and safety of Ganaton (itopride hydrochloride) and mosapride citrate in the management of functional dyspepsia. J Indian Med Assoc 2004; 102: 735–737.
- [6] Keil R. Prokinetika a diabetes mellitus. Vnitřní lékařství 2004; 50: 358–362.
- [7] Lovecek M, Gryga A, Herman J, Svach I, Duda M. Esophageal dysfunction in female patient with diabetes mellitus and achalasia. Bratisl Lek Listy 2004; 105 (3): 101–103.
- [8] Shenoy KT, Veenasree, Leena KB. Efficacy and tolerability of itopride hydrochloride in patients with non-ulcer dyspepsia. J Indian Med Assoc 2003; 101 (6): 387–388.
- [9] Kim YS, Kinm TH, Choi CS, Shon YW, Kim SW, Seo GS, Nah YH, Choi MG, Choi SC. Effect of itopride, a new prokinetic, in patients with mild GERD: a pilot study. World J Gastroenterol 2005; 11 (27): 4210–4214.
- [10] Sawant P, Das HS, Desai N, Kalokhe S, Patil S. Comparative evaluation of the efficacy and tolerability of itopride hydrochloride and domperidone in patients with non-ulcer dyspepsia. J Assoc Physicians India 2004; 52: 626–628.
- [11] Amarapurkar DN, Rane P. Randomised, double blind, comparative study to evaluace the efficacy and safety of Ganaton (itopride hydrochloride) and mosapride citrate in the management of functional dyspepsia. J Indian Med Assoc 2004; 102 (12): 735–737, 760.
- [12] Mushiroda T, Douya R, Takahara E, Nagata O. The involvement of flavin – containing monooxygenase but not CYP3A4 in metabolism of itopride hydrochloride, a gastroprokinetic agent: comparison with cisapride and mosapride citrate. Drug Metab Dospod 2000; 28 (10): 1231–1237.