Karcinom z Merkelových buněk
Souhrn:
Arenberger P. Karcinom z Merkelových buněk. Remedia 2019; 29: 323–325.
Karcinom z Merkelových buněk (Merkel cell cancer, MCC) je vzácný neuroendokrinní nádor kůže charakterizovaný nekontrolovatelným růstem Merkelových buněk lokalizovaných v bazální vrstvě epidermis s agresivním klinickým chováním. Malignita nádoru je převážně spojena s polyomavirem Merkelových buněk. Karcinom je často zaměňován za amelanotický melanom, rychle progreduje a je spojen až s dvojnásobnou letalitou v porovnání s melanomem. Jeho výskyt v posledních desetiletích strmě stoupá a v současnosti dosahuje 2–4 případů na jeden milion obyvatel v USA a v Evropě. Dva roky či déle přežije bez léčby pouze 26 % nemocných. Prognóza závisí jak na lokalizaci, tak i na stadiu onemocnění. Kromě adjuvantní radioterapie a chemoterapie je nově v indikaci MCC ve stadiu IV k dispozici imunoterapie avelumabem (Bavencio®)
Summary:
Arenberger P. Merkel cell cancer. Remedia 2019; 29: 323–325.
Merkel cell cancer (MCC) is a rare neuroendocrine skin tumor characterized by uncontrolled growth of Merkel cells located in the basal layer of the epidermis with aggressive clinical behavior. Tumor malignancy is predominantly associated with Merkel cell polyomavirus. This tumor is often mistaken for amelanotic melanoma. In addition, it progresses rapidly and its lethality is almost double compared to melanoma. Its incidence has increased dramatically in recent decades, currently reaching 2‒4 cases per one million inhabitants in the US and Europe. Only 26% of patients survive more than two years without treatment. Its prognosis depends on both the location and stage of the disease. In addition to adjuvant radiotherapy and chemotherapy, avelumab immunotherapy (Bavencio®) is now available in the MCC stage IV.
Key words: Merkel cell cancer , anti‑PD‑L1, avelumab.
Karcinom z Merkelových buněk (MCC) je vzácný neuroendokrinní nádor kůže s agresivním biologickým chováním, který je charakterizován nekontrolovatelným růstem Merkelových buněk lokalizovaných v bazální vrstvě epidermis. Jeho malignita je podle posledních poznatků ve většině případů ‒ uvádí se kolem 80 % ‒ spojena s polyomavirem Merkelových buněk (MCPyV). Vzhledem připomíná namodralý či nafialovělý červený uzlík, který rychle ulceruje. Je často zaměňován za amelanotický melanom. Predilekčně se vyskytuje v místě expozice kůže UV záření, typicky na obličeji nebo na horních končetinách, převážně u mužů, u osob se světlejší pletí, u lidí starších 50 let a u imunosuprimovaných pacientů, kteří tvoří 10 % všech případů. Jeho výskyt v posledních desetiletích strmě stoupá a v současnosti dosahuje 2–4 případů na jeden milion obyvatel v USA a v Evropě, a dokonce až 8 případů na jeden milion obyvatel v Austrálii. Tento velmi agresivní karcinom rychle progreduje a je spojen až s dvojnásobnou letalitou v porovnání s melanomem. Dva roky či déle přežije bez léčby pouze 26 % nemocných. Prognóza závisí jak na lokalizaci, tak i na stagingu onemocnění [1,2].
Terapeutické možnosti
Z pohledu terapie se v první řadě přistupuje k radikální excizi tumoru s bezpečnostním lemem 2−3 cm. V případě pozitivních resekčních okrajů je nutná jeho reexcize doplněná o biopsii sentinelové uzliny. V současnosti jsou dále k dispozici tyto léčebné postupy:
- Adjuvantní radioterapie je cílena na místo primárního výskytu nádoru, případně na oblast regionálních lymfatických uzlin.
- Indikací pro adjuvantní chemoterapii je rozsáhlé uzlinové postižení.
- Nově je v indikaci metastatického MCC ve stadiu IV k dispozici imunoterapie avelumabem (Bavencio).
Léčba avelumabem
Indikace pro imunoterapii se rok
od roku rozšiřují a pojišťovny postupně schvalují
centrovou úhradu těchto léčiv [3]. Od ledna letošního roku
se dostala u nás do klinické praxe monoklonální
protilátka avelumab. Je to plně humanizovaná IgG1
monoklonální anti PD L1 protilátka s duálním
mechanismem účinku. Specificky se váže na proteinový ligand
PD L1 exprimovaný na povrchu nádorových buněk, čímž
obnovuje blokovanou latentní protinádorovou odpověď
zprostředkovanou T lymfocyty, které by jinak byly navázáním
na tento ligand odsouzeny k apoptóze, tedy k programované
smrti (programmed death, PD). Kromě adaptivní protinádorové
odpovědi navozuje avelumab prostřednictvím buněčné aktivity
závislé na protilátkách (antibody dependent cellular
cytotoxicity, ADCC) i vrozenou imunitní odpověď. Navázáním
Fc fragmentu protilátky na receptor NK (natural killers,
přirození zabíječi) buněk indukuje in vitro jejich
degranulaci (granzym, perforin) s následnou lýzou a zánikem
nádorové buňky. U protilátky je tak využit jak fragment
Fab, sloužící k navázání na PD L1, tak
i fragment Fc. Tímto duálním mechanismem účinku je avelumab
unikátní [4], obrázek 1.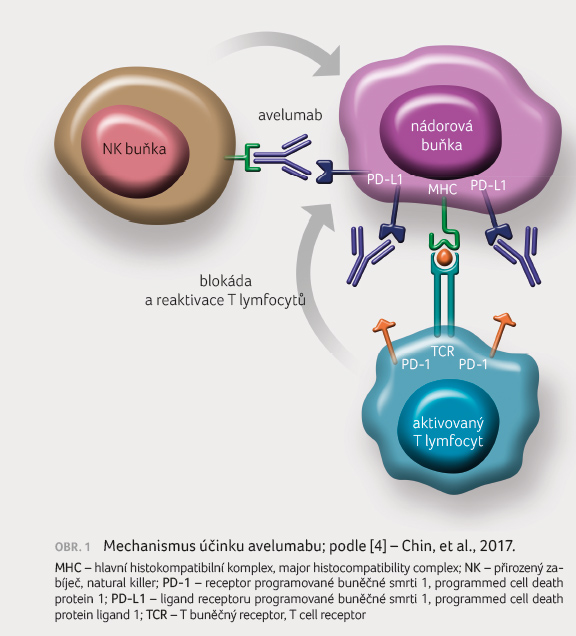
Dávkování léku je obdobou terapeutického postupu podávání anti PD 1 protilátek, které známe z léčby melanomu. Podává se intravenózně v dávce 10 mg/kg tělesné hmotnosti po dobu 60 minut každé dva týdny. Léčba pokračuje do progrese či do neakceptovatelné toxicity. Tak jako i u jiné imunoterapie lze s podáváním avelumabu pokračovat též u pacientů s radiologicky potvrzenou progresí onemocnění, která není doprovázena klinickým zhoršením. Jelikož se jedná o cizorodou protilátku, je třeba při počátečních čtyřech podáních pacienta premedikovat kombinací antihistaminik a paracetamolu. Pokud čtvrtá infuze proběhne bez infuzní reakce, má být premedikace u následujících dávek podána jen podle rozhodnutí lékaře [5–7].
Studie JAVELIN Merkel 200
Účinnost a bezpečnost léčby avelumabem byla prokázána u relativně velké skupiny nemocných (n = 204) s metastatickým MCC v otevřené multicentrické studii fáze II JAVELIN Merkel 200 [8]. Do kohorty A (n = 88) byli zahrnuti pacienti, kteří byli předléčeni alespoň jednou linií chemoterapie, do kohorty B (n = 116) ti, kteří dostali avelumab již v první linii léčby. Hodnocení nádorové odpovědi probíhalo každých šest týdnů pomocí kritérií RECIST (Response Evaluation Criteria in Solid Tumours) verze 1.1.
Jako primární cílový ukazatel v rameni A byla stanovena nejlepší potvrzená celková odpověď (best overall response, BOR), sekundárním parametrem účinnosti bylo trvání odpovědi (duration of response, DOR) a přežití bez progrese (progression free survival, PFS).
Hlavním parametrem účinnosti v rameni B byla dlouhodobá odpověď, která byla definována jako objektivní odpověď (kompletní odpověď [CR] nebo částečná odpověď [PR]) s dobou trvání alespoň šest měsíců. Hodnocené sekundární parametry zahrnovaly BOR, DOR, PFS a celkové přežití (overall survival, OS).
U nově léčených probandů (rameno B – hodnoceno 116 pacientů, kteří dostali alespoň jednu dávku avelumabu a byli sledováni minimálně 7 měsíců) bylo zaznamenáno 39,7 % objektivních odpovědí (95% interval spolehlivosti [CI] 30,7–49,2), u předléčených (rameno A) 33 % (95% CI 23,3–43,8), přičemž kompletní remise dosáhlo 14 % nemocných z ramene B a 11 % z ramene A. V kohortě nepředléčených pacientů dosáhlo delší než tříměsíční odpovědi na léčbu 89 % nemocných (95% CI 75–95) a delší než šestiměsíční odpovědi 78 % nemocných (95% CI 62–87). V kohortě pacientů již předléčených byla delší odpověď než 12 měsíců zaznamenána u 71 % probandů (95% CI 51–85) a odpověď v délce trvání alespoň 24 měsíců u 67 % (95% CI 47–82).
Závěr
Výzvu pro léčbu metastatického MCC u nás představuje zlepšení jeho záchytu u ambulantních dermatologů a odeslání nemocných do center, kde je pacientům tato nejnovější léčba k dispozici. Co se týče diferenciální diagnostiky, může metastatický MCC připomínat jiné kožní léze včetně amelanotického melanomu. Definitivní diagnózu je možné stanovit až na základě histologického vyšetření, ale i zde mohou patologové někdy váhat, protože histologicky má nádor některé charakteristiky metastázy například plicního karcinomu. Pokud se dermatologové setkají s útvarem, který by mohl být metastatickým MCC, doporučuje se nečekat na definitivní potvrzení diagnózy a pacienta ihned odeslat tam, kde jsou schopni mu nabídnout účinnou léčbu – do některého z komplexních onkologických center nebo tří specializovaných dermatologických center (FN Královské Vinohrady a Všeobecná fakultní nemocnice v Praze či FN Ostrava). Zbytečnou ztrátou času je nemocného vybavit žádankou ke spolupracujícímu spádovému onkologovi. Karcinom z Merkelových buněk je totiž sice velmi vzácné, ale zároveň velmi agresivní onemocnění. Pacienti s metastatickým MCC mají extrémně špatnou prognózu, která je výrazně horší než u nemocných s melanomem; pouze 26 % z nich bez léčby přežije více než dva roky.
V České republice je na rozdíl například od Rakouska či Slovenska záchyt pacientů s diagnózou metastatického MCC extrémně nízký. Není to způsobeno tím, že „za hranicemi svítí více sluníčka“, ale tím, že dříve, než se pacientům v ČR dostane adekvátní léčby, na tuto diagnózu, nebo dokonce pod jinou diagnózou, zemřou. Je tedy třeba zvýšit záchyt tohoto onemocnění již v první linii u ambulantních dermatologů, kteří jediní mohou nemocného poslat tam, kde se mu dostane skutečně účinné pomoci.
Seznam použité literatury
- [1] Arenberger P. První a jediná schválená imunoterapie pro pacienty s karcinomem z Merkelových buněk. 6. dermatologický update, Česká dermatovenerologická společnost ČLS JEP. Cubex Centrum Praha, 26. února 2019.
- [2] Šiffnerová H. Karcinom z Merkelových buněk (poster). XXII. jihočeské onkologické dny, Česká onkologická společnost ČLS JEP, Český Krumlov, 15.–17. října 2015.
- [3] Samimi M. Immune checkpoint inhibitors and beyond: An overview od immune‑based therapies in Merkel cell carcinoma. Am J Clin Dermatol 2019; 20: 391–407.
- [4] Chin KK, Chand VK, Nuyten DSA. Avelumab: clinical trial innovation and collaboration to advance anti‑PD‑L1 immunotherapy. Annals Oncol 2017; 28: 1658‒1666.
- [5] D’Angelo SP, Russell J, Lebbé C, et al. Efficacy and safety of first line avelumab treatment in patient with stage IV Merkel cell carcinoma: a preplanned interim a nalysis of a clinical trial. JAMA Oncol 2018; 4: e180077.
- [6] Del Marmol V, Lebbé C. New perspective in Merkel cell carcinoma. Curr Opin Oncol 2019; 31: 72–83.
- [7] Shirley M. Avelumab: a review in metastatic Merkel cell carcinoma. Target Oncol 2018; 13: 409–416.
- [8] Kaufman HL, Russell JS, Hamid O, et al. Updated efficacy of avelumab in patients with previously treated metastatic Merkel cell carcinoma after ≥ 1 year of follow up: JAVELIN Merkel 200, a phase 2 clinical trial. J Immunother Cancer 2018; 6: 7.