Lipidový komplex amfotericinu B – stále významná role mezi ostatními antimykotiky v léčbě invazivní aspergilózy.
U invazivní aspergilózy pozorujeme v posledních letech vzestup jak incidence, tak mortality, která souvisí jednak se zvyšujícím se počtem léčebných výkonů, jednak s imunosupresivní léčbou autoimunitních chorob a s pandemií HIV. K léčbě invazivní aspergilózy se vedle amfotericinů vázaných na tukové vehikulum používají nové triazoly 2. generace s protiaspergilovým účinkem (vorikonazol, posakonazol) a echinokandiny (zatím je dostupný kaspofungin, v příštím roce očekáváme anidulafungin a micafungin). Cílem sdělení je vymezení role lipidového komplexu amfotericinu B (ABLC) v léčbě invazivní aspergilózy, hlavní těžiště přehledu je v klinické oblasti. Srovnání ABLC s ostatními antimykotiky potvrzuje jeho roli 2. linie léčby v současné paletě antimykotik s účinkem proti aspergilům. Jeho předností je i nejvyšší koncentrace v plicní tkáni a v plicních alveolárních makrofázích ve srovnání s ostatními lékovými formami amfotericinu B.
V posledních letech dochází ke změně incidence invazivních mykóz. Výskyt invazivní kandidózy po zavedení nových tri-azolových antimykotik postupně klesá s výjimkou jednotek intenzivní péče [1]. U invazivní aspergilózy (IA) však pozorujeme vzestup incidence i mortality [2]. Vzestup incidence souvisí jednak se zvyšujícím se počtem léčebných výkonů, mezi něž patří intenzivní protinádorová léčba, allogenní a autologní transplantace kostní dřeně, transplantace solidních orgánů, jednak s imunosupresivní léčbou autoimunitních chorob a pandemií HIV [3]. Incidence IA u nemocných léčených pro akutní leukémie se pohybuje mezi 4,3–9,5 %, po allogenní transplantaci kostní dřeně mezi 4,5–28 % [4], resp. 10,8–14,8 % [5, 6], po autologní transplantaci mezi 0,7–1,5 % [5, 7]. V případě nemyeloablativních léčebných režimů u allogenní transplantace kostní dřeně se celková incidence IA od myeloablativních režimů zásadně neliší [8]. Incidence IA po transplantaci jater se pohybuje mezi 7–42 %, po transplantaci ledvin mezi 0–14 % a po transplantaci plic mezi 15–27 %. Mortalita na rozvinutou IA je velmi vysoká ve všech výše zmíněných skupinách pacientů a dosahuje 25–90 % [3, 9, 10].
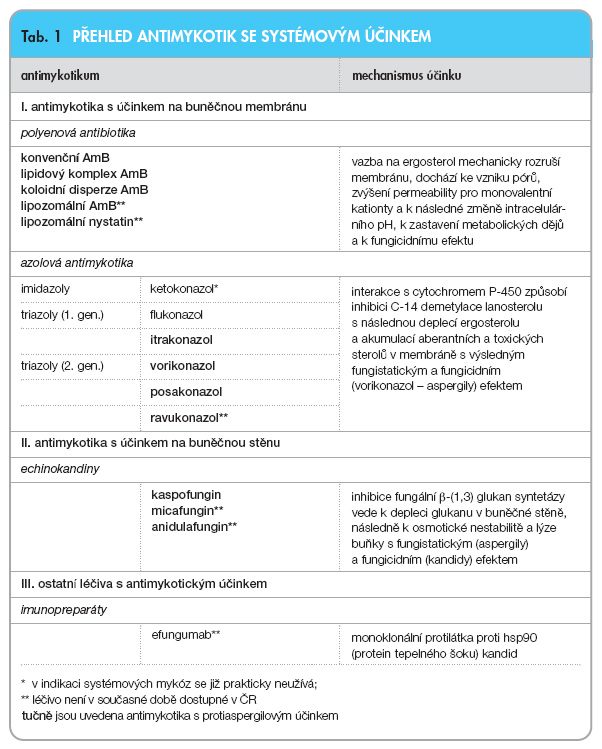
Cílem sdělení je vymezení role lipidového komplexu amfotericinu B (ABLC) v léčbě invazivní aspergilózy. Současná nabídka antimykotik s účinkem proti aspergilům se v posledních letech významně rozšíři-la (tab. 1), a tak můžeme při volbě léčiva zohlednit nejen léčebné výsledky klinických studií, ale i farmakologické vlastnosti jednotlivých preparátů s ohledem na stav organismu a jednotlivých orgánů. Podrobné farmakologické údaje o ABLC byly publikovány dříve [11], hlavní těžiště současného přehledu bude v klinické oblasti.
Konvenční amfotericin B (c-AmB) byl zlatým standardem již více než 40 let – pro klinické použití je dostupný od roku 1958 [12]. I přes široké spektrum účinku, minimální a spíše epizodický výskyt rezistencí na c-AmB je limitujícím faktorem použití jeho výrazná nefrotoxicita [13]. S léčbou c-AmB je nepřímo spojena i 2,7krát vyšší mortalita [14], neboť poškození ledvin bylo často důvodem snížení dávky a tedy i nižší účinnosti léčby. Tyto důvody vedly k intenzivnímu farmaceutickému výzkumu a výsledkem byly amfotericiny vázané na tukové vehikulum – lipidový komplex AmB (ABLC), koloidní disperze AmB (ABCD) a lipozomální AmB (L-AmB). Jejich významnou předností proti c-AmB je nefrotoxicita redukovaná na cca 20 %. Vedle toho se objevily nové triazoly 2. generace s protiaspergilovým účinkem (vorikonazol, posakonazol) a echinokandiny (zatím je dostupný kaspofungin, v příštím roce očekáváme anidulafungin a micafungin).
Klinické zkušenosti s podáváním ABLC
V roce 2005 byla vytvořena databáze CLEAR (The Collaborative Exchange of Antifungal Research program), která shromáždila informace o nemocných léčených pro invazivní mykózy jedním preparátem – lipidovým komplexem AmB. Je to dosud nejširší databáze, která shrnuje data z dosavadních studií a obsahuje demografické charakteristiky, laboratorní výsledky a výsledky léčby. V současném přehledu budou údaje této databáze základem srovnání výsledků léčby invazivní aspergilózy mezi ABLC a dalšími antimykotiky.
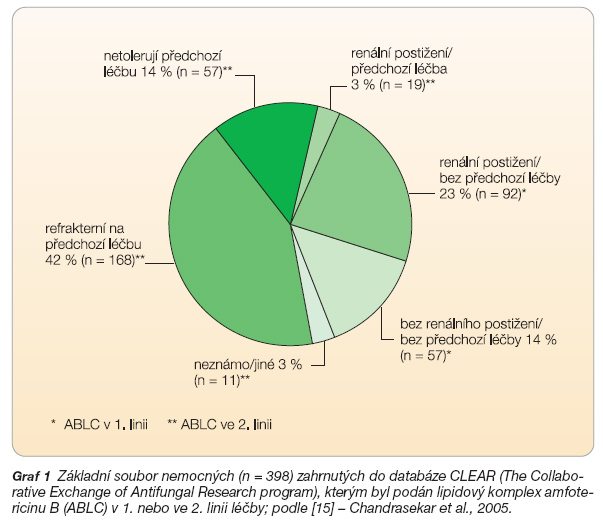
Účinnost ABLC u invazivní aspergilózy v rámci CLEAR [15] byla hodnocena u 398 nemocných. Soubor tvořili nemocní pouze s prokázanou aspergilózou podle kritérií EORTC-MSG [16]. Z toho bylo 25 % (101/398) po transplantaci hematopoetických kmenových buněk, dalších 25 % (101/398) s jinou hematologickou malignitou a 27 % (109/398) po transplantaci solidních orgánů. Převážně šlo o postižení plic (71 %), paranazálních dutin (8 %) a CNS (2 %), v ostatních případech byly infekce multiorgánové. ABLC byl podáván většinou ve druhé linii (graf 1), po selhání nebo pro intoleranci předchozí léčby, medián délky podávání byl 15 dní (1–274 dní). Celkem 94 nemocných dostávalo současně itrakonazol, 56 bylo léčeno itrakonazolem před ABLC. Medián kumulativní dávky ABLC byl 4125 mg (18,9–74 000 mg).
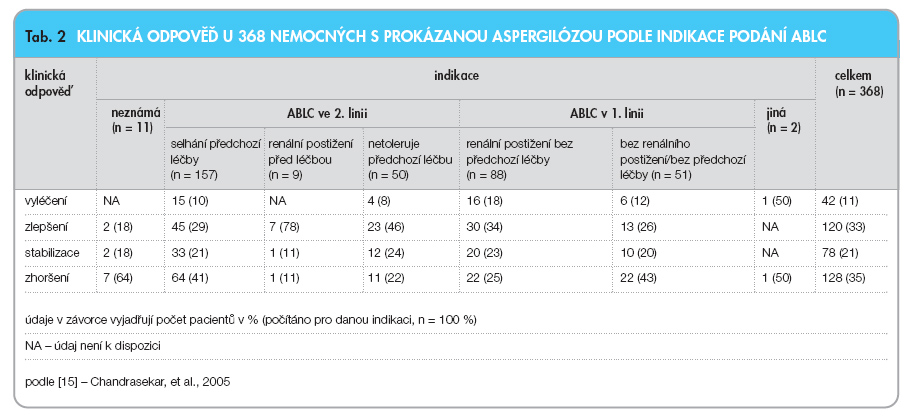
Z celkového počtu 368 hodnotitelných nemocných s prokázanou aspergilózou podle kritérií EORTC-MSG [16] dosáhlo příznivé odpovědi celkem 65 % nemocných, z toho 44 % (162/368) bylo vylé-čeno nebo došlo ke zlepšení jejich stavu (= kompletní + částečná remise) a 21 % (78/368) dosáhlo na konci léčby stabilizace onemocnění (tab. 2, 3).
Klinické odpovědi dosáhlo více nemocných po transplantaci solidních orgánů (52 %), proti těm, kteří podstoupili transplantaci kostní dřeně pro hematologickou malignitu (34 %, p = 0,014). Tento fakt souvisí s neutropenií (< 0,5 x 109/l), která byla negativním faktorem úspěchu léčby. Významně vyšší klinická odpověď (55 %, 23/42) byla dosažena u těch, u nichž se počet leukocytů na konci léčby normalizoval, než u těch, u nichž leukopenie přetrvávala i na konci léčby (10 %, 4/42). Nemocní bez neutropenie po celou dobu léčby dosáhli klinické odpovědi ve 49 %.
Celkově nebyl zásadní rozdíl mezi těmi, kteří dosáhli klinické odpovědi při podání ABLC v 1. linii (47 %, n = 65/139) a ve 2. linii (44 %, n = 94/216). Vyššího procenta klinické odpovědi však dosáhli ti nemocní, jimž byl podán ABLC jako léčba 1. volby z důvodů předcházejícího renálního poškození – celkem 52 % (46/88), a ti, kteří předchozí léčbu netolerovali (54 %, 27/50). Významně nižší klinická odpověď byla u podskupiny nemocných, kteří dosta-li ABLC z důvodů selhání předchozí léčby (38 %, 60/157). Nejvyšší odpověď byla zaznamenána u podskupiny nemocných, u kterých byla předchozí léčba nahrazena léčbou ABLC (78 %, 7/9) z důvodů nefrotoxicity. Z uvedených dat je významné zjištění rozdílu v dosažení odpovědi mezi podáním ABLC v 1. linii (47 %) a ve 2. linii po selhání předchozí léčby (38 %).
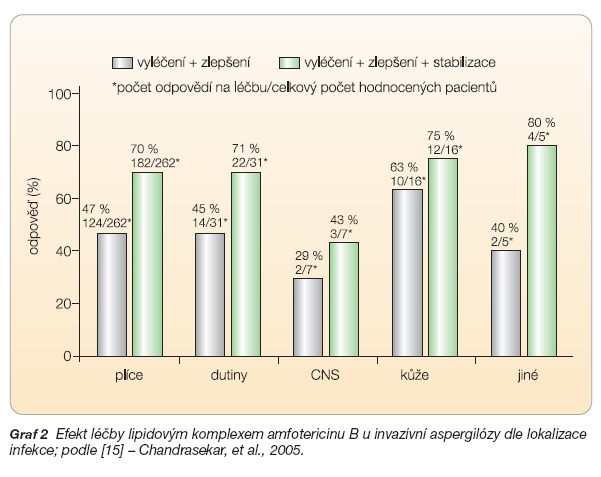
Efekt léčby podle lokalizace infekce uvádí graf 2.
Léčba plicní aspergilózy byla úspěšná ve 47 %, podobně jako léčba infekce paranazálních dutin (45 %), nejméně příznivých výsledků bylo dosa-ženo při léčbě nitrolební aspergilózy (29 %).
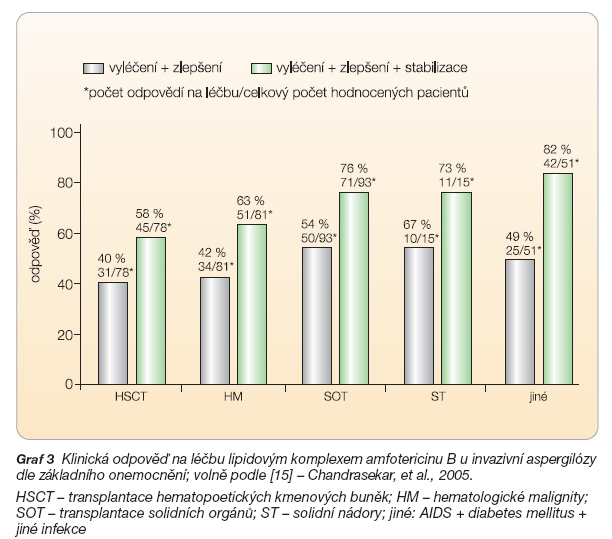
Podobných výsledků bylo dosaženo u nemocných po transplantaci hematopoe-tických kmenových buněk a u nemocných s hematologickými malignitami (42 %), u méně rizikové skupiny pacientů se solidními nádory byla klinická odpověď vyšší (67 %), viz graf 3.
Dílčí součástí studie CLEAR je práce z roku 1998 [17], ve které byla hodnocena účinnost a toxicita ABCL u souboru 556 nemocných s invazivní mykotickou infekcí. Zařazeni byli nemocní: 1. po selhání předchozí léčby (n = 292; 52,5 %; 48,5 % c-AmB, 4 % jiná antimykotika), 2. s projevy nefrotoxicity po předchozí léčbě c-AmB (n = 181; 32,6 %), 3. s výraznými projevy akutní toxicity po podání c-AmB (n = 30; 5 %) a 4. se snížením renálních funkcí již před zahájením antimykotické léčby (n = 50; 9 %), kteří dostali alespoň 4 dávky ABLC. Léčivo bylo podáváno v obvyklé dávce 5 mg/kg po dobu nejméně 4 týdnů. Z celého souboru bylo 130 nemocných s jistou a pravděpodobnou aspergilózou. Klinické odpovědi (úplná a částečná odpověď) bylo dosaženo u 42 % (55/130) nemocných s invazivní aspergilózou. Tolerance léčby byla velmi dobrá, zejména jsou zajímavé výsledky hodnocení nefrotoxicity. U 162 nemocných z celého souboru s abnormální vstupní hodnotou kreatininu došlo během léčby ABCL k signifikantnímu poklesu hladiny kreatininu (p ≤ 0,0003), viz graf 4.
Srovnání účinnosti ABLC s dalšími antimykotiky v léčbě invazivní aspergilózy
Lékem volby invazivní aspergilózy je vorikonazol. Jeho pozice je založena na Herbrechtově studii [18], ve které vorikonazol u jisté a pravděpodobné aspergilózy do-sáhl proti c-AmB celkově o 21,2 % lepší klinické odpovědi (RR) 52,8 % vs. 31,6 % a také statisticky významně lepších výsledků i z hlediska přežití (70,8 % vs. 57,9 %). Klinická odpověď u prokázané aspergilózy byla 44,8 % vs. 19,5 % a u pravděpodobné diagnózy 59,7 % vs. 37,0 %. U nemocných po allogenní transplantaci kostní dřeně byla neutropenie negativním faktorem úspěchu léčby s nižší klinickou odpovědí 32,4 % vs. 13,3 %, podobně jako v souboru CLEAR, kde byla celková odpověď 40 %. Srovnání těchto dvou studií blíže není dobře možné, neboť proti relativně homogennímu souboru prospektivní srovnávací studie Herbrechta stojí nehomogenní soubor retrospektivních dat studie CLEAR.
Mezi antimykotika 2. volby léčby invazivní aspergilózy patří vedle lipidového komplexu AmB (ABLC) dále koloidní disperze AmB (ABCD), kaspofungin, itrakonazol a posakonazol.
O účinnosti ABCD ve srovnání s c-AmB v primární léčbě invazivní aspergilózy publikovali Bowden a kol. [19], viz tab. 3. Celkem randomizovali 174 pacientů (ABCD n = 88, c-AmB n = 86) s jistou a pravděpodobnou aspergilózou. Většina nemocných měla hematologickou malignitu (75 % vs. 64 %), allogenní transplantaci kostní dřeně podstoupilo 38 % vs. 35 %, většina měla hodnotu neutrofilů > 0,5 x 109/l (71 % vs. 65 %) a většina před zařazením do studie byla již dříve léčena c-AmB (80 % vs. 77 %). Převážně šlo o diagnózu invazivní plicní aspergilózy (67 % vs. 65,1 %), o postižení paranazálních dutin (12,5 % vs. 17,4 %) a postižení CNS (5,7 % vs. 8,1 %). Medián trvání léčby byl 13 dní (1–375) vs. 14,5 dní (1–87), medián kumulativní dávky ABLC byl 4684 mg (4–87 208 mg ) a c-AmB 857 mg (55–6271 mg). Celková klinická odpověď u 50 hodnotitelných pa-cientů (modified intent to treat, MITT, kritérium MITT > 7 dní léčby) byla 52 % při léčbě ABCD a 51 % u 53 pacientů při léčbě c-AMB (p = 0,96). Rozdíly nebyly statisticky významné. V celém souboru (intent to treat, ITT, kritérium ITT alespoň jeden den léčby) byly dosažené výsledky stejné v obou skupinách – 35 %. Ani v ostatních sledovaných parametrech nebyly výsledky statisticky rozdílné, v některých případech jen naznačovaly trendy: u neutropenických pacientů (51 % vs. 51 %), u hematologických malignit (50 % vs. 52 %), v celkové mortalitě 36 % vs. 45 %, v celkovém úmrtí na mykózu 32 % vs. 26 % a u hodnotitelných skupin 40 % vs. 36 %. Ve skupině ABCD přerušili léčbu pro renální toxicitu 3 nemocní, ve skupině c-AmB 16 nemocných, celkový výskyt toxicity byl významně nižší u skupiny léčené ABCD (25 % vs. 49 %; p = 0,002). Významné je, že pro akutní nežádoucí účinky vázané na aplikaci infuze (třesavka) přerušilo terapii 8 nemocných léčených ABCD, ale jenom tři nemocní léčení c-AmB. Závěr studie neprokázal lepší účinnost ABCD proti c-AmB, a jak uvádí Patterson v úvodním článku k uvedené studii, při hodnocení celého souboru (zařazení podle ITT) byla klinická odpověď „zklamáním", tedy velmi nízká – 12,5 % při léčbě ABCD a 15,1 % při léčbě c-AmB [20]. Zvláště nepříznivým zjištěním byla vyšší incidence akutních nežádoucích účinků po aplikaci ABCD, tedy horší tolerance léčby.
Na malém souboru 31 nemocných ověřoval účinnost itrakonazolu u invazivní aspergilózy Caillot a kol. [21]. Itrakonazol byl podáván první dva dny nitrožilně v dávce 2krát 200 mg, dalších 12 dní 1krát 200 mg a následně 12 týdnů ve formě perorálních kapslí v dávce 2krát 200 mg. Klinickou odpověď zaznamenali u 15 ne-mocných (48 %) a stabilizaci nemoci u 6 nemocných (19 %). Podrobnosti složení souboru nemocných jsou uvedeny v tab. 3. Je škoda, že po této „pilotní" studii nenásledovaly žádné další s větším souborem a s možností lepšího hodnocení.
Efekt kaspofunginu v léčbě invazivní aspergilózy byl poprvé dokumentován v nekomparativní otevřené studii [22], viz tab. 3. Většina zařazených nemocných dostala kaspofungin po selhání konvenčních antimykotik, včetně amfotericinů vázaných na tukové vehikulum (n = 66; 79,5 %), po selhání profylaxe (n = 5; 6 %) a jen malý počet pro intoleranci předchozí léčby (n = 12; 14,5 %). Celkem bylo hodnoceno 83 nemocných, 64 z nich mělo aspergilózu plic – jistá + pravděpodobná (n = 34; 41 % + n = 30; 36,1 %), u čtyř (4,8 %) byly postiženy paranazální dutiny a u 13 (15,7 %) byla infekce diseminovaná. Kaspofungin byl dávkován standardně (70 mg úvodní dávka, dále 50 mg denně), léčba trvala celkově nejméně 28 dní a minimálně dalších 7 dní po odeznění příznaků infekce. Základním onemocněním byly převážně hematologické malignity (n = 60; 72,3 %). Celková klinická odpověď (kompletní + částečná odpověď) byla zaznamenána u 45 % pacientů (37/83), v podskupině plicní invazivní aspergilózy celkem u 50 % pacientů (32/64), z toho u prokázané aspergilózy byla celková klinická odpověď zaznamenána u 38,2 % pacientů (13/34) a u nemocných s pravděpodobnou aspergilózou v 63,3 % (19/30). U pacientů s diseminovanou formou byla klinická odpověď dosažena ve 23 % (3/13). Významnější rozdíly jsou patrné při hodnocení efektu léčby podle základního onemocnění. U hematologických malignit byla klinická odpověď dosažena ve 41,7 % (25/60), po allogenní transplantaci kostní dřeně pouze ve 14,3 % (3/21), po transplantaci solidních orgánů byla klinická odpověď vyšší (44,4 %; 4/9), nejvyšší klinické odpovědi bylo dosaženo u pacientů se solidními nádory (100 %; 3/3). Lepší výsledky vykazovali nemocní bez neutropenie (50 %; 32/64) než nemocní s neutropenií (26,3 %; 5/19). Výsledky jsou srovnatelné s léčbou 2. linie ostatními antimykotiky, včetně rozdílů v hodnocení podle základního onemocnění. Tolerance léčby byla velmi dobrá, pouze 2 nemocní museli léčbu přerušit.
Dobré výsledky v léčbě 2. linie u invazivní aspergilózy prokázal zcela nedávno posakonazol. V otevřené multicentrické studii [23] byl podáván posakonazol (orální suspenze, 800 mg/den v rozdělených dávkách buď 2krát 400 mg ambulantně, nebo 4krát 200 mg za hospitalizace) jako monoterapie nemocným s prokázanou a pravděpodobnou diagnózou invazivní aspergilózy, kteří netolerovali předchozí léčbu nebo u nichž léčba po nejméně 7 dnech aplikace selhala. Při předchozí léčbě byl aplikován konvenční amfotericin B (n = 33) a jeho lipidové formy (n = 71), itrakonazol (n = 48), vorikonazol (n = 5) a echinokandiny (n = 5). Celkem bylo prospektivně zařazeno 107 pacientů s převážně hematologickou malignitou (79/107; 79 %) a po transplantaci kostní dřeně (55/107; 51 %), kteří dostali alespoň jednu dávku posakonazolu (intent to treat population, ITT). Externí kontrolní skupinu tvořilo 86 nemocných po selhání první linie léčby, z nichž většina (70/86; 81 %) měla také hematologické malignity nebo byli po transplantaci kostní dřeně (38/86; 44 %). Kontrolní skupina byla vybrána a zařazena podle definovaných kritérií retrospektivně. Celková odpověď, hodnocená nezávislou komisí expertů na konci léčby, byla 42 % ve skupině léčené posakonazolem a 26 % v kontrolní skupině (p = 0,006). Celková odpověď se lišila v jednotlivých podskupinách vytvořených podle lokalizace infekce: plicní (39 %; 31/79 vs. 25 %; 17/67), diseminovaná forma (44 %; 4/9 vs. 0 %; 0/8), podle základního onemocnění: hematologické malignity (37 %; 29/79 vs. 23 %; 16/77), autologní transplantace kostní dřeně (86 %; 6/7 vs. 0 %; 0/4), allogenní transplantace kostní dřeně (31 %; 15/48 vs. 21 %; 7/34), solidní nádory (46 %; 6/13 vs. 20 %; 1/5), podle hloubky neutropenie na konci léčby (neutrofily < 0,5 x 109/l: 32 %; 6/19 vs. 0 %; 0/18, neutrofily > 0,5 x 109/l: 48 %; 39/82 vs. 35 %; 20/56) a podle důvodu zařazení do studie: selhání léčby (43 %; 40/94 vs. 19 %; 13/68), intolerance předchozí léčby (41 %; 16/39 vs. 15 %; 3/20). Signifikantně lepší efekt posakonazolu potvrdila i křivka přežití, kdy 30. den a na konci léčby přežívalo 74 % pacientů proti 38 % pacientů v kontrolní skupině (p = 0,0003). Nežádoucí účinky léčby posakonazolem byly zaznamenány u 47 ze 107 nemocných (44 %), a to převážně gastrointestinální (nevolnost 12 %, zvracení 5 %, nechutenství 3 %, bolesti břicha 2 %), vzestup hladiny jaterních enzymů (3 %), exantém (4 %).
Diskuse
Tab. 3 přináší souhrnné údaje z výše uvedených studií. Nejvyšší kvalitu z hlediska medicíny založené na důkazech (evidence based medicine) má studie Herbrechtova [18], jejíž výsledky favorizují vorikonazol jako lék 1. volby. A to i bez ohledu na kritickou analýzu publikovanou pracovní skupinou Cochrane, která konstatuje určité nedostatky v designu studie, zejména z hlediska zajištění aplikace konvenčního amfotericinu B (hydratace, suplementace iontů) [24]. Podobné „trhliny" však můžeme při podrobném studiu ostatních studií nalézt také.
Ze srovnání klinické odpovědi je patrné, že mezi preparáty není zásadní rozdíl, výsledky se pohybují mezi 42–52 %. Nejnižší váhu bychom z tohoto hlediska přisoudili studii Caillota [21], ve které bylo nekomparativně hodnoceno pouze 31 ne-mocných.
Za povšimnutí stojí relativně malé procento kompletních remisí (CR), v tabulce jsou záměrně uvedeny i počty nemocných, kteří CR dosáhli. Nejvyšší procento úspěchu uvádějí studie početně nejmenší [21, 25], z nichž jedna [21] dokonce převyšuje výsledky dosažené při léčbě vorikonazolem [18].
Ani jedna ze studií neodpovídá na otázku, jak dlouho pacienty léčit. Jediná racionální odpověď je, že tak dlouho, až dosáhneme léčebného úspěchu, bez ohledu na čas. Hodnocení efektu v protokolem stanoveném čase může být zavádějící a neodráží vždy reálnou klinickou situaci, neboť nemusí „poskytnout léku" dostatečný čas k plnému léčebnému efektu. Příkladem může být studie Walshe [17], kdy medián léčby byl 22 dní, průměr 33 dní a rozmezí 1–510 dní, ale i práce Bowdena [19] s mediánem trvání léčby 13 dní (1–375).
Výsledky léčby invazivní aspergilózy po allogenní transplantaci kostní dřeně (alloBMT) jsou ve všech studiích horší než při léčbě nemocných s hematologickou malignitou. Poměr výsledků léčby v zásadě kopíruje poměr výsledků léčby u nemocných s neutropenií a bez ne-utropenie. Nejvíce klinických odpovědí po alloBMT bylo ve 2. linii léčby při podání ABLC (40 %), výsledky byly podobné při podání vorikonazolu v 1. linii léčby (32,4 %) a při podání posakonazolu ve 2. linii léčby (31 %).
Stojí za povšimnutí, jak významně nižší jsou výsledky léčby u prokázané asper-gilózy (podle současných kritérií [16]) proti diagnóze pravděpodobné aspergilózy. Rozdíly svědčí i o tom, že stále nemáme dostatečné diagnostické prostředky k potvrzení diagnózy, a dále o tom, že mnoho tzv. plicních aspergilóz ve skutečnosti aspergilózou není a že v případě nejistoty je indikované verifikovat diagnózu histologicky [26, 27].
Nejčastější formou IA je plicní postižení, ale při negativitě současných diagnostických možností (CT, antigenémie) je nutné myslet na postižení ORL oblasti a také, i když vzácněji, na formu nitrolební. Znalost klinických forem v tomto případě ovlivní i celkové výsledky léčby, neboť nedojde k prodlevě v zahájení terapie.
Mortalita je stále neuspokojivě vysoká, se stoupající incidencí aspergilózy se tato infekce stává nejčastější infekcí u hematologických malignit a je pozorován alarmující vzestup výskytu také na jednotkách intenzivní péče a anesteziologicko-resuscitačních odděleních.
Srovnání lipidového komplexu amfotericinu B s ostatními antimykotiky potvrzuje stále jeho roli 2. linie léčby v současné paletě antimykotik s účinkem proti aspergilům. Jeho předností je i nejvyšší koncentrace v plicní tkáni a v plicních alveolárních makrofázích (PAM) ve srovnání s ostatními lékovými formami amfoterici-nu B [28, 29] a synergní účinek s PAM. V experimentu byl při plicní aspergilóze srovnatelně účinný jako lipozomální amfotericin B [30], je účinný při nitrolební aspergilóze [31]. Jeho role v současné době vzrůstá i s možností kombinované léčby preparáty s různým mechanismem účinku.
I když je nefrotoxicita ABLC proti c-AmB významně nižší, stále zůstává určitým rizikem. Podávání ABLC vyžaduje dostatečnou hydrataci a pečlivé monitorování renálních funkcí, iontogramu a zvážení rizik současné terapie nefrotoxickými léčivy. Podobné zvýšené opatrnosti je však třeba i při léčbě některými triazoly 2. generace (nitrožilní formy itrakonazolu a vorikona-zolu), u nichž je potenciální nefrotoxicita způsobena vehikulem Na rozdíl od jiných antimykotik, zejména triazolových, má však ABLC jinou cestu biodegradace, a tak i rizika lékových interakcí jsou prakticky nulová.
Seznam použité literatury
- [1] Wisplinghoff H, Bischoff T, Tallent SM, et al. Nosocomial bloodstream infections in US hospitals: analysis of 24,179 cases from a prospective nationwide surveillance study. Clin Infect Dis 2004; 39: 309–317.
- [2] Ho PL, Yuen KY. Aspergillosis in bone marrow transplant recipients. Crit Rev Oncol Hematol 2000; 34: 55–69.
- [3] Lin SJ, Schranz J, Teutsch SM. Aspergillosis Case-Fatality Rate: Systematic Review of the Literature. Clin Infect Dis 2001; 32: 358–366.
- [4] Alangaden GJ, Wahiduzzaman M, Chandrasekar PH, and the Bone Marrow Transplant Group Aspergillosis: The Most Common Community-Acquired Pneumonia with Gram-Negative Bacilli as Copathogens in Stem Cell Transplant Recipients with Graft-versus-Host Disease. Clin Infect Dis 2002; 35: 659–664.
- [5] Cornet M, Fleury L, Maslo C, et al. Invasive Aspergillosis Surveillance Network of the Assistance Publique-Hopitaux de Paris. Epidemiology of invasive aspergillosis in France: a six-year multicentric survey in the Greater Paris area. J Hosp Infect 2002; 51: 288–296.
- [6] George B, Mathews V, Srivastava A, Chandy M. Infections among allogeneic bone marrow transplant recipients in India. Bone Marrow Transplant 2004; 33: 311–315.
- [7] Marr KA, Carter RA, Boeckh M, et al. Invasive aspergillosis in allogeneic stem cell transplant recipients: changes in epidemiology and risk factors. Blood 2002; 100: 4358–4366.
- [8] Fukuda T, Boeckh M, Carter RA, et al. Risks and outcomes of invasive fungal infections in recipients of allogeneic hematopoietic stem cell transplants after nonmyeloablative conditioning. Blood 2003; 102: 827–833.
- [9] Öner-Eyüboglu F, Karacan Ö, Akcay S, et al. Invasive pulmonary fungal infections in solid organ transplant recipients: a four-year review. Transplat Proceedings 2003; 35: 2689–2691.
- [10] Singh N, Arnow PM, Bohnam A, et al. Invasive aspergillosis in liver transplant recipients in the 1990s. Transplantation 1997; 64: 716–720.
- [11] Haber J. Lipidový komplex amfotericinu B. Remedia 2001; 5: 298–307.
- [12] Kleinberg M. What is the current and future status of conventional amphotericin B? Int J Antimicron Agents 2006; 27 (Suppl.): 12–16.
- [13] Wingard JR, Kubilis P, Lee L, et al. Clinical significance of nephrotoxicity in patients treated with amphotericin B for suspected or proven aspergillosis. Clin Infect Dis 1999; 29: 1402–1407.
- [14] Harbarth S, Burke JP, Lloyd JF, et al. Clinical and economic outcomes of conventional amphotericin B-associated nephrotoxicity. Clin Infect Dis 2002; 35: 120–127.
- [15] Chandrasekar PH, Ito JI. Amphotericin B Lipid Complex in the Management of Invasive Aspergillosis in Immunocompromised Patients. Clin Infect Dis 2005; 40: S392–S400.
- [16] Ascioglu S, Rex HJ, de Pauw B, et al. Defining Opportunistic Invasive Fungal Infections in Immunocompromised Patients with Cancer and Hematopoietic Stem Cell Transplants: An International Consensus. Clin Infect Diseases 2002; 34: 7–14.
- [17] Walsh TJ, Hiemenz JW, Seibel NL, et al. Amphotericin B lipid complex for invasive fungal infections: analysis of safety and efficacy in 556 cases. Clin Infect Dis 1998; 26:1383–1396.
- [18] Herbrecht R, Denning DW, Patzterson TF, et al. Voriconazole versus amphotericin B for primary therapy of invasive aspergillosis. N Engl J Med 2002; 8; 347: 408–415.
- [19] Bowden R, Chandrasekar P, White MH, et al. A Double-Blind, Randomized, Controlled Trial of Amphotericin B Colloidal Dispersion versus Am-photericin B for Treatment of Invasive Aspergillosis in Immunocompromised Patients. Clin Infect Dis 2002; 35: 359–366.
- [20] Patterson TF. New Agents for Treatment of Invasive Aspergillosis. Clinical Infectious Diseases 2002; 35: 367–369.
- [21] Caillot D, Bassaris H, McGeer A, et al. Intravenous itraconazole followed by oral itraconazole in the treatment of invasive pulmonary aspergillosis in patients with hematologic malignancies, chronic granulomatous disease, or AIDS. Ann Intern Med 2001; 135: 412–422.
- [22] Maertens J, Raad I, Petrikkos G, et al. Efficacy and safety of caspofungin for treatment of invasive aspergillosis in patients who area refractory to or intolerant of conventional antifungal therapy. Clin Infest Dis 2004; 39: 1563–1571.
- [23] Walsh TJ, Raad I, Pattersn TF, et al. Treatment of invasive aspergillosis with posaconazole. Clin Infect Dis 2007; 44: 2–12.
- [24] Jo/rgensen KJ, Johansen HK, Go/tzsche PC. Flaws in design, analysis and interpretation of Pfizer´s antifungal trials of voriconazole and uncritical subsequent quotations. Trials 2006; 7: 3.
- [25] Kartsonis NA, Saah AJ, Lipka CJ, et al. Salvage therapy with caspofungin for invasive aspergil-losis: results from caspofungin compassionate use study. J Infect 2005; 50: 196–205.
- [26] Kim K, Lee MH, Kim J, et al. Importance of Open Lung Biopsy in the Diagnosis of Invasive Pulmonary Aspergillosis in Patients With Hematologic Malignancies. Am J Hematol 2002; 71: 75–79.
- [27] Zihlif M , Khanchandani G, Ahmed HP, et al. Surgical lung biopsy in patients with hematological malignancy or hematopoietic stem cell transplantation and unexplained pulmonary infiltrates: Improved Outcome with specific diagnosis. Am J Hematol 2005; 78: 94–99.
- [28] Groll AH, Lyman CA, Petraitis V, et al. al. Compartmentalized Intrapulmonary Pharmacokinetics of Amphotericin B and Its Lipid Formulations. Antimicrob Agents Chemother 2006; 50: 3418–3423.
- [29] Matot I, Pizov R. Pulmonary extraction and accumulation of lipid formulations of amphotericin B. Crit Car Med 2000; 28: 2528–2532.
- [30] Olson JA, Adler-Moore JP, Schwartz J, et al. Comparative Efficacies, Toxicities, and Tissue Concentrations of Amphotericin B Lipid Formulations in a Murine Pulmonary Aspergillosis Model. Antimicrob Agents Chemother 2006; 50: 2122–2131.
- [31] Imai J, Singh G, Fernandez B, et al. Efficacy of Abelcet and caspofungin, alone or in combination, against CNS aspergillosis in a murine model. J Antimicrob Chemother 2005; 56: 166–171.
- [32] Denning DW, Ribaud P, Milpied N, et al. Efficacy and safety of voriconazole in the treatment of acute invasive aspergillosis. Clin Infect Dis 2002; 34: 563–571.