Migréna – když léčba nepomáhá
Ve dnech 30.−31. ledna 2019 se v plzeňském Parkhotelu Congress Center uskutečnila VI. konference Neurologie pro praxi, pořádaná pod odbornou záštitou Neurologické kliniky LF UK a FN Plzeň. Na odborném setkání zazněla řada zajímavých sdělení z oblasti neurologie a přítomní měli možnost diskutovat aktuální odborná témata. Přinášíme shrnutí informací z přednáškového bloku Migréna – když léčba nepomáhá. Odborným garantem a zároveň první přednášející byla přednostka Neurologické kliniky 3. LF UK a Thomayerovy nemocnice v Praze MUDr. Jolana Marková, FEAN.
„Migrénu je možné léčit, je
třeba ji léčit a je třeba ji léčit včas, aby nedošlo
k rozvinutí dlouhotrvajícího a silného záchvatu. Je
třeba k tomu užít dostatečně účinnou medikaci ve vhodné
formě a zároveň poučit pacienta o možnostech záchranné
medikace, pokud prvně zvolená léčba nepomůže,“ zahájila
svoji prezentaci paní přednostka. Je třeba rozlišit pacienty
s frekventní a nefrekventní epizodickou migrénou, při
častém užití triptanů nebo jiných analgetik hrozí významné
riziko nadužívání akutní analgetické medikace a vznik tzv.
medication overuse headache. V indikovaných případech je
třeba zahájit profylaktickou léčbu. Lékem první volby akutní
ataky jsou triptany, specifická antimigrenika. Jedná se
o selektivní agonisty serotoninových receptorů působící
na podtypech 5 HT 1B, 1D a 1F. Vyvolávají
vazokonstrikci primárně dilatovaných meningeálních cévek.
K jejich dilataci dochází při rozvoji migrenózního záchvatu
uvolněním mediátorů z trigeminálních neuronů. Receptory
5 HT 1B jsou umístěny ve stěnách drobných
meningeálních cévek a dalších cévek a podtyp 1F je
lokalizován v centrálním nervovém systému (CNS) a přispívá
k přenosu bolesti z trigeminového jádra do podkorových
center bolesti a dále do mozkové kůry, kde dochází
k uvědomění si bolesti.
Jednotlivé triptany se liší selektivitou a afinitou k serotoninovým receptorům, rychlostí absorpce a průniku do CNS, tj. farmakokinetikou. Délka biologického poločasu může ovlivnit výskyt rekurencí, tedy návrat migrenózní bolesti po odléčení první ataky. Přípravky z dané lékové skupiny se liší i výskytem nežádoucích účinků, interakcemi a cenou.
Sumatriptan je na trhu dostupný i v řadě generických přípravků a jako jediný triptan i v různých lékových formách (dostupné jsou 50mg, 100mg tablety, nosní sprej a injekce). Eletriptan je dostupný ve 40mg a 80mg tabletách; naratriptan (2,5mg tablety) s pomalým nástupem účinku je výhodný tam, kde razantní triptany mají nežádoucí účinky nebo dochází k rekurencím. Frovatriptan s dlouhým biologickým poločasem, který byl s výhodou užíván u dlouhých, pomalu nastupujících záchvatů, již bohužel není na našem trhu k dispozici. Z trhu zmizel rovněž zolmitriptan, almotriptan se na trh u nás nedostal.
Pro účinnou léčbu je třeba mít stanovenu přesnou diagnózu, musíme zvolit vhodnou lékovou formu triptanu a zvládnout i načasování podání léku. Triptany jsou efektivní v léčbě všech forem migrény a v léčbě cluster headache, nepomáhají u jiných typů bolestí hlavy, ať už se jedná o primární tenzní bolesti hlavy, ve velké většině i o rychlé trigeminové autonomní neuralgie, nebo o některou z forem sekundární bolesti hlavy. V případě neúčinnosti triptanů je třeba zvážit, zda byla diagnóza stanovena správně. Co se týče volby konkrétního triptanu, je třeba vzít v úvahu, jak rychle nastupuje ataka, jak dlouho obvykle trvá, a dle toho zvolit léčivo i konkrétní lékovou formu. Pokud pacient v časné fázi ataky zvrací, je vhodné užít namísto tablety nosní sprej, případně injekci. Volba krátkodobě působícího triptanu může vést k rekurenci (návratu bolesti do 24 hodin). Někteří pacienti popisují nepříjemné nežádoucí účinky (tlak na hrudi, pocit tepla v obličeji, parestezie v oblasti krku, celková malátnost, pocit otupění), které nejsou nebezpečné, ale nemocní je mohou špatně snášet, pokud nejsou před užitím léku informováni. Někdy i navzdory úlevě od bolesti tuto léčbu odmítají.
Paní přednostka Marková shrnula, že u sporadické migrény (tj. 2–3 ataky měsíčně) je zásadní včasné podání léku hned při prvních známých příznacích, které každý nemocný pozná. Upozornila, že u migrény s aurou je možné užít triptan až po odeznění aury. Triptan by mohl svým vazokonstrikčním působením auru prodloužit, znepříjemnit. U pacientů s frekventní migrénou je indikování triptanů třeba zvážit dle četnosti výskytu záchvatů, nadužívání je definováno od užívání trvajícího deset dnů v měsíci po dobu tří a více měsíců.
V další části přednášky se paní přednostka zaměřila na situace, kdy navzdory správné diagnóze i náležitému podání vhodného léku k úlevě od bolesti nedochází. Je možné doporučit nesteroidní antiflogistika (NSA, indometacin v čípku, nimesulid nebo ibuprofen v granulátu). U migrény s aurou je možné volit kombinaci NSA s triptany, v první fázi podat NSA v rychle vstřebatelné formě a při začátku bolesti podat triptan. U rychle nastupujícího migrenózního záchvatu s rekurencemi po 8–10 hodinách lze u dobře spolupracujících pacientů zvolit kombinaci triptanů. V začátku tedy užít krátkodobě působící sumatriptan nebo eletriptan a při rekurenci bolesti pak déle působící naratriptan. Od zahájení profylaktické medikace očekáváme zmírnění závažnosti a frekvence atak i zlepšení efektu akutní léčby. Je třeba také ověřit, že se nejedná o „medication overuse headache“, protože užití další dávky akutní medikace situaci dále zhoršuje.
Co se týká bezpečnosti v graviditě, dle posledních dat z německého registru pacientek nebyly doloženy statisticky významné rozdíly ve výskytu předčasných porodů, spontánních potratů ani závažných porodních defektů [1]. U triptanů se tedy nepředpokládají teratogenní účinky. Vzhledem k tomu, že v klinických hodnoceních byl nejvíce užíván sumatriptan, je považován za nejvíce prostudovaný přípravek a pro užití v graviditě jako první volba.
Současné možnosti profylaktické
léčby migrény
Druhé přednášky se ujal MUDr. Rudolf Kotas, Ph.D., z Neurologické kliniky LF UK a FN Plzeň, který přítomným představil téma Současné možnosti profylaktické léčby migrény a věnoval se rovněž její patofyziologii. Migréna je třetím nejčastějším onemocněním na světě a zaujímá přední místo mezi neurologickými nemocemi, které způsobují zneschopnění pacienta. Záchvaty znemožňují vykonávání běžných denních aktivit, omezují práceschopnost a využití volného času. Pro společnost představuje toto onemocnění ekonomickou zátěž, z čehož vyplývá nutnost migrénu co nejúčinněji léčit.
Přednášející shrnul současné možnosti léčby. U léčby akutního záchvatu odkázal na předchozí přednášku; k dispozici jsou nespecifická antimigrenika (jednoduchá analgetika, NSA), která jsou účinná u záchvatů nižší a střední intenzity, částečně specifická léčiva (ergotamin) pro středně těžké záchvaty a dále specifické triptany. Cílem je co nejrychleji potlačit bolest hlavy včetně doprovodných příznaků u již probíhajícího záchvatu. Indikací pro profylaktickou léčbu jsou časté (≥ 4/měsíc) nebo dlouhotrvající (≥ 48 hodin) ataky, dále neúčinnost terapie, závažné nežádoucí účinky nebo kontraindikace akutní terapie. Další indikaci představují ataky, kdy hrozí určité riziko trvalého neurologického deficitu, jako je hemiplegická migréna nebo migréna s kmenovou aurou. Cílem profylaxe je snížení frekvence, intenzity a trvání záchvatů a omezení spotřeby akutní medikace (snížení rizika overuse medication headache).
Doktor Kotas zhodnotil současné možnosti profylaktické léčby jako ne zcela optimální. Profylaktická léčba není využívána v dostatečné míře (dva ze tří vhodných nemocných ji nedostávají). Adherence pacientů k profylaktické léčbě je poměrně nízká, hlavními důvody k přerušení terapie jsou často se vyskytující nežádoucí účinky a limitovaný efekt léčby. U betablokátorů (používány hlavně propranolol 40–240 mg, metoprolol 100–200 mg) se mezi nežádoucími účinky objevují hypotenze, bradykardie, závratě, prekolapsové stavy, u antiepileptik to jsou parestezie, kognitivní postižení a deprese (topiramát 50–100 mg). Řada nežádoucích účinků doprovází podávání valproátu (450–600 mg; nauzea, bolesti břicha, průjem, zácpa, závratě, třes, ospalost), riziko mohou představovat jeho teratogenní účinky, diskutována je jeho souvislost s polycystickými ovarii, s ovariální dysfunkcí a s nepravidelnostmi menstruačního cyklu. Z tohoto důvodu není tato léčba podávána mladým ženám. Blokátory kalciového kanálu (flunarizin 5–10 mg, cinarizin 50–100 mg) vykazují extrapyramidové nežádoucí účinky, deprese a často vzestup tělesné hmotnosti, u verapamilu (180–240 mg) se objevuje pokles krevního tlaku, AV blok, v případě antidepresiv (amitriptylin do 50–75 mg) jsou udávány ranní ospalost, sucho v ústech, sexuální dysfunkce a retence moči. Relativně lépe je snášen venlafaxin (75–150 mg).
Limitovaný efekt znamená, že profylaktická léčba snižuje frekvenci záchvatů o 50 % a více zhruba u 40–50 % pacientů. Dle odborných diskusí má až 80 % nemocných zkušenost alespoň s jedním profylaktikem, které nebylo účinné.
Relativně novější možností je léčba botulotoxinem, který se injekčně aplikuje do svalů čela, spánku a šíje v pevně stanovených bodech. Efekt terapie byl potvrzen ve dvou rozsáhlých dvojitě zaslepených studiích kontrolovaných placebem (program PREEMPT) [2].
Uvedené lékové skupiny používané v profylaxi migrény mají hlavní indikaci pro léčbu jiného onemocnění, účinky u migrény byly zjištěny „náhodou“, kdy došlo k úlevě od bolesti při užívaní této medikace a následnému využití. V posledních desetiletích se výzkum nové léčby opírá o znalosti patofyziologie nemoci. Příkladem jsou již triptany, agonisté serotoninových receptorů 5 HT1B/1D, kde k vývoji lékové skupiny vedly znalosti o úloze serotoninu a funkci jednotlivých podtypů receptorů.
V současnosti se pozornost zaměřila na jednu z klíčových molekul, calcitonin gene related peptide (CGRP). Ten, jak se zdá, hraje příčinnou úlohu při vzniku bolesti hlavy u migrény. Podstatou bolesti hlavy je stimulace (depolarizace) nociceptivních trigeminových vláken, která patří k trigeminovaskulárnímu systému. Vlákna obklopují piální, durální arterie, velké mozkové cévy a velké žilní splavy. Při stimulaci se uvolňují neurotransmitery, zejména CGRP, v menší míře substance P a neurokinin A. Dochází k vazodilataci meningeálních cév, k rozvoji sterilního perivaskulárního zánětu, na němž se podílejí serotonin, histamin, prostaglandiny a další substance; CGRP se uplatňuje i při centrální transmisi bolestivých impulzů po trigeminové dráze do mozku. Ke stimulaci trigeminovaskulárního systému dochází aktivací tzv. TRP kanálů (transient receptor potential channels), které jsou na stejných nociceptivních vláknech a obsahují také CGRP.
U migrény s aurou je schopna tyto kanály aktivovat elektrická porucha v mozkové kůře (korová šířící se deprese elektrické aktivity). Má se za to, že ta je zodpovědná za klinické příznaky aury. Dochází k postupné depolarizaci neuronů a k postupnému vyhasnutí synaptické aktivity neuronů s poklesem mozkového krevního průtoku (viditelné na vyšetření SPECT). Analogická porucha se pravděpodobně vyskytuje i u migrény bez aury (jak dokládají vyšetření PET), ale bez klinického korelátu. TRP kanály mohou být aktivovány i některými exogenními činiteli, jako jsou alkohol nebo složky cigaretového kouře – známé provokační faktory migrény.
Během ataky migrény se hodnoty CGRP v krvi (vena jugularis externa) zvyšují. Bylo zjištěno, že intravenózní injekce CGRP vyvolává u migreniků záchvat migrény, ale nikoliv u kontrolních jedinců. Na základě těchto poznatků se farmaceutický výzkum zaměřil na vývoj monoklonálních protilátek proti CGRP nebo jeho receptoru. První dostupnou protilátku v České republice představuje erenumab (v dávkách 70 a 140 mg), další v pořadí by měly být fremanezumab (225 a 675 mg), galkanezumab (120 a 240 mg) a eptinezumab (100 a 300 mg). S výjimkou eptinezumabu, který se podává intravenózní infuzí, jsou tyto monoklonální protilátky aplikovány jako subkutánní injekce obvykle v intervalu jednou za čtyři týdny (fremanezumab ve vyšší dávce také kvartálně). Výsledky klinických hodnocení, která proběhla, jsou slibné. Efekt po subkutánní aplikaci začíná být patrný již v prvním týdnu léčby. Studie s erenumabem a fremanezumabem dokládají účinnost i u nemocných s chronickou migrénou s nadužíváním akutní medikace, a dále u pacientů, u nichž byla dosud neúčinná jiná profylaktická léčba.
Refrakterní migréna
Jako poslední v přednáškovém bloku vystoupil MUDr. Tomáš Nežádal, Ph.D., z Neurologického oddělení Ústřední vojenské nemocnice v Praze s tématem Refrakterní migréna – možnosti specializovaného centra pro diagnostiku a léčbu bolestí hlavy.
Migréna je dle žebříčku Světové zdravotnické organizace šestou nejvíce handicapující diagnózou, dle Global Burden of Disease se řadí za cévní mozkovou příhodu a demence na třetí místo. Udává se, že jen u 56,2 % nemocných je stanovena diagnóza. Prevalence migrény (17,1 % u žen a 5,6 % u mužů) vykazuje v posledních letech rostoucí tendenci. Nejčastěji se onemocnění vyskytuje mezi třicátníky až čtyřicátníky, chronickou migrénu zaznamenáváme u 3–5 % nemocných. Zhruba u jednoho procenta migreniků se jedná o bolest hlavy vyvolanou nadužíváním medikace (medication overuse headache) [3,4].
Chronická migréna je definována bolestí hlavy, která se vyskytuje 15 a více dní za měsíc, přičemž v osmi a více dnech se jedná o migrénu. U těchto nemocných je doložena vyšší prevalence komorbidit a horší kvalita života. Nadužívání medikace je u těchto pacientů udáváno v 50 % a více. Profylaktická léčba snižuje frekvenci, tíži a trvání atak.
Vliv chronické migrény na každodenní aktivity a fyzickou odolnost je výrazný. Epizodická migréna může do chronické migrény progredovat, dochází k tomu zejména u pacientů s více komorbiditami. Vliv má i frekvence záchvatů a nadužívání medikace. Bolest vyvolaná nadužíváním medikace je bolest, která se vyskytuje 15 a více dní v měsíci u pacienta s preexistujícím syndromem bolesti hlavy, u něhož nebylo možné stanovit jinou diagnózu. Její prevalence ve světě se významně liší, pravděpodobně dle dostupné léčby. Nejčastěji se s ní setkáváme u migrény a tenzních bolestí hlavy. Medication overuse headache je významným faktorem chronifikace primárních bolestí hlavy. Rizikovost je nejnižší u triptanů, ergotaminu, vysoká u kombinovaných analgetik a opioidů. Důležitá je v této problematice prevence – instruovat pacienta o vztahu mezi nadměrným užíváním akutní medikace a progresí bolesti hlavy. Pozitivní pro zvýšení povědomí se v tomto směru ukázaly informační kampaně zaměřené na nežádoucí účinky a způsob podávání analgetik.
První fází léčby bolesti hlavy
z nadužívání medikace je její kompletní odnětí.
U triptanů, derivátů ergotaminu, monokomponentních
i kombinovaných analgetik je možné ihned, v případě
barbiturátů, benzodiazepinů a opioidů se podávání
ukončuje postupně. Podle motivace, délky trvání, typu léků
a komorbidit volíme ambulantní léčbu nebo hospitalizaci,
uplatňuje se zde multidisciplinární program.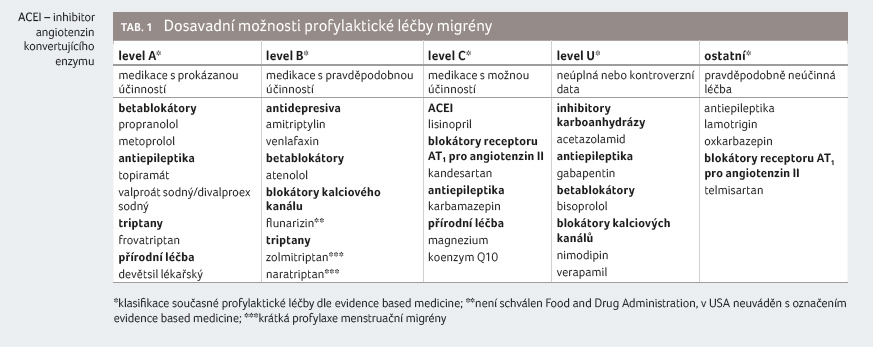
Doktor Nežádal se v další části svého vystoupení zaměřil na profylaktickou léčby migrény. Akutní medikaci užívá asi 98 % pacientů, profylaktickou léčbu jen zhruba 12,4 % (poměr žen a mužů 2 : 1). Profylaktika, která jsme měli dosud k dispozici, shrnuje tabulka 1. Perzistence je u profylaktické léčby obecně nízká (25 % po šesti měsících, 14 % po 12 měsících). Jako nejčastější důvod je uváděna ztráta účinnosti nebo výskyt nežádoucích účinků. Objevit se může také tzv. pseudofarmakorezistence. Nejčastějšími příčinami jsou chybná diagnóza, nezahájení nebo nesprávná volba profylaktické léčby, nízké nebo neúčinné dávky léčiv, krátká doba podávání a špatná compliance (tj. nepravidelné užívání léků, nevhodný životní styl – nepravidelný režim, spánková deprivace, abúzus alkoholu či jiných návykových látek, další provokační vlivy).
V diferenciální diagnostice migrény je např. užitečné zaměřit se i na její prodromální fázi. Pacienti s migrénou znají typické prodromy, které se objevují 2–48 hodin před záchvatem. Patří mezi ně únava, změna nálady (pomýšleno na tenzní bolesti), zhoršení koncentrace, zívání, tuhnutí šíje (zaměňováno za cervikogenní bolest), zvýšená chuť k jídlu, polyurie/polydipsie, fotofobie, fonofobie, nauzea nebo kraniální autonomní symptomy (odlišení trigemino autonomních bolestí).
Při neúčinnosti terapie je možné zkusit kombinovanou akutní léčbu (např. sumatriptan + naproxen) nebo kombinovanou profylaktickou léčbu (valproát + propranolol, topiramát + magnezium, antiepileptikum + blokátor kalciového kanálu). Účinnost prokázaly, nicméně v tzv. off label použití, zonisamid a levetiracetam.
Jako farmakorezistentní migrénu
definujeme migrénu, u níž došlo k selhání nejméně
dvou profylaktik s různým mechanismem účinku a s prokázanou
účinností. Může se jednat o epizodickou migrénu
s četnějšími záchvaty (4–14/měsíc), chronickou migrénu
(≥ 15 záchvatů/měsíc) nebo migrénu v souvislosti
s nadužíváním medikace. Jako další (centrová) terapie zde
přichází v úvahu aplikace botulotoxinu (onabotulinum toxin
A) u chronické migrény, není ale hrazen zdravotní
pojišťovnou; aktuálně anti CGRP protilátky
a neurostimulace. Přehled anti CGRP protilátek je uveden
v tabulce 2.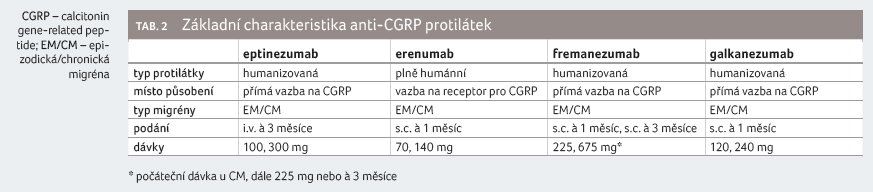
Výsledky klinických hodnocení dokládají vysokou účinnost anti CGRP léčby oproti placebu jak u epizodické, tak u chronické migrény. Dle panelu odborníků a recentních doporučených postupů [5] by měly být tyto protilátky nabídnuty pacientům s epizodickou nebo chronickou migrénou, u nichž selhaly alespoň dvě dostupné účinné profylaktické léčby (viz tab. 1 – level A, B) nebo u nichž nelze využít perorální preventivní terapii z důvodu komorbidit, nežádoucích účinků nebo nedostatečné compliance. Předpokládaná délka léčby je 6–12 měsíců. Anti CGRP protilátky by neměly být podávány těhotným a kojícím ženám, pacientům s abúzem alkoholu a drog a se závažným kardiovaskulárním a cerebrovaskulárním onemocněním a se závažnou mentální poruchou.
V případě selhání těchto metod je možné použít pro léčbu migrény stimulační metody. Mezi neinvazivní patří transkraniální magnetická stimulace, transkutánní supraorbitální neurostimulace, neinvazivní stimulace nervus vagus a kalorická vestibulární stimulace. Principem metody je periferní působení na nervová zakončení a ovlivnění periferní i centrální senzitizace. Minimálně invazivní metodou je stimulátor okcipitálního nervu. Recentně renovovanou metodu úlevy od bolesti u chronické migrény představuje blokáda ganglion sphenopalatinum intranazální aplikací 4% lidokainu.
Redakčně zpracovala PharmDr. Kateřina Viktorová
Seznam použité literatury
- [2] Dodick DW, Turkel CC, DeGryse RE, et al.; PREEMPT Chronic Migraine Study Group. OnabotulinumtoxinA for treatment of chronic migraine: pooled results from the double‑blind, randomized, placebo‑controlled phases of the PREEMPT clinical program. Headache 2010; 50: 921–936
- [3] Vos T, Abajobir AA, Abate KH, et al. Global, regional, and national incidence, prevalence, and years lived with disability for 328 diseases and injuries for 195 countries, 1990‑2016: a systematic analysis for the global burden of disease study 2016. Lancet 2017; 390: 1211–1259.
- [4] Burch R, Rizzoli P, Loder E. The Prevalence and Impact of Migraine and Severe Headache in the United States: Figures and Trends From Government Health Studies. Headache 2018; 58: 496–505.
- [5] Sacco S, Bendtsen L, Ashina M, et al. European headache federation guideline on the use of monoclonal antibodies acting on the calcitonin gene related peptide or its receptor for migraine prevention. J Headache Pain 2019; 20: 6.