Nový inzulin glargin 300 U/ml
Souhrn:
Dlouhodobě působící inzulinová analoga mají udržovat konstantní a vyrovnanou inzulinemii tak, aby napodobovala endogenní bazální sekreci inzulinu zdravých jedinců. Inzulin glargin s obsahem 100 jednotek inzulinu v 1 ml přípravku (Gla 100) představuje jako bazální inzulin v současnosti „standard“ léčby diabetes mellitus 1. i 2. typu. Nový inzulinový přípravek glargin o koncentraci 300 jednotek/ml (Gla 300) má vyrovnanější a prolongovanější farmakokinetic-ký a farmakodynamický profil ve srovnání s Gla 100. Inzulin Gla 300 je ve snižování glykemie srovnatelně účinný s inzulinem Gla 100, navíc je však léčba Gla 300 spojena se sníženým nebo srovnatelným rizikem vzniku hypoglykemie a s dalšími potenciálně výhodnými charakteristikami.
Key words: basal insulin – glargine 300 U/ml – glargine 100 U/ml – type 1 diabetes mellitus – type 2 diabetes mellitus.
Summary:
Long acting insulin analogues are designed to establish constant and sustained insulin concentrations over the course of a day, and aim to mimic the endogenous fasting insulin production seen in healthy individuals. Insulin glargine containing 100 units of insulin in 1ml solution (Gla 100) is – as a basal insulin – a „standard“ in the treatment of type 1 and type 2 diabetes mellitus. New insulin glargine 300 U/ml (Gla 300) has been shown to have more even and prolonged pharmacokinetic and pharmacodynamic profiles compared with Gla 100. Gla 300 is an insulin that exhibits glucose lowering effect similar to that of Gla 100, with a reduced or similar risk of hypoglycemia and some other potentially advantageous characteristics.
Úvod
Cílem vývoje nových dlouhodobě působících inzulinových analog je získat přípravek, který by zajistil dlouhodobě konstantní a vyrovnanou plazmatickou koncentraci inzulinu kopírující endogenní bazální sekreci inzulinu u zdravých jedinců. U pacientů s diabetes mellitus 1. typu představují tyto inzulinové přípravky substituci chybějící tvorby endogenního inzulinu, zatímco u pacientů s diabetes mellitus 2. typu doplňují neadekvátní sekreci inzulinu, později též chybějící sekreci. Problémem je, že subkutánní podání a jedna denní dávka znemožňují přesnou reprodukci fyziologicky oscilující sekrece inzulinu. Ideální dlouhodobě působící inzulinový analog by měl mít nízkou diurnální fluktuaci a vysokou mezidenní reprodukovatelnost [1,2].
Inzulin glargin 100 (Gla‑100) s koncentrací 100 jednotek na 1 ml přípravku poskytuje po podání jedné subkutánní dávky 24hodinové pokrytí bazální potřeby inzulinu a v posledním desetiletí se stal standardem léčby diabetu. Nový inzulinový přípravek glargin 300 (Gla‑300), obsahující trojnásobnou koncentraci, tj. 300 jednotek inzulinu glarginu v 1 ml přípravku, se z podkožního depa uvolňuje pomaleji než Gla‑100; to má za následek plošší a prolongovanější farmakokinetický a farmakodynamický profil s delší kontrolou glykemie, přesahující 24 hodin [3]. Taková farmakokinetika přípravku pomáhá zajistit efektivní využití inzulinu, umožní adekvátní dávkování a titraci a potenciálně zlepší glykemickou kontrolu při snížení rizika vzniku hypoglykemie [1,2]. Inzulin Gla‑300 i Gla‑100 mají podobnou účinnost a bezpečnostní profil, ale léčba inzulinem Gla‑300 je spojena s limitovaným přírůstkem tělesné hmotnosti a s nižší nebo srovnatelnou incidencí hypoglykemie [4].
Charakteristika léčiva
Inzulin glargin napodobuje fyziologickou bazální sekreci inzulinu. Zpomaleného vstřebávání z podkoží je dosaženo náhradou kyseliny asparagové na pozici A21 glycinem a přidáním dvou molekul argininu na konci řetězce A. V kyselém roztoku je rozpustný, ale při fyziologickém pH po subkutánní aplikaci precipituje, pomalu se uvolňuje a vstřebává.
Na rozdíl od inzulinových přípravků, které si po injekční aplikaci zachovávají rozpustnost, změna koncentrace inzulinu glarginu na 300 U/ml injikovaného roztoku je spojena se změnou kinetiky jeho absorpce. Předpokládá se, že velikost, a tím i povrch subkutánního depa určuje rychlost uvolňování [5].
Po subkutánní aplikaci glarginu (M0) a jeho uvolnění ze subkutánního depa dochází obdobně jako u maturace humánního inzulinu v buňkách β pankreatu k enzymatickému odštěpení C‑terminálního argininu za vzniku 21A‑glycin‑humánního inzulinu (metabolit M1) [6]; M1 je hlavním cirkulujícím metabolitem, který odpovídá za metabolické účinky Gla‑100 u pacientů s diabetes mellitus 1. i 2. typu [7]. Následnou ztrátou threoninu v pozici 30B vzniká 21A‑Gly‑des‑30B‑Thr‑humánní inzulin (metabolit M2). Metabolity M1 i M2 mají nižší afinitu k receptoru pro IGF‑1 (insulin‑like growth factor 1) než humánní inzulin a terapeutické koncentrace mateřské molekuly a jejích metabolitů jsou výrazně nižší než koncentrace s možným mitogenním potenciálem [7–9].
Metabolismus Gla‑300 je stejný jako u Gla‑100; M1 je hlavní cirkulující aktivní molekulou v krvi u obou přípravků. K ustálenému stavu koncentrace M1 dochází za dva dny při aplikaci Gla‑100 a za čtyři dny při podávání Gla‑300 [10].
Farmakokinetické a farmakodynamické studie
Výsledky euglykemického clampu po aplikaci jedné dávky inzulinu Gla‑300 u zdravých jedinců, ale následně i u diabetiků 1. typu prokázaly nižší diurnální variabilitu hypoglykemizujícího účinku oproti stejné dávce Gla‑100 [6,11].
Přestože výsledky první studie byly ovlivněny endogenní sekrecí inzulinu (zdraví jedinci), představovaly impuls k vývoji inzulinu Gla‑300. V práci Beckera a spol. bylo v rámci dvojitě zaslepené randomizované překřížené studie sledováno 50 pacientů s diabetes mellitus 1. typu, kteří podstoupili 24hodinový euglykemický clamp po dosažení ustáleného stavu – po šesti injekcích Gla‑300 v dávce 0,4 U/kg aplikovaných jednou denně. Účastníci dostávali buď standardní Gla‑300 (ve formě zásobníku do pera, cartridge) v první léčebné periodě a Gla‑300 s přidaným polysorbátem 20 ke zvýšení stability ve druhé léčebné periodě, anebo opačně. Tato studie hodnotila bioekvivalenci těchto dvou forem Gla‑300. Účinek inzulinu byl v obou formách srovnatelný, predikovatelný, rovnoměrně rozložený v průběhu 24 hodin, s nízkou fluktuací a vysokou reprodukovatelností. Poukazuje to na postupnější a prolongovanější uvolňování inzulinu glarginu z podkožního depa v případě Gla‑300 [11].
Další studie zaměřená na farmakokinetický a farmakodynamický profil Gla‑300 po dosažení ustáleného stavu potvrdila výhody Gla‑300. V této studii s 30 pacienty s diabetes mellitus 1. typu byla srovnávána farmakokinetika a farmakodynamika Gla‑300 v dávkách 0,4 U/kg a 0,6 U/kg s Gla‑100 podávaným v dávce 0,4 U/kg. Po dosažení ustáleného stavu (po 8 dnech léčby) byl u pacientů proveden euglykemický clamp. Poté došlo k překřížení studie a pacienti tak absolvovali hodnocení se všemi dávkami obou inzulinů. Koncentrace inzulinu a rychlost infuze glukózy byly stabilnější a vyrovnanější po podání Gla‑300 ve srovnání s Gla‑100. Doba trvání účinku byla rovněž delší a těsná kontrola glykemie byla udržena přibližně o 5 hodin déle při aplikaci Gla‑300 [5].
Glargin 300 U/ml v klinických studiích
Progr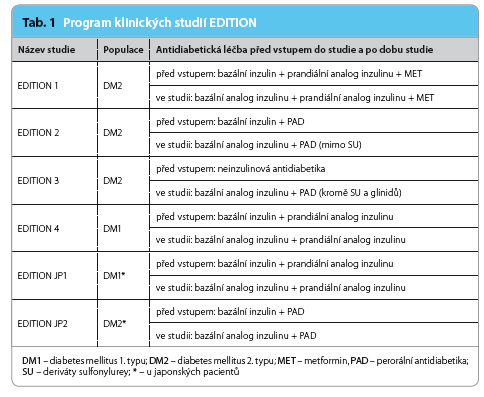 am vývoje nového inzulinového přípravku Gla‑300 zahrnul široké spektrum stadií diabetes mellitus 2. typu. Inzulin Gla‑300 byl studován v klinickém programu EDITION, do kterého bylo v šesti klinických studiích 3. fáze zahrnuto více než 3 500 pacientů (tab. 1). Čtyři studie fáze 3a srovnávaly účinnost a bezpečnost Gla‑300 s inzulinem Gla‑100 v různých populacích pacientů s diabetes mellitus 2. typu.
am vývoje nového inzulinového přípravku Gla‑300 zahrnul široké spektrum stadií diabetes mellitus 2. typu. Inzulin Gla‑300 byl studován v klinickém programu EDITION, do kterého bylo v šesti klinických studiích 3. fáze zahrnuto více než 3 500 pacientů (tab. 1). Čtyři studie fáze 3a srovnávaly účinnost a bezpečnost Gla‑300 s inzulinem Gla‑100 v různých populacích pacientů s diabetes mellitus 2. typu.
První, EDITION 1, hodnotila 807 pacientů s diabetes mellitus 2. typu s neuspokojivou kompenzací při léčbě kombinací bazálního inzulinu (≥ 42 jednotek denně) s inzulinem prandiálním. Jednalo se o multicentrickou, randomizovanou, otevřenou studii. Pacienti byli po šesti měsících léčby randomizováni do dvou skupin – s léčbou Gla‑300 nebo Gla‑100 – a sledováni dalších šest měsíců. Po dobu léčby došlo v obou skupinách k obdobnému zlepšení kompenzace diabetu, ale u pacientů s Gla‑300 bylo o 22 % nižší relativní riziko potvrzené (< 3,9 mmol/l) nebo těžké noční hypoglykemie a nebyl pozorován vyšší výskyt denních hypoglykemií [12].
Do studie EDITION 2 byli zařazeni pacienti již léčení bazálním inzulinem a v kombinaci s perorálními antidiabetiky. Jednalo se o 811 pacientů s průměrnou vstupní hodnotou glykovaného hemoglobinu 8,24 %. Inzulin Gla‑300 byl v této studii stejně účinný jako Gla‑100. Dávka inzulinu Gla‑300 byla o 10 % vyšší. Riziko vzniku hypoglykemie bylo opět nižší ve skupině pacientů léčených Gla‑300, a to o 29 % v případě potvrzených (< 3,9 mmol/l) nočních nebo závažných hypoglykemií a o 10 % v případě hypoglykemie zaznamenané kdykoli v průběhu 24 hodin [13].
Studie EDITION 3 se účastnilo 878 pacientů, kteří byli před zařazením do studie tzv. inzulin‑naivní, léčení jenom perorálními antidiabetiky. I v této studii byl zaznamenán nižší výskyt noční hypoglykemie u pacientů léčených Gla‑300, a to zejména ve fázi titrace dávky inzulinu v prvních osmi týdnech léčby (o 26 %) [14].
Ritzel se spolupracovníky provedl metaanalýzu prvních tří studií z klinického programu EDITION. Výsledky nám ukazují, že v široké populaci pacientů s diabetes mellitus 2. typu byl Gla‑300 stejně účinný jako Gla‑100 ve zlepšení glykemické kontroly v průběhu šesti měsíců. Inzulin Gla‑300 navíc vedl ke snížení výskytu potvrzených (< 3,9 mmol/l) nočních nebo závažných hypoglykemických příhod v![Graf 1a, b Kumulativní střední počet potvrzených (≤ 3,9 mmol/l) nebo těžkých hypoglykemických příhod na pacienta (a) kdykoli během dne (24 h) a (b) během noci (0:00–5:59); podle [15] – Ritzel, et al., 2015. Gla-100 – glargin o koncentraci 100 U/ml; Gla-300 – glargin o koncentraci 300 U/ml](https://www.remedia.cz/photo-a-30328---.jpg) jakékoli části dne, ale také během noci [15], graf 1a, b. Redukce těchto hypoglykemií byla zřetelná již během prvních osmi týdnů léčby. Dále byl zaznamenán mírně nižší přírůstek tělesné hmotnosti oproti pacientům léčeným Gla‑100 (p = 0,039). Dávka bazálního inzulinu se během šestiměsíční doby trvání studie zvýšila v obou skupinách, a to zejména v prvních 12 týdnech léčby. Dávka bazálního inzulinu byla ve skupině léčené Gla‑300 o 12 % vyšší oproti skupině léčené Gla‑100. Tento výsledek byl pozorován ve všech třech analyzovaných studiích EDITION. Vysvětlením může být efekt subkutánního depa. Je možné, že delší doba perzistence Gla‑300 v podkoží (konzistentní se stabilnějším a prolongovaným farmakokinetickým a farmakodynamickým profilem Gla‑300 ve srovnání s Gla‑100) [5] může vést ke zvýšení enzymatické inaktivace tkáňovými peptidázami v místě injekce [15]. Přes potřebu vyšší dávky Gla‑300 oproti Gla‑100 bylo dosaženo obdobné glykemické kontroly při nižším riziku vzniku hypoglykemie a současně byl u pacientů léčených Gla‑300 zaznamenán nižší přírůstek hmotnosti ve srovnání s těmi, kteří byli léčeni Gla‑100.
jakékoli části dne, ale také během noci [15], graf 1a, b. Redukce těchto hypoglykemií byla zřetelná již během prvních osmi týdnů léčby. Dále byl zaznamenán mírně nižší přírůstek tělesné hmotnosti oproti pacientům léčeným Gla‑100 (p = 0,039). Dávka bazálního inzulinu se během šestiměsíční doby trvání studie zvýšila v obou skupinách, a to zejména v prvních 12 týdnech léčby. Dávka bazálního inzulinu byla ve skupině léčené Gla‑300 o 12 % vyšší oproti skupině léčené Gla‑100. Tento výsledek byl pozorován ve všech třech analyzovaných studiích EDITION. Vysvětlením může být efekt subkutánního depa. Je možné, že delší doba perzistence Gla‑300 v podkoží (konzistentní se stabilnějším a prolongovaným farmakokinetickým a farmakodynamickým profilem Gla‑300 ve srovnání s Gla‑100) [5] může vést ke zvýšení enzymatické inaktivace tkáňovými peptidázami v místě injekce [15]. Přes potřebu vyšší dávky Gla‑300 oproti Gla‑100 bylo dosaženo obdobné glykemické kontroly při nižším riziku vzniku hypoglykemie a současně byl u pacientů léčených Gla‑300 zaznamenán nižší přírůstek hmotnosti ve srovnání s těmi, kteří byli léčeni Gla‑100.
V tříměsíční podstudii EDITION 1 (109 pacientů) a EDITION 2 (89 pacientů) bylo sledováno flexibilní vs. fixní dávkování inzulinu Gla‑300. Flexibilita aplikace Gla‑300 v rozmezí ±3 hodiny neovlivnila glykemickou kontrolu a frekvenci hypoglykemií [16].
Další klinické hodnocení, EDITION 4, bylo provedeno u pacientů s diabetes mellitus 1. typu (n = 549, průměrná doba trvání diabetu 21 let, průměrná hodnota glykovaného hemoglobinu 8,1 %). Pacienti byli randomizováni v poměru 1 : 1 : 1 : 1 k léčbě Gla‑300 nebo Gla‑100 podávaným jednou denně ráno nebo večer, a to při pokračujícím podávání prandiálního inzulinu. Ve studii byla potvrzena non‑inferiorita v účinnosti Gla‑300 proti Gla‑100. Výskyt potvrzených hypoglykemií (< 3,9 mmol/l) a těžkých hypoglykemií kdykoli v průběhu dne byl podobný; výskyt nočních hypoglykemií byl nižší ve skupině léčené Gla‑300 v prvních osmi týdnech léčby. Glykemická kontrola ani výskyt hypoglykemií nezávisely na době aplikace (ráno vs. večer). Pacienti léčení Gla‑300 potřebovali vyšší dávku inzulinu. Vzestup tělesné hmotnosti byl signifikantně nižší u pacientů léčených Gla‑300 [17].
Studie EDITION JP1 byla provedena u 243 japonských pacientů s diabetes mellitus 1. typu. Také zde došlo k poklesu hodnot glykovaného hemoglobinu ve skupině pacientů léčených Gla‑300 obdobnému jako ve skupině pacientů, kteří byli léčeni Gla‑100. U pacientů, kteří dostávali Gla‑300, byl pozorován nižší výskyt potvrzených a nočních hypoglykemií [18].
Rovněž studie EDITION JP2 hodnotila japonské pacienty. Do studie bylo zařazeno 241 pacientů s diabetes mellitus 2. typu a obdobně jako u předchozích studií bylo zjištěno, že léčba Gla‑300 vedla ke stejnému zlepšení kompenzace diabetu jako léčba Gla‑100, ale s nižším výskytem hypoglykemií [19].
Využití v praxi
Bazální inzulin představuje v kombinaci s prandiálním inzulinem základ léčby pacientů s diabetes mellitus 1. typu.
Diabetes mellitus 2. typu je komplexní a heterogenní onemocnění a požadavky na zahájení inzulinoterapie závisejí na různých okolnostech, např. na životním stylu anebo na stadiu onemocnění. V iniciálních fázích je často možné dosáhnout glykemické kontroly změnou životního stylu a užíváním jednoho nebo více perorálních antidiabetik. Při progresi nemoci je ale u mnohých pacientů nutná léčba exogenním inzulinem. Preferovaným iniciálním inzulinovým režimem je často bazální inzulin, protože tato léčba je spojena s nižším rizikem hypoglykemie a vede k nižšímu přírůstku tělesné hmotnosti ve srovnání s premixovaným inzulinem nebo s intenzifikovaným inzulinovým režimem [20]. Bazální inzulin by měl být účinný v celém spektru stadií onemocnění, od inzulin‑naivních pacientů až po ty, kteří vyžadují kombinovanou léčbu, s minimálním narušením jejich denního životního rytmu.
Tyto požadavky splňuje nový inzulinový přípravek Gla‑300. Ten byl původně vyvíjen pro pacienty s potřebou větších dávek inzulinu, u kterých podávání koncentrovanějšího inzulinového přípravku představuje výhodu ve smyslu zmenšení objemu aplikované dávky a tím zvýšení pohodlí při aplikaci. Tento inzulin má ale i další výhody. Nižší diurnální variabilita expozice inzulinu má klinický význam v tom, že snižuje riziko vzniku hypo‑ a hyperglykemie. Nižší riziko hypoglykemie může pomoci odbourat strach z takových epizod a odstranit tak jednu z hlavních překážek dosažení žádoucí glykemické kontroly [21]. Výhodu v klinických podmínkách představuje i nižší mezidenní variabilita a vyšší reprodukovatelnost účinku, díky předvídatelnější expozici inzulinu je umožněna jednodušší titrace jeho dávky.
Dalším klinicky důležitým aspektem tohoto přípravku je limitovaný přírůstek tělesné hmotnosti při léčbě a také větší flexibilita času aplikace (±3 hodiny před obvyklou dobou podání nebo po ní) v případě pacientovy potřeby. To jsou charakteristiky, které mohou u pacientů příznivě ovlinit compliance s léčbou.
Závěr
Přes velké pokroky v léčbě pacientů s diabetes mellitus se u mnohých nemocných nedaří dosáhnout žádoucí glykemické kontroly. Příčiny mohou být různé: nedostatečná titrace dávky inzulinu, problematická adherence pacientů k léčbě, ale často i obava z hypoglykemie.
Lepší farmakokinetický a farmakodynamický profil Gla‑300 je spojen s nižší variabilitou účinku inzulinu a tím i s nižším rizikem hypoglykemie, zejména v nočních hodinách. Léčba inzulinem Gla‑300 vede k nižšímu vzestupu tělesné hmotnosti ve srovnání s Gla‑100 a poskytuje možnost flexibilní aplikace. Inzulin Gla-300 tak představuje novou perspektivu léčby bazálním inzulinem u diabetiků 1. i 2. typu.
Seznam použité literatury
- [1] Becker RH, Frick AD, Teichert L, et al. Fluctuation and reproducibility of exposure and effect of insulin glargine in healthy subjects. Diabetes Obes Metab 2008; 10: 1105–1113.
- [2] Gerich J, Becker RH, Zhu R, et al. Fluctuation of serum basal insulin levels following single and multiple dosing of insulin glargine. Diabetes Technol Ther 2006; 8: 237–243.
- [3] Pieber TR, Eugene Jolchine I, Derobert E. Efficacy and safety of HOE 901 versus NPH insulin in patients with type 1 diabetes. The European Study Group of HOE 901 in type 1 diabetes. Diabetes Care 2000; 23: 157–162.
- [4] Sutton G, Minguet J, Ferrero C, et al. U300, a novel long acting insulin formulation. Expert Opin Biol Ther 2014; 14: 1849–1860.
- [5] Becker RH, Dahmen R, Bergmann K, et al. New insulin glargine 300 units.ml 1 provides a more even activity profile and prolonged glycemic control at steady state compared with insulin glargine 100 units.ml 1. Diabetes Care 2015; 38: 637–643.
- [6] Tillner J, Bergmann K, Teichert L, et al. Euglycaemic single dose clamp profile of new insulin glargine formulation in subjects with type 1 diabetes is flat and prolonged. Diabetologia 2013; 56 (Suppl. 1): S415.
- [7] The Expert Committee On The Diagnosis And Classification Of Diabetes Mellitus. Report of the expert committee on the diagnosis and classification of diabetes mellitus. Diabetes Care 1998; 21: S5–S19.
- [8] Seino Y, Nanjo K, Tajima N, et al. Report of the Committee on the classification and diagnostic criteria of diabetes mellitus. Diabetol Int 2010; 1: 2–20.
- [9] Kashiwagi A, Kasuga M, Araki E, et al. International clinical harmonization of glycated hemoglobin in Japan: from Japan Diabetes Society to National Glycohemoglobin Standardization Program values. J Diabetes Investig 2012; 3: 39–40.
- [10] Steinstraesser A, Schmidt R, Bergmann K, et al. Investigational new insulin glargine 300 U/ml has the same metabolism as insulin glargine 100 U/ml. Diabetes Obes Metab 2014; 16: 873–876.
- [11] Becker RH, Hahn AD, Boderke P, et al. Long acting formulations of insulins. European patent application 111664415.7. 17 May 2011.
- [12] Riddle MC, Bolli GB, Ziemen M, et al. New insulin glargine 300 units/ml versus glargine 100 units/ml in people with type 2 diabetes using basal and mealtime insulin: glucose control and hypoglycemia in a 6 month randomized controlled trial (EDITION 1). Diabetes Care 2014; 37: 2755–2762.
- [13] Yki Jarvinen H, Bergenstal R, Ziemen M, et al. New insulin glargine 300 units/ml versus glargine 100 units/ml in people with type 2 diabetes using oral agents and basal insulin: glucose control and hypoglycemia in a 6 month randomized controlled trial (EDITION 2). Diabetes Care 2014; 37: 3235–3243.
- [14] Bolli GB, Riddle MC, Bergenstal RM, at al. New insulin glargine 300 U/ml compared with glargine 100 U/ml in insulin naive people with type 2 diabetes on oral gluco-se lowering drugs: a randomized controlled trial (EDITION 3). Diabetes Obes Metab 2015; 17: 386–394.
- [15] Ritzel R, Roussel P, Bolli GE, et al. Patient level meta analysis of EDITION 1, 2 and 3: glycaemic control and hypoglycaemia with new insulin glargine 300 U/ml versus glargine 100 U/ml in people with T2DM. Diabetes Obes Metab 2015; 17: 859–867.
- [16] Jeandidier N, Riddle MC, Bolli GB, et al. New insulin glargine 300 U/ml: efficacy and safety of flexible vs. fixed dosing intervals in people with type 2 diabetes mellitus. Abstracts of the 50th EASD Annual Meeting. Diabetologia 2014; 57: Suppl.: P961.
- [17] Home PD, Bergenstal RM, Bolli GB, et al. New Insulin Glargine 300 Units/mL Versus Glargine 100 Units/mL in People With Type 1 Diabetes: A Randomized, Phase 3a, Open Label Clinical Trial (EDITION 4). Diabetes Care 2015, doi: 10.2337/dc15 0249.
- [18] Matsuhisa M, Koyama M, Cheng X, et al. New insulin glargine 300 U/ml: glycaemic control and hypoglycaemia in Japanese people with type 1 diabetes mellitus (EDITION JP1). Abstracts of the 50th EASD Annual Meeting. Diabetologia. 2014; 57 (Suppl.): P975.
- [19] Terauchi Y, Koyama M, Cheng X, et al. Glycaemic control and hypoglycaemia in Japanese people with type 2 diabetes mellitus receiving new insulin glargine 300 U/ml in combination with OADs (EDITION JP2). Abstracts of the 50th EASD Annual Meeting. Diabetologia 2014; 57 (Suppl.): P976.
- [20] Holman RR, Farmer AJ, Davies MJ, et al. Three year efficacy of complex insulin regimens in type 2 diabetes. N Engl J Med 2009; 361: 1736–1747.
- [21] Crye PE. Hypoglycemia is the limiting factor in the management of diabetes. Diabetes Metab Res 1999; 15: 42–46.