Dermatitis herpetiformis Duhring u pacienta s psoriázou léčeného ustekinumabem
Souhrn:
Psoriáza je chronické zánětlivé onemocnění postihující kolem 2–4 % středoevropské populace. Choroba neohrožuje život pacienta přímo, má však nesporný vliv na fyzické, sociální a psychické aspekty života. V současné době již víme, že lupénka není omezena pouze na kožní povrch, ale je rovněž spojena s řadou komorbidit, jakými jsou psoriatická artritida (přibližně u 25 %), Crohnova choroba, ulcerózní kolitida, Bechtěrevova choroba a zejména nemoci tzv. metabolického syndromu, jako je např. diabetes mellitus 2. typu, arteriální hypertenze nebo dyslipidemie. Popsán je i častější výskyt celiakie, většinou bez kožního postižení. Zde popisujeme případ pacienta s psoriázou a dermatitis herpetiformis Duhring léčeného dlouhodobě kombinací ustekinumabu a sulfonů.
Key words:
psoriasis – ustekinumab – dermatitis herpetiformis Duhring.
Summary:
Psoriasis is a chronic inflammatory disease affecting about 2–4% of the Central European population. The disease does not threaten the patient’s life directly, but it has an undeniable impact on the physical, social, and psychological aspects of life. Nowadays, we know that psoriasis is not limited to skin surface, but is also associated with many comorbidities such as psoriatic arthritis (approximately 25%), Crohn’s disease, ulcerative colitis, Bechterew’s disease, and – in particular – diseases of the so called metabolic syndrome, such as type 2 diabetes mellitus, arterial hypertension or dyslipidemia. Increased incidence of celiac disease is also mentioned in literature, often without the skin lesions. Here we describe a patient with psoriasis and dermatitis herpetiformis Duhring undergoing long term treatment with combination of ustekinumab and sulfones.
Úvod
Psoriáza je chronické zánětlivé onemocnění postihující kolem 2–4 % středoevropské populace. I když přesná etiologie není dosud známa, předpokládá se genetický podklad onemocnění, kdy u predisponovaných jedinců dojde ke spuštění patogenetických pochodů, ve kterých mají zásadní roli T‑lymfocyty [1]. Choroba neohrožuje život pacienta přímo, avšak má nesporný vliv na fyzické, sociální a psychické aspekty života [2]. Dle současného hodnocení jsou pacienti se středně těžkou až těžkou psoriázou řazeni na druhé místo v žebříčku negativního dopadu chorob na kvalitu života – ihned za depresí – a jejich postižení je srovnatelné s jinými závažnými onemocněními (revmatoidní artritida, malignity, choroby srdce) [3].
V současné době již víme, že lupénka není omezena pouze na kožní povrch, ale je rovněž spojena s řadou komorbidit, jakými jsou psoriatická artritida (přibližně u 25 %), Crohnova choroba, ulcerózní kolitida, Bechtěrevova choroba a zejména nemoci tzv. metabolického syndromu, jako je např. diabetes mellitus 2. typu, arteriální hypertenze nebo dyslipidemie, což může snížit délku života psoriatika o 3,5–10 let ve srovnání se zdravou populací [4,5]. V literatuře se dokonce popisuje i častější výskyt celiakie u psoriatických pacientů [6]. Kromě systémových obtíží může způsobit i kožní projevy ve formě dermatitis herpetiformis Duhring, ale koincidence psoriázy a samotné morbus Duhring je vzácná [7]. Při výskytu jakékoliv komorbidity je pak výzvou pro ošetřujícího lékaře, jakou léčbu zvolit, aby dosáhl pokud možno remise obou onemocnění.
Kasuistika
Muž, 48let, s anamnézou psoriasis vulgaris je sledován na našem oddělení od roku 2006, kdy k nám byl předán k zahájení biologické léčby. Kromě psoriázy trpěl arteriální hypertenzí (léčena dvojkombinací antihypertenziv), hyperlipidemií (léčena statinem), hyperurikemií (léčena allopurinolem) a nealkoholickou jaterní steatózou. Kouřil 10 cigaret denně. Rodinná anamnéza týkající se lupénky a dalších kožních onemocnění byla negativní.
 V předchozím období byl pacient léčen methotrexatem a fototerapií UVB‑311 nm; podávání ciclosporinu bylo kontraindikováno pro hypertenzi a acitretin nemohl užívat z důvodu hyperlipidemie. Biologická léčba byla zahájena efalizumabem, který již není na našem farmaceutickém trhu k dispozici, a pokračovala 12 měsíců. Z důvodu ztráty odpovědi na terapii byla léčba efalizumabem změněna na etanercept, který vykazoval dobrou účinnost po dobu 2,5 roku. Po selhání i této terapie byla léčba změněna – pacientovi byl podáván adalimumab následujících 1,5 roku.
V předchozím období byl pacient léčen methotrexatem a fototerapií UVB‑311 nm; podávání ciclosporinu bylo kontraindikováno pro hypertenzi a acitretin nemohl užívat z důvodu hyperlipidemie. Biologická léčba byla zahájena efalizumabem, který již není na našem farmaceutickém trhu k dispozici, a pokračovala 12 měsíců. Z důvodu ztráty odpovědi na terapii byla léčba efalizumabem změněna na etanercept, který vykazoval dobrou účinnost po dobu 2,5 roku. Po selhání i této terapie byla léčba změněna – pacientovi byl podáván adalimumab následujících 1,5 roku.
Po selhání i adalimumabu, jakožto druhého přípravku anti‑TNFα, jsme se rozhodli změnit léčbu na jinou skupinu biologik, než jsou léčiva blokující TNFα, a začít podávat ustekinumab – monoklonální protilátku proti interleukinu (IL) 12/23.
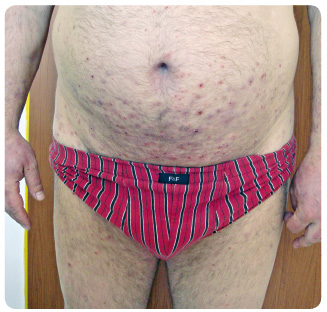
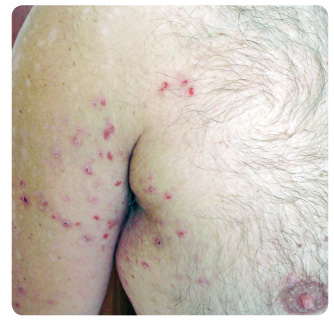
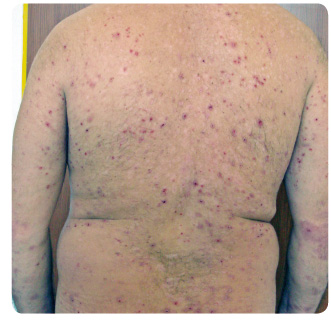
Léčba ustekinumabem byla zahájena dávkou 90 mg, protože tělesná hmotnost pacienta byla vyšší než 100 kg (108 kg), v klasickém schématu, tedy druhá aplikace po čtyřech týdnech a poté každých 12 týdnů. Před léčbou bylo skóre PASI (Psoriasis Area and Severity Index) 25 a hodnocení PGA (Physician Global Assessment) se rovnalo 3. Po čtyřech týdnech od první injekce se PASI snížilo na 2,6 a PGA na hodnotu 1. Byla podána druhá 90mg dávka ustekinumabu. Tři týdny po aplikaci byl pacient vyšetřen na naší klinice pro velmi svědivou vyrážku na krku, ve spodní části břicha, v axilách, na zádech, hýždích a na dolních končetinách s maximem pruritu v průběhu dne. Dominovaly mnohočetné exkoriované projevy (obr. 1 , 2, 3). V diferenciální diagnóze jsme uvažovali o scabies a eventuálně o dermatitis herpetiformis Duhring, proto jsme provedli probatorní excizi na histologické vyšetření včetně přímé imunofluorescence. Než byly k dispozici výsledky biopsie, zvolili jsme pro jistotu léčbu permethrinem, která však zůstala bez efektu. Přímá imunofluorescence potvrdila diagnózu dermatitis herpetiformis Duhring.
Pacient neměl žádné gastrointestinální potíže. Sérová koncentrace imunoglobulinu IgA byla normální, protilátky proti endomysiu a tkáňové transglutamináze byly negativní. Nechtěli jsme přerušit terapii ustekinumabem vzhledem k výborné účinnosti na psoriázu, 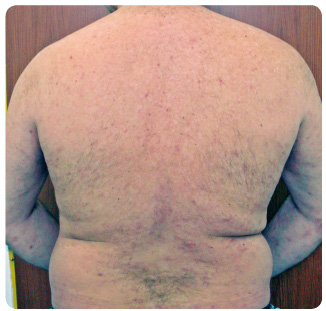 a proto jsme začali s terapií dapsonem v dávce 50 mg/den a s bezlepkovou dietou. Po dvou měsících léčby došlo k výraznému zlepšení stavu pacienta a dávka byla snížena na 25 mg denně (obr. 4). Kombinovaná léčba ustekinumabem a dapsonem pokračuje již po dobu 48 měsíců, dapson je podáván v udržovací dávce 25 mg/den. Funkce ledvin a jater, krevní obraz a hodnoty methemoglobinu jsou v normálním rozmezí, pouze kvůli lehké hemolytické anemii provázející léčbu dapsonem jsme přidali kyselinu listovou v dávce 10 mg denně. Pacient je nyní déle než čtyři roky léčen u
a proto jsme začali s terapií dapsonem v dávce 50 mg/den a s bezlepkovou dietou. Po dvou měsících léčby došlo k výraznému zlepšení stavu pacienta a dávka byla snížena na 25 mg denně (obr. 4). Kombinovaná léčba ustekinumabem a dapsonem pokračuje již po dobu 48 měsíců, dapson je podáván v udržovací dávce 25 mg/den. Funkce ledvin a jater, krevní obraz a hodnoty methemoglobinu jsou v normálním rozmezí, pouze kvůli lehké hemolytické anemii provázející léčbu dapsonem jsme přidali kyselinu listovou v dávce 10 mg denně. Pacient je nyní déle než čtyři roky léčen u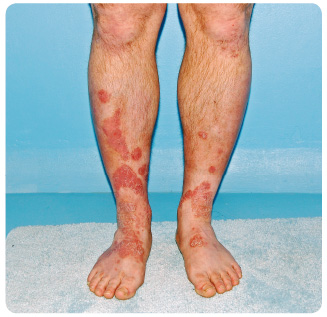 stekinumabem s velmi dobrou účinností na psoriázu, zpravidla asi 7–10 dní před další aplikací dochází k mírnému zhoršování psoriázy, které ale po další aplikaci ihned vymizí (obr. 5). Dapson je podáván i nadále, také s dobrým účinkem, pacient ale vzhledem ke své profesi (elektrotechnik pracující zejména v terénu – ranní i noční služby) není schopen stoprocentně dodržovat bezlepkovou dietu, a proto občas dochází k mírnému výsevu projevů m. Duhring.
stekinumabem s velmi dobrou účinností na psoriázu, zpravidla asi 7–10 dní před další aplikací dochází k mírnému zhoršování psoriázy, které ale po další aplikaci ihned vymizí (obr. 5). Dapson je podáván i nadále, také s dobrým účinkem, pacient ale vzhledem ke své profesi (elektrotechnik pracující zejména v terénu – ranní i noční služby) není schopen stoprocentně dodržovat bezlepkovou dietu, a proto občas dochází k mírnému výsevu projevů m. Duhring.
Závěr
Koexistence psoriasis vulgaris a celiakie je popsána v literatuře. Cianci se spolupracovníky popsal u dermatitis herpetiformis, psoriázy, a psoriatické artritidy související genetické predispozice v patogenezi těchto chorob [8]. Na druhé straně, spojení s dermatitis herpetiformis je velmi vzácné a ve světové literatuře se nachází pouze jednotlivé kasuistiky. Většina z těchto pacientů byla léčena pouze bezlepkovou dietou [7]; to u našeho pacienta nebylo možné, protože nedokázal bezvýhradně udržet dietu vzhledem k povaze svého povolání. Žádný z pacientů, u nichž se onemocnění vyskytla společně, nebyl léčen biologickou léčbou, a ani nejsou dostupné informace o kombinaci biologické terapie a sulfonů.
Našemu pacientovi je aplikován ustekinumab v kombinaci s dapsonem již několik let bez vzniku jakýchkoliv nežádoucích účinků. Jeho psoriáza a dermatitis herpetiformis Duhring zůstávají pod kontrolou. Na uvážení je otázka, zda ustekinumab mohl vyvolat konkomitantní morbus Duhring. Myslíme si, že spíše ne, protože činnost neutrofilů by tímto léčivem neměla být ovlivněna, a ani jiné případy nejsou hlášeny. Ustekinumab u našeho pacienta má velmi dobré dlouhodobé výsledky, a proto jsme neuvažovali o přerušení této léčby, navíc v minulosti byl pacient léčen několika přípravky anti‑TNFα a účinnost byla vždy jen přechodná.
Počet pacientů léčených dlouhodobě biologickou léčbou stoupá, a proto i v budoucnosti můžeme očekávat, že budeme muset řešit podobné situace jako u našeho pacienta, které nejsou popsány v literatuře a mohou vyžadovat kombinaci biologických léků s jinými imunomodulačními přípravky.
Seznam použité literatury
- [1] Nestle FO, Kaplan DH, Barker J. Psoriasis. N Engl J Med 2009; 361: 496–509.
- [2] Gkalpakiotis S, Arenberger P, Adenubiová E. Psychosociální aspekty života pacientů s psoriázou v České republice. Čes slov Derm 2013; 4: 189–196.
- [3] Schmitt JM, Ford DE. Role of depression in quality of life for patients with psoriasis. Dermatology 2007; 215: 17–27.
- [4] Christophers E. Comorbidities in psoriasis. J Eur Acad Dermatol Venereol 2006; 20: 52–55.
- [5] Cohen AD, Dreiher J, Birkenfeld S. Psoriasis associated with ulcerative colitis and Crohn‘s disease. J Eur Acad Dermatol Venereol 2009; 23: 561–565.
- [6] Nagui N, El Nabarawy E, Mahgoub D, et al. Estimation of (IgA) anti gliadin, anti endomysium and tissue transglutaminase in the serum of patients with psoriasis. Clin Exp Dermatol 2011; 36: 302–304.
- [7] Agusti Mejias A, Messeguer F, García Ruiz R, et al. Concomitant dermatitis herpetiformis and plaque psoriasis: possible skin manifestations of celiac disease. Actas Dermosifiliogr 2011; 102: 471–473.
- [8] Cianci R, Giambra V, Mattioli C, et al. Increased frequency of Ig heavy chain HS1,2 A enhancer *2 allele in dermatitis herpetiformis, plaque psoriasis, and psoriatic arthritis. J Invest Dermatol 2008; 128: 1920–1924.