Durvalumab jako adjuvantní léčba po úspěšné konkomitantní chemoradioterapii nemalobuněčného karcinomu plic
Souhrn:
Krákorová G, Důrová J, Šindelářová B, Baxa J. Durvalumab jako adjuvantní léčba po úspěšné konkomitantní chemoradioterapii nemalobuněčného karcinomu plic. Remedia 2021; 31: 241–244.
Karcinom plic patří na čelná místa mezi zhoubnými nádory s ohledem na incidenci i mortalitu. Většina nemocných s karcinomem plic se dostaví k lékaři už s lokálně pokročilým či metastazujícím onemocněním, ve stadiu III−IV. U nemocných s neresekabilním stadiem III je standardem léčby konkomitantní chemoradioterapie. I přes radikální léčebný záměr většina nemocných za méně než 12 měsíců progreduje. Imunoterapie durvalumabem jako první přinesla v rámci adjuvantní léčby po úspěšné chemoradioterapii prospěch. Durvalumab je indikován po úspěšné konkomitantní chemoradioterapii, při expresi ligandu receptoru programované buněčné smrti 1 (PD‑L1) ≥ 1 %. Léčba musí být zahájena do 42 dnů od ukončené chemoradioterapie. Dále autoři předkládají kazuistiku nemocného léčeného adjuvantní imunoterapií s durvalumabem.
Summary:
Krakorova G, Durova J, Sindelarova B, Baxa J. Durvalumab as an adjunct therapy after successful concomitant chemotherapy of non‑small cell lung cancer. Remedia 2021; 31: 241–244.
Lung cancer belongs to the top among malignant tumors with respect to incidence and mortality. Majority of patients with lung cancer visit their physician with already locally advanced or metastasized disease of stage III‑IV. In patients with non‑resectable stage III, concomitant chemotherapy is the standard approach. Despite radical treatment intention, most patients progress within less than 12 months. Immunotherapy with durvalumab brought benefit as first in the context of adjuvant therapy after successful chemotherapy. Durvalumab is indicated after successful concomitant chemotherapy when the expression of programmed cell death receptor ligand 1 (PD‑L1) is ≥ 1%. The treatment must be initiated within 42 days after the chemotherapy is finished. Furthermore, authors present a case study of a patient treated with adjuvant immunotherapy with durvalumab.
Key words: non‑small cell lung cancer, chemoradiotherapy, immunotherapy, durvalumab, adjuvant therapy
Úvod
Karcinom plic patří na přední místa mezi zhoubnými nádory s ohledem na incidenci i mortalitu. Ročně diagnostikujeme v České republice kolem 6 500 nových případů karcinomu plic. Tři čtvrtiny případů představují nemalobuněčné karcinomy plic (non small cell lung carcinoma, NSCLC) [1]. Resekabilita karcinomu plic je nízká, pohybuje se kolem 10−20 %. Většina nemocných se dostaví k lékaři už s lokálně pokročilým či metastazujícím onemocněním, ve stadiu III−IV. U nemocných s neresekabilním stadiem III je standardem léčby konkomitantní chemoradioterapie (concomitant chemoradiotherapy, CChRT) [2].
Kromě stagingu a morfologie potřebujeme u nemocných zvažovaných k systémové léčbě NSCLC znát expresi ligandu receptoru programované buněčné smrti 1 (programmed death ligand 1, PD L1) a u neskvamózních karcinomů ještě vyšetření genetické (ke zjištění přítomnosti mutací EGFR, ALK, ROS, ev. BRAF). Ke stanovení exprese PD L1 je potřeba přítomnosti alespoň 100 buněk, to však není cytologie schopna zajistit. Nesmíme tedy zapomínat, že u každého pacienta s NSCLC s plánovanou systémovou léčbou (chemoterapie, imunoterapie, biologicky cílená léčba) či s kombinovanou léčbou musí být získán materiál na histologické vyšetření tumoru (vzorek tumoru či cytoblok), aby bylo možné příslušná vyšetření provést.
Pětileté přežití nemocných s NSCLC stadia III je poměrně nízké, pohybuje se v závislosti na stadiu (IIIA−IIIC) v rozmezí 13−36 % [3]. Přibližně 30 % nemocných stadia IIIA a IIIB je neresekabilních [3]; novější práce hovoří až o 30−50 % případů stadia III [4]. I přes radikální léčebný záměr chemoradioterapie je medián přežití bez progrese kratší než jeden rok a u devíti z 10 pacientů (90 %) s neresekabilním NSCLC stadia III dojde k progresi, většinou na metastazující onemocnění [5,6].
Durvalumab po chemoradioterapii
s prospěchem přežití
Po více než 10 letech zkoumání nových postupů v léčbě neresekabilního stadia III NSCLC je durvalumab prvním lékem, který přinesl jednoznačný prospěch u nemocných léčených CChRT. Ostatní přístupy ve snaze o vylepšení výsledků CChRT selhaly. Efekt na přežití neměla přidaná indukční léčba ani adjuvantní léčba chemoterapií, biologicky cílená léčba, potenciace radioterapie cetuximabem či snaha o navýšení dávky radioterapie nebo profylaktické ozáření mozku po CChRT [7]. První studií, která zkoumala efekt konsolidační léčby imunoterapií a doložila její efekt, je studie PACIFIC s adjuvantním durvalumabem.
Studie PACIFIC s adjuvantním
durvalumabem
Jedná se o randomizovanou, placebem kontrolovanou studii fáze III u nemocných, u nichž byl zaznamenán efekt předchozí chemoradioterapie podané minimálně ve dvou cyklech. Primárními cílovými ukazateli studie byly přežití bez progrese (progression free survival, PFS) a celkové přežití (overall survival, OS), sekundární cílové ukazatele zahrnovaly míru objektivní odpovědi (response rate, RR), vyhodnocení toxicity a hodnocení pacientem.
Konsolidace durvalumabem byla spojena s prodloužením mediánu PFS z 5,6 na 16,8 měsíce a času do vzniku metastáz nebo úmrtí z 14,6 na 23,2 měsíce [8]. Novější data ukázala ve skupině s durvalumabem zlepšení PFS na 17,2 měsíce (stratifikovaný poměr rizik [hazard ratio, HR] pro progresi nebo úmrtí 0,51; 95% interval spolehlivosti [confidence interval, CI] 0,41–0,63) a intervalu do metastáz či úmrtí z 16,2 měsíce v placebové skupině na 28,3 měsíce (stratifikovaný HR 0,53; 95% CI 0,41−0,68) [9]. Celková léčebná odpověď (overall response rate, ORR) ve skupině s durvalumabem činila 30 % (95% CI 25,8−34,5), ve skupině s placebem 17,8 % (95% CI 13,0–23,6; p < 0,001). Mediánu trvání odpovědi ve skupině s durvalumabem nebylo dosaženo (95% CI 27,4−NR) a v placebové skupině činil 18,4 měsíce (95% CI 6,7–24,5). Profil bezpečnosti byl srovnatelný − viz dále Nežádoucí účinky durvalumabu po CChRT.
Vhodnost podání durvalumabu
Durvalumab by měl tedy být podáván vždy, pokud je to možné. Podle úhradových podmínek v ČR musí mít nemocný pozitivní expresi PD L1 v tumoru ≥ 1 % a musí být doložen efekt CChRT minimálně ve smyslu stabilizace (pomocí výpočetní tomografie [CT], ev. pozitronové emisní tomografie [PET]/CT po ukončení léčby). Durvalumab se podává do progrese onemocnění nebo do výskytu nepřijatelné toxicity nebo maximálně 12 měsíců. Aplikuje se dávka 10 mg na 1 kg tělesné hmotnosti, podává se každých 14 dní jako intravenózní infuze po dobu 60 minut nebo jako fixní dávka 1 500 mg každé čtyři týdny.
Kdy nelze durvalumab indikovat
Jak už bylo řečeno, durvalumab nelze indikovat u negativních expresorů PD L1 a také tehdy, pokud jsou kontraindikace léčby imunoterapií – jestliže je pacient dlouhodobě léčen systémovými kortikosteroidy v dávce prednisonu nad 10 mg denně (či odpovídajícím ekvivalentem) nebo jinou imunosupresivní léčbou, má li diagnostikováno závažné aktivní systémové autoimunitní onemocnění a významné postižení plicního intersticia.
Omezení indikace na komplexní
onkologická centra
Léčba durvalumabem po definitivní CChRT je omezena na komplexní onkologická centra (KOC). Je vhodné, aby nemocný vždy při stanovení diagnózy prošel KOC z důvodu nastavení ideální léčby pro daného nemocného v rámci multidisciplinárního týmu. Důležitá je nejen správná volba, ale i kvalita diagnostiky a kvalita provedení léčby – jak chemoterapie, tak především radioterapie. Pokud nemocný iniciálně KOC neprošel, měl by do něj být odeslán bezprostředně po skončení CChRT a potvrzení efektu této léčby prostřednictvím zobrazovacích metod a s pozitivním výsledkem exprese PD L1 (doloženým příslušnou laboratoří).
Význam včasného zahájení léčby
Léčba durvalumabem by měla být po úspěšné CChRT zahájena co nejdříve. Ideální je ihned po skončení chemoradioterapie indikovat provedení radiografických vyšetření (CT nebo PET/CT) a při potvrzeném efektu léčby, minimálně pod obrazem stabilizace, terapii durvalumabem zahájit. Dle výsledků studie PACIFIC je okamžik zahájení léčby durvalumabem naprosto zásadní. Čím dříve se s aplikací léku začalo, tím byly výsledky lepší. Interval od ukončení CChRT do začátku léčby durvalumabem by neměl přesáhnout 42 dní.
Nežádoucí účinky durvalumabu
po CChRT
Durvalumab má spektrum nežádoucích účinků obdobné spektru těchto příhod u jiných imunoterapeutik, která patří do skupiny inhibitorů kontrolních bodů imunitní reakce. Jedná se o projevy snížené tolerance vlastních tkání (obdobně jako u autoimunitních onemocnění) – nejčastěji to bývá pneumonitida, kolitida, nefritida či renální dysfunkce, endokrinopatie či kožní projevy (vyrážka atd.). Nežádoucí účinky mohou mít ale různou podobu, včetně postižení CNS, polyneuropatií, kloubních a svalových postižení atd., a je nutné na možnost i atypických příznaků v souvislosti s imunoterapií myslet. Závažné nežádoucí účinky jsou relativně vzácné, vyskytují se přibližně u 2 % pacientů. Jsou li včas rozpoznány, jsou obvykle dobře zvládnutelné kortikosteroidní léčbou. Při podávání durvalumabu po CChRT panovala – vzhledem k léčbě imunoterapií po radioterapii plic – vstupně obava zejména z výskytu pneumonitid. Nežádoucí účinek stupně 3 a 4 byl zaznamenán ve skupině s durvalumabem u 30,5 % pacientů, ve skupině s placebem u 26,1 % pacientů. Překvapivě nebyl zjištěn ani výrazně vyšší podíl pneumonitid vedoucích k ukončení léčby; 4,8 % ve skupině s durvalumabem a 2,6 % ve skupině s placebem.
Kazuistika
Kazuistika se týká nemocného
léčeného na plicní klinice Fakultní nemocnice v Plzni.
U pacienta ve věku 57 let byl v únoru 2020
(obr. 1, 2A–D) diagnostikován lokálně
pokročilý plicní adenokarcinom, rozsahu a stadia T4N2M0,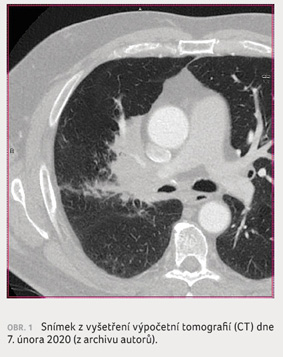 stupně IIIA, s postižením distální části pravého
hlavního bronchu a kmene plicnice. Onemocnění bylo
neřešitelné radikální resekcí pro víceetážové postižení
stupně IIIA, s postižením distální části pravého
hlavního bronchu a kmene plicnice. Onemocnění bylo
neřešitelné radikální resekcí pro víceetážové postižení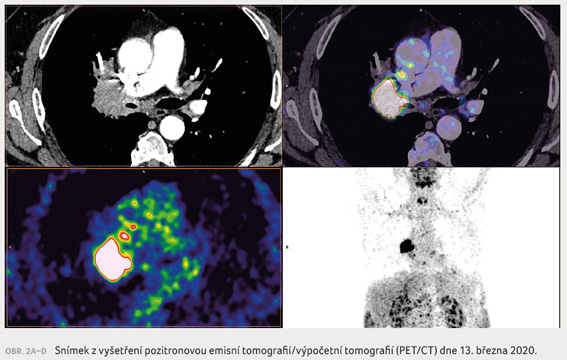 mediastinálních uzlin. Exprese PD L1 byla pozitivní v 60 %
nádorových buněk, mutace ALK a ROS byly negativní. Mutace
receptoru epidermálního růstového faktoru (EGFR) nebylo možno
stanovit pro nedostatek materiálu. Pacient podstoupil radikální
CChRT; chemoterapii ve složení vinorelbin, cisplatina (schéma
dle Zatloukala [10]) na Klinice pneumologie a ftizeologie
v Plzni, souběžně s radioterapií tumoru pravé plíce,
pravého hilu plicního a mediastinální lymfadenopatie
(skupina 4 a 7) v dávce 66 Gy – léčba probíhala
do července 2020 na Onkologické a radioterapeutické
klinice FN Plzeň. Bezprostředně po ukončení ozáření bylo
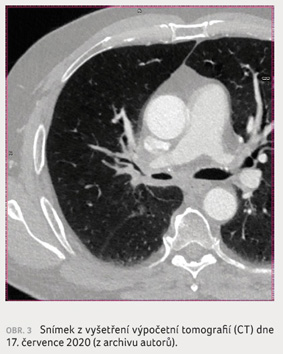
indikováno kontrolní CT hrudníku, které prokázalo parciální
remisi onemocnění (obr. 3). Následovalo adjuvantní
podávání durvalumabu. K datu 15. dubna 2021 nemocný
absolvoval 13 sérií podání durvalumabu v dávce 10 mg/kg
mediastinálních uzlin. Exprese PD L1 byla pozitivní v 60 %
nádorových buněk, mutace ALK a ROS byly negativní. Mutace
receptoru epidermálního růstového faktoru (EGFR) nebylo možno
stanovit pro nedostatek materiálu. Pacient podstoupil radikální
CChRT; chemoterapii ve složení vinorelbin, cisplatina (schéma
dle Zatloukala [10]) na Klinice pneumologie a ftizeologie
v Plzni, souběžně s radioterapií tumoru pravé plíce,
pravého hilu plicního a mediastinální lymfadenopatie
(skupina 4 a 7) v dávce 66 Gy – léčba probíhala
do července 2020 na Onkologické a radioterapeutické
klinice FN Plzeň. Bezprostředně po ukončení ozáření bylo
indikováno kontrolní CT hrudníku, které prokázalo parciální
remisi onemocnění (obr. 3). Následovalo adjuvantní
podávání durvalumabu. K datu 15. dubna 2021 nemocný
absolvoval 13 sérií podání durvalumabu v dávce 10 mg/kg
 každých 14 dní. Léčbu snáší dobře, bez projevů nežádoucích
účinků, bez známek relapsu onemocnění. Dle kontrolního CT
z března 2021 (obr. 4) trvá parciální remise
onemocnění a je přítomna jeho další mírná regrese. Jako
vedlejší nález byla zachycena trombóza břišní aorty v oblasti
subrenální, která omezuje průsvit o 35 %, a je
plánováno vyšetření cévním chirurgem. Pacient má dobrou
kvalitu života, zvládá lehkou práci, je aktivní.
každých 14 dní. Léčbu snáší dobře, bez projevů nežádoucích
účinků, bez známek relapsu onemocnění. Dle kontrolního CT
z března 2021 (obr. 4) trvá parciální remise
onemocnění a je přítomna jeho další mírná regrese. Jako
vedlejší nález byla zachycena trombóza břišní aorty v oblasti
subrenální, která omezuje průsvit o 35 %, a je
plánováno vyšetření cévním chirurgem. Pacient má dobrou
kvalitu života, zvládá lehkou práci, je aktivní.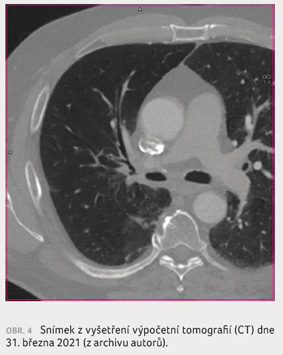
Závěr
Adjuvantní léčba durvalumabem po úspěšné konkomitantní chemoradioterapii je pro nemocné s nemalobuněčným karcinomem plic šancí na déletrvající přežití bez progrese a prodloužení celkového přežití. Je důležité již před vlastním zahájením léčby chemoterapií a zářením myslet na to, že pro indikaci durvalumabu musíme mít expresi PD L1 ≥ 1 %, a tudíž je nutné poslat bioptický vzorek na toto vyšetření. Durvalumab po chemoradioterapii by měl být indikován vždy, pokud je to možné, do 42 dnů od ukončení ozáření.
Seznam použité literatury
- [1] https://www.svod.cz/report.php?diag=C34. Navštíveno dne 13. 4. 2021.
- [2] Aupérin A, Le Péchoux C, Rolland E, et al. Meta‑analysis of concomitant versus sequential radiochemotherapy in locally advanced non‑small cell lung cancer. J Clin Oncol 2010; 28: 2181–2190.
- [3] Scorsetti M, Navarria P, Mancosu P, et al. Large volume unresectable locally advanced non‑small cell lung cancer: acute toxicity and initial outcome results with rapid arc. Radiat Oncol 2010; 5: 94.
- [4] Yoon SM, Shaikh T, Hallman M. Therapeutic management options for stage III non‑small cell lung cancer. World J Clin Oncol 2017; 8: 1–20.
- [5] Albain KS, Swann RS, Rusch VW, et al. Radiotherapy plus chemotherapy with or without surgical resection for stage III non‑small‑cell lung cancer: a phase III randomised controlled trial. Lancet 2009; 374: 379−386.
- [6] Bradley JD, Paulus R, Komaki R, et al. Standard‑dose versus high‑dose conformal radiotherapy with concurrent and consolidation carboplatin plus paclitaxel with or without cetuximab for patients with stage IIIA or IIIB non‑small‑cell lung cancer (RTOG 0617): a randomised, two‑by‑two factorial phase 3 study. Lancet Oncol 2015; 16: 187−199.
- [7] Krákorová G, Steinbergerová H, Pešek M, et al. Imunoterapie a radioterapie u lokálně pokročilého (metastazujícího) nemalobuněčného karcinomu plic. Onkologická revue 2020; 7 (1 Spec. vyd.): 25–30.
- [8] Antonia SJ, Villegas A, Daniel D, et al. Durvalumab after chemoradiotherapy in stage III non‑small‑cell lung cancer. N Engl J Med 2017; 377: 1919–1929.
- [9] Antonia SJ, Villegas A, Daniel D, et al. Overall survival with durvalumab after chemoradiotherapy in stage III NSCLC. N Engl J Med 2018; 379: 2342–2350.
- [10] Zatloukal P, Petruzelka L, Zemanova M, et al. Concurrent versus sequential chemoradiotherapy with cisplatin and vinorelbine in locally advanced non‑small cell lung cancer: a randomized study. Lung Cancer 2004; 46: 87−98.