Jak zlepšit péči o pacienty s revmatoidní artritidou
Souhrn:
Pavelka K. Jak zlepšit péči o pacienty s revmatoidní artritidou. Remedia 2020; 30: 33–38.
Ve vybraných evropských státech byla provedena multicentrická studie s cílem zmapovat poskytování péče o pacienty s revmatoidní artritidou (RA) a s komorbiditami. Skupina 18 kliniků, z nichž 12 bylo revmatologů, vybrala 12 specializovaných center v zemích Evropské unie a ve Švýcarsku. Výzkum byl realizován ve třech krocích, které zahrnuly literární rešerši vyhodnocující problematiku na základě tzv. evidence based practice. Dále se uskutečnila návštěva 12 center, v nichž bylo provedeno 180 interview a pozvaným zdravotnickým pracovníkům byly kladeny otázky o způsobech klinické praxe při léčbě pacientů s RA. V posledním kroku následovalo setkání expertů (revmatologů, specialistů na komorbidity, sestry a pacienta) nad získanými výsledky a diskuse o prioritách i nedostatcích, příprava abstrakt a rukopisu. Výsledky studie ukazují značnou heterogenitu při přístupu k pacientům s komorbiditami v různých fázích RA. Účastníci se také domnívají, že by byla vhodná další publikace s doporučeními pro péči o pacienty s RA a s komorbiditami.
Summary:
Pavelka K. How to improve the care for patients with rheumatoid arthritis. Remedia 2020; 30: 33–38.
A multicentric study has been performed in selected European countries aiming to map the provision of care for patients with rheumatoid arthritis with comorbidities. A group of 18 clinical physicians of which 12 were rheumatologists chose 12 specialized centers in countries of the European Union and Switzerland. The research was performed in three steps that included a literature review evaluating the problematics using so called evidence‑based practice. Furthermore, all 12 centers were visited, and 180 interviews were performed. Invited medical professionals were asked questions about the approaches to clinical practice regarding the treatment of patients with rheumatoid arthritis. In the last step, an expert panel was gathered (rheumatologists, specialists for comorbidities, nurses and patients) where acquired results were reviewed and priorities and disadvantages were discussed together with the preparation of abstracts and the review. The results of the study show significant heterogeneity in the approach to patients with comorbidities at different stages of rheumatoid arthritis. Participants also believe that more publications with recommendations regarding the care for patients with rheumatoid arthritis with comorbidities is needed.
Key words: rheumatoid arthritis, therapy, comorbidities
Úvod
Revmatoidní artritida (RA) je
chronické zánětlivé autoimunitní onemocnění, které postihuje
až 1 % populace. Choroba vyvolává u svých nositelů
značnou disabilitu, zhoršení kvality života a zvyšuje
rovněž mortalitu, neboť zkracuje život pacientů o 7‒10
let [1]. Při léčbě RA došlo v posledních 20 letech
k revolučním změnám, které umožnily mnohem účinněji
potlačit zánětlivou aktivitu a tím i postupující
destrukce (obr. 1)
[2,3]. Mezi nejvýznamnější faktory, které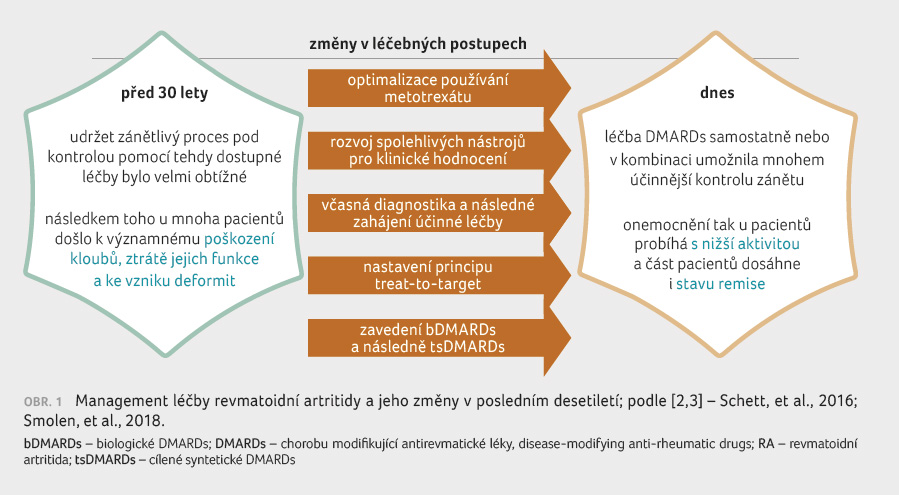 zlepšily osud
nemocných s RA, řadíme: racionálnější používání
metotrexátu, zavedení biologických, biosimilárních a později
i cílených syntetických chorobu modifikujících
antirevmatických léků (disease modifying anti rheumatic
drugs, DMARDs), nová kritéria pro časnou diagnostiku, zavedení
principů léčby k cíli (treat to target, T2T) ‒
obrázek 2 ‒
a vytvoření a validizace ukazatelů aktivity nemoci
i odpovědi na léčbu [4]. Cílem léčby každé RA by
mělo být navození remise, nebo alespoň stavu nízké aktivity
nemoci [5]. Důvody, proč máme usilovat o dosažení remise,
jsou následující: zlepšení kvality života, zlepšení fyzických
funkcí, zlepšení produktivity práce, snížení nutnosti
ortopedických operací a snížení výskytu kardiovaskulárních
komplikací.
zlepšily osud
nemocných s RA, řadíme: racionálnější používání
metotrexátu, zavedení biologických, biosimilárních a později
i cílených syntetických chorobu modifikujících
antirevmatických léků (disease modifying anti rheumatic
drugs, DMARDs), nová kritéria pro časnou diagnostiku, zavedení
principů léčby k cíli (treat to target, T2T) ‒
obrázek 2 ‒
a vytvoření a validizace ukazatelů aktivity nemoci
i odpovědi na léčbu [4]. Cílem léčby každé RA by
mělo být navození remise, nebo alespoň stavu nízké aktivity
nemoci [5]. Důvody, proč máme usilovat o dosažení remise,
jsou následující: zlepšení kvality života, zlepšení fyzických
funkcí, zlepšení produktivity práce, snížení nutnosti
ortopedických operací a snížení výskytu kardiovaskulárních
komplikací.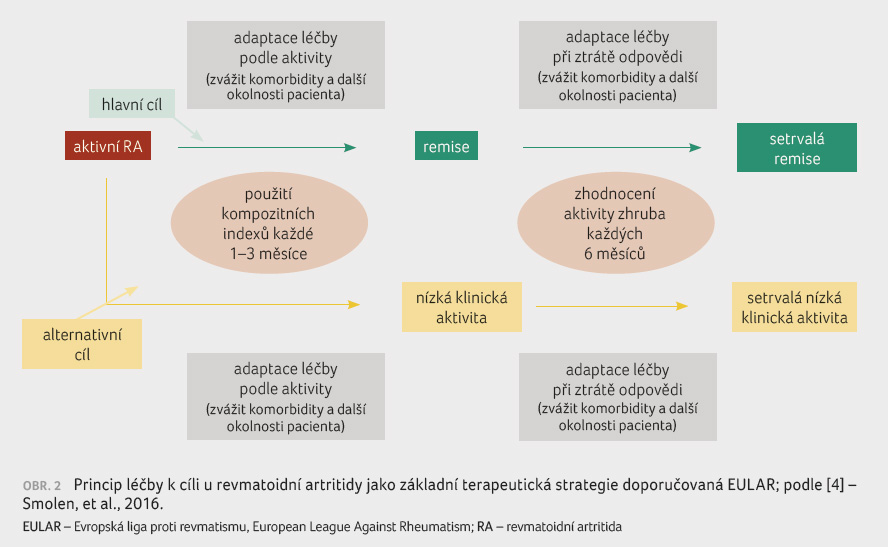
Bohužel je z praxe registrů známé, že žádoucího cíle léčby je dosaženo pouze asi u 40‒60 % pacientů [6], což také odpovídá výsledkům v českém národním registru ATTRA (nepublikovaná data u autora). Je však také patrné, že řada pacientů má i při dosažení remise (zvláště při použití mírnějších kritérií remise, jako je DAS28 – Disease Activity Score 28) reziduální obtíže. Například v přehledné práci Ishidy a kol. [7] trpěli pacienti klasifikovaní jako jedinci v remisi velmi často bolestí, ztuhlostí, depresí, zhoršenou schopností pracovat a celkově zhoršenou kvalitou života.
Důležitým faktorem, který komplikuje dosažení výrazného zlepšení kvality života nemocných s RA, je výskyt komorbidit [8]. Pojem komorbidity revmatických onemocnění se začal šířeji používat relativně nedávno. Spektrum onemocnění či příznaků, které se řadí mezi komorbidity, není jednotné. První alternativou je definice, že mezi komorbidity patří onemocnění, jež přímo nesouvisejí s mechanismem choroby, ale vyskytují se u daného revmatického postižení častěji než v běžné populaci, nebo mají závažnější průběh. Řadíme k nim infekce, kardiovaskulární onemocnění, deprese, osteoporózu, nádory, onemocnění ledvin a plicní onemocnění. Druhou alternativou výkladu pojmu komorbidit je, že jde o choroby, které mohou, ale nemusejí souviset se základním onemocněním (příklad: Je akutní přední uveitida u spondyloartritid komorbiditou, nebo součástí vlastního onemocnění?).
O významu komorbidit svědčí i fakt, že Evropská liga proti revmatismu (European League Against Rheumatism, EULAR) publikovala dokument s názvem „Body ke zvážení při hlášení, screeningu a prevenci komorbidit“ [9]. Dokument se především soustřeďuje na screening a prevenci komorbidit, ale již méně na praktické provádění klinické praxe. V jeho rámci bylo vyšetřeno 4 586 pacientů v 17 evropských zemích. Jako nejčastější komorbidity byly zaznamenány deprese (15 %), astma (6,6 %), kardiovaskulární onemocnění (6 %), solidní nádory (4,5 %) a chronické plicní onemocnění (3,5 %).
Cílem studie bylo provést multicentrickou sondu o klinické praxi při léčbě RA s komorbiditami napříč evropskými státy. Nakonec bylo vybráno 11 států Evropské unie a Švýcarsko a v nich zdravotnická zařízení zvolená na základě předem daných kritérií hodnotících ochotu k inovačním metodám. Šlo vesměs o terciární centra a s velkou převahou o univerzitní kliniky.
Metodologie studie
Uvedená studie byla podpořena
společností sanofi aventis. Na základě osobních
vyhodnocení bylo vybráno 18 účastníků, z nich 16 bylo
kliniků, z toho 12 revmatologů, jeden kardiolog, jeden
pneumolog, jeden psycholog a jeden diabetolog, dále jedna
specializovaná sestra a jeden pacient. Studie byla provedena
ve 12 centrech, vždy v jednom v každé zemi (Norsko,
Francie, Česká republika, Španělsko, Velká Británie, Belgie,
Švýcarsko, Portugalsko, Švédsko, Dánsko, Nizozemsko, Itálie).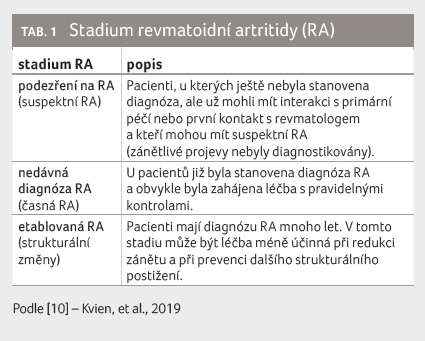
Výzkum probíhal ve třech krocích:
- Literární rešerše vyhodnocující problematiku na základě tzv. evidence based practice.
- Návštěva 12 center, v nichž bylo provedeno 180 interview, pozvaným zdravotnickým pracovníkům byly kladeny otázky o způsobech klinické praxe při léčbě pacientů s RA.
- Diskuse a setkání expertů (revmatologů, specialistů na komorbidity, sestry a pacienta) nad získanými výsledky. Diskuse o prioritách i nedostatcích, příprava abstrakt a rukopisu.
Skupina expertů se na začátku projektu dohodla, že sledovanými komorbiditami v tomto projektu budou kardiovaskulární onemocnění, deprese, plicní onemocnění a diabetes mellitus.
Dále bylo rozhodnuto o hodnocení klinické praxe ve třech stadiích (tab. 1) [10]:
- podezření na RA (suspektní RA),
- časná RA,
- etablovaná RA.
Výsledky
Prostřednictvím studie byla identifikována celá řada problémů v péči o pacienty s RA a s komorbiditami. Dále byly popsány příčiny, které tyto problémy vyvolávají.
Zjištěné problémy v péči
o pacienty zahrnovaly zpoždění ve vyhledání lékařské
péče (více než 12 týdnů), zpoždění v odeslání
k revmatologovi (medián čtyř návštěv u praktického
lékaře před odesláním k revmatologovi), zpoždění
v diagnóze (v některých zemích může být až rok
od začátku symptomů), špatná adherence pacienta k léčbě
(30‒80 %), nedostatky v monitoringu (tab. 2) [10].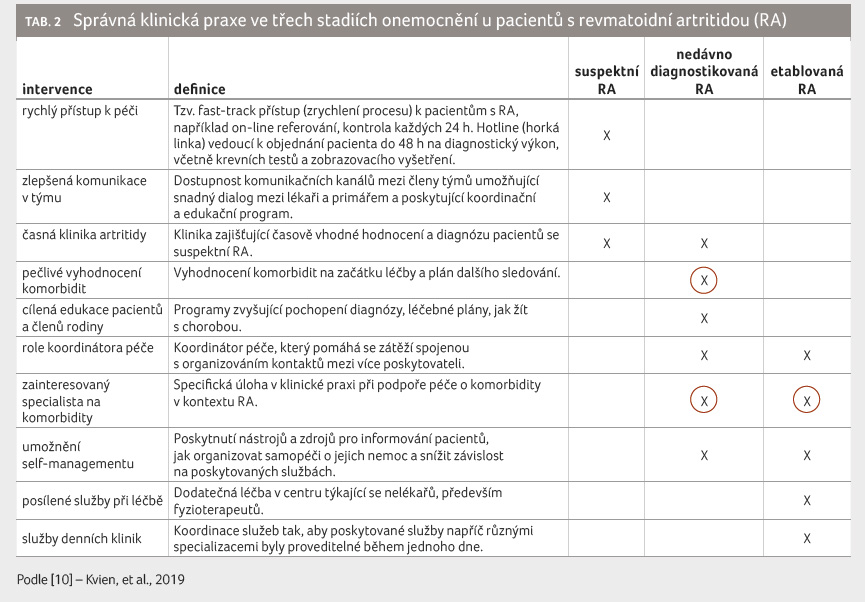
Stadium podezření na revmatoidní artritidu
Na samém počátku stojí neznalost pacientů a nedostatek osvěty, které vedou k pozdnímu vyhledání lékařské péče. Druhou stránkou problému v této časné fázi mohou být nedostatek praktických lékařů, nedostatečné znalosti praktického lékaře o symptomech revmatických chorob, dlouhé čekací doby u specialistů a nedostatečná povědomost praktického lékaře o tom, jak vůbec pacienta odesílat (tab. 3) [9‒17]. Faktem rovněž je, že kloubní ztuhlost a zánět jsou přítomny u celé řady onemocnění.
Je žádoucí, aby diagnóza RA u pacienta byla stanovena co nejdříve a také co nejdříve zahájena léčba, která je nejúčinnější (tzv. koncept window of opportunity). Jedním z možných řešení je zřízení kliniky časné artritidy, kde jsou pacienti vyšetřováni prakticky okamžitě. Problémem je triáž pacientů (třídění podle závažnosti zdravotního stavu), kteří mají reálné podezření na zánětlivé revmatické onemocnění (je známo, že 70‒90 % osob toto podezření nemá, v některých případech může jít také o zneužití této rychlé cesty k vyšetření). Triáž je někdy prováděna lékaři přímo na klinice během orientačního vyšetření, v jiných zařízeních je náplní práce edukované sestry na základě několika strukturovaných otázek (systém podobný jako na emergency). Na jedné španělské klinice se osvědčila oboustranná on line kom

unikace mezi praktickými lékaři a revmatologem. Obecně je kladen důraz na zvýšenou komunikaci s primární péčí ‒ např. slavný Hôpital Cochin v Paříži vyvinul ke zvýšení komunikace s praktiky tzv. Hospital and City Rheumatology Network, jenž zahrnuje mimo jiné tzv. horkou linku mezi praktikem a revmatologem během 48 hodin.
Součástí screeningu suspektní RA by již mělo být alespoň orientační vyšetření na komorbidity, které může být přínosné pro vlastní diagnostiku.
Stadium časné artritidy
Základním problémem je zpoždění v diagnóze, jež může být způsobeno nedostatkem revmatologů nebo dlouhou čekací dobou na první návštěvu revmatologa. Problémem však může být i vlastní diagnostika u revmatologa (tab. 3) [10]. Překážku představuje např. problém v dosažitelnosti zobrazovacích metod nebo zkušených specialistů k jejich interpretaci či finanční restrikce oddělení k provádění speciálních vyšetření včetně laboratorních. Ve fázi časné artritidy je již plně indikováno vyšetření komorbidit. Ukázalo se, že diagnostika, monitorování a léčba komorbidit jsou v praxi velmi rozdílné a kolísají mezi jednotlivými státy, ale i mezi jednotlivými klinikami. V běžné klinické praxi je často ponecháno zcela na individuálním lékaři, jak ke komorbiditám přistupuje. Často spoléhá na osvědčené kontakty mezi lékaři, s nimiž je zvyklý vzájemně komunikovat. Na řadě klinik však naopak fungují mechanismy k lepší organizaci péče o komorbidity ‒ jako příklad lze uvést pravidelné semináře či konzultace, např. mezi revmatology a pneumology, kardiology nebo dermatology. Některé nemocnice mají kombinované kliniky, např. revmatologicko kardiologickou nebo revmatologicko plicní, jež řeší problematiku plicních fibróz. Centrum v Kodani má kliniku pro odvykání kouření a kliniku zabývající se problematikou poruch spánku u nemocných s RA. Optimálním řešením péče o komorbidity je zřízení lékařské pozice koordinátor péče o komorbidity, který funguje například ve zmiňované nemocnici Cochin v Paříži. Organizuje komplexní péči o komorbidity a kromě toho také třeba pravidelné vyhodnocování komorbidit v šestiměsíčních intervalech.
Důležitým faktorem pro úspěšnou léčbu je její včasné zahájení, protože i několikatýdenní zpoždění zhoršuje výsledky terapie. Limitujícím faktorem adekvátní léčby mohou být i finanční rozpočtová omezení pro biologickou a cílenou léčbu nebo příliš restriktivní doporučení, především v případě pojišťoven. Přestože existují doporučení pro léčbu EULAR a národních společností, v praxi se vyskytují početné odchylky od těchto guidelines, jinými slovy doporučení nejsou v praxi dodržována, zvláště princip T2T není často respektován. S tím souvisí i nedostatečně pravidelné monitorování účinnosti léčby. Dalším evidovaným problémem je pacientova adherence k léčbě, která představuje problém především u seniorů, ale i u mladistvých a u nemocných ze slabších sociálních vrstev.
Na začátku léčby by měl být pacient náležitě edukován. Tato edukace by měla obsahovat nejen informace o onemocnění RA, ale i o tom, co lze očekávat od léčby a také o možných nežádoucích účincích. Zmíněny by měly být intervaly vyšetření, prováděné odběry a forma vyšetření. Důležité jsou informace o vhodných změnách životního stylu, včetně pohybových aktivit a stravovacích zvyklostí. Uvedené informace by měly být podávány multidisciplinárním týmem, který sestává jednak z lékařů různých specializací (revmatolog, rehabilitační lékař, internista, ortoped a podle přítomnosti komorbidit i lékař další specializace), jednak z nelékařských pracovníků, jako je specializovaná sestra, psycholog nebo ergoterapeut. Tito nelékařští pracovníci často přinášejí rozdílnou dimenzi péče a celkově přispívají k holistickému přístupu péče o pacienta. Nezřídka se též hovoří o systému péče soustředěné na pacienta. Výzkum v této studii ukázal, že v edukačních aktivitách existují mezi jednotlivými klinikami výrazné rozdíly. Jedním z nadřazených principů léčby RA EULAR je doporučení o sdíleném rozhodnutí mezi lékařem a pacientem při zahajování a změnách léčby [4]. Vzdělaný pacient je v tomto procesu samozřejmě lepším partnerem. Edukační aktivity by také měly potencovat schopnosti pacienta týkající se samoléčby (self management). Na řadě klinik jsou již pacienti zaškolováni v samohodnocení aktivity onemocnění a v dalších možnostech.
Ve stadiu časné artritidy je vhodné zařadit pacienta do registru. Může jít o registr biologické či cílené léčby, ale také o registr s observačními cíli hodnotící např. prediktivní faktory progrese, různé biomarkery, ale i farmakoekonomické či sociálně ekonomické aspekty onemocnění. Registry slouží samozřejmě primárně výzkumu, ale už svou podstatou pečlivého sledování jsou přínosné také pro pacienty, což je však před podpisem informovaného souhlasu nutné nemocnému pečlivě vysvětlit.
Stadium etablované revmatoidní
artritidy
Základním problémem této fáze je léčba se suboptimálními výsledky, která dlouhodobě nezlepšuje kvalitu života pacienta s RA. Především jde o malou adherenci k principu T2T. Při dotazníkových akcích se sice většina revmatologů k používání principu T2T hlásí, ale v praxi ho nerespektuje a upřednostňuje svoji klinickou zkušenost a odhad. Desítky klinických studií však potvrdily užitečnost tohoto principu. Důležitý je i poznatek, že dosažení cíle (remise, stavu nízké aktivity) musí být dlouhodobé, nejlépe trvalé. Značně rozšířené armamentarium DMARDs skutečně umožňuje vyhledat pro každého pacienta optimální lék.
Ve stadiu etablované, či dokonce pozdní RA se již objevují problémy s destrukcemi kloubů, zhoršení funkce a mobility, mohou se manifestovat nežádoucí účinky léků (gastrointestinální obtíže, osteoporóza), často vzniká částečná nebo plná invalidita, velmi často je přítomna deprese a úzkost. Je zjevné, že optimální péče o takového pacienta musí být komplexní a nejlepší formu představuje týmová péče v čele s revmatologem. V pražském Revmatologickém ústavu, ale i na řadě dalších klinik jsou k dispozici pravidelné indikační schůzky s revmatochirurgem či s fyzioterapeutem. Pravidelné konzultace poskytuje i kardiolog. Ne vždy je k dispozici pneumolog či diabetolog nebo psycholog. Je ale dobré, pokud je takový specialista alespoň nasmlouván k pravidelné spolupráci, a to formou etablovaného referování s adekvátně krátkými objednacími dobami.
Bylo prokázáno, že v průběhu času přibývají komorbidity. Proto se výzkum orientoval na způsob, jakým jsou komorbidity diagnostikovány a zejména monitorovány (tab. 3). Především pak bylo hodnoceno, jakým způsobem jsou monitorovány rizikové faktory komorbidit. Jak je uvedeno výše, výzkum této skupiny se koncentroval pouze na čtyři diagnózy. Nejdůležitější komorbiditou RA jsou kardiovaskulární onemocnění. Odborníci shledali několik základních elementů možností zlepšení péče o pacienty s RA s kardiovaskulárními chorobami. Otázkou zůstává, jak nejlépe kardiovaskulární riziko hodnotit. Všeobecně bývá doporučováno používat ukazatel SCORE a násobit jej u revmatiků 1,5krát. Tento systém však nemusí u řady pacientů vyhovovat a např. přidání informace o aterosklerotických plátech na karotidách pomůže zlepšit klasifikaci rizikové skupiny (p = 30‒60 %) [18]. Problémem bývá komunikace kardiologů působících na revmatologickém pracovišti nebo mimo ně. Bylo dokumentováno, že komplexní konzultace pro pacienta, která zahrnuje podání léků na redukci hodnot lipidů, podání antihypertenziv a doporučení pro nefarmakologickou prevenci (úprava životního stylu), může být efektivně docíleno během tří sezení u 80‒90 % pacientů [19]. U ošetřujícího revmatologa nebývá vždy dostatečná dokumentace o tom, jak je pacientovo kardiovaskulární onemocnění léčeno a monitorováno.
Intervence podle priorit v jednotlivých stadiích RA u pacientů s komorbiditami
V rámci interview byli účastníci
dotazováni také na priority intervencí. Ve stadiu
podezření na RA lékaři považovali za důležitější
rychlý přístup k péči, zlepšenou komunikaci s primárním
centrem a zřízení kliniky časné artritidy (tab. 4).
Ve stadiu nedávno diagnostikované RA byla prioritou opět
klinika časné artritidy, umožnění self managementu pacienta
a pečlivé vyšetření komorbidit. Ve stadiu etablované
RA pak šlo opět o umožnění self managementu, péče
specialisty na komorbidity a integraci pacientů
do pacientských registrů podle diagnózy.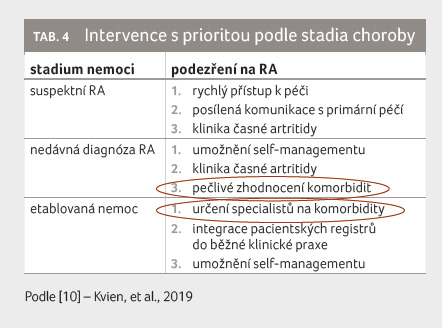
Diskuse
Komorbidity při RA terapii vždy komplikují, což je známo z literatury, ale potvrdila to i tato studie. V ní bylo rovněž zjištěno, že existují velké rozdíly v přístupu k pacientům s RA a s komorbiditami. Studie mimo jiné též doložila, že by bylo potřeba vytvořit nová konsenzuální doporučení pro léčbu komorbidit pacientů s RA.
Studie má ale řadu limitací. První z nich je absence pacientů při provádění interview, což bylo částečně kompenzováno přítomností nemocného při tvorbě rukopisu. Další limitací je výběr center, který se omezil na větší univerzitní centra a nemapoval situaci v terénu. Výsledky lze hodnotit také z hlediska, že šlo o vytvoření jakéhosi optimálního modelu v těchto špičkových centrech, který by pak mohl být implementován i do běžné praxe.
Další limitaci představuje fakt, že tento přehled se soustředil na čtyři hlavní komorbidity, tzn. kardiovaskulární onemocnění, intersticiální plicní onemocnění, diabetes a deprese. Nicméně z literárního přehledu vyplývá, že i další komorbidity jsou velmi důležité. Například bylo prokázáno, že osteoporóza se vyskytuje dvakrát častěji u pacientů s RA ve srovnání s kontrolami ve stejném věku [20] a že fraktury jsou časté [21]. Organizace péče k podpoře primární a sekundární prevence osteoporózy je důležitá a snižuje morbiditu pacientů. Další komorbiditou jsou infekce. Zde je možné zmínit, že EULAR nedávno publikoval doporučení pro vakcinaci [22] a některé editorialy diskutovaly důležité otázky hepatitidy a tuberkulózy v této populaci. Návody na screening malignit a gastrointestinálních obtíží nebyly hodnoceny, ale je konstatováno, že tyto komorbidity vedou ke špatným výsledkům u pacientů s RA.
Závěr
Za nejdůležitější přínos považujeme popis způsobů správné klinické praxe ve specializovaných centrech. Může sloužit jako určitý model pro další zařízení, jakým způsobem optimálně provádět služby při léčbě revmatických pacientů.
Práce byla podpořena projektem
Ministerstva zdravotnictví koncepčního rozvoje výzkumné
organizace 00023728 Revmatologický ústav.
Seznam použité literatury
- [1] Angel J, Akeson K, Amadio PC, et al. The burden of musculosceletal conditions at the start of new milenium. World Health Organ Tech Rep Ser 2003: 919‒1218.
- [2] Schett G, Emery P, Tanaka Y, et al. Tapering biological and conventional DMARD therapy in rheumatoid arthritis: current evidence and future directions. Ann Rheum Dis 2016; 75: 1428–1437.
- [3] Smolen JS, Aletaha D, Barton A, et al. Rheumatoid arthritis. Nat Rev Dis Primers 2018; 4: 18001.
- [4] Smolen J, Breedveld FC, Burmester G, et al. Treating rheumatoid arthritis to target: 2014 update of recommendation of an international task force. Ann Rheum Dis 2016; 75: 3‒15.
- [5] Smolen J, Landewé R, Bijlsma J, et al. EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease modifying antirheumatic drugs 2016 update. Ann Rheum Dis 2017; 76: 960‒977.
- [6] You CH, Jin S, Wang Y, et al. Remission rate and predictors of remission in patients with rheumatoid arthritis under treat to target strategy in real‑world studies: a systematic review and metaanalysis. Clin Rheumatol 2019; 38: 727‒738.
- [7] Ishida M, Kuroiwa Y, Yoshida E, et al. Residual symptoms and disease burden among patients with rheumatoid arthritis in remission or low disease activity: a systematic literature review. Mod Rheumatol 2017; 28: 789‒799.
- [8] Dougados M, Soubrier M, Antunez A, et al. Prevalence of comorbidities in rheumatoid arthritis and evaluation of their monitoring: results of an international, cross sectional study (COMORA). Ann Rheum Dis 2014; 73: 62‒68.
- [9] Baillet A, Gossec L, Carmona L, et al. Points to consider for reporting, screening for a preventing selected comorbidities in chronic inflammatory rheumatic diseases in daily practise. A EULAR initiative. Ann Rheum Dis 2016; 75: 965‒973.
- [10] Kvien TK, Pavelka K, Polido‑Pereira J, et al. Considerations for improving quality of care of patients with rheumatoid arthritis and associated comorbidities. EULAR 2019 (Abstr THU0638). Dostupné na: https://ard.bmj.com/content/78/Suppl_2/613.2 [v tisku].
- [11] Raghu G, Remy‑Jardin M, Myerset J, et al. Diagnosis of Idiopathic Pulmonary Fibrosis. An Official ATS/ERS/JRS/ALAT Clinical Practice Guideline. Am J Respir Crit Care Med 2018; 198: 44–68.
- [12] Skold RM. Idiopatisk Lungfibros, Vårdprogram. Swedish Respiratory Society 2019 (ISBN 978‑91‑87514‑47‑0).
- [13] Agca R, Heslinga S, Rollefstad S, et al. EULAR recommendations for cardiovascular disease risk management in patients with rheumatoid arthritis and other forms of inflammatory joint disorders: 2015/2016 update. Ann Rheum Dis 2017; 76: 17‒28.
- [14] Mach F, Baigent C, Catapano A, et al. 2019 European Society of Cardiology / European Atherosclerosis Society Guidelines for the management of dyslipidaemias: lipid modification to reduce cardiovascular risk. Eur Heart J 2020; 41: 111‒188.
- [15] Andreu Sanchez JL, Balsa A, Gualda E, et al. GUIPCAR Group. Update of the clinical practice guideline for the management of rheumatoid arthritis in Spain. Spanish Society of Rheumatology 2011.
- [16] André‑Vert J, Guillez P, Scémama O. Clinical practice guidelines: Rheumatoid Arthritis ‒ Medical, social and organisational aspects of treatment (excluding surgery and drugs). Haute Autorite De Sante 2017.
- [17] Goldberg D, et al. Depression in adults with a chronic physical health problem: recognition and management. NICE 2009. Dostupné na: https://www.nice.org.uk/guidance/cg91/resources/depression‑in‑adults‑with‑a‑chronic‑physical‑health‑problem‑recognition‑and‑management‑pdf‑975744316357
- [18] Semb AG, Ikdahl E, Hisdal J, et al. Exploring cardiovascular disease risk evaluation in patients with inflammatory joint diseases. Int J Cardiol 2016; 23: 441‒436.
- [19] Rollestad S, Kvien TK, Holme I, et al. Treatment to liquid targets in patients with inflammatory joint diseases in a preventive cardio‑rheuma clinic. Ann Rheum Dis 2013; 72: 1968‒1974.
- [20] Haugeberg G, Uhlig T, Falch JA, et al. Reduced bone mineral density in male rheumatoid arthritis patients: frequencies and associations with demographic and disease variables in ninety‑four patients in the Oslo County Rheumatoid Arthritis Register. Arthritis Rheum 2000; 43: 2776‒2784.
- [21] Ørstavik RE, Haugeberg G, Mowinckel P, et al. Vertebral deformities in rheumatoid arthritis: a comparison with population‑based controls. Arch Intern Med 2004; 164: 420‒425.
- [22] Furer V, Rondaan C, Heijstek M, et al. 2019 update of EULAR recommendations for vaccination in adult patients with autoimmune inflammatory rheumatic diseases. Ann Rheum Dis 2020; 79: 39‒52.