Kabazitaxel – zkušenosti z běžné praxe
Souhrn:
Katolická J, Filipenský P. Kabazitaxel – zkušenosti z běžné praxe. Remedia 2018; 28: 357–360.
Karcinom prostaty je nejčastějším nádorovým onemocněním u mužů. Kabazitaxel je semisyntetický derivát taxanů. Podání této látky v kombinaci s prednisonem statisticky signifikantně prodlužuje přežití u pacientů s metastatickým kastračně rezistentním karcinomem prostaty (metastatic castration resistant prostate cancer, mCRPC) po předchozí léčbě docetaxelem. Sekvenční podání chemoterapie, ARTA přípravků (léky s vlivem na androgenní receptor) a radionuklidu radium‑223 dosahuje významného prodloužení přežití pacientů s mCRPC.
Summary:
Katolicka J, Filipensky P. Cabazitaxel – real-life experience. Remedia 2018; 28: 357–360.
Prostate cancer is the most common cancer in men. Cabazitaxel is a semisynthetic taxane derivative. Cabazitaxel with prednisone statistically and significantly prolongs survival in patients with metastatic castration resistant prostate cancer (mCRPC) after previous treatment with docetaxel. Sequential administration of chemotherapy, ARTA (androgen receptor targeted agents) and radionuclide radium‑223 results in a significant prolongation of the survival of mCRPC patients.
Key words: cabazitaxel, metastatic castration resistant prostate cancer , sequential therapy.
Úvod
Karcinom prostaty je nejčastějším nádorovým onemocněním u mužů. Díky výsledkům dlouhodobého výzkumu a vývoje se velmi významně rozšířily možnosti léčby metastatického kastračně rezistentního karcinomu prostaty (metastatic castration resistant prostate cancer, mCRPC). Nové terapeutické možnosti přinesly prodloužení přežití a pozitivní ovlivnění kvality života takto nemocných.
Kabazitaxel
Kabazitaxel je semisyntetický derivát taxanů. Je částečně syntetizován jako jednoduchý diastereoizomer z 10 deacetylbaccatinu III, hlavního přírodního taxoidu získaného z jehlic tisu (Taxus sp.). Má široké spektrum antitumorózní aktivity. Svým účinkem urychluje tvorbu mikrotubulů a stabilizuje již vytvořené tubuly, čímž blokuje mitózu a následně vede k buněčné smrti [1]. Kabazitaxel je svojí strukturou odlišný od docetaxelu, hydroxylová skupina docetaxelu je u této molekuly nahrazena methoxy skupinou.
Kabazitaxel v klinických studiích
Kabazitaxel ve studii fáze II ukázal, že je aktivní a dobře tolerovatelný ve skupině pacientů rezistentních na taxany [2]. Jeho účinnost a bezpečnost u mužů s mCRPC předléčených docetaxelem hodnotila studie fáze III ‒ TROPIC [3]. Do tohoto hodnocení bylo zařazeno 775 mužů s progresí onemocnění během léčby docetaxelem nebo po ní, kteří při léčbě perorálním prednisonem v dávce 10 mg/den byli randomizováni do ramene s mitoxantronem (infuze 12 mg/m2 každé 3 týdny; n = 377) nebo do ramene s kabazitaxelem (infuze 25 mg/m2 každé 3 týdny; n = 378). Primárním cílovým ukazatelem studie bylo hodnocení celkového přežití (overall survival, OS); sekundární cílový ukazatel zahrnoval přežití bez progrese onemocnění, hodnocení odpovědi na léčbu, měření bolesti a bezpečnost podání. Pacienti léčení kombinací kabazitaxel/prednison měli signifikantně delší OS ve srovnání s režimem mitoxantron/prednison (15,1 měsíce vs. 12,7 měsíce; poměr rizik [HR] 0,70; 95% interval spolehlivosti [CI] 0,59‒0,83; p < 0,0001). Doba přežití bez progrese onemocnění, hodnocení odpovědi na léčbu a hodnocení odpovědi sérové koncentrace prostatického specifického antigenu (PSA) byly také statisticky signifikantní ve prospěch ramene s kabazitaxelem. Odpověď tumoru na léčbu ve skupině s kabazitaxelem byla zaznamenána u 14,4 % léčených ve srovnání s 4,4 % ve skupině s mitoxantronem. Závěrem studie TROPIC lze konstatovat, že kombinace kabazitaxelu s prednisonem statisticky signifikantně prodlužuje přežití u pacientů s mCRPC po předchozí léčbě docetaxelem. Toxicita kabazitaxelu byla vzhledem k předchozím zkušenostem s docetaxelem přijatelná a předvídatelná. Vzhledem k dobré účinnosti kabazitaxelu po předchozím podání docetaxelu byla v klinické studii fáze III FIRSTANA [4] testována možnost zařazení kabazitaxelu v dávce 20 mg/ m2 i.v. nebo 25 mg/m2 i.v. v léčebném algoritmu mCRPC namísto docetaxelu. Kabazitaxel však ani v jednom z dávkovacích režimů neprokázal signifikantní prodloužení přežití ve srovnání s docetaxelem u kastračně rezistentního chemoterapií nepředléčeného karcinomu prostaty (HR 1,01, p = 0,99, srovnávající docetaxel s kabazitaxelem 20 mg/m2; HR 0,97, p = 0,76, srovnávající kabazitaxel 25 mg/m2). Nebyly zaznamenány žádné nové informace o rozdílech v bezpečnostním profilu mezi oběma taxany.
Kabazitaxel v sekvenčním podání
Výsledky prokázané registračními studiemi fáze III v monoterapii jak kabazitaxelu, tak léků s vlivem na androgenní receptor (ARTA, androgen receptor targeted agents – abirateron acetát, enzalutamid) i radia 223 nabízejí možnosti terapie mCRPC. Sekvenční podání se nyní jeví jako nejvhodnější postup. Nabízí několik variant ve dvou, třech, případně čtyřech a více liniích, např. docetaxel/kabazitaxel/enzalutamid nebo docetaxel/kabazitaxel/abirateron, docetaxel/ARTA/kabazitaxel, docetaxel/ARTA/kabazitaxel/radium 223, docetaxel/radium 223/kabazitaxel/ARTA atd.
Terapií kabazitaxel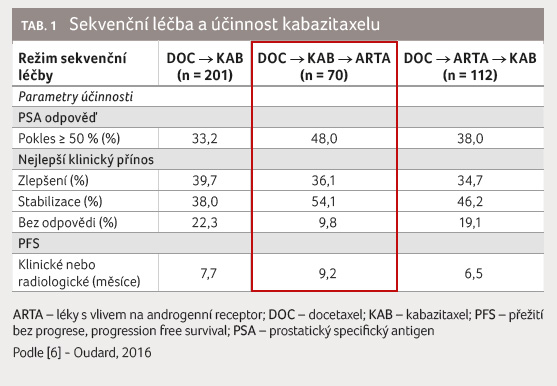 em a sekvenční
léčbou mCRPC aplikovanou po předchozí léčbě docetaxelem
se zabývalo zhodnocení výsledků od 574 pacientů z evropské
databáze FLAC ze 44 center v šesti evropských zemích.
Kabazitaxel byl podáván ve všech hodnocených skupinách.
Aktualizace dat z roku 2017 [5] ukázala, že retrospektivně
podávaná sekvence docetaxel/kabazitaxel/ARTA vykazuje ve srovnání
s dvojsekvencí docetaxel/kabazitaxel a s trojsekvencí
docetaxel/ARTA/kabazitaxel nejdelší dobu celkového přežití.
Medián počtu podání kabazitaxelu byl 6, medián trvání léčby
ARTA přípravkem byl 4,4 měsíce v případě, že abirateron
nebo enzalutamid byly podány ihned po docetaxelu a byly
následovány kabazitaxelem. V případě zařazení ARTA
přípravku na poslední místo trojsekvence byl medián doby
užívání kabazitaxelu 5,9 měsíce. Z hlediska hodnocení OS,
počítáno od podání prvního cyklu docetaxelu, měla
trojsekvence docetaxel/kabazitaxel/ARTA nejdelší dobu, a to
40,1 měsíce (95% CI 34,6‒51,8). Doba OS po podání ARTA
přípravku po docetaxelu a následovaného kabazitaxelem
byla 37,1 měsíce (95% CI 32,5‒40,5). Nejkratší dobu vykázala
dvojsekvence docetaxel/kabazitaxel ‒ 30,1 měsíce (95% CI
26,8‒32,7). Další hodnocení s trojsekvenční léčbou
u 383 nemocných ukazuje na přínos podání kabazitaxelu
ihned po selhání docetaxelu (tab. 1) [6].
em a sekvenční
léčbou mCRPC aplikovanou po předchozí léčbě docetaxelem
se zabývalo zhodnocení výsledků od 574 pacientů z evropské
databáze FLAC ze 44 center v šesti evropských zemích.
Kabazitaxel byl podáván ve všech hodnocených skupinách.
Aktualizace dat z roku 2017 [5] ukázala, že retrospektivně
podávaná sekvence docetaxel/kabazitaxel/ARTA vykazuje ve srovnání
s dvojsekvencí docetaxel/kabazitaxel a s trojsekvencí
docetaxel/ARTA/kabazitaxel nejdelší dobu celkového přežití.
Medián počtu podání kabazitaxelu byl 6, medián trvání léčby
ARTA přípravkem byl 4,4 měsíce v případě, že abirateron
nebo enzalutamid byly podány ihned po docetaxelu a byly
následovány kabazitaxelem. V případě zařazení ARTA
přípravku na poslední místo trojsekvence byl medián doby
užívání kabazitaxelu 5,9 měsíce. Z hlediska hodnocení OS,
počítáno od podání prvního cyklu docetaxelu, měla
trojsekvence docetaxel/kabazitaxel/ARTA nejdelší dobu, a to
40,1 měsíce (95% CI 34,6‒51,8). Doba OS po podání ARTA
přípravku po docetaxelu a následovaného kabazitaxelem
byla 37,1 měsíce (95% CI 32,5‒40,5). Nejkratší dobu vykázala
dvojsekvence docetaxel/kabazitaxel ‒ 30,1 měsíce (95% CI
26,8‒32,7). Další hodnocení s trojsekvenční léčbou
u 383 nemocných ukazuje na přínos podání kabazitaxelu
ihned po selhání docetaxelu (tab. 1) [6].
Klinická zkušenost s kabazitaxelem – kazuistika
Muž, narozený v roce 1951, byl v dubnu 2014 praktickým lékařem odeslán na urologické vyšetření pro elevaci PSA na hodnotu 5,96 μg/l. Klinickým vyšetřením byla zjištěna neohraničená prostata s nálezem tumorózní infiltrace v oblasti pravého laloku. Biopsie prokázala adenokarcinom prostaty, Gleasonovo skóre (stupeň diferenciace nádorů prostaty) 4 + 4. Vstupní scintigrafie skeletu a CT vyšetření břicha a pánve neprokázaly vzdálenou diseminaci onemocnění. Pacient byl ve velmi dobrém stavu, ECOG PS (Eastern Cooperative Oncology Group performance status) 0, z přidružených chorob léčen pouze pro hypertenzi, užíval betablokátor, neudával alergie. Žil v oblasti Mikulova velmi aktivním životem vinaře. V červnu 2014 byla provedena radikální prostatektomie s lymfadenektomií, histologicky potvrzen adenokarcinom prostaty, ale s vyšším Gleasonovým skóre než v biopsii, a to 5 + 5, zařazení podle TNM klasifikace zhoubných novotvarů pT2cpN0M0. Po operaci byla zaznamenána močová inkontinence 1. stupně. Dále byl nemocný sledován v urologické ambulanci. V květnu 2016 přichází pro bolesti v zádech, RTG Th, L páteře prokazuje metastatické postižení obratlů Th9, Th11 a L2. Následně doplněná scintigrafie skeletu prokazuje vícečetná ložiska ve skeletu. V rámci analgetické léčby jsou podána nesteroidní antirevmatika a následně pro jejich nedostatečný účinek fentanylová náplast. Byla zahájena kastrační léčba GnRH antagonistou gonadotropiny uvolňujícího hormonu (GnRH) degarelixem v úvodní dávce 240 mg s.c., a poté každý měsíc v dávce 80 mg s.c. Jako prevence kostních komplikací (skeletal related event, SRE) z důvodu rozsáhlého kostního postižení byl každých 28 dní podáván denosumab v dávce 120 mg s.c. Je dosaženo kastrační koncentrace testosteronu > 0,09 nml/l. Účinek kastrační terapie trval šest měsíců, do prosince 2016, kdy dochází ke klinické progresi choroby, nově se objevily lymfedémy dolních končetin. CT vyšetření břicha a malé pánve prokázalo uzlinové postižení v retroperitoneu. Nemoc přechází do stadia kastračně rezistentního a pacient je odeslán na onkologické pracoviště k další léčbě.
Vzhledem k tomu, že se jedná o symptomatické onemocnění s krátkodobou odpovědí na kastrační léčbu, je u pacienta s PS 1 podána chemoterapie docetaxel v dávce 75 mg/m2 i.v. každých 21 dnů v kombinaci s prednisonem. Nadále je ponechána léčba denosumabem a kastrační terapie. Po čtyřech cyklech léčby docetaxelem, za tři měsíce, dochází opět k progresi choroby, nově se na CT vyšetření prokázala metastatická ložiska plicní. Vzhledem k tomu je v březnu 2017 zahájeno podání kabazitaxelu v dávce 25 mg/m2 i.v. a prednisonu 10 mg/den p.o. s preventivním užíváním pegfilgrastimu s.c. 24 hodin po ukončení chemoterapie jako další linie léčby kastračně rezistentního onemocnění s rychlou progresí choroby a s viscerálním postižením. Pacient je stále v dobrém klinickém stavu, bolesti jsou kompenzované fentanylem, přetrvává lymfedém dolních končetin.
Aplikace nového taxanu kabazitaxelu přinesla pacientovi velmi významný klinický prospěch. Již po dvou podáních dochází k ústupu lymfedémů, zmírnila se bolest a nemocný mohl přejít na podávání menších dávek fentanylu. Celkem proběhlo 10 aplikací kabazitaxelu tak, jak umožňuje úhradová vyhláška. Nebyla prokázána hematologická toxicita stupně 3/4, z nehematologické toxicity se objevil průjem 2. stupně, nevolnost 2. stupně, celková únava stupně 1/2, alopecie. Během léčby nebylo nutné navyšovat dávky analgetik, přínosem byla dobrá kvalita života. Za čtyři a půl měsíce po ukončení léčby kabazitaxelem kontrolní CT vyšetření prokázalo progresi metastatického postižení, objevily se metastázy, jaterní a onkologická léčba byla vzhledem ke zhoršení celkového stavu ukončena. Nemocný byl léčen pouze symptomatickou terapií a v lednu 2018 zemřel. Kabazitaxel muži s karcinomem prostaty, Gleasonovým skóre 5 + 5, ve fázi symptomatického kastračně rezistentního onemocnění s metastatickým postižením plic, kostí a uzlin retroperitonea jako jediná ze všech léčebných možností významně prodloužil přežití a zlepšil kvalitu života.
Postavení kabazitaxelu v léčbě kastračně rezistentního karcinomu prostaty
Podání kabazitaxelu v léčebném algoritmu mCRPC je indikováno po předchozím podání docetaxelu v tzv. post chemo indikaci [7]. Je možné pacienta zaléčit hned po selhání předchozí léčby docetaxelem nebo po podání docetaxelu s následným užitím některého z ARTA. V rámci úhradové vyhlášky [8] pro nemocné léčené v České republice jsou stanoveny podmínky, kdy kabazitaxel v kombinaci s prednisonem je hrazen u pacienta s mCRPC se stavem výkonnosti ECOG 0‒1, předléčenost docetaxelem je možná v jedné až dvou liniích. Terapie je hrazena do progrese onemocnění, která je definována elevací PSA nebo bolestí nebo radiologicky či výskytem nepříznivé skeletální příhody. Maximálně je možné podat 10 léčebných cyklů. Tímto přípravkem není možné léčit pacienty s neuropatií nebo se stomatitidou druhého a vyššího stupně nebo pacienty se závažnými komorbiditami včetně duplicitních malignit.
Závěr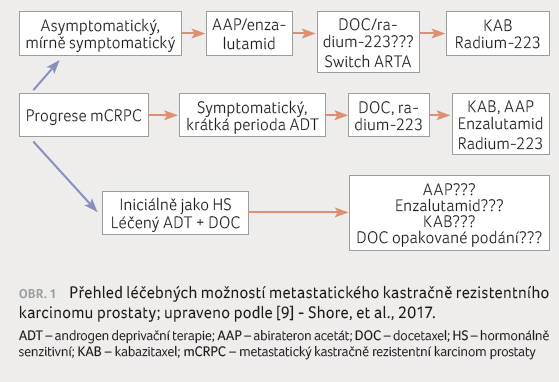
Léčebné možnosti dostupné v posledních letech výrazně změnily přístup k pacientům s kastračně rezistentním karcinomem prostaty. V současné chvíli je to onemocnění, u kterého včasně zahájenou léčbou s řadou možností sekvenčního podání dosahujeme významného prodloužení přežití (obr. 1). Multioborová spolupráce spočívající v přístupu k léčbě a ve využití všech léčebných variant je základem úspěchu.
Seznam použité literatury
- [1] Jordan MA, Wilson L. Microtubules as a target for anticancer drugs. Nature Rev Cancer 2004; 4: 253‒265.
- [2] Pivot X, Koralewski P, Hidalgo J, et al. A multicenter phase II study of XPR6258 administered as a 1‑h i.v. infusion every 3 weeks in taxane‑resistant metastatic breast cancer patients. Ann Oncol 2008; 19: 1547‒1552.
- [3] De Bono JS, Oudard S, Ozguroglu M, at al. Prednisone plus cabazitaxel or mitoxantrone for metastatic castration‑resistant prostate cancer (mCRPC) progressing after docetaxel treatment: a randomized open‑label trial. Lancet 2010; 376: 1147‒1154.
- [4] Sartor AO, Oudard S, Sengelov L, et al. Cabazitaxel vs docetaxel in chemotherapy‑naive (CN) patients with metastatic castration‑resistant prostate cancer (mCRPC): A three‑arm phase III study (FIRSTANA) ASCO meeting 2016, Chicago, Abstract 5006.
- [5] Delanoy N, Angelergues A, Efstathiou E, et al. Sequencing in metastatic castration‑resistant prostate cancer (mCRPC): Updated results of the FLAC International Database. Dostupné na: http://ascopubs.org/doi/abs/10.1200/JCO.2017.35.6_suppl.267
- [6] Oudard S. Management of prostate cancer. Optimal sequens in metastatic castration-resistant prostate cancer (mCRPC): Preliminary results of the FLAC International study, Onco-urology academy, Roma 2016, oral presentation.
- [7] Dostupné na: http://www.linkos.cz
- [8] Dostupné na: http://www.olecich.cz
- [9] Shore N, Heidenreich A, Saad F. Predicting response and recognizing resistance: Improving outcomes in patients with castration-resistant prostate cancer. Dostupné na: http://dx.doi/abs/10.1016/j.urology.2017.04.062